原發性膽汁性膽管炎有無合并干燥綜合征的異同
文振華,姚芳玲,凌 青,李敬揚
原發性膽汁性膽管炎(PBC)是一種表現為慢性膽汁淤積的器官特異性自身免疫病。PBC可以合并多種自身免疫病,文獻報道,高達35.3%的PBC患者合并干燥綜合征(SS)[1]。SS是一種多系統受累的免疫性疾病,合并SS的PBC在治療上較單純的PBC復雜,前者預后更差[1],但更早的文獻認為,在兩種疾病共存的情況下,PBC和SS的病情均相對較輕[2]。這些尚未達成共識的臨床問題值得人們進一步探索。
1 資料與方法
1.1 病例資料 選擇2008年12月~2018年11月株洲市中心醫院住院和門診治療的112例成年初治的PBC患者(住院69例,門診43例),將其中PBC合并SS患者作為PBC-SS組,單純PBC患者作為PBC組。入組標準:符合PBC國際診斷分類標準(美國肝臟病學會2000年版)[3],并除外肝外膽管梗阻及其他肝病,如各種急慢性病毒性肝炎、藥物性肝炎、酒精性肝病、α-抗胰蛋白酶缺乏癥及其他自身免疫性肝病等;合并SS的診斷同時滿足SS的國際診斷分類標準(2002年美國歐洲共識小組修訂版)[4],并除外其他結締組織病繼發的SS,只納入原發性SS患者。
1.2 評價指標 收集患者初次確診時下列指標檢測或評價結果:(1)生化和免疫學指標:肝功能、類風濕因子(RF)、凝血酶原時間(PT)和免疫球蛋白(Ig)等生化指標均由本院臨床檢驗中心完成;抗核抗體譜(ANA)、抗SSA和抗SSB抗體采用歐盟試劑公司試劑盒通過免疫印記法檢測;抗gp210、抗AMA和抗sp100抗體采用德國胡曼公司試劑盒通過免疫印記法檢測,以上抗體檢測均由醫院風濕免疫科實驗室完成。(2)肝功能:根據患者臨床表現和肝功能檢測結果,按照Child-Pugh分級標準[5]進行肝功能評分。(3)肺間質病變:對胸部X片可疑雙下肺間質病變或有相關呼吸道癥狀或體征(如慢性干咳、氣促和雙下肺Velcro啰音等)的患者,進行肺部高分辨CT檢查確診。(4)SS的客觀檢查:對于有口干眼干主觀癥狀的患者進行專科檢查。眼科檢查:包括角膜染色和Schirmer試驗;口腔科檢查包括唾液流率和唇腺活檢。陽性結果參照2002年干燥綜合征國際診斷分類標準判定[4]。
1.3 統計學方法 應用SPSS 17.0統計軟件分析,計數資料以頻數和百分率表示,組間比較采用χ2檢驗;符合正態分布的計量資料以x±s表示,組間比較采用t檢驗;P<0.05為差異有統計學意義。
2 結果
2.1 一般情況 PBC-SS組共49例,PBC合并SS的發病率為43.8%,病程平均為(18.71±8.72)個月,平均年齡(48.71±9.22)歲,其中男 2 例(4.1%);PBC組共 63例,平均病程(16.59±9.83)個月,平均年齡(50.12±10.59)歲,其中男 3 例(4.8%)。 合并癥:高血壓病15例 (13.4%,其中PBC-SS組7例、PBC組8例),糖尿病 6例(5.4%,其中 PBC-SS組 4例、PBC組2例);家族史:一級親屬患有SS者2例(1.8%,均在PBC-SS組)。兩組性別、年齡、病程及合并疾病等比較均無統計學差異(P>0.05)。
2.2 臨床資料比較 相比于PBC組,PBC-SS組的口干、眼干癥狀更常見(P<0.05),肺間質病變更多見(P<0.01),肝功能的 Child-Pugh評分更低(P<0.05),見表 1。
2.3 免疫學指標比較 相比于PBC組,PBC-SS組的抗SSA/SSB抗體陽性率更高,免疫球蛋白IgG升高更多見,RF的滴度更高(P<0.05,表 2)。
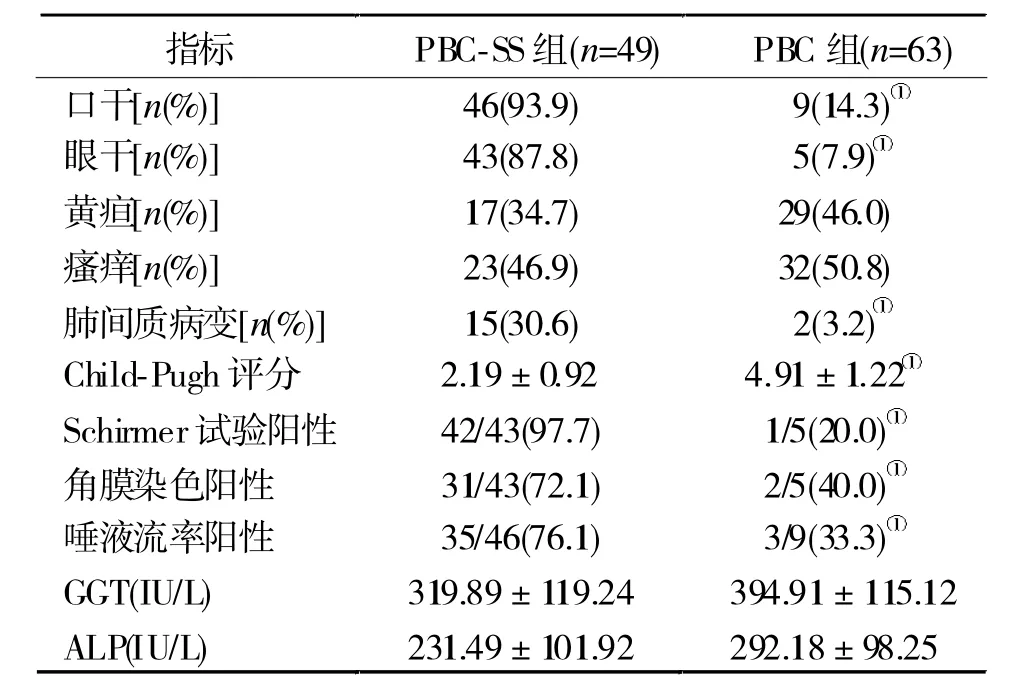
表1 兩組臨床資料比較
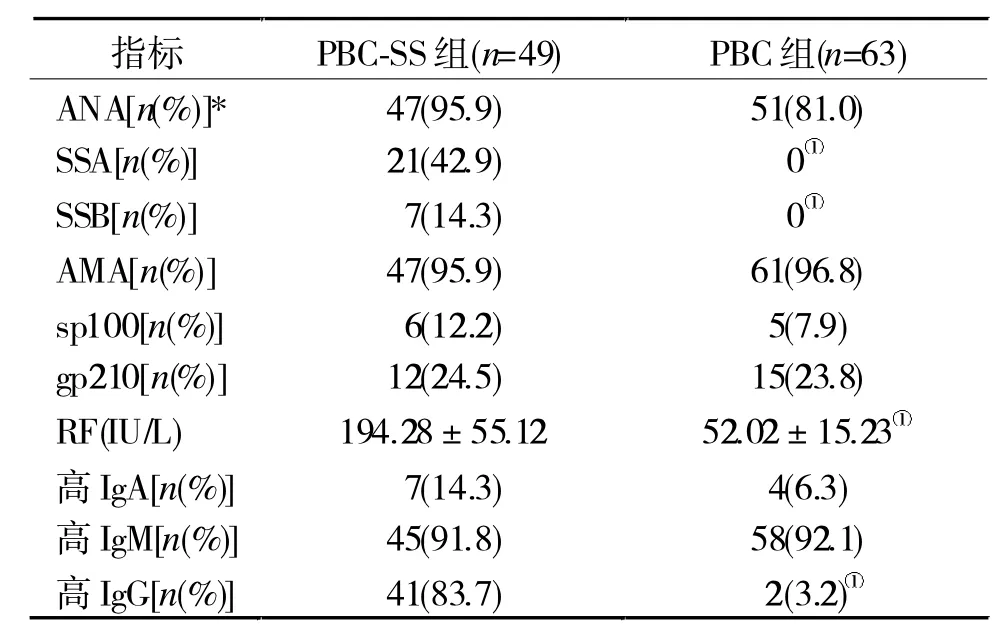
表2 兩組免疫學指標比較
3 討論
PBC和SS均為自身免疫病,PBC和SS有類似的發病機理,兩者都是典型的自身免疫性上皮炎,靶組織中CD4+T細胞的浸潤凋亡、分泌性IgA的作用十分類似[6-7],因此,兩者常常合并出現,國內外的文獻報道,PBC合并SS的發生率從21%到81%不等[8]。本組PBC合并SS的發病率為43.8%,與我國臺灣地區報道的35.3%發病率最接近[1],提示人種或地區差異在發病中的作用不同。
PBC和SS還有類似的臨床表現,如單純PBC可以出現類似SS的口干眼干癥狀,但唾液流率和角膜染色等客觀指標往往達不到SS的診斷標準;單純SS也可以出現肝損傷,少數患者甚至可以出現類似PBC明顯升高的ALP和GGT,但一般同時合并轉氨酶的升高,把SS合并PBC與SS原發病導致的肝損傷進行鑒別診斷的意義重大,因為SS的肝損傷激素治療療效佳,且極少發展為肝硬化,但PBC的肝損傷對激素的反應差,易進展為肝硬化,熊去氧膽酸才能延緩或阻止其發展為肝硬化。這類患者若能檢出PBC的特異性抗體則鑒別診斷不難,但部分抗體陰性的病人可能需要肝活檢才能確診。本文PBC-SS組就有2例沒有PBC的特異性抗體,因為GGT、ALP明顯升高且對激素反應差,行肝活檢后確診為PBC。Matsumoto等[9]報道,PBC-SS比單純PBC更容易出現淋巴細胞浸潤性非化膿性膽管炎。
PBC和SS又有不同,從易感基因、免疫學、臨床表征到治療均有很大差異。PBC具有器官和組織特異性,常隱匿起病,主要累及肝內小膽管,導致慢性膽汁淤積,早期往往無臨床癥狀,甚至直到肝硬化才就診。而SS的免疫損傷相對廣泛,其中外分泌腺為主要靶器官,患者常因淚腺和涎腺的功能受損而出現眼干、口干。本研究也發現,PBC-SS組的眼干口干明顯更多見(客觀專科檢查也證實了這一點),這些不適往往促使患者及時求醫,這也解釋了為什么本研究中PBC-SS組的Child-Pugh評分更低,肝硬化更少見。Uddenfeldt等[2]也報道,合并SS的PBC肝臟病理多在早期階段(肝臟組織學的Ⅰ~Ⅱ期)。這種現象并不意味著合并SS的PBC更輕,而是SS相關的臨床癥狀會讓PBC患者更早就醫、更早確診。在更長隨訪時間的研究中,合并SS的PBC與單純PBC患者的肝硬化發生率類似,但長期預后更差,其中SS導致的肺間質病變可能是兩者生存期差異的重要原因[1]。本研究中PBC-SS組肺間質病變的發生率明顯升高(30.6%vs 3.2%),這是否會成為影響患者長期預后的決定性因素,尚需要進一步觀察。值得一提的是,雖然與文獻報道一樣,單純PBC也可以出現肺間質病變[10],但PBC繼發的肺間質病變臨床罕見,故首先應該明確是否因為合并了SS。
自身免疫病大多有相對特異的自身抗體,如抗AMA抗體是PBC的特異性抗體,而抗SSA抗體與SS密切相關。因此,本研究中PBC-SS組抗SSA抗體自然更常見。抗SSB抗體陽性率低,一般只伴隨抗SSA抗體出現,它們均屬于抗核抗體譜,檢測價格較為昂貴,且檢驗流程復雜,不宜作為初篩。本研究還發現,RF和IgG在PBC-SS組明顯更高,尤其是高IgG在PBC-SS組多見(83.7%),而單純PBC組極少見(3.2%),提示IgG有成為PBC是否合并SS初篩指標的潛質。Selmi等[6]指出,PBC可以引起免疫球蛋白IgM升高,但IgG的明顯升高多見于合并SS的患者。值得注意的是,針對SS的激素和免疫抑制劑治療可以降低IgG水平,因此,IgG檢測在初治病人中更有價值。
在治療方面,張烜等[11]指,出糖皮質激素和(或)免疫抑制劑可以改善合并SS或IgG升高的PBC的生化指標。在IgG和(或)ALT明顯升高的PBC患者中,除了考慮合并SS,還要注意有無合并自身免疫性肝炎,糖皮質激素和(或)免疫抑制劑改善的是這兩種合并疾病的肝損傷,而對單純PBC的療效缺乏足夠證據(布地奈德除外)[12]。此外,PBC-SS患者還要兼顧肝外臟器的治療,尤其是肺間質病變的療效可能決定患者的長期預后。
綜上所述,PBC有無合并SS在臨床和免疫學上均有很大不同,使得治療和臨床結局上也有不同。應充分掌握這些異同,熟悉SS的臨床表現,可以使隱匿的PBC患者更早確診,而早期識別合并SS的PBC才能更全面的治療。

