過表達SlMYB75 對番茄幼苗、果實及種子的影響
張 振,徐志璇,王麗娜,李 強,陳春花,任仲海
山東農業大學園藝科學與工程學院,山東果蔬優質高效生產協同創新中心/農業部黃淮地區園藝作物生物學與種質創制重點實驗室,作物生物學國家重點實驗室,山東 泰安271018
番茄(Solanum lycopersicum)是世界范圍內的重要經濟作物之一。MYB 轉錄因子參與植物的生長調節、對生物和非生物脅迫的響應等。在擬南芥和水稻中,MYB 家族已被鑒定和研究[1,2]。擬南芥R2R3-MYB 轉錄因子MYB15 參與ABA 信號轉導,MYB15過表達株系對ABA 的敏感性增強,抗逆性增強[3]。生長素作為一種重要的激素,在頂端優勢、調控生長及向性等方面有重要作用,擬南芥轉錄因子MYB77 響應生長素信號,在MYB77突變體中生長素應答基因的表達量顯著下降[4]。研究表明,擬南芥AtMYB33 蛋白能夠結合在花分生組織特性基因LEAFY啟動子8 bp 的序列上,在開花時調控GA 信號[5]。擬南芥R2R3MYB 蛋白FLP 與MYB88 共同調控生長素輸出載體基因PIN從而來影響根系的向重力性[6]。已有研究證明番茄中MYB74、MYB92、MYB78、MYB102、MYB62、MYB2、MYB64、MYB116、MYB113、MYB11能夠被NaCl 所誘導[7]。番茄SLFSM1 是果實特異的MYB 類轉錄因子,它可以與FSB1和另一個MYB 轉錄因子形成三重復合物共同調控細胞的擴增,在SLFSM1高量表達番茄株系中,果實小、中果皮薄、中果皮細胞較小,且還抑制了下胚軸子葉細胞的伸長[8]。有研究報道,擬南芥AtMYB30 轉錄因子,可以影響ANNs 蛋白介導的特異的胞內鈣信號的產生,從而調控植物響應氧化脅迫和熱脅迫[9]。擬南芥AtMYB97,AtMYB101和AtMYB120能夠調控花粉管接受花粉,從而影響受精作用[10]。過表達菊花CmMYB2植株較野生型開花延遲,葉片數目增多,在擬南芥中過表達CmMYB2,能夠增強轉基因擬南芥對干旱和鹽脅迫的耐受性[11]。
在番茄中過表達MYB75能夠增強番茄的抗熱性,在煙草中過表達MYB75能夠增強煙草抗冷性[12],且MYB75在煙草中異源表達和番茄中過表達都能夠分別增加煙草和番茄花青苷的合成,并增強植株的非生物脅迫能力[13]。前人研究表明,在番茄中過表達MYB75能改變果實顏色,Kiferle 等在Ailsa Craig(AC)中過表達MYB75使果實顏色變為紫色;孟夏等在中蔬6 號中過表達MYB75能使果實顏色由紅色變為橙黃色,類胡蘿卜素含量顯著提高。
本文發現在AC 中過表達SlMYB75能夠改變果實顏色和大小,種皮以及幼苗下胚軸顏色也亦明顯變化,且能夠提高果實含糖量以及果實硬度等。這為進一步研究SlMYB75基因的功能奠定了基礎。
1 材料與方法
1.1 試驗材料
以AC 和AC 為背景過表達SlMYB75的轉基因番茄為實驗材料,分別培養于山東農業大學園藝試驗站、山東農業大學本部科技創新大樓植物培養室以及光照培養箱中。本研究所使用的的煙草為實驗室保存的本生煙,培養于山東農業大學本部科技創新大樓植物培養室。
本試驗所用的大腸桿菌(E.Coli)菌株為DH5α,購自北京全式金生物技術有限公司;農桿菌菌株為LBA4404,由本實驗室自行保存。本實驗所用的載體為克隆載體pEASY-Blunt,購自北京全式金生物技術有限公司;表達載體pBI121 由本實驗室自行保存。
1.2 總RNA 的提取以及實時熒光定量PCR 分析
采用TRIZOL 法來進行轉基因番茄各組織的RNA 提取,以提取的總RNA 為模板,按照北京全式金生物技術有限公司EasyScript One-Step gDNA Removal and cDNA Synthesis Super mix 試劑盒說明書進行。PCR 反應體系為:1 μL Anchored Oligo(dT)18Primer(0.5 μg/μL),10 μL 2×ES Reaction Mix,1 μLEasyScriptRT/RI Enzyme Mix,1 μL gDNA Remover,水與RNA 共7 μL。PCR 反應程序為:42 ℃15 min,85 ℃5 s;PCR 產物1%瓊脂糖凝膠電泳。熒光定量PCR 使用的儀器為BIO-RAD IQ5,所有PCR 反應都設3 次重復。PCR 反應體系為:2×Realtime PCR Super mix 10 μL,上、下游引物濃度為0.5 μmol·L-1,模板1 μL,加去離子水至20 μL。PCR 反應程序為:95 ℃預變性1 min,95 ℃15 s,60 ℃15 s,72 ℃30 s 40 個循環[14]。
1.3 轉基因番茄果實可溶性糖含量的檢測
取成熟期轉基因和非轉基因果實各30 個,用糖度計進行檢測果實含糖量并進行統計,記錄每個果實含糖量。本文所有多重比較分析方法均為LSD 單因素方差分析,P<0.05 為顯著性差異,P<0.01為極顯著性差異。
1.4 過表達載體的構建
克隆的含有BamHI 和SalI 酶切位點的SlMYB75的CDS 片段連接到pEASY 克隆載體上,連接后進行大腸桿菌DH5α的轉化、用PCR 技術進行陽性克隆菌落的篩選、加入相應抗性激素進行搖菌、之后送鉑尚公司進行序列測序、再提取質粒、用限制性內切酶BamHI 和SalI 分別酶切測序正確的克隆載體質粒和pBI121 表達載體質粒。通過瓊脂糖凝膠電泳,在紫外燈下切去膠片段,用試劑盒進行目的條帶的回收,用T4連接酶將載體與目的片段25 ℃連接并轉化大腸桿菌。進行PCR 檢測后選陽性菌點、進行質粒提取,再進行酶切驗證,根據測序結果與已知序列比對確認,然后用電擊轉化法轉入農桿菌。
1.5 亞細胞定位
選取BamHⅠ和XhoⅠ兩個限制性內切酶酶切位點,將SlMYB75基因從peasy-Blunt 載體切下,并用試劑盒進行回收,對pROKⅡ表達載體用相同的酶切位點進行酶切后回收,再用T4連接酶在25 ℃將兩者進行連接,之后轉化大腸桿菌,鑒定陽性克隆。構建pROKⅡ-SlMYB75-GFP 載體完成后通過凍融法將質粒pROKⅡ-SlMYB75-GFP 和p19 轉入農桿菌LBA4404。在進行本生煙的侵染時,我們采用農桿菌注射法。挑取陽性克隆接種到含卡那霉素的LB 液體培養基(25 mg·L-1Rif,50 mg·L-1Kan),以每分鐘220 rpm 在28 ℃振蕩培養培養箱震蕩培養12 h。之后將以上兩種農桿菌菌液在4000×g 的水平離心機中離心10 min,懸浮(懸浮緩沖液:10 mmol·L-1MgCl2,10 mmol·L-1MES,150 μmol·L-1As)。p19 的菌液與pROKⅡ-SlMYB75-GFP 菌液等體積混合成一管溶液,在分光光度計儀器中測定OD600值,并使其在在0.6~0.8 之間。室溫黑暗處靜置3 h 后用去針頭針管注射長勢較好的煙草葉片,48~96 h 內觀察結果。進行熒光觀察時,要撕取出較薄的下表皮進行觀察。GFP 經488 nm 激光激發,通過550~590 nm 濾鏡后獲得熒光信號[15]。
2 結果與分析
2.1 SlMYB75 蛋白結構域分析
為了解SlMYB75蛋白的功能結構域,利用SMART[16]工具分析,發現SlMYB75含有275 個氨基酸,包含兩個典型的SANT 結構域,構成了經典的R2R3MYB 結構[17]。且含有兩個簡單的未知功能結構域,根據以上分析結果,利用IBS.1.0 軟件繪制如圖1 所示SlMYB75結構:
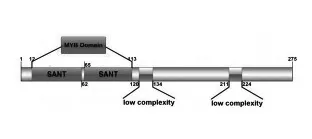
圖1 SlMYB75 蛋白結構域Fig.1 SlMYB75 protein domain
2.2 SlMYB75 的亞細胞定位
為了明確SlMYB75蛋白在細胞中的作用部位,利用農桿菌介導的瞬時轉化法,將培養好的帶有SlMYB75與GFP 融合蛋白載體的農桿菌注射到煙草葉片,培養兩天后在顯微鏡下觀察融合蛋白在煙草葉片細胞中的分布部位情況。以空載體注射煙草的結果作為對照。結果顯示:SlMYB75蛋白定位在細胞核中,說明該蛋白主要在細胞核中表達(圖2)。
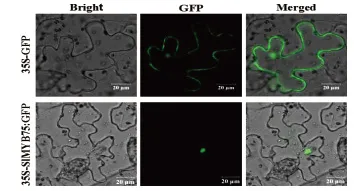
圖2 SlMYB75-GFP 在煙草葉片細胞中的定位(標尺長度=20 μm)Fig.2 Localization of SlMYB75-GFP in tobacco leaf cells(Ruler length=20 μ m)
2.3 SlMYB75 基因的遺傳轉化、過表達株系表達量檢測以及組織表達特異性分析
為了探究SlMYB75基因在番茄中的功能,我們構建了過表達載體,并在番茄中進行遺傳轉化。取野生型(wild type,WT)和轉基因植株兩個株系OE1 和OE2 的嫩葉,通過Trizol 法提取RNA,反轉錄為cDNA,再通過熒光定量檢測SlMYB75表達量。在兩個轉基因株系中,該基因表達量均顯著高于WT(圖3a);另外,為了檢測SlMYB75基因在各組織中表達情況,分別取WT 與過表達SlMYB75株系幼根、嫩莖、幼葉、花(開花當天)、綠熟期果實,通過Trizol 法提取RNA,反轉錄為cDNA,通過熒光定量檢測過表達株系中SlMYB75基因在各個組織中的表達量,發現SlMYB75基因在果實中表達量較高,在花中表達量較低(圖3b)。
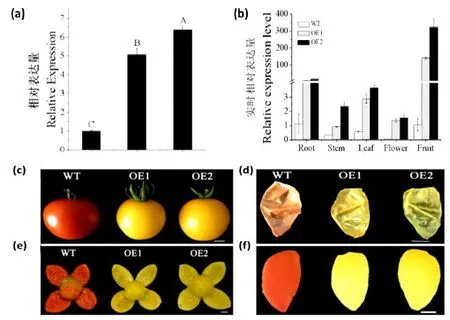
圖3a SlMYB75 在WT 和過表達株系中的表達量(P<0.01);圖3 b SlMYB75 基因的組織表達分析;圖3 c 果實整體顏色觀察;圖3 d 果實外果皮顏色觀察;圖3 e 過表達與WT 果實解剖觀察;圖3 f 果實果肉顏色觀察(標尺=1 cm)Fig.3a Expression analysis of SlMYB75 in wild type and transgenic lines (P<0.01);Fig.3 b Tissue-specific expression profiles of SlMYB75;Fig.3 c Observation of the overall fruit color;Fig.3 d Observation of fruit outer skin color;Fig.3 e Overexpression and WT fruit anatomical observation;Fig.3 f Observation of fruit pulp color(Bars=1 cm)
2.4 過表達SlMYB75 改變果實顏色
通過觀察表型發現,過表達SlMYB75株系與WT 相比,完全成熟果實顏色發生明顯變化,解剖并分離果皮、果肉,發現過表達株系果實的果皮和果肉顏色均由紅色變為橙黃色(圖3c-f)。
2.5 過表達SlMYB75 對果實重量以及含糖量影響
通過對果實重量測量統計,過表達株系完全成熟果實單果平均重量與WT 相比顯著下降(圖4a)。利用果實糖度計檢測成熟期轉基因與WT 番茄果實的含糖量,結果顯示:轉基因株系與WT 果實含糖量相比顯著上升,可溶性糖含量提高約18%,且具有顯著性差異(圖4b)。利用硬度計檢測成熟期轉基因與WT 番茄果實的硬度,結果顯示:轉基因株系與WT 果實硬度相比顯著上升。結果顯示:轉基因株系與WT 果實硬度相比顯著上升,硬度提高約42%,且具有顯著性差異(圖4c)。
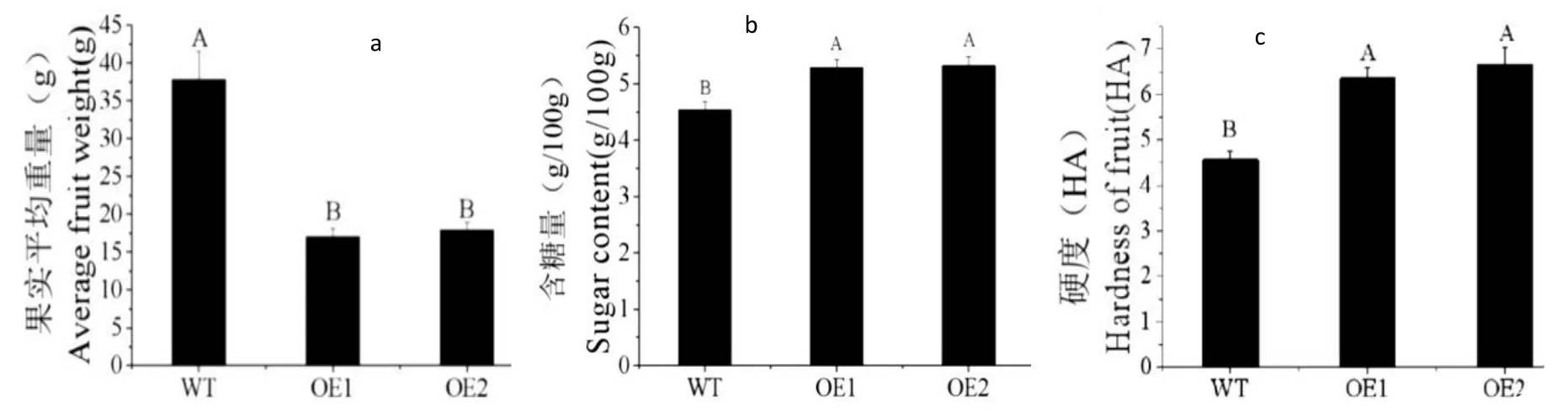
圖4(a) SlMYB75 過表達株系與WT 完全成熟果實平均重量比較(P<0.01);圖4 (b)SlMYB75 過表達株系與WT 完全成熟果實平均可溶性糖含量比較(P<0.01);圖4 (c)SlMYB75 過表達株系與WT 完全成熟果實平均硬度比較(P<0.01);Fig.4(a) Average weight comparison between SlMYB75 overexpression lines and the total mature fruit of WT(P<0.01);Fig.4 (b)Average soluble sugar content comparison between SMYB75 overexpression lines and the total mature fruit of WT(P<0.01);Fig.4 (c)Average firmness comparison between SlMYB75 overexpression strain and WT fully mature fruit(P<0.01)
2.6 過表達SlMYB75 使果實外果皮細胞變小
通過掃描電鏡觀察發現,相同發育時期(完熟期)的過表達SlMYB75株系果實外果皮細胞的平均面積與WT 相比明顯變小,通過掃描電鏡拍照、Image.J 軟件統計,表皮細胞面積顯著下降(圖5)。

圖5a WT果實外果皮細胞,標尺=100 μm;圖5 b,c SlMYB75 過表達轉基因果實外果皮細胞標尺=100 μm;圖5d 面積大小統計(P<0.01)Fig.5a:Scanning electron micrographs of wild-type fruit exocarp cells,bars=100 μm;Fig.5b-c: SlMYB75 over-expressed transgenic fruit outer rind cells,scanning electron microscope,Bars=100 μm;Fig.5d:picture shows area size statistics.(P<0.01)
2.7 過表達SlMYB75 株系種皮顏色與WT 存在明顯差異,種子千粒重沒有變化
將同時期收取的轉基因與非轉基因種子烘干后,通過觀察發現,過表達株系種皮顏色明顯深于WT 種皮。為了檢測種子千粒重是否發生變化,隨機挑選OE1、OE2 和WT 種子進行測重,結果顯示:過表達SlMYB75并沒有使種子千粒重發生改變(圖6)。
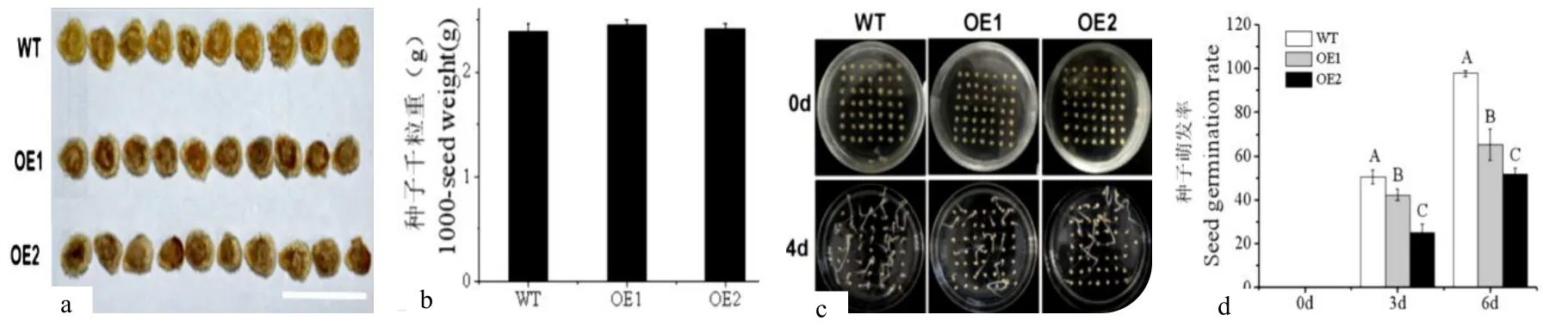
圖6a 轉基因與非轉基因種子的顏色比較。標尺=1 cm;圖6 b 轉基因與非轉基因烘干后的種子千粒重量化圖;圖6 c,d 轉基因與WT 種子萌發率統計(P<0.01)Fig.6a:Color comparison between transgenic and non-transgenic seeds.(Bar=1 cm);Fig.6 b:Thousand seed weight after transgenic and non-transgenic drying;Fig.6 c,d:Germination rate statistics of transgenic and wild-type seeds(P<0.01).
2.8 過表達SlMYB75 株系種子萌發率降低
為了檢測過表達株系種子萌發能力,取WT、OE1 與OE2 三個株系的種子,分別用75%酒精和4%次氯酸鈉徹底消毒后,均勻播種于MS 固體培養基表面,放置于恒溫培養箱(28 ℃)進行暗培養,每天觀察拍照并統計種子萌發情況,統計結果如圖6c,d,圖6(c)為0~4 d 種子萌發情況,圖6(d)為萌發率量化統計。結果顯示:過表達株系種子萌發率顯著低于WT,第6 d 時,WT 種子基本完全萌發,但轉基因兩個株系種子萌發率不超過70%,因此,過表達SlMYB75使種子萌發率顯著下降。
2.9 過表達SlMYB75 株系幼苗下胚軸紫色消失
轉基因與WT 幼苗下胚軸顏色有明顯差異,WT 子葉下胚軸呈現紫色,而過表達轉基因株系下胚軸沒有紫色物質積累,紫色物質應是花青素,說明過表達SlMYB75抑制了花青素的合成或積累(圖7)。
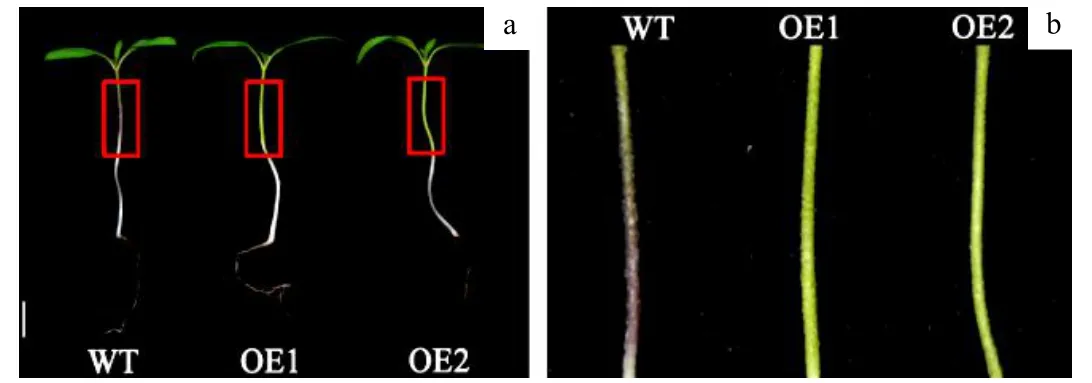
圖7 轉基因與WT 株系子葉下胚軸對比Fig.7 Comparison of cotyledon hypocotyls between transgenic and WT strains
3 討論
MYB 作為植物轉錄因子中最大家族之一,主要參與調控植物激素的應答[18]、植物的非生物脅迫響應[19]、調控植物的形態建成[20]、調控植物次生代謝反應[21,22]等過程。本文通過組織表達特異性分析發現,SlMYB75基因在WT 番茄的根、葉和果實中表達量較高,在根和果實中最高;檢測過表達株系各組織中SlMYB75的表達量,發現轉基因株系植株的根、葉和果實表達量升高較顯著,其中果實中表達量最高。另外,結合表達量(圖3)與種子萌發率(圖6c,d)發現,基因表達量越高種子萌發率越低。這說明SlMYB75基因可能在番茄種子萌發以及幼苗和果實的生長發育中起著重要的調控作用。
類黃酮物質的合成是由一系列轉錄因子包括MYB、bHLH和WD重復蛋白組成的三重復合物共同調節的[23]。目前,已有擬南芥AtMYB75/PAP1的研究報道,擬南芥中PAP1能夠促進愈傷組織中花青苷的合成。在擬南芥中通過RNAi的方法沉默PAP1基因導致幼苗中花青苷的積累減少,另外,沉默PAP1基因的同源基因PAP2,MYB113和MYB114也會降低花青素的合成[24]。在啤酒花中異源表達AtPAP1/MYB75會顯著增加啤酒花幼葉和花中花青素的積累[25]。研究表明,在番茄(AC)中過表達擬南芥At/PAP1/MYB75同源基因SlMYB75,會導致番茄花和果實等器官中花青素的積累,果實顏色由紅色變為紫色[26]。孟夏等在中蔬六號中過表達SlMYB75使果實顏色由紅色變為黃色,且花雄蕊中花青素積累增多。在本文中,在AC過表達SlMYB75使果實顏色由紅色變為黃色,且幼苗子葉下胚軸中花青素積累減少(圖7),該表型與之前研究不同。因此,SlMYB75基因在番茄中的功能有待進一步研究。
番茄果實內可溶性葡萄糖和果糖的合成是在果實的發育和成熟過程中進行的,蔗糖濃度在開花后會不斷下降,在果實成熟期由于轉化酶的作用使其持續保持較低水平[28,29,30]。我們利用糖度計檢測成熟期轉基因與WT 果實含糖量,結果顯示(圖4b),WT 番茄含糖量在4.53 g/100 g 鮮重,過表達SlMYB75轉基因株系果實可溶性糖含量在5.31 g/100 g 鮮重,兩者之間存在顯著性差異。這說明過表達SlMYB75能夠提高成熟番茄果實可溶性糖含量。通過種子萌發實驗發現過表達SlMYB75株系種皮顏色變深(圖6a),幼苗期子葉下胚軸與WT 相比紫色物質積累消失(圖7),且種子萌發率降低(圖6c,d)。這說明SlMYB75能夠影響番茄種子和幼苗的發育。但是SlMYB75基因影響番茄果實含糖量以及對種子和幼苗發育的機理尚不清楚需進一步研究。
4 結論
番茄SlMYB75編碼275 個氨基酸,該蛋白定位在細胞核中。過表達番茄SlMYB75能夠改變成熟番茄果實顏色和大小,果實含糖量顯著升高。種皮顏色加深,種子萌發率下降,且幼苗下胚軸顏色消失。這說明番茄SlMYB75基因能夠在番茄種子、幼苗和果實中發揮作用。

