播娘蒿對雙氟磺草胺的抗性水平及靶標抗性分子機理
孫鵬雷,王恒智,劉偉堂,趙 寧,王 豪,朱寶林,王金信
(1.山東農業大學植物保護學院,山東泰安 271018;2.山東省農藥毒理與應用技術重點實驗室,山東泰安 271018)
播娘蒿(DescurainiasophiaL.)為十字花科播娘蒿屬一年或越年生闊葉雜草,是我國黃淮海區域麥田主要惡性雜草之一[1-2]。雙氟磺草胺(florasulam) 是一種三唑并嘧啶磺酰胺類(triazolopyrimidine sulfonanilides,TP)內吸傳導型除草劑,由美國陶氏農業科學公司開發,具有低毒高效、在低溫下穩定、殺草徹底及對人畜等高等動物安全等特點,是繼苯磺隆之后,我國麥田廣泛應用于闊葉雜草防治的另一重要乙酰乳酸合成酶(acetolactate synthase,ALS,EC2.2.1.6)抑制劑類除草劑品種[3]。近年來,由于該除草劑持續大量使用,其在黃淮海區域麥田對播娘蒿的防治效果逐年下降,部分地區麥田播娘蒿對雙氟磺草胺已經表現出明顯的抗性。
ALS能夠高效地催化植物體內的部分生物反應,參與多種氨基酸的合成過程,對植物的正常生長具有重要作用[4-5]。以ALS 為靶標的除草劑主要有5種類型:咪唑啉酮(imidazolinones,IMI)、磺酰脲類(sulfonylureas,SU)、三唑并嘧啶類(triazolopyrimidines,TP)、嘧啶硫代苯甲酸酯類(pyrimidinylthiobenzoates,PTB)和磺酰胺羰基三唑啉酮類(sulfonylaminocarbonyl-triazoli-nones,SCT)[6]。由于ALS 抑制劑類除草劑作用位點單一,雜草易對其產生抗藥性。據統計,從20世紀50年代至今,在全球已報道的512種抗性雜草生物型中,對ALS抑制劑類除草劑產生抗性的雜草生物型已有165種[7]。研究發現,植物體內ALS基因突變,是其對ALS抑制劑類除草劑的敏感性降低的重要原因[8]。此外,近年來非靶標(代謝)抗性機理導致的雜草對ALS抑制劑類除草劑的抗藥性現象在多種雜草中被頻繁報道[9-10]。
自1992年首次報道毒萵苣(LactucaserriolaL.) 和地膚(KochiascopariaL.)因ALS 第197位氨基酸突變引起對磺酰脲類除草劑氯磺隆產生抗性以來,ALS 基因測序分析在雜草對ALS 抑制劑類除草劑的抗性機理研究中被廣泛應用。據統計,目前被證實可以導致雜草產生抗性的ALS氨基酸序列位點共報道了8個:第122、197、205、376、377、574、653和第654位點,氨基酸取代形式已有29種[11]。Cui等[12]和Deng等[13-14]分別發現播娘蒿在ALS基因發生突變會導致其對SU、IMI、PTB、TP、SCT類藥劑產生不同程度的抗性;Yang等[10]發現,馬拉硫磷對抗苯磺隆播娘蒿存在逆轉作用,證實馬拉硫磷可以抑制磺酰脲類除草劑的代謝,從而逆轉基于代謝的抗性。與靶標抗性相比,非靶標抗性更復雜且不可預測。目前,在播娘蒿對ALS抑制劑類除草劑的抗性研究中,對苯磺隆的抗性研究居多[15-17],但是,目前尚未見有關黃淮海區域麥田播娘蒿對雙氟磺草胺抗性的報道。
本研究采用整株-劑量響應法測定山東省泰安市多年用雙氟磺草胺和未用除草劑小麥田播娘蒿種群對雙氟磺草胺的抗性水平,比較兩個播娘蒿種群對雙氟磺草胺的敏感性,并分析其ALS基因序列差異,以探究播娘蒿對雙氟磺草胺產生抗性的分子機理,為播娘蒿的科學防治及延緩抗藥性產生提供科學依據。
1 材料與方法
1.1 供試材料
播娘蒿種子:種群G130于2018年采自中國山東省泰安市泰山區小麥田(N36.19°, E117.17°),該田塊自2013年以來長期使用雙氟磺草胺;種群TS采自山東泰山(N36.05°, E117.01°),從未使用過任何除草劑。
除草劑:50 g·L-1雙氟磺草胺懸浮劑,山東勝邦綠野化學有限公司生產; 97%雙氟磺草胺原藥,山東濱農科技有限公司生產。
1.2 試驗方法
1.2.1 播娘蒿對雙氟磺草胺的抗性水平測定
采用整株-劑量響應法[18]測定。選取飽滿的播娘蒿種子,以30% H2O2浸泡30 min,用清水沖洗干凈后,在50 ℃溫水中浸泡40~60 min,將處理好的種子放于9 cm的含濾紙培養皿中,加入 0.05% GA3置于光照培養箱(光/暗時間 14 h/10 h;溫度25 ℃/20 ℃)中浸泡12~24 h,用清水沖洗干凈;保持濕潤繼續培養至種子露白;挑選長勢良好的15粒種子種植在直徑15 cm的一次性塑料盆缽中,均勻覆土,放置在溫度為 20~25 ℃、相對濕度為50%~75%的自然光照可控溫室中進行常規培養。2~3葉期時,間苗至10株。于4~5葉期進行莖葉雙氟磺草胺噴霧處理(ASS-4 型定量噴霧塔,噴液量450 L·hm-2,噴霧壓力275 kPa)。不同種群雙氟磺草胺處理劑量(有效成分)不同,其中TS種群劑量分別為0、0.006、0.03、 0.15、0.75、3.75、18.75 g·hm-2;G130種群劑量分別為0、 0.15、0.75、 3.75、18.75、93.75、468.75 g·hm-2。每處理設置3個重復,整體試驗重復2次。藥劑處理后 21 d,剪取播娘蒿地上部分莖葉置于牛皮紙袋中,在75 ℃恒溫干燥箱中烘72 h后,稱干重。
1.2.2 播娘蒿種群ALS基因檢測
根據1.2.1方法分別催芽、種植兩個種群播娘蒿,待播娘蒿長至4~6葉期后,剪取單株播娘蒿的幼嫩葉片,進行液氮處理后,-80 ℃保存備用。播娘蒿DNA采用CTAB法[19]提取。PCR擴增參照許 賢等[20]的方法,ALS基因序列擴增引物為5′-CGCTCCTCTCCTGAAGCTCACCA-3′(F)和5′-CAAACAAACAGCAGTAGC GTC TGAAG-3′(R),目標長度2 100 bp。反應體系共25 μL:18.25 μL dd H2O,2.5 μL10 × Easy Taq Buffer,1 μL d NTPs,正、反向引物各1 μL(10 μmol·L-1),1 μL模板,0.25 μL Easy Taq DNA Polymerase。PCR 反應條件:94 ℃預變性3 min;94 ℃變性30 s,59 ℃退火30 s,72 ℃延伸 1.5 min,共34個循環;72 ℃終延伸10 min,4 ℃保存。擴增序列覆蓋全部被報道過的8個ALS區域突變位點。
PCR 擴增結束后,將擴增產物用1%瓊脂糖凝膠電泳檢測。使用EasyPure Quick Gel Extraction Kit 對陽性目的條帶進行回收,使用pEASY-T1 Simple Cloning Kit 對膠回收產物進行連接反應,轉化培養。將培養好的菌液進行陽性克隆鑒定并送生工生物工程(上海)有限公司測序,采用DNAMAN v 6 軟件對測序結果進行分析。
1.2.3 離體ALS對雙氟磺草胺敏感性測定
播娘蒿催芽方法依照1.2.1,露白后種植在50孔育苗盤中。待播娘蒿長至4~6葉期時,分別剪取兩個種群播娘蒿葉片,迅速置于液氮中處理,-80 ℃保存備用。播娘蒿ALS提取及活性測定參照Han等[21]和Yu等[22]的方法,并稍加改動。ALS離體活性測定所用雙氟磺草胺濃度通過預試驗結果制定,設定敏感種群雙氟磺草胺濃度分別為0、0.000 256、0.001 28、0.006 4、 0.032、0.16、0.08和4 μM;抗性種群濃度分別為0、0.001、0.01、 0.1、1、10、100和1 000 μM,暗反應時間設為45 min,試驗結束后,用Spectra Max M2 新多功能酶標儀在530 nm下測定其吸光度值。試驗設置3個重復,整體試驗重復2次。
1.3 數據處理
采用SPSS 25.0軟件的ANOVA 方法進行差異顯著性分析。通過SigmaPlot 12.5軟件的雙邏輯非線性回歸方程y=C+{(D-C)/[1+(x/GR50)b]}計算干重抑制中量GR50。式中,C表示劑量反應下限;D表示劑量反應上限;x表示除草劑用量;b表示曲線斜率;GR50表示植株干重減少50%所需除草劑劑量;y表示在某一除草劑劑量下干重占空白對照比值。計算其抗藥性指數(RI),即抗性種群(G130)的GR50與敏感種群(TS)的GR50的比值,分析其抗藥性指數(RI)(高水平抗性RI>10)[23]。以I50替換回歸方程中的GR50計算抑制播娘蒿ALS酶活性50%所需除草劑濃度。
2 結果與分析
2.1 播娘蒿對雙氟磺草胺的抗性水平
抗性水平測定結果(表1)顯示,雙氟磺草胺對敏感種群TS 的GR50值為0.10 g·hm-2,對抗性種群G130的GR50達10.86 g·hm-2,與敏感種群TS相比,播娘蒿種群G130對雙氟磺草胺已產生高水平抗藥性,抗藥性指數為108.6。

表1 播娘蒿對雙氟磺草胺的抗性水平
2.2 抗性、敏感播娘蒿種群ALS基因差異
將兩個播娘蒿種群的ALS測序結果與NCBI上登記的擬南芥ALS基因序列(X51514)在線BLAST,有90%以上的同源性,確定所擴增序列為目的序列。用DNAMAN 6.0.3軟件將所測不同種群播娘蒿核苷酸序列翻譯后進行氨基酸比對分析,在G130種群中,發現了兩種突變:第197位脯氨酸突變為蘇氨酸,第574位色氨酸突變為亮氨酸(圖1),有些單株中同時存在著197蘇氨酸和574亮氨酸突變。為明確在G130種群中各突變形式的發生頻率,本研究隨機挑選100株該種群植株進行了基因組DNA提取、PCR擴增、鏈接轉化和菌液測序。結果表明,在G130種群中三種突變形式及突變頻率如圖2所示,其中33%的植株存在197蘇氨酸突變,40%的植株存在574亮氨酸突變,27%植株同時存在兩種突變。該兩種突變形式已被證實可以導致雜草對ALS抑制劑類除草劑產生抗性[14]。隨著雙氟磺草胺選擇壓的持續增加,對雜草產生抗性有貢獻的突變比例會不斷升高,雜草防治工作將更加困難。
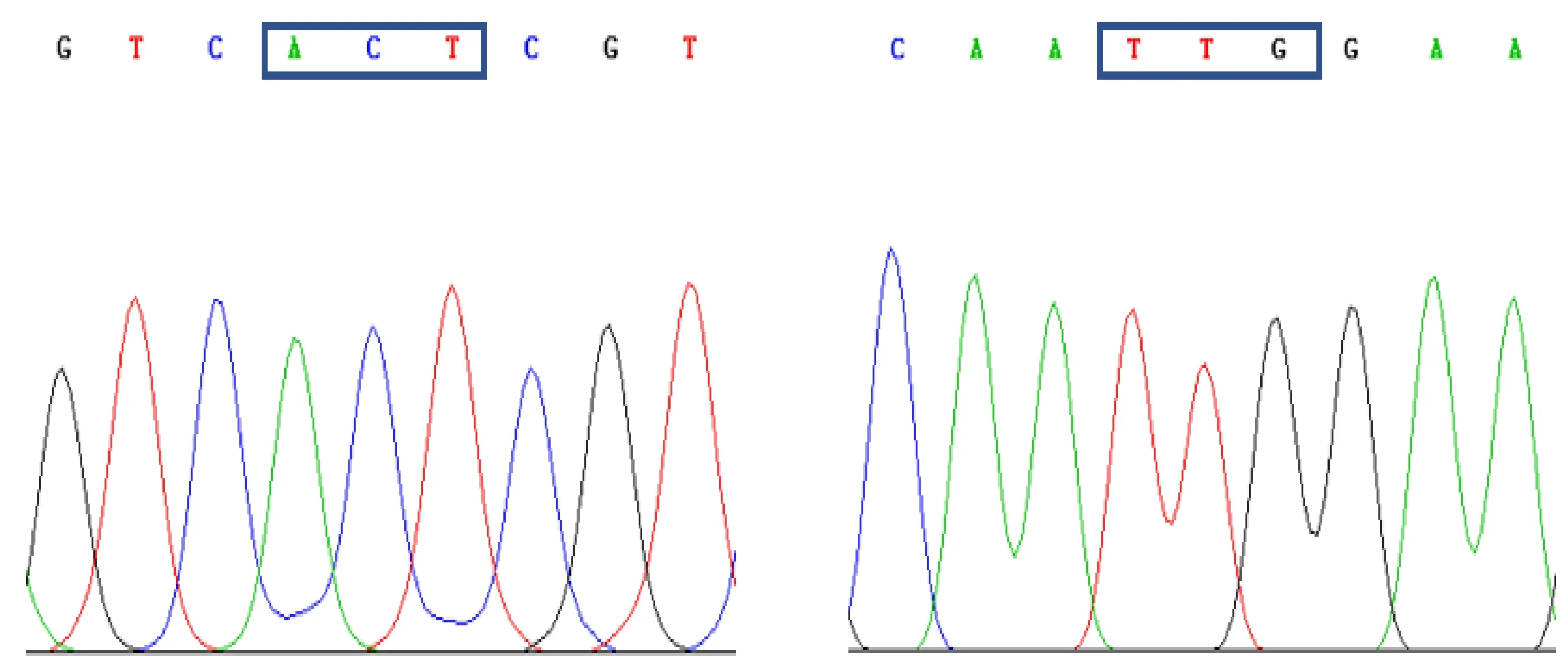
圖1 播娘蒿抗性種群G130的ALS基因突變形式
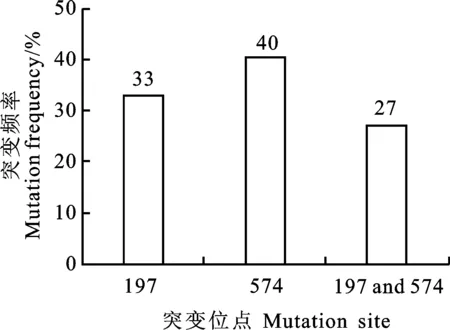
圖2 抗性播娘蒿突變位點及突變頻率
2.3 ALS離體活性測定
靶標酶ALS離體活性測定結果表明,G130種群的ALS總催化活性為16.52 nmol·mg-1·min-1,敏感種群TS總催化活性為14.60 nmol·mg-1·min-1。當雙氟磺草胺濃度達到1 μM時,抗性種群ALS活性未受明顯抑制,而敏感種群在雙氟磺草胺濃度為 0.8 μM時ALS活性抑制率已近80%。抗性種群G130的I50為 3.584 μM,為敏感種群的137.8倍(表3)
3 討 論
自雙氟磺草胺2001年進入中國市場(以普瑞麥Prumus在我國獲得臨時登記)一度被作為苯磺隆的替代藥劑[24],近年來被廣泛使用于冬小麥田防除闊葉雜草。張朝賢等[25]發現,ALS 抑制劑類除草劑連續重復使用3~5年以上,極易導致雜草對該類除草劑產生抗性。雙氟磺草胺作為典型的ALS抑制劑類除草劑,雜草對該藥劑產生抗性足以預見。2014年,馬鵬生[26]報道了河南省豬秧秧對雙氟磺草胺產生抗性;2018年,Bai等[27]在抗苯磺隆的牛繁縷種群中發現對雙氟磺草胺也產生交互抗性。本研究中,G130種群采自連續7年使用雙氟磺草胺的麥田,該種群對雙氟磺草胺產生了高水平抗性(108.6倍)。
雜草對ALS抑制劑類除草劑抗性的產生主要是由于靶標酶ALS對藥劑的敏感性下降造成的。本研究發現,敏感播娘蒿種群(TS)對雙氟磺草胺非常敏感,ALS活性受雙氟磺草胺抑制較強,增加雙氟磺草胺濃度后,ALS活性迅速下降;而抗性播娘蒿種群(G130)ALS對雙氟磺草胺的敏感性顯著降低,增加雙氟磺草胺濃度,ALS活性下降緩慢,其I50為敏感種群的137.8倍,說明播娘蒿靶標酶ALS對雙氟磺草胺敏感性降低是其產生抗性的主要原因之一,推測I50值較高是因為該種群存在多種突變。本研究結果與反枝莧對煙嘧磺隆抗性[28]及播娘蒿[29]、薺菜[30]、麥家公[31]等對苯磺隆抗性結果一致。

表2 雙氟磺草胺對播娘蒿乙酰乳酸合成酶的抑制活性差異
雜草ALS空間構象因其保守區關鍵位點氨基酸被代替而發生變化,導致除草劑無法正常結合靶標位點,從而使雜草對除草劑敏感性下降,這是雜草對ALS抑制劑類除草劑產生抗性的分子機理之一。目前,已證實ALS 序列中8個氨基酸被取代后會導致雜草對ALS 抑制劑類除草劑產生不同水平的抗性。本研究在對播娘蒿抗性種群(G130)和敏感種群(TS) ALS 基因的測序后,對比發現G130種群植株存在ALS 區域197位點和574位點氨基酸序列的改變。其中197位點發生了脯氨酸突變為蘇氨酸,574位點色氨酸突變為亮氨酸。推測抗性種群(G130)ALS基因兩種突變是導致播娘蒿對雙氟磺草胺產生抗性的重要原因之一。
崔海蘭[32]發現,抗苯磺隆播娘蒿ALS 第197位脯氨酸突變為亮氨酸后,對IMI類、PTB類、TP類藥劑產生交互抗性。Deng等[14]報道,抗苯磺隆播娘蒿ALS 第197位脯氨酸突變為蘇氨酸或第574位色氨酸突變為亮氨酸時,對TP類除草劑均產生交互抗性。至于抗性種群G130產生兩種突變方式是否由雙氟磺草胺應用導致的結果,尚無法確定。從以上報道的結果看,苯磺隆抗性播娘蒿種群同時對TP類藥劑產生交互抗性,小麥田苯磺隆應用歷史較長,苯磺隆導致的播娘蒿抗性種群也可能對雙氟磺草胺產生抗性。播娘蒿抗性種群(G130)與苯磺隆等ALS抑制劑是否存在交互抗性,還有待于進一步研究。
對100株抗性種群植株測序發現,197位點突變占33%,574位點突變占40%,同時發生兩種突變占27%。Deng等[14]分別對197位點、574位點單一突變的植株噴施TP類藥劑發現,在574位點發生單一突變的植株較在197位點發生單一突變的植株存活率高。本研究所測突變類型中以574Leu突變比例最高,這與前人報道一致。推測不同抗性突變的檢出頻率可能與雜草物種、除草劑應用歷史以及抗性雜草的適合度有關[33]。雜草抗藥性的產生也與植株對除草劑的吸收、轉運、代謝和隔離等非靶標抗性機理相關,該種群是否存在非靶標抗性仍待進一步研究。
綜上所述,本研究表明,播娘蒿種群G130對雙氟磺草胺產生了高水平抗性,靶標酶基因突變導致ALS 對雙氟磺草胺的敏感性下降是G130產生抗性的重要原因之一。為避免或延緩抗藥性的發生發展,建議避免連續使用同一作用機理藥劑,將不同作用機理藥劑科學混用、輪用,做到合理施藥;結合農業措施、物理措施等進行綜合治理,以延緩抗藥性的發生。

