高考中熱點電化學試題分析與評價
徐俊龍

筆者分析近幾年全國各地高考試題與高考模擬題,對電化學這部分的熱門考點進行相關整理,從必備知識、關鍵能力、思維方法、核心素養等角度闡述命題規律,供各位同學在今后的高考備考參考。
一、原電池裝置的考查變遷
對于原電池的認識,從必修二中簡單的原電池,到選修四化學反應原理中的帶鹽橋的原電池,以及后續高中出現帶隔膜的原電池,均是化學核心素養中的證據推理與模型認知、科學探究與創新意識的具體應用,也是學生思維螺旋式上升的具體體現。高考試題對這些方面也進行了細致考查,下面通過具體實例來說明。
【例1】[2013年廣東卷,33題(2)節選]設計兩種類型的原電池,探究其能量轉化效率。限選材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq),銅片,鐵片,鋅片和導線。
(2)①完成原電池甲的裝置示意圖(補充完整圖1),并作相應標注。
要求:在同一燒杯中,電極與溶液含相同的金屬元素。
②銅片為電極之一,CuSO4(aq)為電解質溶液,只在一個燒杯中組裝原電池乙,工作一段時間后,可觀察到負極_____________________。
③甲、乙兩種原電池中可更有效地將化學能轉化為電能的是________,其原因是_______________________________。
【分析與解答】①根據題給信息,找出金屬活動性的差異,將不同的金屬片置于燒杯中,注入含對應陽離子的溶液,組裝好裝置,并標清楚電極、溶液、導線,可以繪出三種合理的組合(由物理知識可知金屬活動性差異越大,電勢差越大),當年高考時有些同學沒有畫出溶液或電極與導線相連的示意圖,或沒有標注電極或標清楚溶液等導致扣分。具體參考答案見圖2所示:
②乙池的示意圖見圖3所示,此時負極的現象:既有電化學腐蝕的現象(溶解),也有直接接觸的化學腐蝕,產生銅附著在鋅的表面。本問與下面③問是一脈相承,具體規范答案是兩個方面來回答:A. 電極逐漸溶解;B. 有紅色固體析出。
③在原電池甲(圖2)中,負極不與CuSO4溶液直接接觸,所發生的化學反應只有原電池反應,而在原電池乙(圖3)中,負極Zn與CuSO4溶液直接接觸,所發生的化學反應除原電池反應以外,還有非原電池反應,產生熱量損失,因此,在原電池甲和乙中,甲可更有效地將化學能轉化為電能。本問的答案為:裝置甲;電池乙的負極可與CuSO4溶液直接發生反應,導致部分化學能轉化為熱能;電池甲的負極不與所接觸的電解質溶液反應,化學能在轉化為電能時損耗較小。
【評注】帶鹽橋的原電池中考查鹽橋的作用,在高考范疇中首次全面考查就是2013年廣東卷的這道題,幾乎所有教輔資料均有轉載,而②問的答案絕大多數教輔資料上是以訛傳訛,只給第一條,沒有答化學腐蝕直接反應生成紅色固體的現象。關于鹽橋的作用,在中學階段不妨從以下三點來理解(嚴格講鹽橋還有消除液接電勢的重要作用,但超出課程標準要求):(1)構成閉合回路,形成原電池;(2)避免電極與電解質溶液直接反應,有利于最大程度地將化學能轉化為電能;(3)鹽橋中的陰、陽離子定向遷移,使溶液保持電中性,反應持續進行,能長時間穩定放電。回顧自2004年實施新課標以來的新高考(2007年起)試題中,帶鹽橋的裝置已經多次考查。例如:2020年全國I卷第27題(2)考到電池裝置中鹽橋中的電解質溶液的選擇問題,強調鹽橋中陰、陽離子不與溶液中的物質發生化學反應,并且給出信息,離子的電遷移率(u∞)應盡可能地相近。再如:廣東卷2008年第5題考了帶鹽橋原電池的細節問題,只是該題并未給出裝置圖,同學們可以自己腦補一下。此外,2007年海南卷第14題是新課標(2003年版)高考中具有里程碑意義的首次考帶鹽橋的高考題。此后,考查情境不斷翻新和升級,圖4列舉了幾道經典的帶隔膜的原電池裝置:2014年福建卷第11題考帶隔膜的,當年得分率極低,2015年全國I卷第11題考微生物燃料電池是帶隔膜裝置,2015年天津卷第4題考帶隔膜裝置等等……這些都是帶鹽橋的裝置的進一步的創新。在電解原理應用中,帶隔膜的裝置也普遍出現,值得大家研究和厘清相關問題。
二、常考的各種新型化學電源考查方式
眾所周知,現代生活與各種電源息息相關,例如手機等移動設備中的電池等。近幾年高考中電化學題型多以新型化學電源為背景,而這些電池大多取材于真實的文獻素材,經過加工處理編制成試題呈現在大家面前。面對新穎奇特的電池相關試題,該如何快速得出答案,這成為每位考生必須直面的問題。梳理一下,不難發現有規律可循,具體實例如下:
【例題2】(2020年全國III卷,12題)一種高性能的堿性硼化釩(VB2)-空氣電池如圖5所示,其中在VB2電極發生反應:VB2+16OH--11e- = VO■+2B(OH)-4+4H2O該電池工作時,下列說法錯誤的是
A.負載通過0.04 mol電子時,有0.224 L(標準狀況)O2參與反應
B.正極區溶液的pH降低、負極區溶液的pH升高
C.電池總反應為4VB2+11O2+20 OH-+6H2O = 8B(OH)-4+4VO■
D.電流由復合碳電極經負載、VB2電極、KOH溶液回到復合碳電極
【分析與解答】關于硼化釩的堿性燃料電池幾年前就見報道,并出現在各類高考模擬題,本題素材是真實的學術背景,題給裝置圖和負極反應,結合所學知識,不難解決:當負極通過0.04mol電子時,根據電子守恒可知,正極也通過0.04 mol電子,可判斷本題裝置中用的是陰離子交換膜,根據正極的電極方程式:O2+4e-+2H2O= 4OH-可知,通過0.04 mol電子消耗0.01 mol O2,而0.01 mol O2在標準狀況下體積為0.224 L,A正確;放電過程中,根據兩極電極反應式可知:正極生成大量的OH-會使正極區pH升高,正極產生的OH-會通過陰離子交換膜遷移到負極,負極消耗OH-使負極區OH-濃度減小pH降低,B錯誤;寫出正極電極反應式和負極電極反應相加,使電子守恒,即可得出電池的總反應為:4VB2+11O2+20 OH-+6H2O = 8B(OH)-4+4VO■,C正確;電池放電時,外電路中,電子由負極(VB2電極)經導線和負載流向正極(復合碳電極),電子沒有流經溶液!電流方向是正電荷的流向,外電路中電流方向與電子流向相反,內電路中(溶液中陽離子移向正極)電流由負極流向正極,故電流流向為復合碳電極→負載→VB2電極→KOH溶液→復合碳電極,D正確。
【例題4】(2014年北京卷,28題)用FeCl3酸性溶液脫除H2S后的廢液,通過控制電壓電解得以再生。某同學使用石墨電極,在不同電壓(x)下電解pH=1的0.1 mol·L-1的FeCl2溶液,研究廢液再生機理。記錄如下(a、b、c代表電壓數值):
(1)用KSCN檢驗出Fe3+ 的現象是____________________。
(2)I中,Fe3+ 產生的原因可能是Cl-在陽極放電,生成的Cl2將Fe2+ 氧化。寫出有關反應:________________________
___________________________。
(3)由II推測,Fe3+ 產生的原因還可能是Fe2+在陽極放電,原因是Fe2+具有_________性。
(4)II中雖未檢驗出Cl2,但Cl- 在陽極是否放電仍需進一步驗證。電解pH=1的NaCl溶液做對照實驗,記錄如下:
①NaCl的濃度是_________ mol·L-1。
②IV中檢測Cl2的實驗方法_________________________
___________________________。
③與II對比,得出的結論(寫出兩點):______________
___________________________。
【分析與解答】本題背景是真實工業情境的應用,在2013年福建卷第23題和2013年天津卷第9題均有考查,曾引起廣泛討論。2014年北京卷就是在此背景下,通過具體真實實驗來設問。(1)用KSCN檢驗出Fe3+的現象是溶液變紅,學生多數能答對,個別答成紅色沉淀而不得分;(2)根據表格中I描述的現象可知,陽極產生了Cl2和Fe3+,一種普遍的觀點認為陰離子在陽極放電,故先生成氯氣,氯氣再氧化Fe2+,具體涉及到的反應為:2Cl--2e-=Cl2↑和Cl2+2Fe2+=2Fe3++2Cl-;(3)II和I對比,電壓降低了,無Cl2產生,則有的觀點認為是Fe2+的還原性比Cl-強,因此Fe2+先放電;(4)采用控制單一變量法進行實驗:陽離子換成無還原性的Na+,陰離子Cl-的濃度保持不變,故①NaCl的濃度應該選用0.2 mol·L-1;②檢驗氯氣,可以利用其氧化性,注意氯氣在溶液中有一定的溶解度,故具體應該為:取少量陽極附近的溶液,滴在淀粉碘化鉀試紙上,試紙變藍;③因為在電壓為a時有Cl2和Fe3+ 產生,在電壓為b時無Cl2有Fe3+ 產生,電壓小于b兩者均無,現在控制單一變量,氯離子濃度相同,無Fe2+ 存在,在電壓a和b之間再引入一個中間量的電壓c,得出IV和V的結論,因此說明:A. 通過控制電壓,證實了產生Fe3+ 的兩種原因都成立;B. 通過控制電壓,證實了產生Fe2+先于Cl-放電。
【評注】電解的相關考查中,學生最大困惑就是電極放電順序問題,導致電極反應式書寫出錯。一些教輔資料過多總結,例如認為:“陰離子在陽極放電,陽離子在陰極放電”,這在很多同學腦海里根深蒂固,認為這是一成不變的!本題從實際出發設計巧妙,考查學生的宏觀辨識與微觀探析、證據推理與模型認知、科學探究與創新意識等化學核心素養。讓他們認識到電極放電的影響因素其實很多,例如電壓、粒子濃度、電極材料、電極距離和面積等因素有很大關系。其實高考考查陽離子在陽極放電也有很多,例如2014年全國II卷第27題(3)考查:Pb2++2H2O-2e-=PbO2+4H+;最高價含氧酸根也有可能放電:例如2009年江蘇卷第16題(4)考查: 2SO■-2e-=S2O■等;此外電解池中并不一定是非自發的反應才用電解,若是自發反應,采用電解則速率更快,例如2012年上海卷第14題考查:Zn+2H+=Zn2++H2↑,給出一個不完整的圖,考查應該如何設計的問題,值得各位同學認真思考。
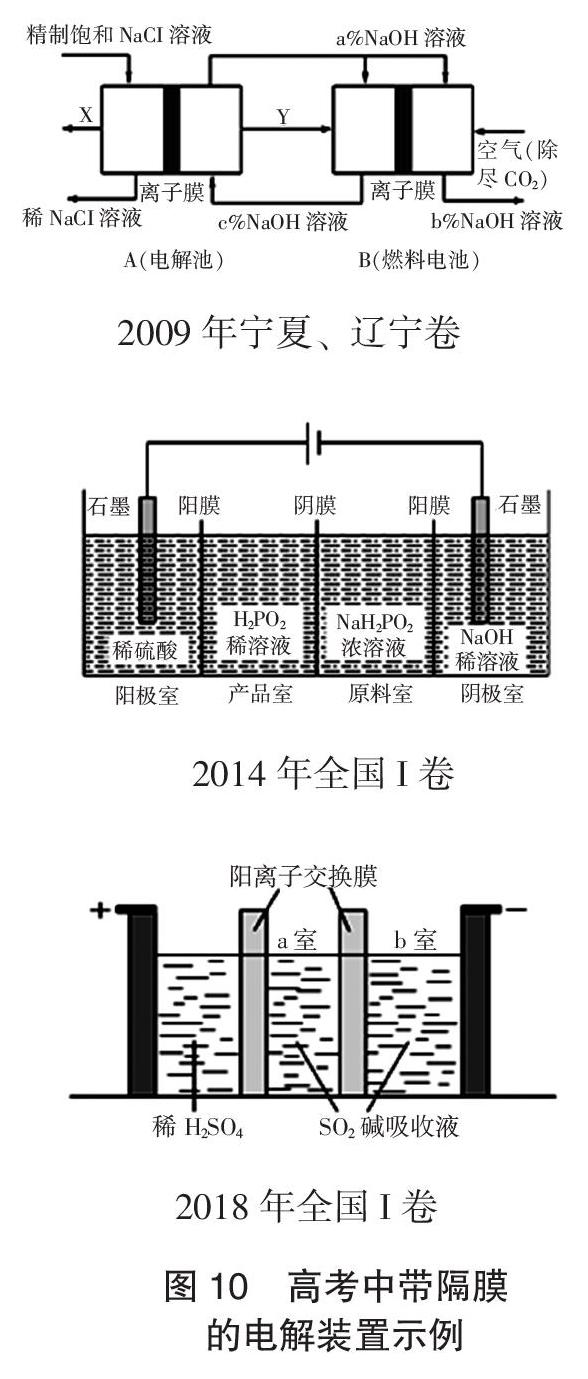
此外,各種帶隔膜的電解裝置的考查也是不少老師進行的重點專題復習,值得仔細研究。圖10列出幾道高考題的裝置圖,請大家找到對應高考題自己仔細研究:2009年寧夏、遼寧卷第27題(3),2014年全國I卷第27題(4),2018年全國I卷第27題(3),去深刻領會命題人的命題立意,觸類旁通,在今后就能夠創造性的解決各種新問題。
電解的有關計算,需要看清楚是并聯電路還是串聯電路,看清楚電解前溶液中是否發生了反應,例如離子反應生成沉淀或氣體等,電解過程中是否存在后續反應,例如先生成什么,后生成什么等等。另外還可能考查法拉第電解定律及法拉第常數,法拉第常數F=9.65×l04C·mol-1,這個在2010年新課標全國卷第35題(4)(湖南省用的化學與生活選考題中),2012年海南卷第16題(3)、2013年全國卷I第28(5)、2015年全國II卷第26(2)均考查有關法拉第常數計算的應用。
四、金屬的腐蝕及防護在高考中的考查方式
金屬的腐蝕問題是世界性的難題,防護就顯得尤為重要,課本上介紹的一些腐蝕和防護的原理在實際生產和生活中息息相關,對化學核心素養中除了上述的幾個維度外,專門對科學態度與社會責任這個維度進行了很好的闡述和考查。平時同學們對課本不夠重視,因此考到實際問題學生容易出錯,下面具體看高考題。
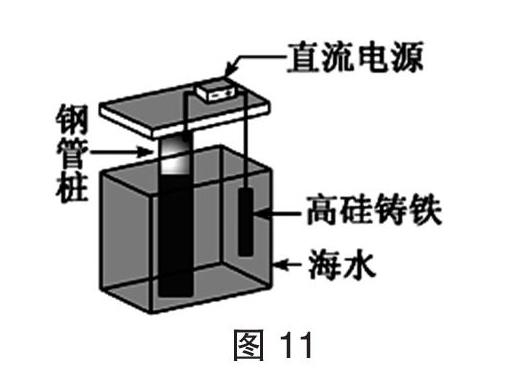
【例題5】(2017年全國I卷,11題)支撐海港碼頭基礎的鋼管樁,常用外加電流的陰極保護法進行防腐,工作原理如圖11所示,其中高硅鑄鐵為惰性輔助陽極。下列有關表述不正確的是( )
A.通入保護電流使鋼管樁表面腐蝕電流接近于零
B.通電后外電路電子被強制從高硅鑄鐵流向鋼管樁
C.高硅鑄鐵的作用是作為損耗陽極材料和傳遞電流
D.通入的保護電流應該根據環境條件變化進行調整
【分析與解答】本題在最新版人教版《反應原理》P113第7題收錄了本題,素材取自老人教版選修四課本86頁(下同)倒數第二段話(最新的人教版反應原理在111頁),圖像取自課本87頁圖4-20略加修改。這道題是2017年全國I卷理綜化學選擇題中得分率最低的一道題目,廣東省全省本題的得分率37%,錯選A、B、D的人數高達63%實在是出乎意料之外。其實仔細閱讀題意,這是外加電流的陰極保護法,鋼管樁為陰極,電子被強制流向被保護的陰極鋼管柱,陰極被保護,鋼管樁表面腐蝕電流是指鐵失去電子形成的電流,接近于零,鐵不容易失去電子,A正確;電解池的外電路中,陽極上發生氧化反應,失去電子,電子由陽極流向正極,由電源的正極經外電路流向陰極,B正確;高硅鑄鐵做陽極,陽極上發生氧化反應,但是題給信息這個高硅鑄鐵是惰性電極,不是普通的鐵做陽極為活潑電極,故陽極不被損耗,陽極上主要是海水中的水被氧化生成氧氣,C錯誤;根據海水對鋼管樁的腐蝕情況,增大或減小電流強度,D正確。本題錯誤的主要原因就在于,不少同學一看到陽極含鐵,就以為是活潑電極,會被損耗,而認為C是正確的,這是思維定式和不看題給信息所造成的,從而錯選其他三個不常見的敘述答案,以為是錯的,其實這三個選項在課本有敘述。像這樣的問題值得我們警示,在后期高考中不要再出現。
【評注】金屬的腐蝕和防護問題課本介紹篇幅較少,平時復習和練習時容易出現盲點,導致考試時容易出現意想不到的問題。因此,有必要把這些系統的搞清楚,選擇恰當的題目進行訓練,例如吸氧腐蝕與析氫腐蝕的問題,有些同學可能出現孤立地看待,其實可以通過2014年安徽卷第28題進一步來訓練學生的各項能力,辯證看待問題。其實腐蝕并不是一無是處,一分為二的來看待,也可以加以利用:例如吸氧腐蝕的原理來測空氣中氧氣的含量、制成雙吸劑(吸氧和吸水)在食品包裝里面、一次性保暖貼等。再例如課本P87科學探究驗證犧牲陽極的陰極保護法,2018年北京卷第12題對這個方法進行改進,值得關注;關注課本的習題及其改編,例如課本P88頁第10題改成的2016年北京卷第12題,這道高考題當年也是得分率極低,值得反思。
電化學中同學們普遍覺得困難的是電極反應式的書寫問題,這個在眾多資料書上有介紹,每位老師都會有專門的講解和針對訓練,限于篇幅,本文不再贅述電極反應的書寫問題。此外,有些題目考查跨學科綜合考查,例如2018年全國I卷,出現比較電極上的電勢高低等。最后,筆者覺得有個題目有必要再提一下,限于篇幅,不具體列出,請各位具體翻看高考原題:2011年廣東卷第32題(4)、2014年山東卷第30題(1)、2015年廣東卷第32題(5),這三年都是重復考離子液體中來電鍍鋁工藝,以陰極反應為例:4Al2Cl-7+3e-=Al+7AlCl-4,這個電極反應式的書寫確實難度較大,后續各種模擬題對這個考點也是層出不窮(最新魯科版《反應原理》中P43第9題也引入此考點),它作為書寫電極反應式來說,是個極好的訓練素材,值得仔細玩味來徹底弄懂,然后再遷移應用到其他,定會妙不可言,屢試不爽。因此,在前人的基礎上研究高考題,找出命題規律和完善自己知識體系、提升自己的關鍵能力,以不變應萬變,從而避免重蹈覆轍,只有這樣才能在高考中立于不敗之地!
責任編輯 李平安

