黏蛋白5B上調高遷移率族蛋白組A1促進乳腺癌細胞侵襲轉移
陳永勝 曾珊珊 鄭文英 賈小婷
廣州醫科大學附屬腫瘤醫院腫瘤研究所,廣州惡性腫瘤治療轉化醫學重點實驗室(廣州510095)
乳腺癌是女性最常見的惡性腫瘤[1]。全國腫瘤登記中心公布我國2014年女性乳腺癌的發病率(新增病例27.89萬例)大約占到整個女性腫瘤的16.51%[2]。手術、放/化療以及免疫治療是乳腺癌常見的治療方式,但90%的乳腺癌患者還是死于遠端轉移[3]。轉移是一個多基因多步驟的復雜生物學過程[4]:細胞丟失其上皮細胞-細胞連接和頂端-基底細胞極性并轉變為具有紡錘狀細胞形狀和增加的低增殖狀態,從而遷移和侵入以產生或再生新的組織。轉移一直被認為是進展性乳腺癌的最終步驟[5]。但是目前轉移的分子機制尚未完全闡明,針對已有的靶點無法滿足臨床的治療需求。因此,闡述乳腺癌轉移的分子機制對于降低乳腺癌遠端轉移率,提高乳腺癌診治水平具有非常重要的意義,也是醫學和生命科學領域面臨的十分緊迫的重大課題。
筆者在前期通過數據庫分析發現黏蛋白5B(mucin 5B,MUC5B)在乳腺癌組織中顯著高表達。MUC5B是黏蛋白家族蛋白,屬于高分子量的O-糖蛋白,通常在上皮細胞表面表達[6-8]。黏蛋白參與多種細胞基本的生命活動:保護和潤滑上皮細胞、維持上皮特征、細胞黏附、分化和免疫[9-12]。已顯示黏蛋白的表達在許多病理狀況如炎性腸病和瘤體形成中被改變[13-15]。筆者通過數據庫分析發現MUC5B在乳腺癌中的表達量顯著高于其在正常組織中的表達量,且生物信息學預測MUC5B可能與高遷移率族蛋白組A1(human high mobility group A1,HMGA1)的表達正相關。本文擬在上述基礎上,探討MUC5B在乳腺癌侵襲轉移中的作用及具體的分子機制。
1 材料與方法
1.1 細胞及培養人乳腺癌細胞T47D、MDA-MB-231、MCF-7、HCC1937、ZR-75-30、BT549和 SKBR3均由本實驗室保存。乳腺癌細胞由1640(Gibco公司)完全培養液(含10%胎牛血清),在5%CO2、37℃的培養箱中培養。正常乳腺上皮細胞MCF-10A的培養基配置如下:含有5%馬血清的DMEM/F12(1∶1)培養基,依次加入表皮生長因子(20 ng/mL)、氫化可的松(0.5 μg/mL)和胰島素(10 μg/mL),培養條件與乳腺癌細胞一致。
1.2 RNA提取及逆轉錄購買RNA Isolation Kit I試劑盒(Omega公司)用于細胞總RNAs的提取。預冷PBS洗滌細胞,700 μL RTK裂解液處理細胞,加入700 μL無水乙醇,12 000g,4 ℃離心15 min。上清加入柱中,10 000g離心1 min。500 μL RW1洗滌柱子,10 000g離心 1 min。700 μL RW2洗滌柱子兩次。空甩,12 000g,3 min。用30 μL無核酶水溶解RNA,靜置2 min。12 000g離心2 min。-80℃保存RNA樣品。
根據說明書,配置逆轉錄體系如下:Random Primer 1 μL,RNA 4 μg,水補足12 μL。65 ℃ 5 min,立即冰置 2 min。加入 4 μL Reaction Buffer,1 μL RNase inhibitor,2 μL dNTP,1μL Reverse trscriptase。42℃ 1 h,70℃ 5 min。-20℃保存cDNA。
1.3 qRT-PCR方法根據說明書,配置qRT-PCR檢測體系:Forward primer 0.8 μL,SYBR 10 μL,cDNA 1 μL,Reverse primer 0.8 μL,用水補足20 μL體系。運行程序:50℃ 2 min,95℃ 2 min,95℃15 s,60 ℃ 30 s(40個循環)。引物序列見表1,根據 2-ΔΔct值計算相對表達量。

表1 引物序列匯總Tab.1 Summary of primers in this study
1.4 Transwell將Transwell小室放在corning 24孔板中,50 μL無血清培養基加入上室,水化基底膜(置于37℃、5%CO2的培養箱中)。30 min后,給上室加入1×105細胞,下室加入600 μL完全培養基。24 h后,固定小室(甲醇)10 min,棉簽擦拭上室的細胞,1%結晶紫染色細胞10 min,流動水沖洗小室,室溫晾干。
1.5 生物信息學預測UALCAN(http://ualcan.path.uab.edu/);The Human Protein Altas(https://www.proteinatlas.org/);starBase(http://starbase.sysu.edu.cn/)
1.6 統計學方法所有實驗重復3次以上,所有的數據均用均數±標準差表示。兩組間比較用獨立樣本t檢驗,以P<0.05為差異有統計學意義。
2 結果
2.1 MUC5B在乳腺癌中高表達如圖1A所示:在線數據庫UALCAN展示了MUC5B在1 097例乳腺癌組織中的表達量顯著高于其在144例癌旁組織中的表達量(P<0.000 1)。這是MUC5B mRNA水平的表達模式,相同的蛋白質水平表達模式見圖1B。在線數據庫The human altas通過免疫組化的方法證實MUC5B在7例乳腺癌中高表達,1例中表達,僅4例低表達。最后,本研究在乳腺正常上皮細胞MCF-10A及多種乳腺癌細胞中檢測MUC5B的表達量。qRT-PCR結果證實MUC5B在乳腺癌細胞中顯著高表達。與MCF-10A相比,MUC5B在MDA-MB-231中的表達量上調7.31倍,在MCF-7中的表達量上調2.20倍(圖1C)。

圖1 MUC5B在乳腺癌中高表達Fig.1 MUC5B is enhanced in breast cancer
2.2 MUC5B促進乳腺癌細胞發生侵襲本研究在MCF-7細胞和MDA-MB-231細胞中干預MUC5B的表達。在MCF-7細胞中轉染MUC5B過表達質粒,MUC5B表達量較對照組上調8.44倍(圖2A)。Transwell實驗發現與對照組相比,MUC5B可明顯增加該細胞的侵襲能力(圖2B)。同樣的,在MDA-MB-231細胞中轉染靶向MUC5B的干擾質粒,qRT-PCR結果證實sh-MUC5B-1#沉默效果最好,可敲低81.67%的MUC5B表達量,用于后續研究(圖2C)。Transwell實驗發現與對照組相比,敲低MUC5B后該細胞的侵襲能力較對照組明顯降低(圖2D)。
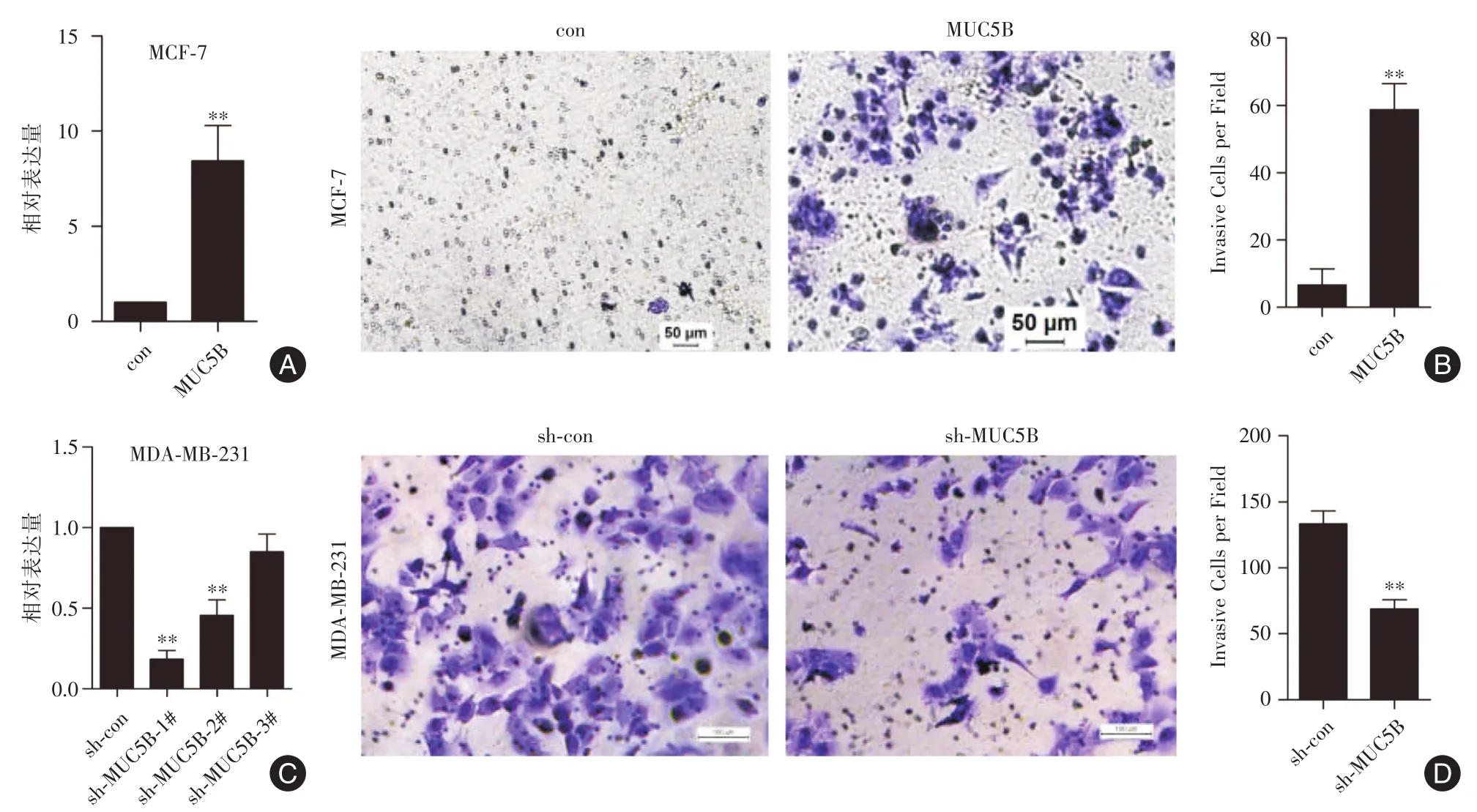
圖2 MUC5B調控乳腺癌細胞的侵襲轉移能力Fig.2 MUC5B modulated invasion of breast cancer cells
2.3 MUC5B促進乳腺癌細胞侵襲的分子機制明確了MUC5B可促進乳腺癌細胞發生侵襲轉移的作用后,本研究將重點探討其發揮作用的具體分子機制。在線軟件starbase預測到MUC5B與HMGA1在1 104例乳腺癌組織中表達正相關(圖3A)。在MCF-7中過表達MUC5B,可上調HMGA1表達量至4.53倍,而在MDA-MB-231細胞中敲低MUC5B則可大大降低HMGA1的表達量(圖3B)。此外,本研究在MCF-7細胞中過表達HMGA1,在MDAMB-231中敲低HMGA1。WB結果證實HMGA1表達量及敲低模型均成功建立(圖3C)。最后,通過transwell實驗發現:在MCF-7中過表達MUC5B,可明顯增加該細胞侵襲能力,但是同時過表達MUC5B和敲低HMGA1,可大大降低該細胞的侵襲能力(圖3D);同樣的,在MDA-MB-231細胞中敲低MUC5B,則該細胞侵襲能力減弱,但若同時敲低MUC5B和過表達HMGA1,又可以逆轉該細胞的侵襲能力(圖3D)。提示MUC5B通過HMGA1發揮促乳腺癌細胞侵襲轉移的作用。
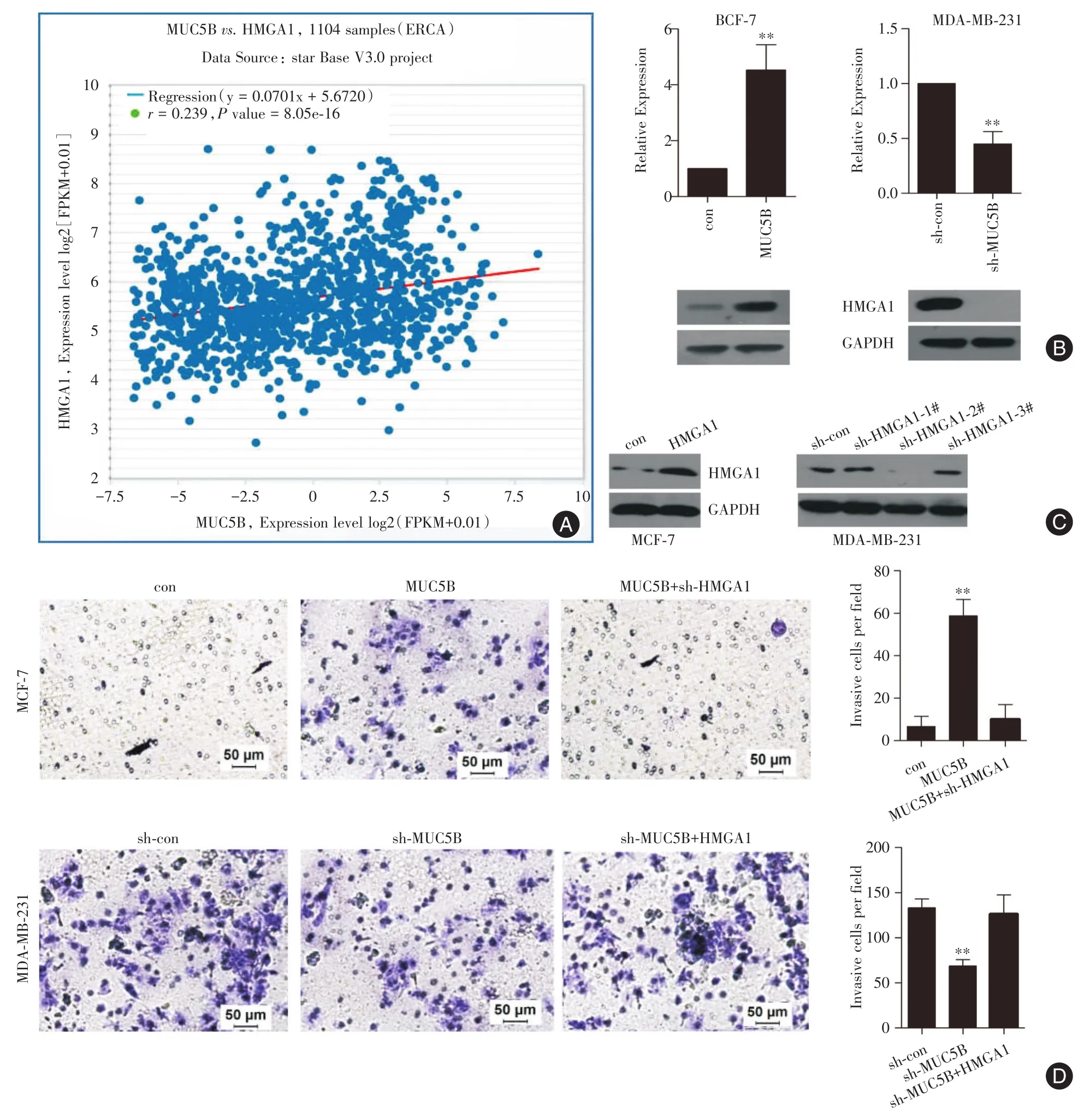
圖3 MUC5B通過調控HMGA1促進乳腺癌細胞侵襲轉移Fig.3 MUC5B promoted breast cancer cells invasion via accelerating HMGA1
3 討論
MUC5B在乳腺癌中的作用備受關注。有學者在乳腺癌細胞中敲低MUC5B的表達后,發現該細胞的黏附性、細胞生長、克隆形成能力均較對照組顯著降低,但是細胞并未發生凋亡。同時還發現MUC5B與乳腺癌較差的化療敏感性有關,降低MUC5B將促進乳腺癌化療增敏[16]。MUC5B在體外側近細胞增殖和浸潤,在體內可促進瘤體生長和細胞擴散[17]。與此相一致的是,本研究在乳腺癌細胞中敲低MUC5B,發現該細胞的侵襲能力降低,反之亦然。為探討MUC5B在乳腺癌中的作用機制,本研究通過生物信息學及實驗驗證發現MUC5B上調HMGA1。HMGA1是核內轉錄因子,能夠結合到富含AT區域的DNA鏈上,調控下游效應基因的轉錄活性[18]。HMGA1通常在胚胎發育中表達量較高,而在成熟組織中低表達[19]。HMGA1在多種腫瘤中高表達,且HMGA1通常與轉移和患者較差的預后正相關[20]。這是因為HMGA1可以調控多種參與細胞增殖和DNA損傷修復相關基因的表達[21]。此外,還發現HMGA1是晚期糖基化終產物特異性受體(receptor of advanced glycation endproducts,RAGE)的配體,可以活化ERK信號通路,參與細胞黏附、遷移與轉移等能力[22]。與這些結果一致的是,在本研究中發現HMGA1可以逆轉敲低MUC5B引起的乳腺癌細胞侵襲轉移能力減弱。而在MCF-7細胞中敲低HMGA1可以逆轉因過表達MUC5B而引起的轉移能力增強。后續筆者將進一步探討MUC5B調控HMGA1的分子機制。

