Luminal型乳腺癌中PD-L1的表達特點及預測價值
郝語晨 畢愷欣 劉曉青 徐毅 陶新楠 張亞芬山西醫科大學(太原030000);山西醫科大學附屬人民醫院(太原0300)
國際癌癥研究中心發布的2018年全球癌癥統計報告顯示乳腺癌居于全球女性癌癥發病率首位,而我國人口基數龐大是不容忽視的乳腺癌大國[1]。根據世界癌癥生存研究CONCORD發布的最新數據,我國乳腺癌年齡標化生存率為83.2%,比澳大利亞、美國等西方發達國家的同期數據落后6%左右[2],延長生存時間、降低病死率是我國乳腺癌疾病管理的重點。PD-1/PD-L1檢查點(programmed cell death-1/programmed death ligand-1 checkpoint)及其抑制劑是最近幾年腫瘤免疫學中備受矚目的研究熱點[3-4],其理論基礎是腫瘤的免疫逃逸機制:正常生理條件下,人體免疫系統存在促進自我耐受防止自身免疫的機制,即T細胞被激活時其表面PD-1表達增加,而攻擊性炎癥因子IFN-γ、TNF-α等刺激特異性免疫細胞表達其配體PD-L1和PD-L2,其中主要為PD-L1,當PD-1與其配體PD-L1結合時,經過一系列酶聯反應抑制下游的PI3K/AKt/mTOR通路,進而抑制T細胞功能,而腫瘤細胞恰恰習得這種逃避免疫攻擊的方法,在其細胞表面大量表達PD-L1,實現免疫逃逸,參與腫瘤增殖、侵襲、轉移等惡性生物學行為[5-6]。
腫瘤組織中腫瘤細胞和腫瘤浸潤淋巴細胞(tumor infiltrating lymphocytes,TILs)均有PD-L1表達[5-6],本研究關注PD-L1在上述兩類細胞的表達特點,分別探索對生存預后有無預測價值。PD-L1在三陰性、Her-2過表達型乳腺癌的預后預測價值已被大量研究[7-13]證實,即PD-L1表達越多,提示預后越差。然而三陰性、Her-2過表達型并非最常見亞型,僅占乳腺癌總體的不到30%,上述研究發現的普適意義有限,因此筆者認為,進一步研究最常見亞型(即Luminal型)對臨床的預后預測和治療指導意義更大。為避免Her-2陽性患者赫賽汀治療不規范影響預后分析,本研究僅納入Luminal(Her-2陰性)型病例。
1 資料與方法
1.1 一般資料本研究為歷史前瞻性研究。本研究入組2013年1-12月于山西省人民醫院乳腺外科住院治療的乳腺浸潤性導管癌病例。納入標準:(1)女性;(2)乳腺癌分期較早可行規范手術治療者;(3)病理類型為浸潤性導管癌;(4)分子類型為Luminal(Her-2陰性)型;(5)相關病例資料完善。排除標準:(1)本次診斷為雙側乳腺癌;(2)既往或本次治療期間有乳腺或其他原發惡性腫瘤病史;(3)因患者無法承受或患者意愿等行姑息性手術者;(4)內分泌治療不規范。
1.2 方法
1.2.1 臨床數據年齡(以身份證出生年月為準);月經狀態(絕經定義為雙側卵巢切除術后/年齡≥60歲/年齡<60歲,自然停經≥12個月/FSH和雌二醇處于絕經后范圍);乳腺/婦科合并癥(定義為乳腺纖維瘤、乳管內乳頭狀瘤/子宮肌瘤、卵巢囊腫等與雌性激素紊亂相關的乳腺/婦科良性疾病);家族史(定義為直系親屬有惡性腫瘤病史)。
1.2.2 病理數據病理學分級、ER%、PR%、TIL%、Ki-67、TNM分期(依據AJCC第九版,記為Ⅰ/Ⅱ/Ⅲ期)、分子分型[將Luminal型分為Luminal A型,即ER和/或PR陽性、Ki-67<14%且Her2陰性;Luminal B(Her2-),即ER和(或)PR陽性、Ki-67≥14%且Her2陰性]。
1.2.3 治療情況手術時間及方式、術后輔助治療類型、具體藥物方案。
1.3 免疫組化本研究采用免疫組化二步法。PD-L1抗體試劑選用中山金橋兔單克隆一抗,克隆號為SP142。PD-L1在腫瘤細胞膜和/或細胞質表達記為TC(tumor-cell),在TILs表達記為IC(immuno-cell),采用David E等的評分方法[14],即計算PD-L1表達細胞在腫瘤區域的占比,以百分比表示(即TC%/IC%);選取1%、5%、10%為截點,即<1%記為TC/IC0分,≥1%且<5%記為TC/IC1分,≥5%且<10%記為TC/IC2分,≥10%記為TC/IC3分。TC和IC的cut-off值均為1,即0分為陰性表達,1、2、3分為陽性表達。
查閱病理報告并記錄病理學分級,調取原始H&E切片判讀ER%、PR%、Her-2±FISH、Ki-67、TIL%。ER、PR判讀參照我國《乳腺癌雌、孕激素免疫組織化學檢測指南(2015版)》。Her-2判讀采用2017年ASCO-CAP會議發布的最新指南[15]。TILs%判讀根據國際TILs工作組2015年版的推薦進行[16]。閱片結果由高年資病理科醫師審核確認。
ER%、PR%、Ki-67采用SOFT&TEXT試驗[17]的截點進行分層,即:ER%分層為<50、≥50;PR%分層為<20、20~ 49、≥ 50;Ki-67分層為<14、14~ 19、20~25、≥26。病理學分級分為1/2/3級。TIL%選取30%、60%為截點,即<30%記為TIL(1+),≥30%且<60%記為TIL(2+),≥60%記為TIL(3+)。
1.4 隨訪通過電話、門診等方式隨訪患者院外內分泌治療情況及生存情況。生存事件定義為與乳腺癌疾病進展相關的死亡。隨訪時間為開始內分泌治療到內分泌治療滿5年。計算總生存期(overall survival,OS)。
1.5 統計學方法使用SPSS 25.0進行分析,計量資料以均數±標準差表示,對其進行正態性檢驗,符合正態性分布者進行獨立樣本t檢驗,不符合正態性分布者進行秩和檢驗。計數資料以率(%)表示,采用χ2檢驗。運用Cox生存分析判斷復發和生存預后的獨立因素。運用Kaplan-Meier法繪制生存曲線,生存率的比較使用Log-rank檢驗。以P<0.05為差異具有統計學意義。
2 結果
2.1 一般資料本研究共納入225例Luminal型乳腺浸潤性導管癌患者,年齡21~78歲,平均(51.17±11.32)歲,中位年齡50歲;左乳癌109例,右乳癌117例。5年生存率為88.9%(200/225)。OS事件23例;刪失19例,其中16例失訪,3例死于其他疾病。
2.2 腫瘤組織中PD-L1表達特點PD-L1在腫瘤細胞和TILs均有表達,見圖1。225個樣本中有86(38.2%)個樣本的腫瘤細胞PD-L1陽性表達,24(10.7%)個樣本的TILs PD-L1陽性表達。納入指標的賦值見表1。

圖1 PD-L1在乳腺癌組織的表達Fig.1 PD-L1 expression in breast cancer tissue

表1 相關因素賦值說明Tab.1 Related factors and assignment instructions
2.2.1 PD-L1的表達與臨床指標的關系對年齡、月經狀態、合并癥、家族史、分期分析顯示:腫瘤細胞和TILs中PD-L1的表達僅在不同分期時差異具有統計學意義,見表2。
2.2.2 PD-L1的表達與病理指標的關系對ER%、PR%、Her2狀態、TIL評分、Ki-67、分子分型統計學分析顯示,不同PR%、TIL評分、Ki-67、分子分型的PD-L1在腫瘤細胞和TILs的表達差異具有統計學意義(P<0.01),另外ER%(P=0.046)也是TILs中PD-L1表達的影響因素,見表3。
2.3 Cox回歸分析計算生存狀態的危險因素,由結果可見,IC評分(RR=2.375,P<0.01)、PR(RR=0.926,P<0.01)、Ki-67(RR=1.026,P=0.01)和病理學分級(RR=4.137,P<0.01)是生存的獨立危險因素,而TC評分在單因素分析時有意義,多因素分析時差異無統計學意義,說明其受其他混雜因素影響,不能獨立影響生存預后。見表4。
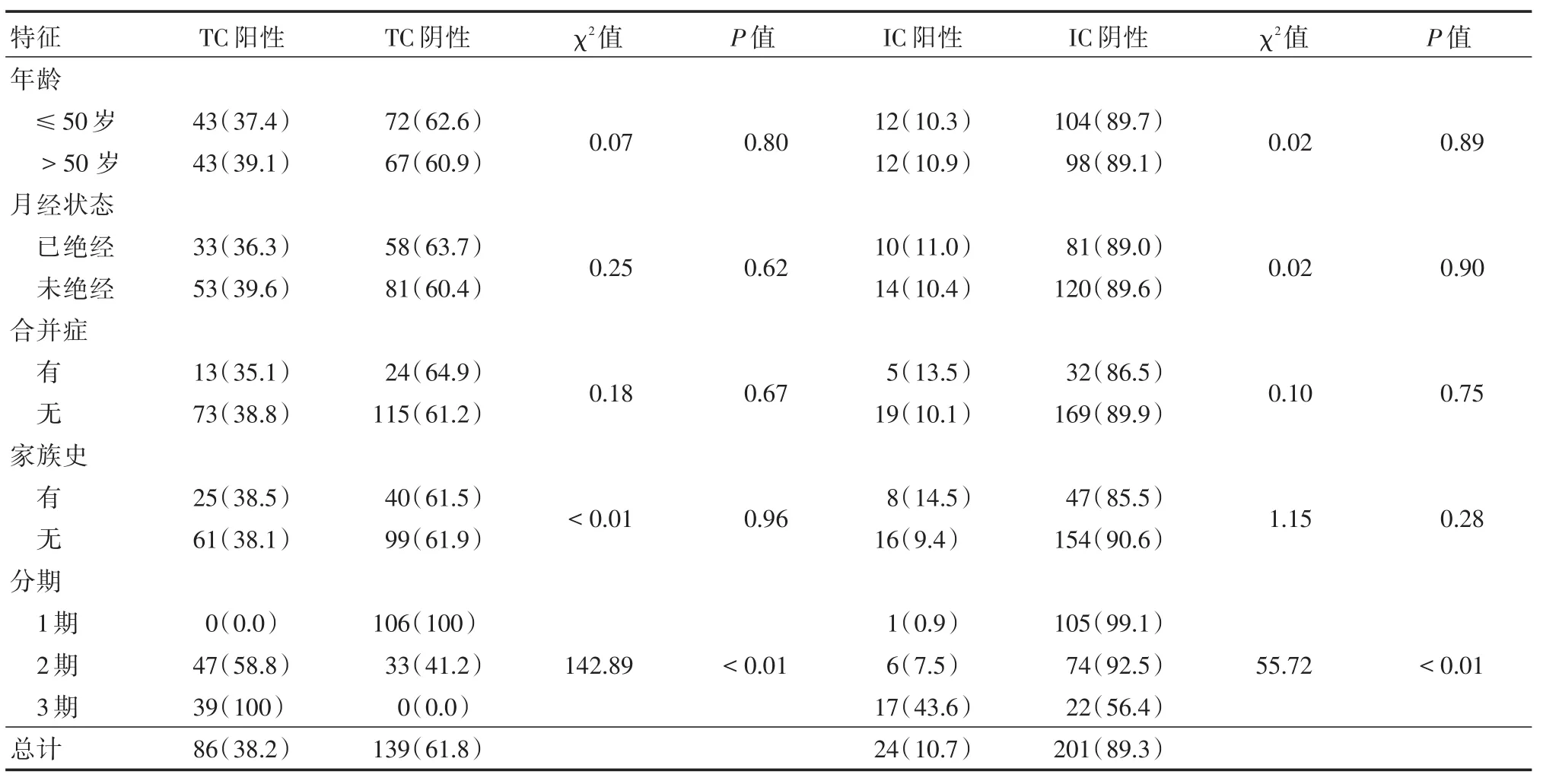
表2 PD-L1表達與臨床指標的關系Tab.2 Relationship between PD-L1 expression and clinical indicators 例(%)
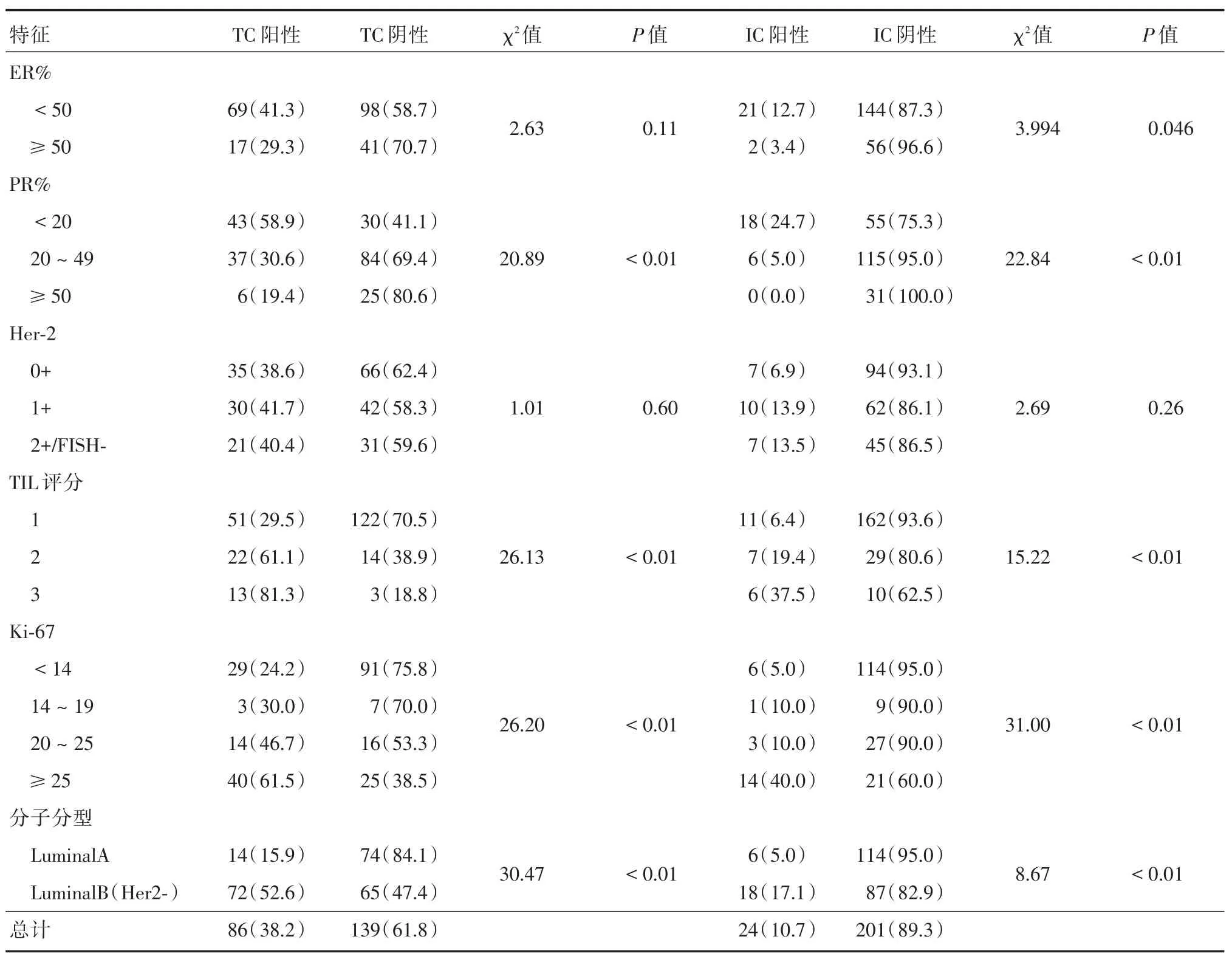
表3 PD-L1表達與病理指標的關系Tab.3 Relationship between PD-L1 expression and pathological indicators 例(%)
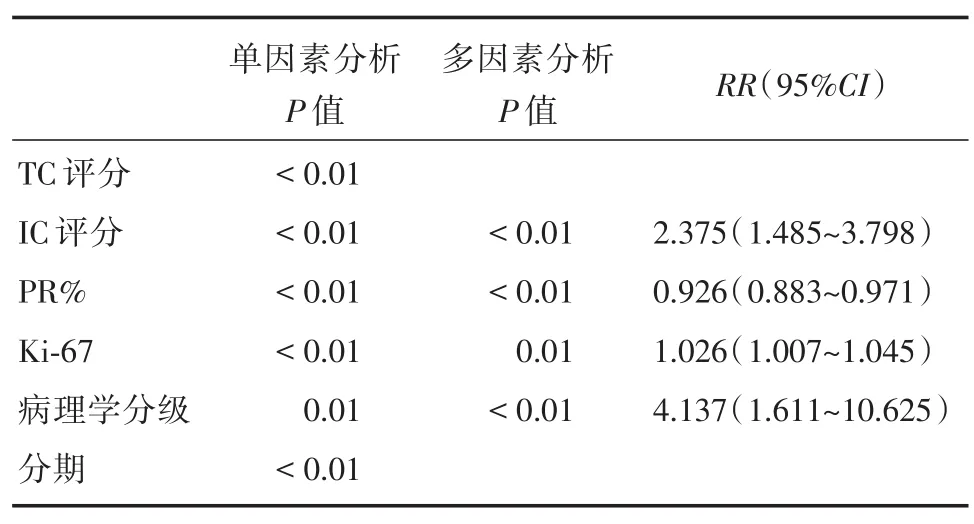
表4 生存狀態的危險因素分析Tab.4 Risk factor analysis of survival status
2.4 生存情況的比較對生存情況分析發現,IC陽性組患者生存率為37.5%(9/24),低于IC陰性組患者生存率96.0%(193/201),差異具有統計學意義(χ2=117.7,P<0.001)。生存曲線見圖2。
3 討論
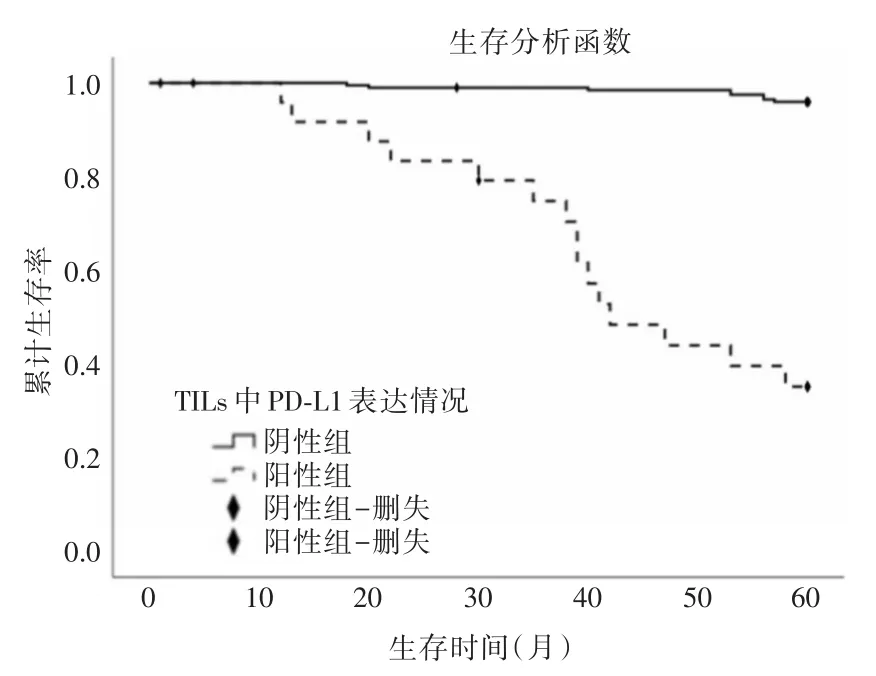
圖2 IC陰性組(n=201)和陽性組(n=24)(TILs中PD-L1表達陰性/陽性)的生存曲線Fig.2 Survival curves of IC negative group(n=201)and positive group(n=24)(negative/positive PD-L1 expression in TILs)
既往研究[7,12,18-19]報道 PD-L1 在 Luminal型乳腺癌細胞的陽性率為14.8%~53.1%,本研究中PD-L1在腫瘤細胞陽性率為38.2%,與上述報道基本一致。之前的研究[12,18,20]僅統計腫瘤細胞中PD-L1的表達,或不區分腫瘤細胞和TILs,籠統地記為腫瘤組織的表達[21],據筆者所知,大部分學者沒有關注PD-L1在TILs的表達并作為一個獨立指標進行研究,因而其陽性率鮮有報道。筆者認為腫瘤微環境的主要有形成分為腫瘤細胞和TILs,綜合考慮兩者的PD-L1表達情況不僅能反映腫瘤的免疫逃逸能力,而且能夠研究免疫系統的應答狀態,與單獨研究腫瘤細胞相比更為嚴謹科學。目前腫瘤細胞陽性表達的判讀標準不盡相同,有的研究[7,21]僅認可細胞膜的著色,而有的研究[10,12,18,22]將細胞膜和/或細胞質的著色均判定為陽性表達,因此相關研究結果可比性較低,難以匯總分析形成大數據支持的結論,亟待統一公認的判讀標準。
本研究發現:PD-L1表達水平與病理學分級、ER、PR、Ki-67、分期顯著相關,PD-L1陽性組織較陰性組織病理學分級較高、ER%較低、PR%較低、TIL評分較高、Ki-67較高、分期較晚,Luminal B(Her2-)型陽性率顯著高于Luminal A型,換言之,無論腫瘤組織或TILs中,PD-L1陽性均提示腫瘤惡性程度較高,預后預期較差,這一結論可用腫瘤免疫逃逸來解釋。
單因素和多因素生存分析均顯示TIL不是生存的影響因素,與其他研究[8,23-24]的發現一致。而χ2檢驗提示不同TILs評分組織的PD-L1表達顯著不同,TILs中PD-L1的表達是死亡的獨立危險因素,因此筆者推測結合TILs和PD-L1能夠提供預后預測的額外信息。本研究發現TILs中PD-L1表達是生存的獨立危險因素,腫瘤細胞的PD-L1表達僅在單因素生存分析時是獨立危險因素,而Luminal A型和Luminal B Her2-型的PD-L1在腫瘤細胞和TILs的表達情況差異具有統計學意義,因此筆者考慮該結論與入組人群中Luminal A型和Luminal B Her2-型相對比例有關,后續研究將對Luminal型進一步細化分析。
PR狀態、Ki-67和病理學分級是公認的預后預測因素。PAN等[25]對EBCTCG數據庫中500 692例激素受體陽性早期乳癌患者內分泌治療5年后20年隨訪研究發現,淋巴結狀態在任意時間段都是強預測因子,組織學分級和Ki-67是最初5年預后的重要獨立預測因子,但在后續時間段僅具有中等預測效力。ORUCEVIC等[26]根據TAILORx研究的最新結果對復發預測風險評分檢驗,納入年齡、腫瘤大小、病理學分級、PR狀態和組織學類型分析發現病理學分級和PR狀態是5個臨床病理特征中復發風險評分高低的最強預測因素。本研究對納入人群隨訪5年,生存分析結果與上述研究相一致,由于Luminal型乳腺癌與其他亞型相比5年后仍有較高復發率,筆者將繼續隨訪以獲取各個時間段腫瘤浸潤淋巴細胞PD-L1表達預測意義的變化。
腫瘤細胞和免疫細胞都能激活PD-1/PD-L1檢查點,上調PD-L1的表達,負性調節抗腫瘤免疫反應[20]。目前研究較為透徹的機制主要為兩條信號通路的激活[27]:PI3K/AKt/mTOR激活介導的細胞內信號通路和IFNGRs/JAK/STAT激活介導的細胞外信號通路。CHEN等[28]報道IFNγ上調外泌體PD-L1表達水平,抑制免疫和促瘤生長;外泌體PD-L1水平變化能夠預測治療后腫瘤細胞對T細胞再活化的適應性反應水平。筆者認為,TILs和外泌體中的PD-L1水平都能反映腫瘤與免疫系統抗衡的結果,其變化規律是治療反應性的重要預測因子,對指導臨床工作具有重要意義,例如對于需要新輔助治療的晚期乳腺癌患者,穿刺獲取組織中PD-L1的表達情況,為患者初始治療時選擇的個體化治療方案,未來條件允許時,密切檢測血液中PD-L1水平變化,掌握免疫系統受壓制程度變化,及時調整用藥選擇。
綜上,PD-L1在TILs的表達對生存預后具有一定的預測價值,可為臨床醫師預后判斷及治療選擇提供一定指導。

