硫酸銨/硫酸體系對不同類型粉煤灰鋁提取的影響
辛海霞,徐玉君,崔富暉,吳艷,林捷,任杭,牟文寧,翟玉春2,
(1.東北大學秦皇島分校資源與材料學院,河北秦皇島,066004;2.秦皇島市資源清潔轉化與高效利用重點實驗室,河北秦皇島,066004;3.中南大學冶金與環境學院,湖南長沙,410083;4.東北大學冶金學院,遼寧沈陽,110819;5.哈爾濱工業大學材料科學與工程學院,黑龍江哈爾濱,150001)
粉煤灰是煤高溫燃燒的產物,隨著我國工業化程度的提高,粉煤灰的排放量急劇增加,預計到2020年,我國粉煤灰堆存量將達到30 多億t[1],粉煤灰已成為我國工業固體廢物的最大單一污染源。粉煤灰的堆存不僅嚴重污染環境,而且造成了資源的浪費,部分地區粉煤灰中氧化鋁質量分數為35%~50%,相當于中等品位的鋁土礦中氧化鋁含量[2-15],其綜合利用備受關注,目前處理粉煤灰的主要方法有酸法、堿法、酸堿聯合法和銨法[16],具體方法由粉煤灰的物料性質決定。粉煤灰的物料性質主要取決于其中的顆粒形貌,粉煤灰中的顆粒形貌主要包含球形顆粒、不規則熔融顆粒和多孔炭粒,球形顆粒為鋁硅玻璃體,其結構致密難以破壞;不規則熔融顆粒疏松多孔,亦為高溫熔融的玻璃體組成;多孔炭粒是未燃盡的炭粒,其孔隙多、比表面積大[17]。不同種類的粉煤灰包含的顆粒形貌不同,本文作者以疏松多孔型粉煤灰和致密光滑型粉煤灰為研究對象,采用硫酸銨/硫酸體系處理2 種粉煤灰,旨在提取粉煤灰中的氧化鋁,結合熟料和溶出渣的特性分析其反應過程及提取氧化鋁的效果。
1 實驗原料及原理
1.1 實驗原料
實驗原料為內蒙某電廠2 種粉煤灰F1 和F2,將2 種粉煤灰分別過75 μm 篩,篩下物用于實驗,其化學成分見表1。從表1可見2 種粉煤灰鋁和硅質量分數差異較大。
圖1所示為粉煤灰的X 線衍射(XRD)譜。從圖1可知:F1粉煤灰中存在大量的無定形組分,硅的主要晶體物相為石英、硅酸鈣化合物及硅酸鈣鐵化合物,鋁的主要晶體物相為鋁酸鈣;F2 粉煤灰結晶度高,其晶體物相主要為石英和莫來石。
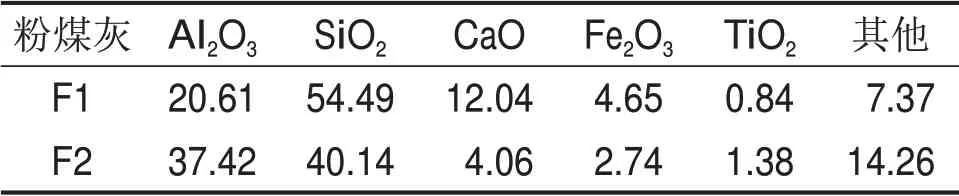
表1 2種粉煤灰的化學成分(質量分數)Table 1 Chemical composition of two kinds of fly ash %
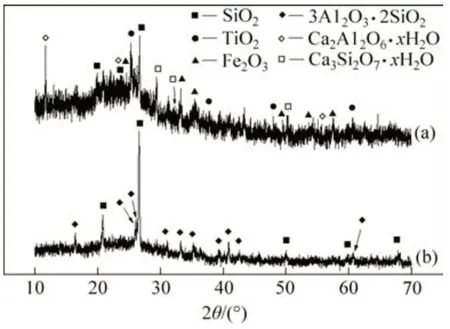
圖1 2種粉煤灰的XRD譜Fig.1 XRD patterns of two kinds of fly ash
采用場發射掃描電鏡對2種粉煤灰形貌進行觀察,結果如圖2所示。由圖2可知:F1粉煤灰形貌疏松多孔,形狀不規則,存在不規則疏松熔融玻璃體、各種顆粒黏聚體和蜂窩狀炭粒;F2 粉煤灰主要由球形玻璃體組成,其中部分玻璃體表面有析晶,根據XRD 圖譜可知,此部分析晶主要為石英和莫來石。
實驗所用硫酸銨和硫酸為分析純試劑,水為去離子水,分析檢測用試劑均為天津科密歐公司生產,采用Rigaku Ultima IV X 線衍射儀和SSX-550型掃描電鏡儀對物質的物相和形貌進行表征。
1.2 實驗方法

圖2 2種粉煤灰原料的SEM像Fig.2 SEM images of two kinds of fly ash
將固體硫酸銨磨細,與質量分數為98%的濃硫酸按照物質的量比1:1混合,常溫下放置10 h后與粉煤灰按一定比例置于氧化鋁坩堝中,充分攪拌后置于電阻絲爐中焙燒,電阻絲爐以10 ℃/min的升溫速率升至某一溫度,保溫一定時間后取出冷卻,加水攪拌溶出,溶出水量為熟料質量的8倍,溶出溫度為80 ℃,溶出時間為1 h,溶出完畢后抽濾,濾渣洗滌2次,采用EDTA返滴定法測定濾液中鋁的濃度,計算鋁的提取率。
1.3 實驗原理
采用硫酸銨焙燒法[16]和硫酸焙燒法[12]提取粉煤灰中的鋁,其焙燒過程中發生的反應主要為:
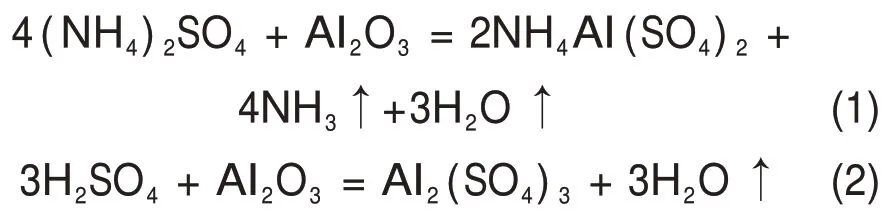
在焙燒過程中,反應式(1)系統會產生大量的氨氣,反應式(2)由于硫酸為強酸,對設備腐蝕性較強,為了降低系統產生氨氣的量及對設備的腐蝕,實驗采用硫酸銨與硫酸混合焙燒法提取粉煤灰中的鋁。
實驗將硫酸銨和硫酸按照物質的量比1:1 混合,常溫下放置10 h 后置于真空干燥箱內,得到的產物進行X線衍射分析,結果如圖3所示。
由圖3可以看出:硫酸銨和硫酸的反應產物為硫酸氫銨,兩者發生的反應為
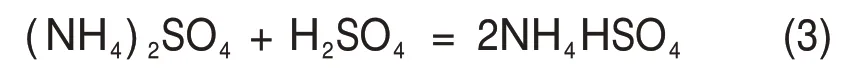
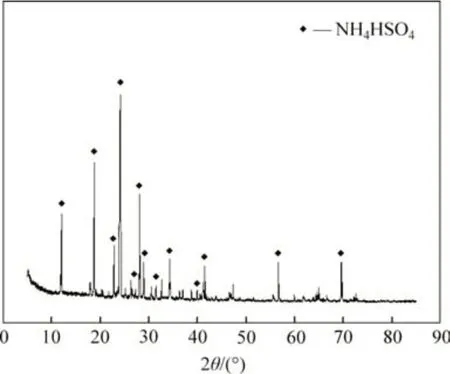
圖3 硫酸銨與硫酸混合物料的XRD譜Fig.3 XRD patterns of mixture of ammonium sulfate and sulfuric acid
因此,硫酸銨和硫酸按照物質的量比1:1混合后的體系實際為硫酸氫銨體系。硫酸氫銨是一種酸化劑,其分解溫度在300~450 ℃之間[18],硫酸氫銨分解形成(NH4)3H(SO4)2,NH2SO3H 和(NH4)2S2O7等中間產物[19-21],這些產物均為酸化劑,可以破壞粉煤灰結構,其與粉煤灰中氧化鋁發生的主要反應為
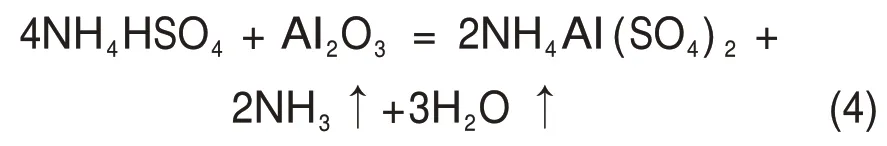
與反應式(1)和(2)相比,此方法可以降低系統產生氨氣的量和對設備的腐蝕性。
2 實驗結果與討論
2.1 焙燒溫度對鋁提取率的影響
當恒溫時間為2.0 h,硫酸銨和硫酸加入質量為按照式(3)和式(4)計算的理論質量3 倍時,考察焙燒溫度對粉煤灰中鋁提取率的影響,實驗結果如圖4所示。由圖4可知:F1粉煤灰自300 ℃后鋁提取率變化較F2 粉煤灰緩慢,說明硫酸氫銨易與疏松多孔型粉煤灰中的氧化鋁發生反應,主要原因為:F1 粉煤灰中氧化鋁大部分以無定形形式存在,其反應所需要的活化能較低。F2 粉煤灰鋁提取率受溫度影響較大,在150~450 ℃時,鋁提取率隨著溫度升高而變大,溫度高于450 ℃時鋁提取率隨溫度升高而降低,主要原因為:F2 粉煤灰中存在化學性質穩定的莫來石和玻璃體,兩者反應所需要的反應活化能均較高,溫度升高反應易于發生。
對400 ℃和450 ℃焙燒2種粉煤灰所得的熟料進行XRD 分析,結果如圖5所示。從圖5可知:2種粉煤灰中鋁的生成產物均為硫酸鋁銨,且隨著硫酸氫銨的分解,生成的硫酸鋁銨越來越多,此結果與圖4實驗測定結果吻合。當溫度為400oC時,硫酸氫銨未完全分解,因此,導致F2 粉煤灰的鋁提取率不高。當溫度為450 ℃時,硫酸氫銨已全部分解,因此,當溫度高于450 ℃時,硫酸氫銨還未與粉煤灰完全發生反應便快速分解,導致鋁提取率下降,此結果與圖4中鋁提取率變化曲線相吻合。
為了進一步研究硫酸氫銨對粉煤灰形貌的破壞及分析F2粉煤灰鋁提取率低的原因,對F1和F2粉煤灰進行掃描電鏡分析,結果如圖6所示。由圖6可以看出:F1 粉煤灰顆粒細小且無熔融玻璃體;F2 粉煤灰中的玻璃體大多未被破壞,有部分玻璃體表面出現被腐蝕后的針狀缺陷,主要原因為:粉煤灰中的玻璃體在形成過程中會有部分莫來石析出,此部分莫來石為針狀析晶,結合光滑玻璃體的EDS 能譜分析,說明此溫度下硫酸氫銨體系不能與結構致密的鋁硅玻璃體發生反應,但可以與露于外層的莫來石發生反應。此結果也可以由圖7所示溶出渣的XRD圖譜來證明,從圖7可知硫酸氫銨可以破壞2種粉煤灰中的含鋁晶體物相,溶出渣中晶體僅有石英。

圖6 溶出渣的SEM像Fig.6 SEM images of slags
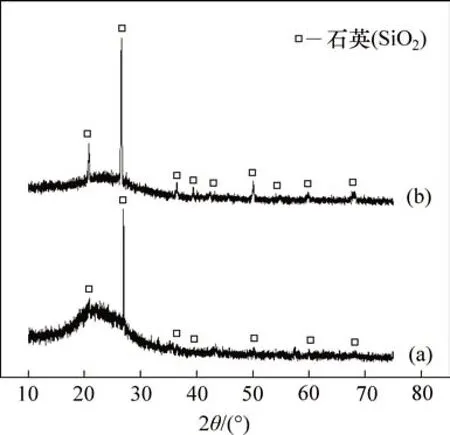
圖7 溶出渣的XRD譜Fig.7 XRD patterns of slag
2.2 恒溫時間對鋁提取率的影響
當焙燒溫度為450 ℃,硫酸銨和硫酸加入質量為按照式(1)和式(2)計算的理論質量3 倍時,考察恒溫時間對鋁提取率的影響,結果如圖8所示。由圖8可知:F1 粉煤灰的反應速率較快,在焙燒0.5 h 時鋁提取率即可達到90%以上,說明無定形狀態存在的鋁的反應很快;F2 粉煤灰在恒溫2.0 h后鋁提取率基本不變,說明在450 ℃時硫酸氫銨在2.0 h內即可分解完全。
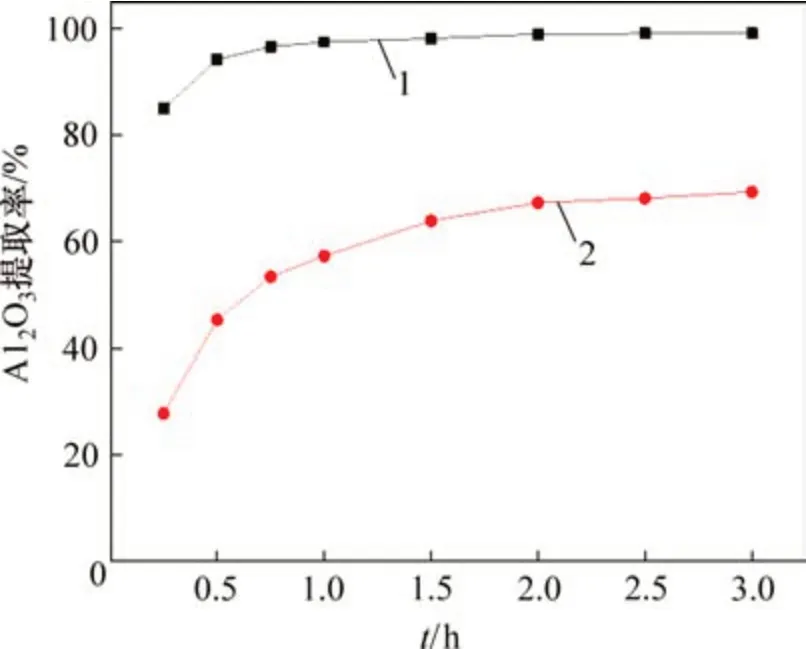
圖8 恒溫時間對鋁提取率的影響Fig.8 Effect of time on extraction of aluminum
2.3 硫酸銨和硫酸加入量對鋁提取率的影響
當焙燒溫度為450 ℃,恒溫時間為2.0 h 時,考察硫酸銨和硫酸加入量(即實際用硫酸銨和硫酸質量(mpractice):理論用硫酸銨和硫酸質量(mtheory))對鋁提取率的影響,結果如圖9所示。由圖9可知:F1粉煤灰所用硫酸銨和硫酸質量為理論質量的1.25倍時,鋁提取率即可達到98%;F2 粉煤灰所用硫酸銨和硫酸質量大于理論質量的2倍時,鋁提取率基本保持為67%,從硫酸銨和硫酸加入量也可以反映出2種粉煤灰破壞性的難易。
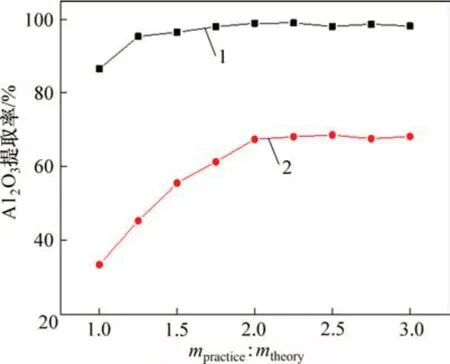
圖9 硫酸銨和硫酸加入量對鋁提取率的影響Fig.9 Effect of ammonium sulfate and sulfuric acid on extraction of aluminum
由上述實驗結果可知:硫酸銨/硫酸體系在破壞疏松多孔型粉煤灰時可取得較好效果,對于致密型粉煤灰體系可以破壞其莫來石結構,但對硅鋁玻璃體結構的破壞效果較差。
3 結論
1)硫酸銨/硫酸體系在處理疏松多孔型粉煤灰時效果較好,而對光滑致密型粉煤灰效果較差。
2)硫酸銨/硫酸體系處理疏松多孔型粉煤灰時,當焙燒溫度為300 ℃、恒溫時間為0.5 h、硫酸銨和硫酸加入質量為理論質量的1.25 倍時,氧化鋁提取率可達到98%。
3)硫酸銨/硫酸體系處理結構致密型粉煤灰時,當焙燒溫度為450 ℃、恒溫時間為2.0 h、硫酸銨和硫酸加入質量為理論質量的2倍時,氧化鋁提取率為67%。

