拔節期干旱脅迫下冬小麥品種間產量及生理響應的差異*
封 富,黃桂榮,王雅靜,張欣瑩,王 濤,鐘秀麗
拔節期干旱脅迫下冬小麥品種間產量及生理響應的差異*
封 富,黃桂榮,王雅靜,張欣瑩,王 濤,鐘秀麗**
(中國農業科學院農業環境與可持續發展研究所/農業部旱作節水農業重點實驗室,北京 100081)
拔節期干旱是影響冬小麥產量的重要災害,揭示不同品種對干旱脅迫生理響應的差異,可為鑒選與培育抗旱品種提供指導。選取黃淮海平原不同冬麥區種植面積較大的晉麥47、洛旱2號、石家莊8號、豫麥18和鄭麥9023共5個品種和1個抗逆性較弱的品種偃麥20,利用防雨棚開展盆栽試驗研究。從籽粒產量以及氣孔特性、膜穩定性和滲透調節特性等方面,分析拔節期受水分脅迫后,各品種抗旱性和干旱脅迫響應途徑的差異。結果表明:(1)灌溉條件下,晉麥47、洛旱2號和石家莊8號產量較高,豫麥18和偃麥20產量較低。拔節期受干旱脅迫后,晉麥47、洛旱2號和豫麥18產量較高,石家莊8號和偃麥20產量較低。可見,以籽粒產量為抗旱性評價的核心指標,晉麥47、洛旱2號和豫麥18抗旱性較強,石家莊8號和偃麥20抗旱性較弱,鄭麥9023抗旱性居中。(2)3個抗旱品種間干旱脅迫響應途徑并不一致。與抗旱性較弱的石家莊8號和偃麥20相比,拔節期干旱脅迫下,豫麥18氣孔導度較低,氣孔調節能力強;洛旱2號細胞滲透勢較低,滲透調節能力較強;洛旱2號膜離子滲漏率較低,膜穩定性較強;晉麥47在氣孔調節、滲透調節和膜穩定性調節方面與抗旱性較弱的品種無顯著差異。研究結果說明,冬小麥品種間響應干旱脅迫的關鍵途徑存在差異。因而品種的抗旱性難以通過單一生理指標科學評價,需要多指標聯合鑒定。
冬小麥;產量;抗旱性;氣孔調節;滲透調節;膜穩定性調節
小麥(L.)是世界上廣為種植的糧食作物,為中國第二大作物[1]。干旱缺水已成為制約中國小麥持續增產的關鍵因素[2]。小麥拔節期,干旱發生頻繁,對產量的危害較重。提高小麥品種的抗旱性是突破雨養地區小麥產量的有效途徑之一。揭示品種之間對干旱脅迫生理響應的差異,可以為品種的抗旱性評價與遺傳改良提供依據。
迄今為止,研究者開展了大量關于植物響應干旱脅迫的生理與分子機理的研究。植物受到干旱脅迫后,早期的響應表現為ABA水平迅速上升,誘導葉片氣孔導度下降,從而抑制蒸騰作用,減少水分喪失[3?4]。ABA水平升高同時還激活多種細胞與生理響應[5],表現為脯氨酸、甜菜堿、可溶性糖等滲透調節物質大量積累[6],降低細胞滲透勢,緩解水分虧缺狀態下細胞原生質以及胞內功能蛋白的脫水脅迫[7]。光合作用隨氣孔導度減小以及光合酶類活性的降低而下降[8]。光合作用與正常呼吸作用因受到干旱脅迫的抑制引起活性氧大量產生,對DNA、蛋白質以及生物膜脂質產生氧化損傷[9]。大量膜脂的過氧化引起生物膜的流動性和穩定性下降,離子大量外滲,打破細胞內離子平衡,細胞正常代謝被破壞。植物已經進化出應對過氧化損傷的策略,如降低光合作用、產生抗壞血酸、谷胱甘肽等抗氧化劑以及過氧化物酶、超氧化物歧化酶等抗氧化酶類清除活性氧[6,10],維持生物膜的穩定性。
植物的抗旱性是多基因控制的數量性狀,植物對干旱脅迫的適應也是多途徑的。但不同作物種類以及同種作物的不同品種之間,在干旱脅迫響應的關鍵途徑方面可能存在差異。本研究選取黃淮海平原不同冬麥區種植面積較大的5個品種和1個抗逆性較弱的品種開展研究,從籽粒產量以及氣孔特性、膜穩定性和滲透調節特性3個方面,分析拔節期受水分脅迫后,抗旱性與干旱脅迫響應途徑之間的差異,以期為利用生理指標進行抗旱性評價和耐旱品種鑒選提供指導。
1 材料與方法
1.1 材料
選用晉麥47、洛旱2號、豫麥18、石家莊8號、鄭9023和偃麥20共6個冬小麥品種為材料,各品種特性見表1。在2017年10月?2018年6月,于中國農業科學院農業環境與可持續發展研究所順義科學實驗站,采用盆栽方法開展實驗。塑料盆直徑36cm,高30cm,底直徑28cm,盆底留直徑1cm的排出孔。取耕層土壤,與有機肥充分混合,先用5mm篩子過篩,再混勻。土壤總氮0.109g×kg?1,有效磷24.5mg×kg?1,速效鉀106mg×kg?1,pH為7.7。每盆先裝土17.0kg,播種后再覆土1.0kg。于2017年10月1日播種,每盆均勻點播40粒種子。出苗后30d第一次間苗,去除長勢弱小幼苗5株。返青后第二次間苗,每盆定苗30株。入冬前將盆體埋入土中越冬,春季氣溫回升后取出。
1.2 水分處理
每個品種均設置兩種水分處理,充分灌溉(WW)和干旱脅迫(DS),土壤含水量分別為最大田間持水量(FC)的75%和45%。FC按如下方法測定:取過篩后混合均勻的土壤適量,裝入3個鋁盒中,帶回實驗室,用烘干法測定土壤含水量。另取3個塑料盆,各裝入18kg土壤,測定土壤最大田間持水量(FC)。具體方法為,先將土壤澆透水,用塑料膜覆蓋盆口防止表面蒸發失水。讓過量的水從盆底排水孔流出,至排水孔不再有水分滲出,即盆中土壤重量不再變化,此時土壤含水量即為土壤FC。按照FC的75%和45%計算WW和DS處理的初始重量。
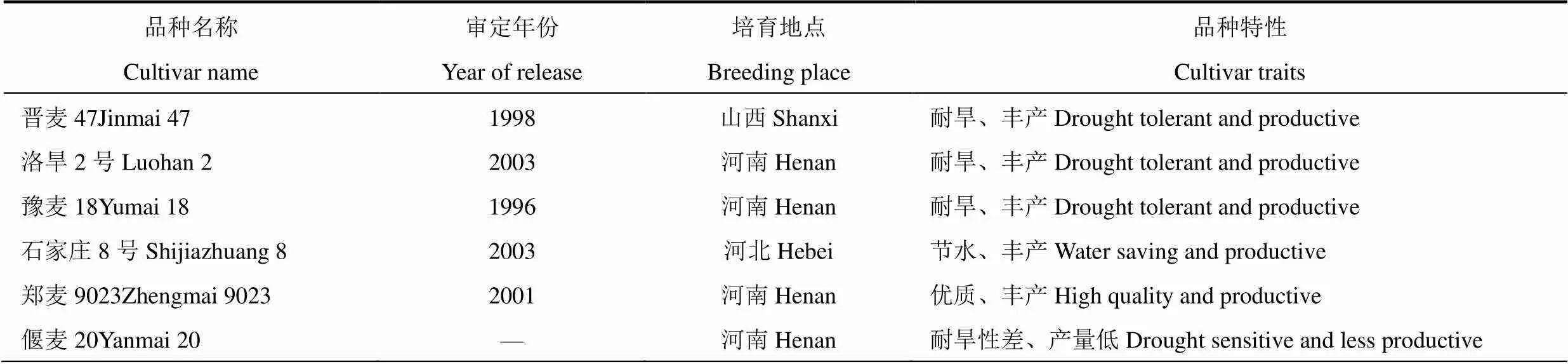
表1 試驗品種名稱及特性
采用稱重法控制土壤水分,每天日落后1~2h澆水,至各處理的初始重量。控水時間從2018年4月5日冬小麥進入拔節期開始,至4月25日冬小麥拔節末期結束。其余時間正常管理。盆栽小麥置于塑料防雨棚內,降雨時放下防雨棚遮蔽雨水,晴天將雨棚卷起,讓植物接受自然光照,并在開放環境下生長。每個品種均進行兩個水分處理,每處理6個重復。
1.3 項目測定
氣孔導度測定:分別于干旱脅迫5d、10d、15d后,利用便攜式近紅外氣體分析儀(LI-COR,美國)測定葉片氣孔導度。取主莖上部第一片完全展開葉,每盆測3片,取均值。
飽和滲透勢測定:將3片小麥葉片置于裝有去離子水的自封袋中,吸水8h,使其達到飽和狀態(RWC=100%);取出,用吸水紙吸干表面水分,密封后迅速放入低溫冰箱中冷凍。測定前取出,室溫下融化30min,榨取汁液,取10μL用冰點滲透壓計(美國)測量滲透摩爾濃度。計算飽和滲透勢,即
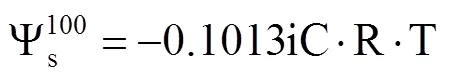
膜離子滲漏率的測定:參照Welti等[11]的方法利用電導儀測定。取3枚小麥葉片,置于25mL去離子水中,在23℃水浴下輕微振蕩1h,測定初電導值;溶液在100℃下煮沸10min,冷卻至23℃,測定總電導值。
離子滲漏率=初電導值/總電導值 (2)
籽粒產量:成熟后,將各盆內植株收獲,裝于網袋,自然曬干后人工脫粒,用電子秤(美國,精確到0.01g)稱重。
單株籽粒產量=總產量/株數 (3)
1.4 數據處理
采用Microsoft Excel 2013作圖,用Origin 2018 64bit軟件統計分析數據。
2 結果與分析
2.1 不同品種冬小麥產量對拔節期干旱脅迫的響應
由圖1可見,在充分灌溉條件下(WW),晉麥47、洛旱2號、石家莊8號產量較高,顯著高于豫麥18和偃麥20(P<0.05),鄭麥9023產量居中。拔節期受干旱脅迫(DS),與WW處理相比,各品種產量均顯著降低。晉麥47、洛旱2號和豫麥18降低幅度較小,分別是57.7%、57.6%和53.5%。鄭麥9023、石家莊8號和偃展20降低幅度較大,分別為58.6%、65.3%和60.1%。導致干旱脅迫下各品種的產量排序發生變化,晉麥47、洛旱2號和豫麥18產量較高,顯著高于石家莊8號和偃麥20(P<0.05),鄭麥9023居中。可見,晉麥47和洛旱2號在灌溉條件下能夠充分利用水分,獲得高產,在干旱條件下,也能夠抵御干旱,獲得較高產量。石家莊8號在灌溉條件下,產量與晉麥47和洛旱2號無顯著差異,但在干旱條件下,產量顯著低于這2個品種。豫麥18與石家莊8號的表現相反,在干旱脅迫下,其產量與晉麥47和洛旱2號無差異,但在灌溉條件下,產量顯著低于晉麥47和洛旱2號。偃麥20在灌溉條件和干旱條件下產量均較低。鄭麥9023在兩種水分條件下均屬于中等產量品種。以產量為抗旱性核心評價指標來看,6個試驗品種中,晉麥47、洛旱2號和豫麥18抗旱性較強,石家莊8號和偃麥20抗旱性較弱,鄭麥9023抗旱性居中。
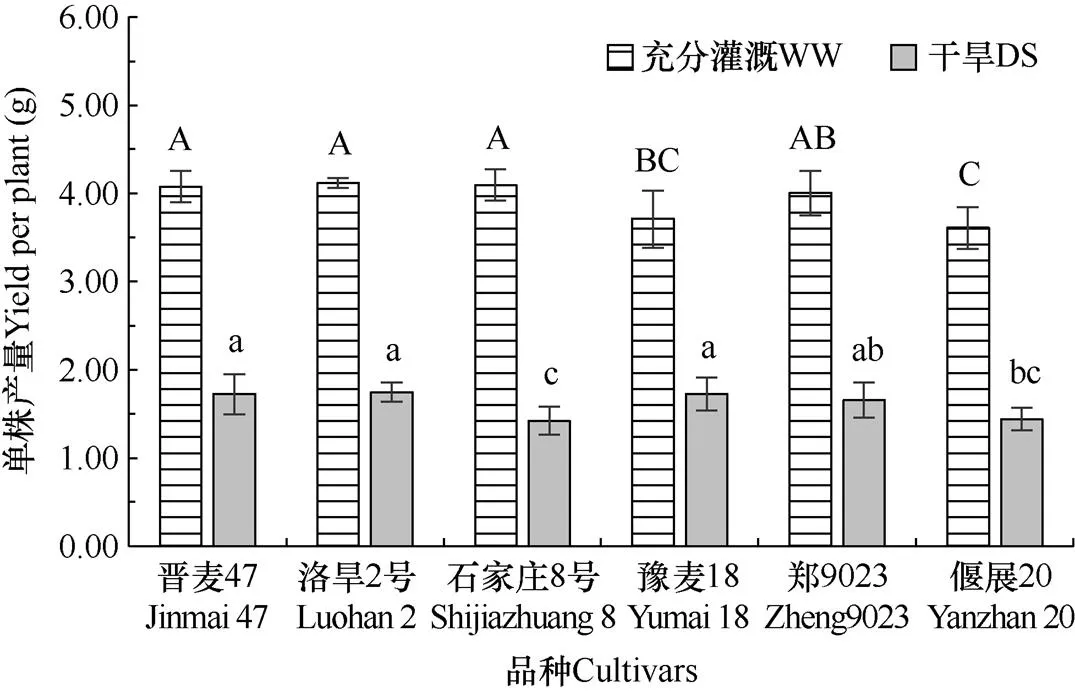
圖1 拔節期灌溉(WW)和干旱(DS)條件下不同冬小麥品種單株籽粒產量的比較
注:小寫字母表示干旱條件下品種間的差異顯著性,大寫字母表示充分灌溉條件下品種間的差異顯著性。短線表示均方差。下同。
Note:Lowercase indicates the difference significance among treatments under DS condition, and capital letter indicates the difference significance among treatments under WW condition. The bar means square error. The same as below.
2.2 不同品種冬小麥葉片氣孔導度對拔節期干旱脅迫的響應
從圖2可以看出,充分灌溉條件下(WW),無干旱脅迫發生時,品種間氣孔導度存在顯著差異。晉麥47、洛旱2號和石家莊8號的氣孔導度較高,顯著高于豫麥18、偃麥20和鄭麥9023(P<0.05)。結合圖1還可知,充分灌溉條件下,品種間氣孔導度的差異與品種間產量的差異趨勢相近。統計分析結果表明,二者之間存在極顯著正相關性(R2=0.89)。干旱脅迫下(DS),不同品種葉片氣孔導度均顯著下降,但品種間下降幅度不同,導致品種間氣孔導度存在顯著差異(P<0.05)。干旱脅迫5d,抗旱性較強的洛旱2號和豫麥18氣孔導度較低,顯著低于抗旱性弱的石家莊8號和偃麥20,晉麥47和抗旱性中等的鄭麥9023氣孔導度居中。但隨著脅迫時間延長至10d,豫麥18 氣孔導度最低,顯著低于鄭麥9023和偃麥20(P<0.05),晉麥47、洛旱2號和石家莊8號居中。脅迫至15d,豫麥18氣孔導度依然最低,顯著低于晉麥47。洛旱2號、石家莊8號、鄭麥9023和偃麥20居中。總體來看,隨著干旱脅迫時間延長,3個抗旱品種僅豫麥18氣孔導度保持最低,而晉麥47和洛旱2號與抗旱性弱的石家莊8號和偃麥20無顯著差異。
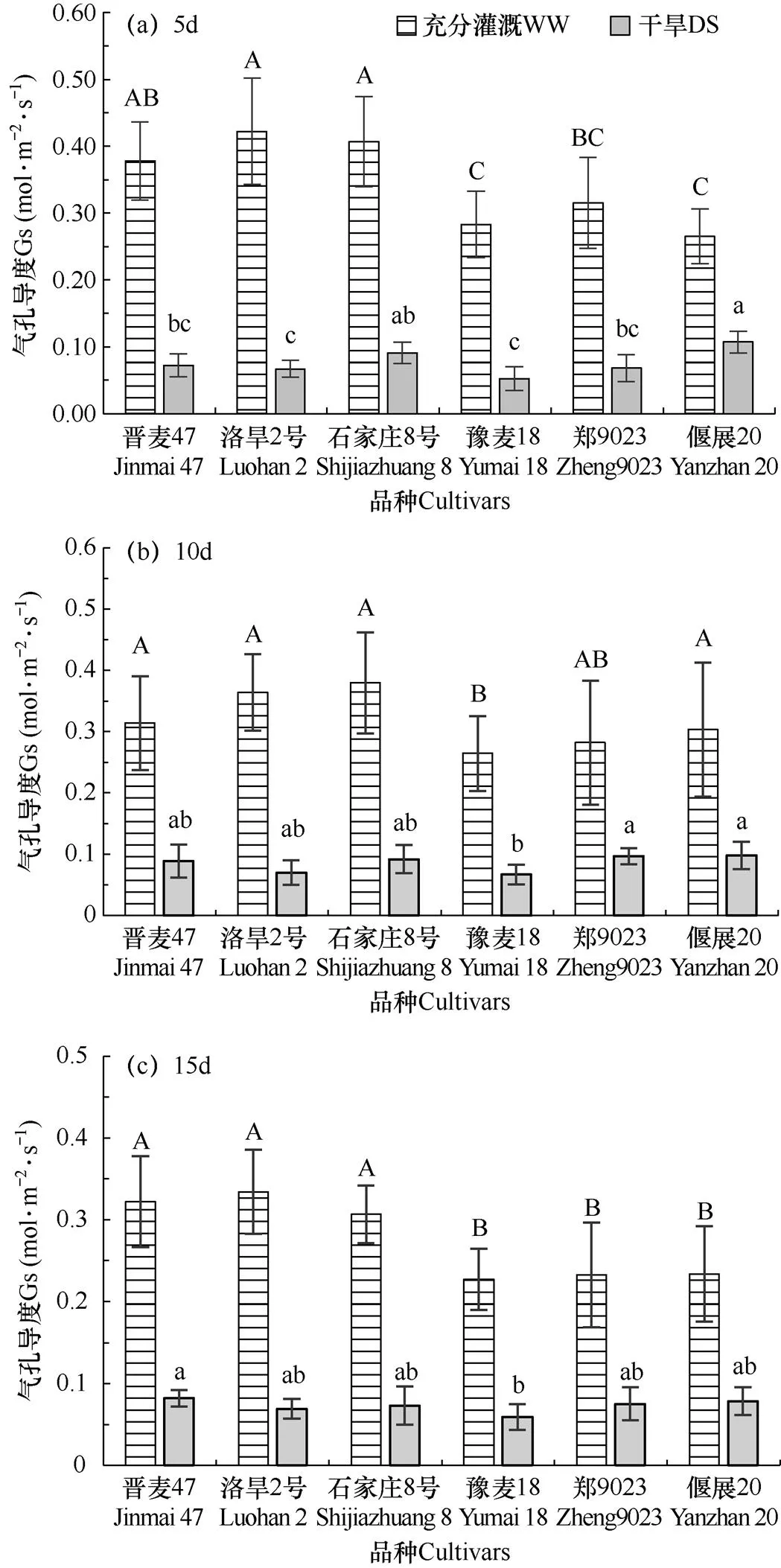
圖2 兩種水分處理(WW和DS)5d、10d和15d后不同冬小麥品種葉片氣孔導度的比較
2.3 不同品種冬小麥葉片細胞滲透勢對拔節期干旱脅迫的響應
在灌溉條件下(WW),無干旱脅迫發生時,6個試驗品種的飽和滲透勢存在顯著差異(表2)。洛旱2號和石家莊8號較低,豫麥18較高(P<0.05)。干旱脅迫下(DS),6個品種均發生滲透調節響應,飽和滲透勢較灌溉條件下顯著下降。干旱脅迫持續10d,各品種的飽和滲透勢與灌溉條件下的差異達到最大。但脅迫持續15d后,處理間的差異并未持續升高,反而低于脅迫10d的差異。表明脅迫時間過長,損傷嚴重時,滲透調節能力下降。由表2還可知,品種間對干旱脅迫的滲透調節響應存在顯著差異(P<0.05)。抗旱品種洛旱2號在脅迫15d內飽和滲透勢一直最低,表明該品種的滲透調節能力顯著高于其它品種。但是,抗旱性強的晉麥47和豫麥18的飽和滲透勢并未降至與洛旱2號相近的水平,只是達到與抗旱性較弱的品種石家莊8號和偃麥20無顯著差異的水平。

表2 兩種水分處理(WW和DS)5d、10d和15d后6個品種葉片細胞滲透勢比較
2.4 不同品種冬小麥葉片細胞膜穩定性對拔節期干旱脅迫的響應
由圖3可以看出,灌溉條件下(WW),沒有干旱脅迫發生時,品種間膜離子滲漏率存在顯著差異(P<0.05)。洛旱2號和石家莊8號較低,顯著低于晉麥47、豫麥18、鄭麥9023和偃麥20。在干旱脅迫15d后,6個品種膜離子滲漏率均顯著上升,但品種間升高幅度不同。抗旱性弱的石家莊8號、偃麥20和抗旱性居中的鄭麥9023升幅均較大,抗旱性強的洛旱2號和豫麥18升幅較小,洛旱2號的膜離子滲漏率最低。抗旱品種晉麥47,無論是干旱脅迫下還是灌溉條件下,其膜離子滲漏率升高的幅度,均與抗旱性較弱的石家莊8號和偃麥20無顯著差異。
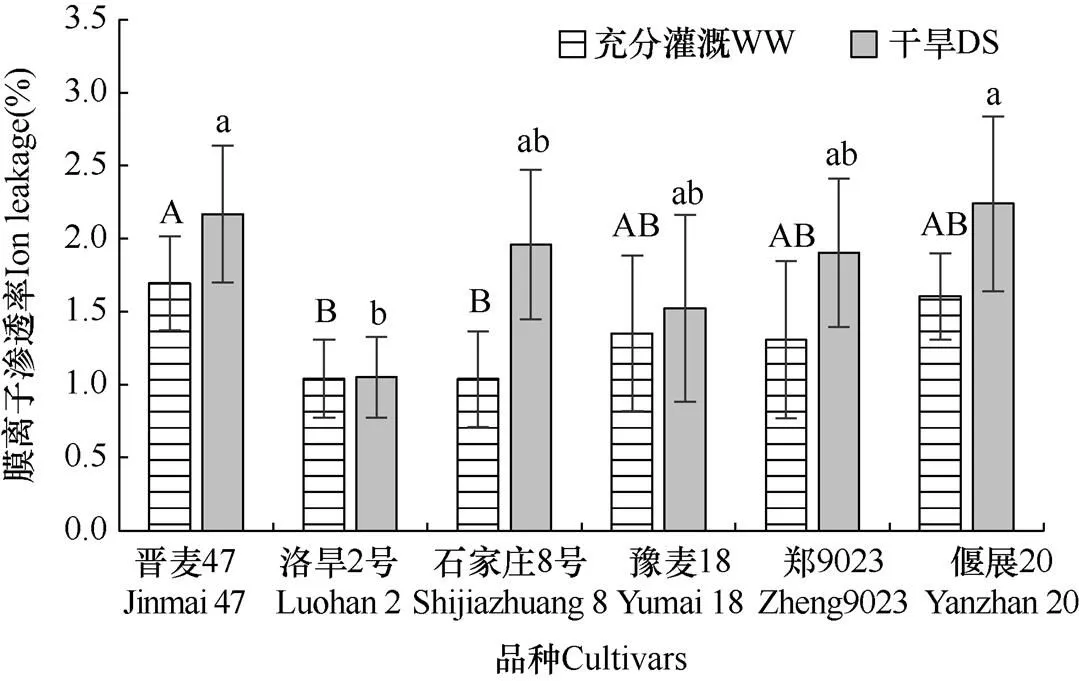
圖3 兩種水分處理(WW和DS)15d后不同品種細胞膜離子滲透率的比較
3 結論與討論
6個試驗品種對水分條件的產量響應存在差異。灌溉條件下,晉麥47、洛旱2號和石家莊8號產量較高,豫麥18和偃麥20產量較低,鄭麥9023居中。拔節期受干旱脅迫后,晉麥47、洛旱2號和豫麥18產量較高,石家莊8號和偃麥20產量較低,鄭麥9023居中。晉麥47 和洛旱2號在灌溉條件下能夠充分利用水分,獲得高產,在干旱條件下,也能夠抵御干旱,獲得較高產量。在灌溉條件下,石家莊8號產量與晉麥47和洛旱2號無顯著差異,為豐產品種,但在干旱條件下,其產量顯著低于這2個品種,因而不適于在降水偏少、又不具備灌溉條件的雨養地區種植。豫麥18在干旱脅迫下產量與晉麥47和洛旱2號無顯著差異,在灌溉條件有限或較干旱地區能夠獲得較高產量,但在灌溉條件下,其產量顯著低于晉麥47和洛旱2號,因而不適宜在降水充沛或者灌溉條件良好的地區種植。偃麥20在灌溉條件和干旱條件下產量均較低。鄭麥9023屬于兩種水分條件下均偏中等的品種。因此,明確品種對不同水分條件的產量響應特性,結合地區水分條件科學選用品種是提高作物產量的有效途徑。
以籽粒產量為抗旱性核心評價指標,晉麥47、洛旱2號和豫麥18抗旱性較強,石家莊8號和偃麥20抗旱性較弱,鄭麥9023抗旱性居中。但不同抗旱品種對干旱脅迫響應的途徑并不一致。氣孔調節是陸地植物適應脅迫環境的重要機制[12]。植物遭受土壤干旱[13?15]、大氣干旱[16?19]和鹽脅迫[20]等逆境均會降低氣孔導度,減少蒸騰失水。但是品種間氣孔響應敏感性[21]、下降幅度[22?23]以及隨脅迫時間下降的規律存在差異[16]。本試驗6個品種在干旱脅迫下氣孔導度均下降。但是抗旱性強的品種僅豫麥18氣孔導度較低,而洛旱2號和晉麥47的氣孔導度與抗旱性弱的石家莊8號和偃麥20并無顯著差異。滲透調節也是植物適應干旱環境的重要途徑[24?26]。干旱脅迫下,植物大量合成滲透調節物質,包括脯氨酸、甜菜堿、可溶性糖(甘露醇、山梨醇、海藻糖等)、有機酸等[6,24]。這些滲透調節物質能夠降低細胞滲透勢,減緩原生質的脫水脅迫[7,25?26]。本試驗中,3個抗旱性較強的品種,僅洛旱2號滲透勢最低,晉麥47和豫麥18滲透勢與抗旱性弱的石家莊8號和偃麥20無顯著差異。逆境脅迫下細胞代謝產生的活性氧會對細胞膜造成氧化損傷,引起細胞膜流動性和穩定性下降,胞內離子大量外滲[27?29]。本試驗中,抗旱性較強的品種僅洛旱2號在干旱脅迫15d后膜離子滲漏率較低,保持較高的膜穩定性。晉麥47和豫麥18的膜離子滲漏率與抗旱性弱的石家莊8號和偃麥20無顯著差異。
干旱脅迫下,抗旱品種豫麥18大幅度降低氣孔導度,而晉麥47和洛旱2號降低幅度較小,即維持相對較高的氣孔導度。Bota等[30?32]的研究也發現,抗旱性較強的品種在脅迫下維持較高的氣孔導度和蒸騰速率以及光合CO2固定能力。Halder等[33?36]將此現象歸因于水分脅迫下氣孔開度減小,蒸騰作用下降,加劇葉綠體光氧化損傷以及葉溫升高導致的高溫損傷。然而,從本研究結果可見,晉麥47和洛旱2號等強抗旱品種在干旱脅迫下氣孔導度降低幅度相對較小,是因為這些品種不以氣孔調節作為關鍵的干旱響應途徑。洛旱2號氣孔導度與敏感品種無差異,但是干旱條件下細胞滲透勢顯著降低,通過加強滲透調節作用減緩原生質的脫水脅迫。同時加強了細胞膜穩定性的調節。晉麥47在干旱脅迫下氣孔導度、細胞滲透勢以及細胞膜穩定性與敏感品種均無顯著差異。但Wang等[37]開展了干旱脅迫下晉麥47蛋白質組學分析,發現抗氧化系統等代謝途徑上的蛋白表達僅微弱上調,但LEA蛋白家族成員和分子伴侶顯著上調,表明干旱脅迫下晉麥47加強脫水保護蛋白的合成以減緩原生質的脫水和維持蛋白質結構與功能是其干旱響應的主要途徑。
農作物以收獲籽粒產量為目標,以產量為核心指標的抗旱指數法鑒定抗旱性可信度最高。但是,其費時費工,不適合大批量品種的鑒定與篩選,因而需要探討可用于大量品種鑒定的可信度高的生理指標。但是,從本研究結果可以看出,不同抗旱品種對干旱脅迫的關鍵響應途徑存在顯著差異。因而,依靠單一生理指標,難以提高抗旱材料鑒選效率和可靠性。因此,需要深入研究品種間干旱脅迫響應的差異及機理,發現可靠的生理指標,建立多指標聯合鑒選體系,發掘優秀抗旱材料。
[1] Sui N,Li M,Tian J C,et al.Photosynthetic characteristics of a super high yield cultivar of winter wheat during late growth period[J].Agricultural Sciences in China,2010,9(3):346-354.
[2] 呂妍,王讓會,蔡子穎.我國干旱半干旱地區氣候變化及其影響[J].干旱區資源與環境,2009,23(11):65-71.
Lv Y,Wang R H,Cai Z Y.Climatic change and influence in arid and semi-arid area of China[J].Journal of Arid Land Resources and Environment,2009,23(11):65-71.(in Chinese)
[3] Wilkinson S,Davies W J.Drought,ozone,ABA and ethylene: new insights from cell to plant to community[J]. Plant Cell & Environment,2010,33(4):510-525.
[4] Lee S C,Luan S.ABA signal transduction at the crossroad of biotic and abiotic stress responses[J].Plant,Cell and Environment, 2012,35(1):53-60.
[5] Hossain Z,Nouri M Z,Komatsu S,et al.Plant cell organelle proteomics in response to abiotic stress[J].Journal of Proteome Research,2012,11(1):37-48.
[6] Chaves M M,Maroco J P,Pereira J S,et al.Understanding plant responses to drought:from genes to the whole plant[J]. Functional Plant Biology,2003,30(3):239-264.
[7] Hare P.Dissecting the roles of osmolyte accumulation during stress[J].Plant Cell Environ,1998,21(6):535-553.
[8] Reddy A R,Chaitanya K V,Vivekanandan M,et al.Drought- induced responses of photosynthesis and antioxidant metabolism in higher plants[J].Journal of Plant Physiology, 2004,161(11):1189-1202.
[9] Mittler R.Oxidative stress,antioxidants and stress tolerance[J]. Trends in Plant Science,2002,7(9):405-410.
[10] Mittler R.Abiotic stress,the field environment and stress combination[J].Trends in Plant Science,2006,11(1):15-19.
[11] Welti R,Li W,Li M,et al.Profiling membrane lipids in plant stress responses:role of phospholipase D alpha in freezing- induced lipid changes in Arabidopsis[J].J Biol Chem, 2002,277:31994-32002.
[12] Hetherington A M,Woodward F I.The role of stomata in sensing and driving environmental change[J].Nature (London),2003,424(6951):901-908.
[13] Belko N,Zaman-Allah M,Cisse N,et al.Lower soil moisture threshold for transpiration decline under water deficit correlates with lower canopy conductance and higher transpiration efficiency in drought-tolerant cowpea[J]. Functional Plant Biology,2012,39(4):306-325.
[14] Kholova J,Hash C T,Kakkera A,et al.Constitutive water- conserving mechanisms are correlated with the terminal drought tolerance of pearl millet[(L.) R.Br.][J].Journal of Experimental Botany,2010,61(2):369-377.
[15] Kholova J,Hash C T,Kumar P L,et al.Terminal drought-tolerant pearl millet[(L.)R.Br.] have high leaf ABA and limit transpiration at high vapour pressure deficit[J].Journal of Experimental Botany,2010, 61(5):1431-1440.
[16] Devi M J,Sinclair T R,Vadez V,et al.Genotypic variation in peanut for transpiration response to vapor pressure deficit [J].Crop Science,2010,50(1):191-196.
[17] Merilo E,Yarmolinsky D,Jalakas P,et al.Stomatal VPD response:there is more to the story than ABA[J].Plant Physiology,2018,176 (1):851-864.
[18] Suzuki M,Umeda H,Matsuo S,et al.Effects of relative humidity and nutrient supply on growth and nutrient uptake in greenhouse tomato production[J].Scientia Horticulturae, 2015,187:44-49.
[19] Talbott L D,Rahveh E,Zeiger E,et al.Relative humidity is a key factor in the acclimation of the stomatal response to CO2[J].Journal of Experimental Botany,2003,54(390): 2141-2147.
[20] Haque M S,Alexandra D S,Cristiano S,et al.Temperature variation under continuous light restores tomato leaf photosynthesis and maintains the diurnal pattern in stomatal conductance[J].Frontiers in Plant Science,2017,8:1602-1615.
[21] Schultz H R.Leaf absorptance of visible radiation inL.:stimates of age and shade effects with a simple field method[J].Scientia Horticulturae(Amsterdam),1996, 66(1-2):93-102.
[22] Condon A G,Richards R A,Rebetzke G J,et al.Improving intrinsic water-use efficiency and crop yield[J].Crop Science, 2002,42(1):122-131.
[23] Lee J C.The stabilization of proteins by sucrose[J].Journal of Biological Chemistry,1981,256(14):7193-7201.
[24] Nambara E,Kawaide H,Kamiya Y,et al.Characterization of an Arabidopsis thaliana mutant that has a defect in ABA accumulation:ABA-dependent and ABA-independent accumulation of free amino acids during dehydration[J]. Plant & Cell Physiology,1998,39(8):853-858.
[25] Berglund A H,Norberg P,Quartacci M F,et al.Properties of plant plasma membrane lipid models-bilayer permeability and monolayer behaviour of glucosylceramide and phosphatidic acid in phospholipid mixtures[J].Physiologia Plantarum,2010,109(2):117-122.
[26] Cooke D T,Burden R S.Lipid modulation of plasma membrane-bound ATPases[J].Physiologia Plantarum,1990, 78(1):153-159.
[27] Liljenberg C,Kates M.Changes in lipid composition of oat root membranes as a function of water-deficit stress[J]. Biochemistry and Cell Biology,1985,63(2):77-84.
[28] Gill S S,Tuteja N.Reactive oxygen species and antioxidant machinery in abiotic stress tolerance in crop plants[J].Plant Physiology and Biochemistry,2010,48(12):909-930.
[29] Jiang M.Water stress-induced abscisic acid accumulation triggers the increased generation of reactive oxygen species and up-regulates the activities of antioxidant enzymes in maize leaves[J].Journal of Experimental Botany,2002,53 (379):2401-2410.
[30] Bota J,Flexas J,Medrano H,et al.Genetic variability of photosynthesis and water use in Balearic grapevine cultivars [J].Annals of Applied Biology,2001,138(3):353-361.
[31] Saeidi M,Abdoli M.Effect of drought stress during grain filling on yield and its components,gas exchange variables, and some physiological traits of wheat cultivars[J].Journal of Agricultural Science and Technology,2015,17(4):885-898.
[32] Ratnayaka I,B?ga M,Fowler D B,et al.Construction and characterization of a BAC library of a cold-tolerant hexaploid wheat cultivar[J].Crop Science,2005,45(4): 1571-1577.
[33] Turan,Ekmekci Y.Activities of photosystem II and antioxidant enzymes in chickpea(L.) cultivars exposed to chilling temperatures[J].Acta Physiologiae Plantarum,2011,33(1):67-78.
[34] Zhang J,Kirkham M B.Drought-stress-induced changes in activities of superoxide dismutase,catalase,and peroxidase in wheat species[J].Plant and Cell Physiology,1994,35(5): 785-791.
[35] 毛浩田,陳夢瑩,吳楠,等.干旱脅迫對不同倍性小麥和八倍體小黑麥苗期光合能力與抗氧化系統的影響[J].麥類作物學報,2018,38(10):114-122.
Mao H T,Chen M Y,Wu N,et al.Effects of drought stress on photosynthetic capacity and antioxidant system in wheat with different ploidy levels and octoploid triticale at seedling stage[J].Journal of Triticeae Crops,2018,38(10): 114-122.(in Chinese)
[36] Halder K P,Burrage S W.Drought stress effects on water relations of rice grown in nutrient film technique[J].Pakistan Journal of Biological Sciences,2003,6(5):441-444.
[37] Wang Y,Zhang X,Huang G,et al.iTRAQ:based quantitative analysis of responsive proteins under peg-induced drought stress in wheat leaves[J].International Journal of Molecular Sciences,2019,20(11):2621-1640.
Cultivar Differences in Yield and Physiological Response of Winter Wheat after Exposed to Drought Stress at Jointing Stage
FENG Fu, HUANG Gui-rong, WANG Ya-jing, ZHANG Xin-ying, WANG Tao, ZHONG Xiu-li
(Institute of Environment and Sustainable Development in Agriculture, Chinese Academy of Agricultural Sciences/Key Laboratory of Dryland Agriculture, Ministry of Agriculture, Beijing 100081, China)
Drought stress occurring at jointing stage has been restricted winter wheat production severely. This study explored the genotypic difference in physiological response to drought, aiming at providing informative guidance for selection and breeding of drought tolerant cultivars. Five cultivars, which were planted in larger areas in different regions of the North China Plain, and one stress sensitive cultivar were selected as materials. Pot cultivation and rain-shelter were adopted to carry out the experiment. In terms of grain yield, as well as stomatal traits, cellular membrane stability, and osmoregulation traits, genotypic difference in drought tolerance along with the drought response pathways after suffering drought stress at jointing stage were compared and analyzed. Under well-watered condition, winter wheat cultivars Jinmai 47, Luohan 2, and Shijiazhuang yielded higher, while Yuami 18 and Yanmai 20 yielded lower, with Zhengmai 9023 moderately yielding. Encountering drought stress at jointing stage, Jinmai 47, Luohan 2, and Yumai 18 yielded higher, in comparison, Shijiazhuang 8 and Yanmai 20 yielded lower, with Zhengmai 9023 moderately yielding. Being evaluated drought tolerance in term of yield after suffering from drought stress, Jinmai 47, Luohan 2, and Yumai 18 were cultivars of higher drought tolerance, while Shijiazhuang 8 and Yanmai 20, lower drought tolerance, and Zhengmai 9023, moderate drought tolerance. The 3 drought tolerant cultivars markedly differed in the key pathways of physiological responses to drought stress. Compared with lower drought tolerant cultivars, Shijiazhuang 8 and Yanmai 20, after exposed to drought stress at jointing stage, Yumai 18 showed significantly lower stomatal conductance, indicating its higher stomatal regulation ability; Luohan 2 had lower cellular osmotic potential, indicating its higher osmotic adjustment capability; Luohan 2 also had lower membrane ion leakage, showing stronger membrane stability; Jinmai 47 showed no significant difference from the lower drought tolerant cultivars in stomatal regulation, osmotic adjustment, and membrane stability. The significant difference among cultivars in the critical pathways of physiological response to drought stress suggested that drought tolerance of wheat cultivars can not be scientifically evaluated through sole physiological index, but through multiple indices.
Winter wheat; Yield; Drought tolerance; Stomatal regulation; Cellular osmotic adjustment; Membrane stability
10.3969/j.issn.1000-6362.2020.01.005
封富,黃桂榮,王雅靜,等.拔節期干旱脅迫下冬小麥品種間產量及生理響應的差異[J].中國農業氣象,2020,41(1):43-50
2019?07?08
鐘秀麗,E-mail:zhongxiuli@caas.cn
國家十三五重點研發計劃課題“化肥減施增效共性技術與評價研究”(2017YFD0201702)
封富,E-mail:82101176076@caas.cn

