多囊卵巢綜合征相關雄性激素的液相色譜-串聯質譜檢測
曹 正,劉 穎,叢宇婷,盧一凡,董 瑩,劉京瑞,唐國棟,3,翟燕紅*
(1.首都醫科大學 附屬北京婦產醫院 檢驗科,北京 100020;2.上海愛博才思分析儀器貿易有限公司,上海 200050;3.北京市海淀區婦幼保健院 產前診斷中心,北京 100080)
多囊卵巢綜合征(PCOS)是一種常見的婦科內分泌疾病,起病多見于青春期,臨床上多以月經不調為主要癥狀,可有不孕[1]、多毛痤瘡、肥胖、黑棘皮癥等多種不同臨床表現[2]。一直以來,PCOS病因未明且缺乏統一的診斷標準[3],給臨床工作造成諸多不便。美國生殖醫學學會與歐洲人類生殖和胚胎學會于2003年修訂PCOS診斷標準[4]:① 稀發排卵或無排卵;② 高雄性激素的臨床或生化表現;③ 經超聲提示單側或雙側卵巢多囊性改變。凡符合上述三條標準中的兩條,并排除其他疾病導致的類似臨床表現即可診斷為PCOS。
高雄性激素血癥被普遍認為是PCOS關鍵的病理生理改變[5],對雄性激素的檢測是臨床診斷PCOS的重要指標[6]。在女性體內存在多種雄性激素,其中,睪酮(T)的血清水平高于其他雄性激素,是PCOS中主要的病源性雄性激素[7]。目前,臨床大多依靠檢測睪酮血清水平判斷患者是否存在高雄性激素血癥[5]。對睪酮的檢測主要有總睪酮(TT)和游離睪酮(FT),其中在人體中發揮有效生物活性的是FT[8]。美國近期的最佳實踐總結中認為FT是診斷女性雄性激素過剩最敏感的指標[7-9]。臨床對FT的直接測定具有較多限制且結果的靈敏度和準確性較低。但可通過檢測TT進而計算FT含量[10]。此外,硫酸脫氫表雄酮(DHEAS)、雄烯二酮(A4)、17-羥基孕酮(17-OHP)、雙氫睪酮(DHT)也是人體內重要的雄性激素類型,一些研究表明,這些激素的血清水平在PCOS患者與正常人群中存在差別[7],可為PCOS的診斷提供參考。50%的PCOS病人會出現血清DHEAS水平的升高,其中5%的患者有且只有DHEAS這一種雄性激素特異性升高”[11],同時檢測T和DHEAS可以提高PCOS的診斷率。A4是T的直接前體,因此往往在評估高雄性激素血癥時會檢測A4,據報道,雄性激素檢測中如果加入A4,大約可以提高9%的PCOS檢出率[9];DHT是睪酮經過5α-Reductase作用轉化而來,其雄性激素活力最強,因此在睪酮水平正常的PCOS病人中,檢測DHT能夠幫助解釋局部目標組織中雄性激素活性過高的現象[9];17-OHP是類固醇合成通路中的中間物質,同時也是鹽皮質激素和雄性激素的前體[9],其血清水平在非典型腎上腺皮質增生(Non-classic CAH)病人中異常升高,因此17-OHP被許多相關專業學會推薦用于PCOS病患診斷,以排除 Non-classic CAH[7,9]。
臨床實驗室多采用自動化免疫法檢測雄性激素,但其特異性差,易受溫度、pH值、離子強度、試劑免疫活性、異噬性抗體等因素干擾而造成假陽性或假陰性結果,特異性和準確性有待提高[12-13]。近年來液相色譜-串聯質譜技術(LC-MS/MS)開始應用于雄性激素的檢測,其因所需樣本量少,可同時檢測多種物質,且精密度和準確性高,被認為是雄性激素檢測的“金標準”[14]。有指南建議,在PCOS診斷中,將LC-MS/MS應用于臨床高雄性激素血癥的檢測,此前有將T和DHT、T和A4進行聯合檢測的報道,其研究結果表明聯合檢測能達到較好的特異性和精確性[15-16],但目前對上述5種雄性激素進行聯合檢測的報道較少。本研究建立了液相色譜-串聯質譜法聯合檢測DHEAS、A4、T、17-OHP、DHT 5種雄性激素的方法。
1 實驗部分
1.1 儀器與試劑
AB SECIX TRIPLE QUADTM5500 三重四級桿串聯質譜儀,配有電噴霧離子源(ESI)以及Analyst 1.4.1數據處理軟件(美國 Applied Biosystem 公司);島津高效液相色譜系統(日本)。96孔蛋白沉淀板(Agela Cleanert Protein Precipitation Plate,CAT#96CD2025-Q),96孔PEP板(Agela Cleanert PEP 96 Well Microplates,CAT#PE00501-MW)。
甲醇、乙腈(Optima@LC/MS,4 L,美國Fisher Scientific公司);標準品:T、A4、DHEAS、DHT、17-OHP均為1.0 mg/mL,1 mL/支;睪酮內標(T-C3)、雄烯二酮內標(A4-C3)、硫酸脫氫表雄酮內標(DHEAS-D5)、雙氫睪酮內標(DHT-C3)、17-羥基孕酮內標(17-OHP-C3)均為100 μg/mL,1 mL/支;上述標準品和內標均購自美國Cerilliant公司。
1.2 實驗條件
1.2.1 色譜條件色譜柱:Agela Venusil MP C18(3.0 mm×50 mm,3 μm),流動相A:蒸餾水(含0.02%甲酸),流動相B:甲醇(含0.1%甲酸),采用梯度洗脫,梯度洗脫程序為:0~0.5 min,55% B;0.5~3.5 min,55%~90% B;3.5~4.5 min,90% B;4.5~4.6 min,90%~55% B;4.6~6.0 min,55% B,流速0.6 mL/min,柱溫40 ℃,進樣量10 μL。
1.2.2 質譜條件離子源為電噴霧離子源(ESI),檢測方式為正-負離子多反應監測模式(MRM)。電噴霧電壓(IS)為5 500 V;霧化溫度(TEM)為550 ℃;碰撞氣(CAD)為8 L/min;氣簾氣(CUR)為35 L/min。霧化氣(GS1)為80 L/min;輔助加熱氣(GS2)為70 L/min。5種雄性激素的質譜參數見表1,選取Q1質量數為母離子,Q3質量數為子離子進行定量分析。
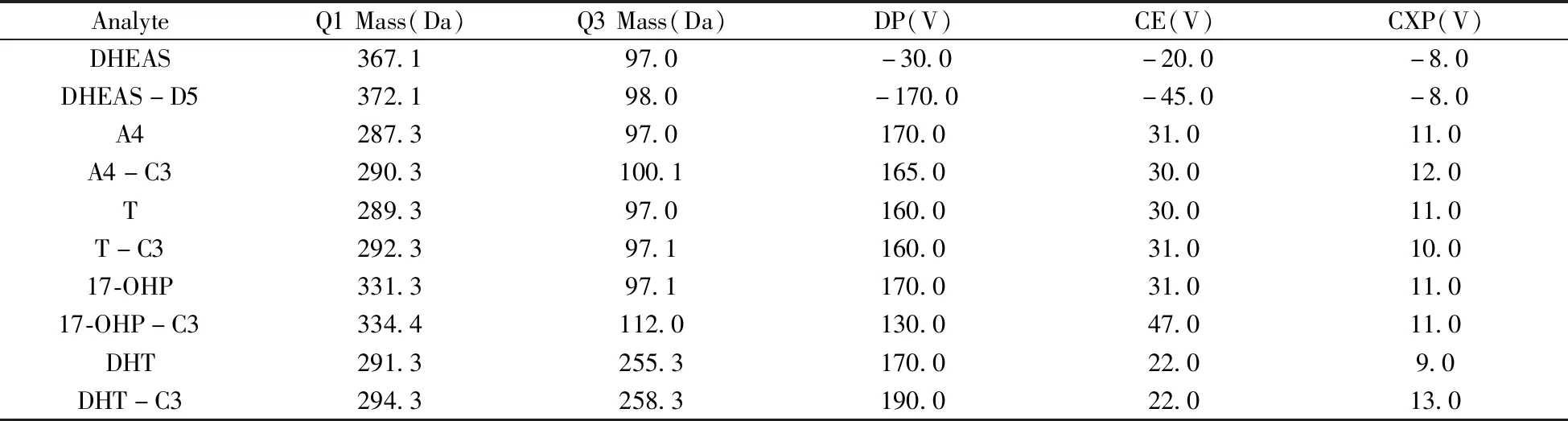
表1 5種雄性激素的質譜參數
*DP:declustering potential;CE:collision energy;CXP:collision cell exit potential
1.3 標準溶液的配制
取適量標準品,用甲醇定容后,用甲醇稀釋成不同質量濃度的系列混合標準溶液。稀釋后A4的質量濃度0.10、0.20、0.40、1.20、6.00、12.00 ng/mL,T、DHT和17-OHP為0.05、0.10、0.20、0.60、3.00、6.00 ng/mL,DHEAS為10.00、20.00、40.00、120.00、600.00和1 200.00 g/mL,上述即為標準曲線C1~C6標準溶液,將標準溶液置于-20℃保存,使用前取出在室溫下放置0.5 h,混勻后,即可進樣分析。DHEAS、A4、T、17-OHP和DHT的內標用甲醇乙腈(1∶1)分別稀釋至5.00、2.00、10.00、2.00、20.00 ng/mL。
1.4 樣本前處理
取50 μL血清樣品,加入10 μL內標溶液和150 μL甲醇,振搖2 min,過蛋白沉淀板,加入150 μL水,振搖1 min。200 μL甲醇和200 μL水活化PEP板,加載樣品,分別經200 μL的 20%乙腈、正己烷淋洗后,用50 μL甲醇洗脫,在洗脫液中加入50 μL水渦旋混勻,取10 μL上機檢測。
2 結果與討論
2.1 實驗條件的優化
2.1.1 前處理方法的優化因雄性激素在體內的含量均較少,因此對樣本的前處理關系到實驗結果的準確性。實驗對比了蛋白沉淀法和固相萃取法,其中前者快速、簡便,但處理的樣品凈化程度低,對于體內含量較少的雄性激素并不是最優方法。本實驗采用蛋白沉淀+固相萃取的方法對樣本進行前處理,將已經進行蛋白沉淀的樣品通過萃取柱,可有效去除樣品基質中的干擾物,濃縮目標分析物,提高檢測靈敏度,減少基質效應,適用于對雄性激素的檢測。
2.1.2 色譜-質譜條件的優化考察了甲醇、乙腈、甲醇-乙腈混合物分別與水、0.1%甲酸、0.02%甲酸組成的不同流動相對5種雄性激素的分離效果及色譜圖峰形的影響。在對比了不同流動相以及加入甲酸前后的分離結果后,最終選擇甲醇與水為流動相體系,并分別加入0.1%甲酸和0.02%甲酸,以使目標分析物的響應強度得到明顯提高,且所得峰形良好。進一步考察了不同柱溫下(35、40、45 ℃)5種雄性激素的響應強度及分離情況,結果表明在柱溫40 ℃下,可得到較理想的實驗結果。
采用ESI正-負離子電離模式掃描分析,在一級質譜分析確定母離子后,進行二級質譜的子離子分析掃描,對去簇電壓(DP)、碰撞能量(CE)以及碰撞室出口電壓(CXP)進行優化,優化后的質譜條件見表1。此時各雄性激素的檢測信號高,峰形良好。
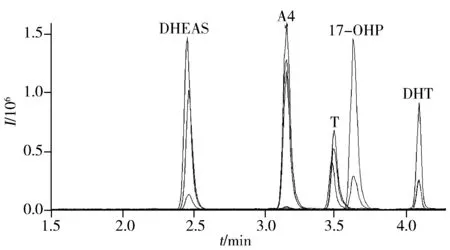
圖1 5種雄性激素的色譜圖
在優化條件下,5種雄性激素的色譜圖見圖1。從圖中可觀察到各雄性激素的色譜圖清晰,峰形良好,在相關保留時間附近無干擾峰,DHEAS、A4、T、17-OHP和DHT的保留時間分別為2.47、3.15、3.49、3.63、4.08 min,表明各雄性激素可在5 min內完成分離檢測。
2.2 線性關系、定量下限及相對標準偏差
將標準溶液按照正常樣本進行處理后進樣分析,考察各雄性激素的線性關系。以樣品中待測物的質量濃度為橫坐標(X,ng/mL),待測物和內標物的峰面積比值作為縱坐標(Y),用加權(1/X2)最小二乘法進行回歸計算,得到回歸方程。結果顯示(見表2),5種雄性激素在一定質量濃度范圍內線性關系良好,相關系數(r2)均大于0.995。以信噪比(S/N)=10,相對標準偏差(RSD)小于20%作為各成分的定量下限(LOQ),計算得到5種雄性激素的LOQ為0.025~5.00 ng/mL,RSD均小于20%,滿足統計學要求。
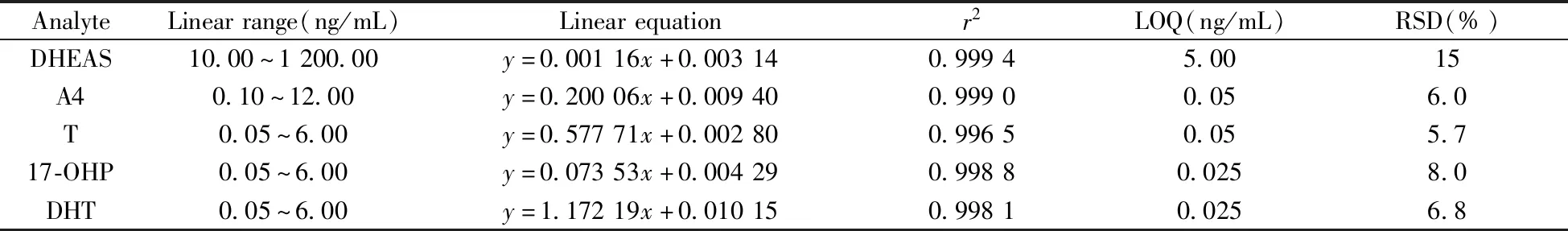
表2 5種雄性激素的線性范圍、相關系數、定量下限及相對標準偏差
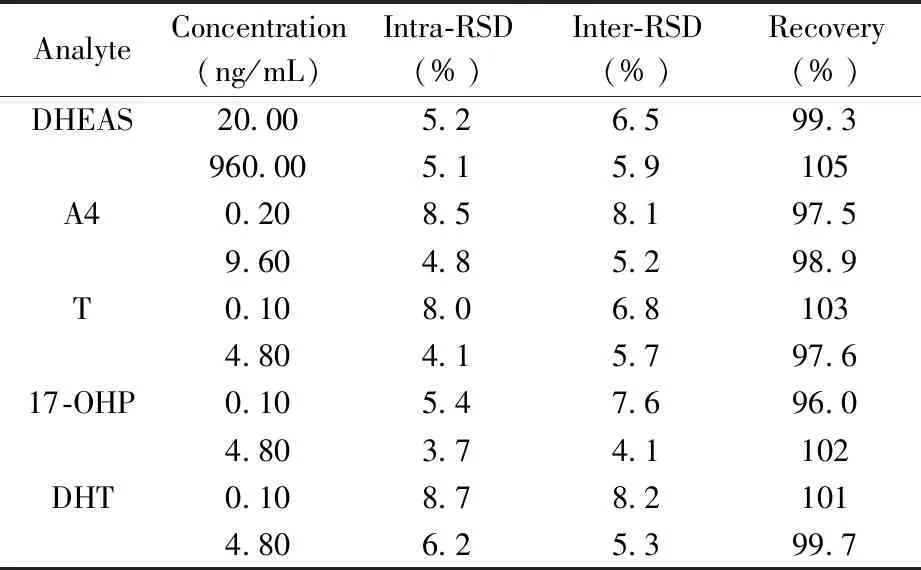
表3 5種雄性激素的批內相對標準偏差、批間相對標準偏差及回收率
2.3 相對標準偏差與加標回收率
以5個患者血清混合作為本底,取40 μL混合人血清與一定量的雄性激素標準溶液混合,制成低、高濃度的質控血清(具體濃度見表3)。在1天內分別對低、高2個濃度水平的質控血清進行10次重復處理,檢測5種雄性激素含量,計算批內相對標準偏差(Intra-RSD);對低、高2個濃度水平的質控血清測定5次,連續測定5 d(n=25),檢測5種雄性激素含量,計算批間RSD(Inter-RSD),觀察精密度,同時計算加標回收率。結果顯示,5種雄性激素的批內RSD為3.7%~8.7%,批間RSD為4.1%~8.2%,加標回收率為96.0%~105%,表明本方法對不同質量濃度標本檢測均具有較好的精密度和準確度。
2.4 樣本的穩定性
取未處理血清樣本,在4 ℃下保存3 d,分別于第0、1、3 d按本方法檢測雄性激素的含量;將第0 d處理后的樣本于15 ℃下放置3天,分別于第0、1、3 d檢測雄性激素含量,將檢測值與第0 d的結果作比較,觀察樣本穩定性。檢測結果顯示(見表4),按本方法處理后的雄性激素樣本,在4 ℃與15 ℃下的穩定性均在80%~120%范圍內,說明本方法的穩定性良好。

表4 5種雄性激素的穩定性
2.5 臨床樣本的檢測
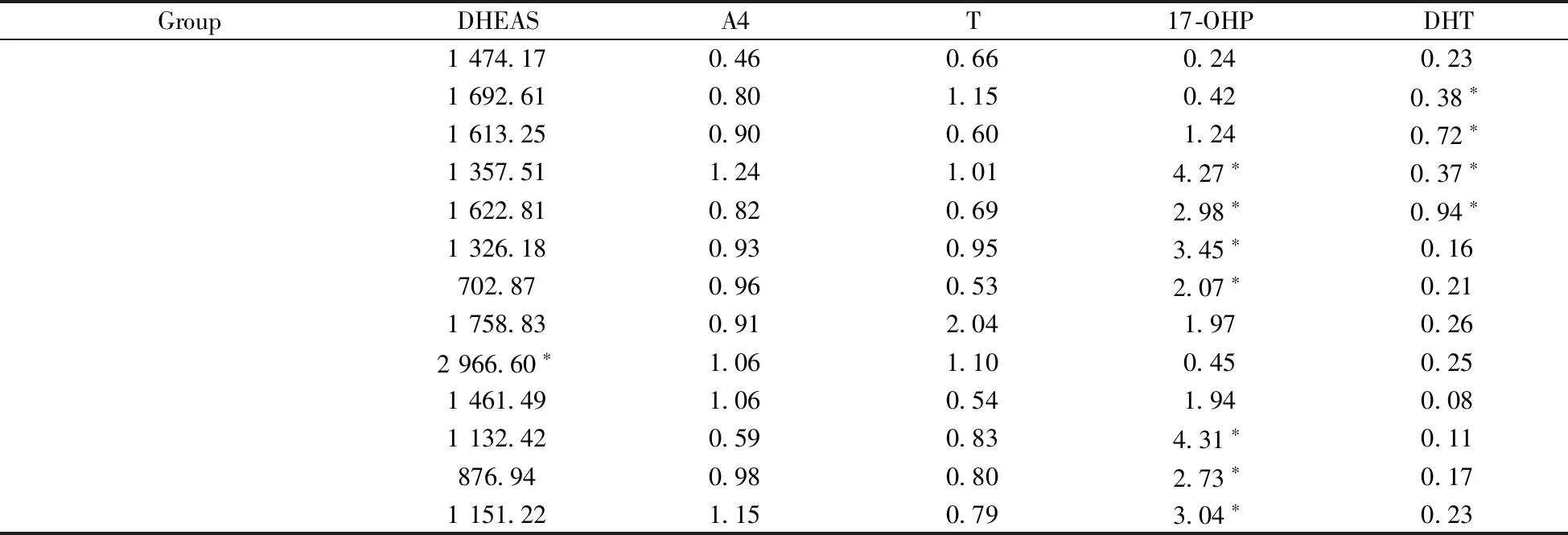
3組不同臨床血清樣本(PCOS病人-血清型高雄性激素、PCOS病人-臨床型高雄性激素、非PCOS-正常女性)各20例,采用上述方法進行樣本前處理,并對血清中DHEAS、A4、T、17-OHP 、DHT進行聯合檢測,以觀察此方法在臨床中的實際應用價值。結果顯示,對PCOS病人中血清型高雄性激素及臨床型高雄性激素患者的檢出率均大于90%,與單純檢測一種雄性激素相比,檢測的精確度與準確性大大提升,在一定程度上解決了女性體內雄性激素水平低、檢測難的問題(見表5)。研究結果表明,利用本方法進行上述5種雄性激素的聯合檢測,對臨床診斷高雄性激素血癥及PCOS病人具有較高的應用價值。
(續表5)
GroupDHEASA4T17-OHPDHT1474.170.460.660.240.231692.610.801.150.420.38?1613.250.900.601.240.72?1357.511.241.014.27?0.37?1622.810.820.692.98?0.94?1326.180.930.953.45?0.16702.870.960.532.07?0.211758.830.912.041.970.262966.60?1.061.100.450.251461.491.060.541.940.081132.420.590.834.31?0.11876.940.980.802.73?0.171151.221.150.793.04?0.23
reference interval:DHEAS:280.00~2 500.00 ng/mL,A4:0.30~2.00 ng/mL,T:0.08~6.00 ng/mL,17-OHP:<2.00 ng/mL,DHT:<0.3 ng/mL
3 結 論
本研究建立了LC-MS/MS聯合檢測血清中DHEAS、A4、T、17-OHP、DHT的分析方法,討論了LC-MS/MS法在臨床中高雄性激素血癥診斷中的應用價值,從而為PCOS的診療提供依據。實驗結果表明,本方法快速簡便,具有較高的精確性和準確性,可保證在血清濃度較低的條件下獲得較為理想的檢測結果,滿足臨床大量檢測的需求,對臨床高雄性激素血癥和PCOS的診斷具有重要意義。

