右歸丸對激素抵抗型腎病綜合征大鼠腎臟組織中JNK/p38信號通路的影響*
王新斌,戴恩來,薛國忠,呂 娟,陳威辛
(甘肅中醫藥大學中西醫結合學院 蘭州 730000)
激素抵抗型腎病綜合征(steroid- resistant nephrotic syndrome,SRNS)是指經規范化激素治療無效的腎病綜合征,屬于難治性腎病綜合征(refractory nephrotic syndrome,RNS)的一種類型[1],是臨床慢性腎臟病中治療最為棘手,預后較差的病種。盡管對SRNS 從B 淋巴細胞抑制、抑制纖維化、基因突變等角度的治療有了一定的進展,但臨床療效仍不盡如人意,且副作用堪憂,故進一步探究SRNS 發病機制,尋找新型藥物治療具有重要的臨床意義。JNK、p38為絲裂原活化蛋白激酶(Mitogen-activated protein kinase,MAPK)家族成員,研究顯示,激活JNK/p38 信號通路后,可誘導腎組織纖維細胞增生,加重腎間質損傷,導致腎間質纖維化、腎衰竭,提示JNK/p38信號通路可能為SRNS 潛在治療靶點[2-3]。右歸丸是由炮附片、熟地黃、肉桂、酒萸肉和山藥等中藥組成,具有填精止遺、溫補腎陽之功效,臨床用于治療慢性腎衰、腎病綜合癥等腎病[4]。本研究通過建立SRNS 動物模型,給予右歸丸干預,旨在探究右歸丸對SRNS 大鼠腎組織的保護作用及可能的作用機制。
1 材料與方法
1.1 實驗動物
SPF 級Wisar 大鼠60 只,雄性,8 周齡,體重(200±10)g,由甘肅中醫藥大學科研實驗中心提供,動物合格證號:6200100000025,許可證號:SCXK(甘)2015-0002。動物飼養于SPF實驗中心,室溫22℃,輻照滅菌SPF級大鼠飼料喂養,給藥前禁食12 h,自由飲水。
1.2 藥物
阿霉素(AD,Solarbio,批號17C024,規格:25 mg/支);醋酸潑尼松片(浙江仙據制藥股份有限公司,批號170146,規格:5 mg/片);右歸丸(北京同仁堂股份有限公司同仁堂制藥廠,批號170528規格:9 g/丸),藥物成分:綠原酸、莫諾苷松、脂醇二葡萄糖苷、馬錢苷、阿魏酸、肉桂酸(見圖1)。
1.3 主要試劑及儀器
肌酐檢測試劑盒(批號:YZB/GER2659-2018);尿素氮檢測試劑盒(批號:YZB/GER0315-2018);總蛋白檢測試劑盒(批號:YZB/GER3253-2018);白蛋白檢測試劑盒(批號:YZB/GER1029-2018);甘油三酯檢測試劑盒(批號:YZB/GER5264-2018);膽固醇檢測試劑盒(批號:YZB/GER1324-2018)均購自Roche Diagnostics GmbH 公司;Masson 染色試劑盒(貨號:G1340)購于美國Solarbio 公司;PAS 染色試劑盒(貨號:DG0007)購自北京雷根生物技術有限公司;HE 染色試劑盒(貨號:C0105)購自碧云天生物技術公司;兔抗鼠Caspase-3(ab179517)、Bcl-2(ab185002)、Bax(ab53154)、β-actin(ab179467)、轉化生長因子-β1(transforming growth factor-β,TGF-β1)(ab92486)、結 締 組 織 生 長 因 子(connective tissue growth factor,CTGF)(ab231824)單 抗抗體購于英國Abcam 公司;p-JNK(AF1205)、JNK(MAB1387)、p-p38(AF8691)、p38(MAB8691)、HRP標記二抗(HAF007)購于美國R&D 公司;光學顯微鏡(日本Olympus 公司,型號CX41);全自動生化儀(上海科華卓越生物工程股份有限公司,型號:450);凝膠成像儀(美國Bio-Rad公司,型號:Gel Doc XR+)。

圖1 HPLC色譜圖
1.4 實驗分組與給藥
1.4.1 模型制備
將60 只雄性SPF 級Wisar 大鼠適應性飼養1 周,隨機分為正常組(10 只)和造模組(50 只)。參照文獻法[5],建立激素抵抗型腎病綜合征大鼠模型,造模組大鼠一次性尾靜脈注射阿霉素(6 mg·kg-1)建立激素抵抗型腎病綜合征大鼠模型,大鼠尾部未發生腫脹、迂曲,表明注射成功;正常組(Control)大鼠注射等劑量生理鹽水。
1.4.2 動物給藥
造模成功后采用隨機數字表法分為模型組、激素治療組(潑尼松片,Prednisone)、激素聯合右歸丸低、中、高組(TL、TM、TH),每組10 只大鼠。依據人與大鼠體表面積換算法計算用藥量。Control 組和Model組:給予等體積生理鹽水灌胃;Prednisone 組:給予潑尼松片混懸液灌胃,劑量為6.3 mg·kg-1·d-1;Prednisone聯合右歸丸低、中、高劑量組:給予潑尼松混合右歸丸的混懸液灌胃,劑量分別為6.3/11600mg·kg-1·d-1、6.3/5600 mg·kg-1·d-1、6.3/2800 mg·kg-1·d-1,連續6周。
1.5 樣本采集、處理
給藥2周、4周、6周,收集大鼠24 h尿液,3000 g離心5 min 后,收集上清液,用于檢測24 h 尿蛋白量。末次治療結束后,將大鼠麻醉處死,收集血液5000 g,離心5 min,收集上清,在-80℃中保存;收集腎組織,平均分為2 部分,一部分置于4%多聚甲醛中固定,常規制備石蠟切片,用于病理觀察以及免疫組化檢測;一部分保存于-80℃用于蛋白檢測。
1.6 檢測指標與方法
1.6.1 大鼠一般狀態
給藥期間,觀察大鼠毛發、進食量、精神、大便、體重情況等。
1.6.2 血清中血脂、腎功能相關指標檢測
參照試劑盒檢測血清中肌酐(Serum creatinine,Scr)、尿素氮(Blood urea nitrogen,BUN)、總蛋白(Total protein,TP)、白 蛋 白(Albumin,ALB)、甘 油 三 酯(Triglyceride,TG)、膽固醇(Total Cholesterol,TC)水平,具體參考試劑盒說明書進行操作,于自動生化檢測儀進行測定。24 h 尿蛋白量采用鄰苯三酚紅/鉬酸鹽比色法檢測。
1.6.3 腎組織病理形態學檢測
腎組織經洗滌、脫水、透明、浸蠟、包埋、切片后行HE、PAS、Masson 染色,光學顯微鏡下觀察腎臟的病理形態學變化。采用半定量積分法對腎組織損傷情況進行評定,主要從腎小球硬化程度、腎小管間質損傷程度方面進行評分,每個大鼠至少評價20 個腎小球(皮質區域),每項評分為0 ~4 分,評分越高代表損傷越嚴重。Masson 染色:膠原纖維染色為藍色,肌纖維染色為暗紅色,采用IPP6.0 分析Masson 染色膠原纖維面積比,膠原纖維比例=染藍區域面積/總面積×100%。
1.6.4 TUNEL原位凋亡檢測腎組織細胞凋亡情況
制備腎組織冷凍切片,50 μL 蛋白酶K,37℃孵育20 min,加入Tunel反應液,于37°C的加濕室中孵育1 h,PBS 緩沖液清洗后,添加過氧化物酶結合抗體在37°C孵育1 h,DAB 染色后用蘇木精復染,脫水、封片后,在顯微鏡下觀察細胞凋亡情況,凋亡細胞核染色呈棕色。用Image-J 軟件定量分析細胞凋亡率,細胞凋亡率(%)=棕色細胞數/細胞總數×100%。
1.6.5 免疫印跡法檢測腎組織中JNK/p38 信號通路、凋亡蛋白表達
取適量腎組織,添加RIPA裂解液冰上反應30 min,提取腎組織總蛋白,BCA 檢測蛋白含量,取50ug 蛋白樣品進行SDS-PAGE 電泳,轉移至PVDF 膜上,封閉后加入兔抗鼠TGF-β1、CTGF、Caspase-3、Bcl-2、Bax、βactin、p-JNK、JNK、p-p38、p38 一抗(1:500),4℃搖床孵育過夜,PBS 緩沖液清洗后,,加入HRP 標記二抗孵育膜(1:5000),清洗后,于膜上加入ECL 反應液5 min后進行曝光、顯影,用凝膠成像儀采集、保存圖像,以β-actin 為內參,采用Image-J 軟件定量分析各蛋白相對表達量。
1.7 統計學分析
本研究數據采用SPSS 22.0軟件進行分析,計量資料以平均數±標準差(±s)描述,多組間比較行單因素方差分析,進一步兩兩對比采用SNK-q 檢驗,當P<0.05時,則差異具有統計學意義。
表1 各組大鼠體重變化情況比較(±s,g)
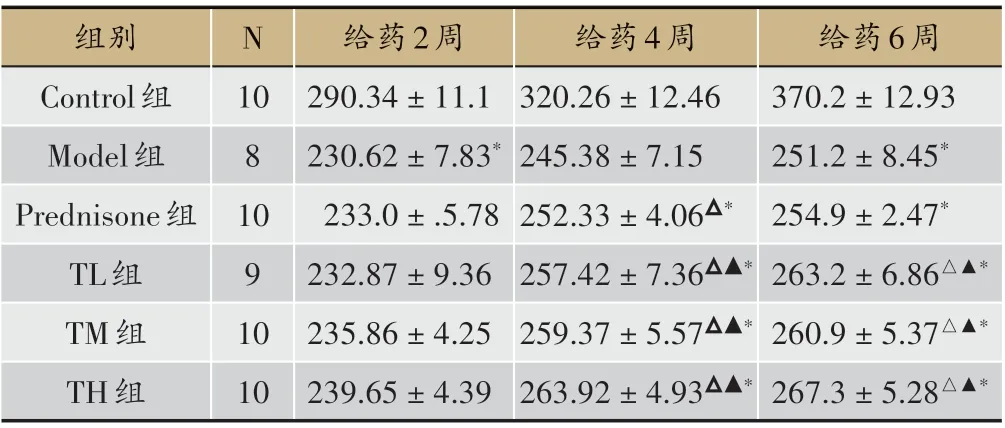
表1 各組大鼠體重變化情況比較(±s,g)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
給藥6周370.2±12.93 251.2±8.45*254.9±2.47*263.2±6.86△▲*260.9±5.37△▲*267.3±5.28△▲*組別Control組Model組Prednisone組TL組TM組TH組N 10 8 10 9 10 10給藥2周290.34±11.1 230.62±7.83*233.0±.5.78 232.87±9.36 235.86±4.25 239.65±4.39給藥4周320.26±12.46 245.38±7.15 252.33±4.06△*257.42±7.36△▲*259.37±5.57△▲*263.92±4.93△▲*
表2 各組24 h尿蛋白量比較(±s,mg)
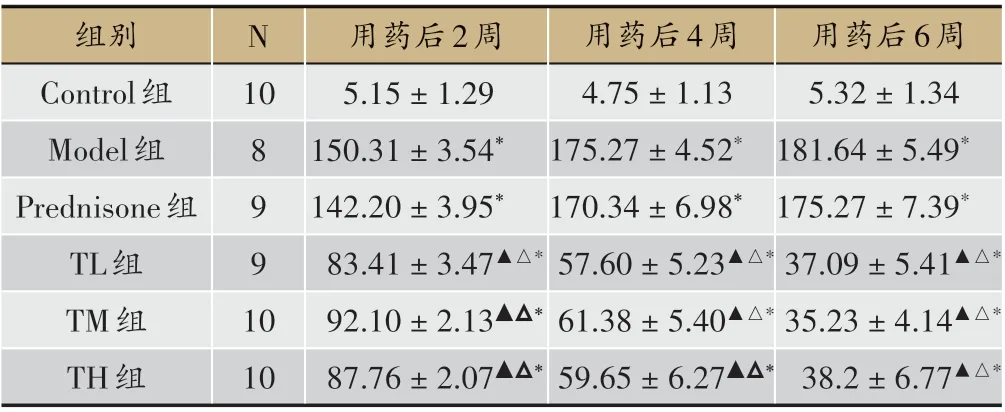
表2 各組24 h尿蛋白量比較(±s,mg)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
用藥后6周5.32±1.34 181.64±5.49*175.27±7.39*37.09±5.41▲△*35.23±4.14▲△*38.2±6.77▲△*組別Control組Model組Prednisone組TL組TM組TH組N 10 8 9 9 1 0 10用藥后2周5.15±1.29 150.31±3.54*142.20±3.95*83.41±3.47▲△*92.10±2.13▲△*87.76±2.07▲△*用藥后4周4.75±1.13 175.27±4.52*170.34±6.98*57.60±5.23▲△*61.38±5.40▲△*59.65±6.27▲△*
2 結果
2.1 各組大鼠一般情況
Control 組大鼠精神狀態良好,反應靈敏,毛發光滑發亮,進食正常。造模后第7 d 大鼠出現尿量減少并伴有少量的腹水,精神狀態日漸萎靡,進食減少,體重下降。1-2 周大鼠腹水顯著增多,24 h 尿蛋白增多;大鼠出現嗜睡、反應遲鈍,有弓背聳肩現象,蜷臥少動,體毛發灰發暗,大便稀溏等體征。Control 組無大鼠死亡;Model組2只大鼠因腹水、進食減少死亡,死亡率20%(2/10)。TL 組、TM 組、TH 組各有1 只因腹水、體重下降而死亡,Prednisone 組1 只死亡。與Model 組相比,TL 組、TM 組、TH 組、Prednisone 組大鼠活躍度增加,精神好轉,毛發漸有光澤。隨著給藥時間的延長,大鼠體重逐漸增加,給藥2周,與Control組相比,Model組體重降低;給藥4 周、6 周,與Model 組、Prednisone 組相比,TL 組、TM 組、TH 組組體重升高,差異均有統計學意義(P<0.05)(見表1)。
2.2 各組大鼠尿蛋白定量變化
與Control組相比,Model組24 h尿蛋白量升高,差異有統計學意義(P < 0.05)。與Model、Prednisone 組相比,TL 組、TM 組、TH 組24 h 尿蛋白量降低,差異有統計學意義P<0.05)(見表2)。
表3 各組血清腎功能、血脂水平比較(±s)
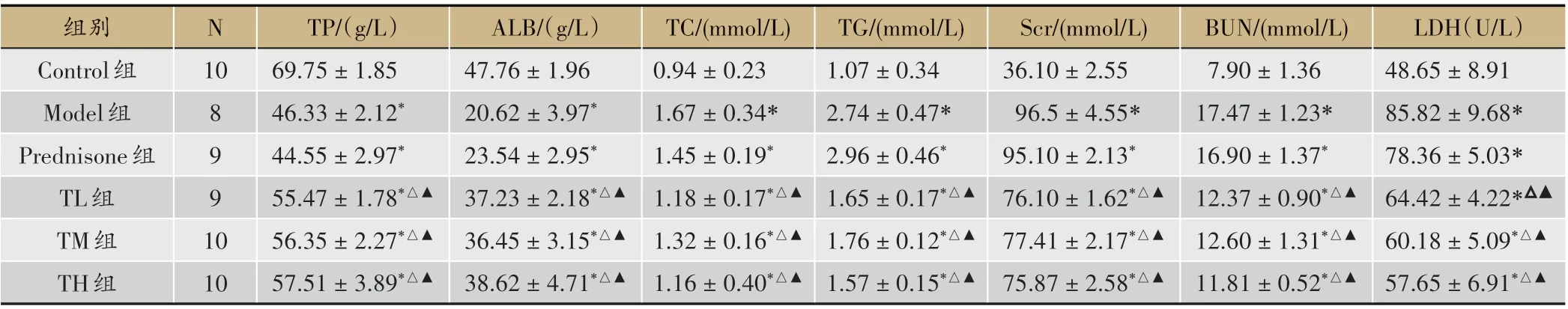
表3 各組血清腎功能、血脂水平比較(±s)
注:與Control組比較,*P<0.05;與Model組比較,△P<0.05;與Prednisone組比較,▲P<0.05
LDH(U/L)48.65±8.91 85.82±9.68*78.36±5.03*64.42±4.22*△▲60.18±5.09*△▲57.65±6.91*△▲組別Control組Model組Prednisone組TL組TM組TH組N 10 8 9 9 1 0 10 TP/(g/L)69.75±1.85 46.33±2.12*44.55±2.97*55.47±1.78*△▲56.35±2.27*△▲57.51±3.89*△▲ALB/(g/L)47.76±1.96 20.62±3.97*23.54±2.95*37.23±2.18*△▲36.45±3.15*△▲38.62±4.71*△▲TC/(mmol/L)0.94±0.23 1.67±0.34*1.45±0.19*1.18±0.17*△▲1.32±0.16*△▲1.16±0.40*△▲TG/(mmol/L)1.07±0.34 2.74±0.47*2.96±0.46*1.65±0.17*△▲1.76±0.12*△▲1.57±0.15*△▲Scr/(mmol/L)36.10±2.55 96.5±4.55*95.10±2.13*76.10±1.62*△▲77.41±2.17*△▲75.87±2.58*△▲BUN/(mmol/L)7.90±1.36 17.47±1.23*16.90±1.37*12.37±0.90*△▲12.60±1.31*△▲11.81±0.52*△▲
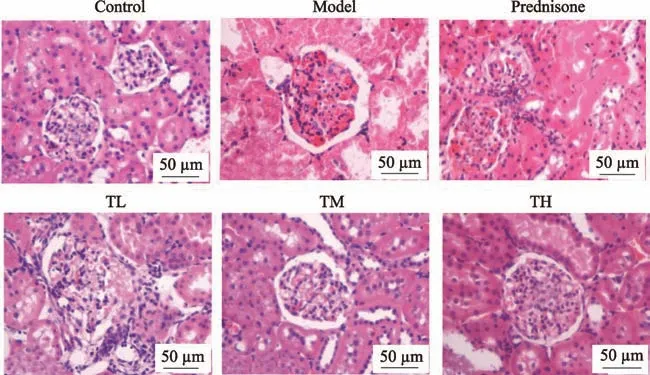
圖2 HE染色觀察腎組織病理形態學變化(200×)
2.3 各組血清血脂、腎功能有關指標變化情況
與Control 組相比,Model 組TP、ALB 水平降低,TC、TG、Scr、BUN、LDH 水平升高,差異有統計學意義(P < 0.05)。與Model、Prednisone 組相比,TL 組、TM組、TH組血清TP、ALB水平升高,TC、TG、Scr、BUN、LDH水平降低,差異有統計學意義(P<0.05)(見表3)。
2.4 HE染色檢測大鼠腎臟病理形態學
Control 組腎小球、腎小管基本正常,球內毛細血管結構清晰;Model 組腎小球囊粘連,細胞增生明顯,周圍間質內較多炎細胞浸潤,毛細血管內呈均質狀透明樣變,腎小管上皮細胞變性,管腔內均有透明管型。經激素及與右歸丸聯合治療后腎小球、腎小管損傷得到一定的改善,病理損傷程度減輕。與Control 組相比,Model 組腎小球硬化評分、腎小管間質損傷評分、膠原纖維比例升高,差異有統計學意義(P < 0.05)。與Model、Prednisone 組相比,TL 組、TM 組、TH 組腎小球硬化評分、腎小管間質損傷評分、膠原纖維比例降低,差異有統計學意義(P < 0.05)(見圖2、圖3、圖4和表4)。
2.5 腎組織細胞凋亡情況
與Control 組相比,Model 組腎組織細胞凋亡率升高,差異有統計學意義(P<0.05)。與Model、Prednisone組相比,TL 組、TM 組、TH 組腎組織凋亡率降低,差異有統計學意義(P<0.05)(見圖5、表5)。
2.6 腎臟組織中纖維化蛋白表達情況
與Control 組相比,Model 組TGF-β1、CTGF 蛋白表達升高,差異有統計學意義(P < 0.05)。與Model、Prednisone 組相比,TL 組、TM 組、TH 組TGF-β1、CTGF蛋白表達降低,差異有統計學意義(P < 0.05)(見圖6、表6)。
2.7 腎臟組織中JNK/p38信號通路蛋白表達情況
與Control 組相比,Model 組JNK、p38 蛋白磷酸化水平升高,差異有統計學意義(P < 0.05)。與Model、Prednisone 組相比,TL 組、TM 組、TH 組JNK、p38 蛋白磷酸化水平降低,差異有統計學意義(P<0.05)(見圖7、表7)。
2.8 腎臟組織中凋亡蛋白表達情況
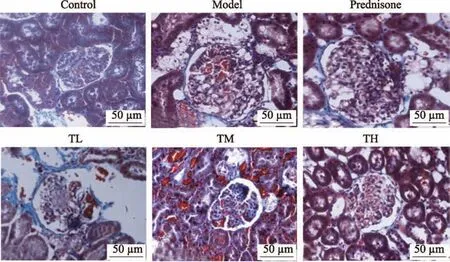
圖3 Masson染色觀察腎組織病理形態學變化(200×)
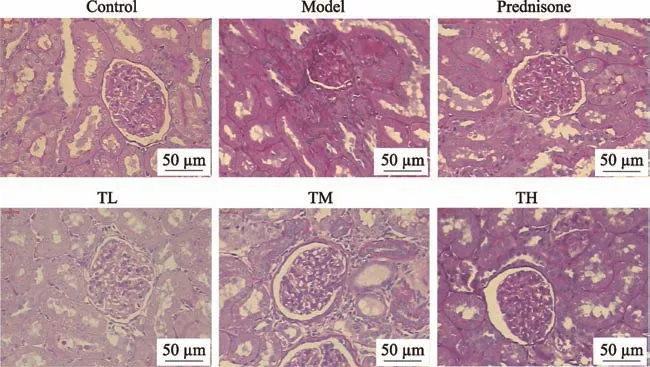
圖4 PAS染色觀察腎組織病理形態學變化(200×)
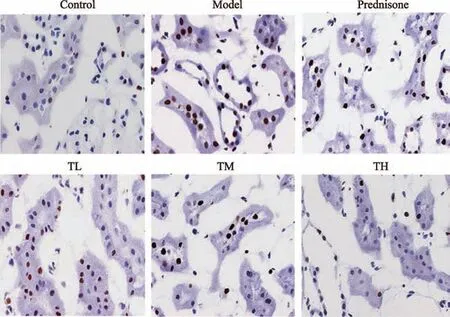
圖5 Tunel聯合免疫組化檢測腎組織凋亡情況(100×)
表4 各組腎組織損傷評分比較(±s)
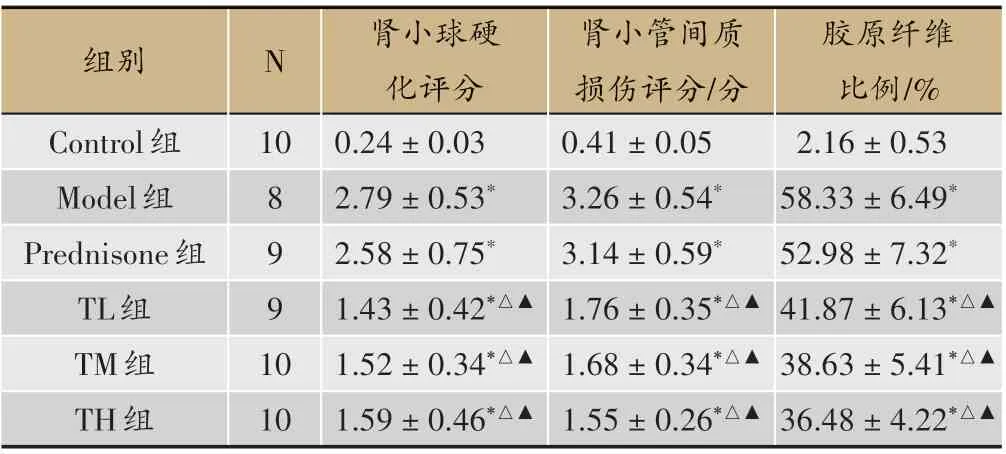
表4 各組腎組織損傷評分比較(±s)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
膠原纖維比例/%2.16±0.53 58.33±6.49*52.98±7.32*41.87±6.13*△▲38.63±5.41*△▲36.48±4.22*△▲組別Control組Model組Prednisone組TL組TM組TH組N 10 8 9 9 1 0 10腎小球硬化評分0.24±0.03 2.79±0.53*2.58±0.75*1.43±0.42*△▲1.52±0.34*△▲1.59±0.46*△▲腎小管間質損傷評分/分0.41±0.05 3.26±0.54*3.14±0.59*1.76±0.35*△▲1.68±0.34*△▲1.55±0.26*△▲
表5 各組腎組織凋亡率比較(±s,%)
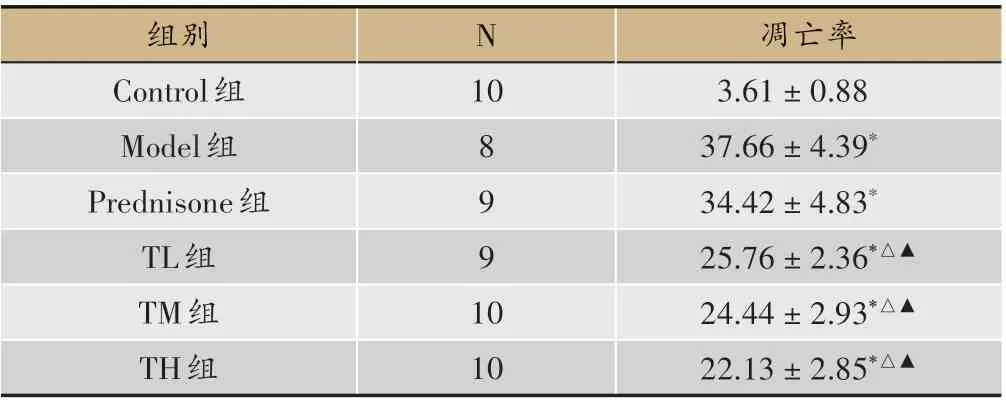
表5 各組腎組織凋亡率比較(±s,%)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
凋亡率3.61±0.88 37.66±4.39*34.42±4.83*25.76±2.36*△▲24.44±2.93*△▲22.13±2.85*△▲組別Control組Model組Prednisone組TL組TM組TH組N 10 8 9 9 1 0 10
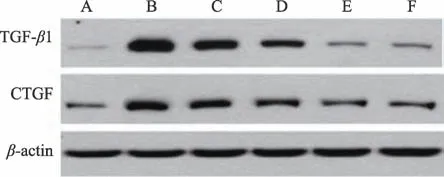
圖6 免疫印跡法檢測腎臟組織中TGF-β1、CTGF信號通路蛋白表達
表6 各組腎組織中TGF-β1、CTGF信號通路蛋白表達比較(±s)
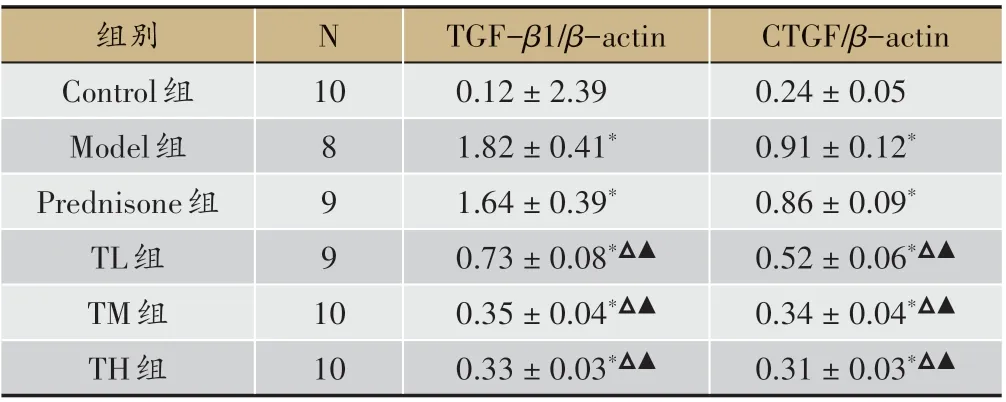
表6 各組腎組織中TGF-β1、CTGF信號通路蛋白表達比較(±s)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
CTGF/β-actin 0.24±0.05 0.91±0.12*0.86±0.09*0.52±0.06*△▲0.34±0.04*△▲0.31±0.03*△▲組別Control組Model組Prednisone組TL組TM組TH組N 10 8 9 9 1 0 10 TGF-β1/β-actin 0.12±2.39 1.82±0.41*1.64±0.39*0.73±0.08*△▲0.35±0.04*△▲0.33±0.03*△▲
與Control 組相比,Model 組Caspase-3、Bax 蛋白表達升高,Bcl-2 蛋白表達降低,差異有統計學意義(P<0.05)。與Model、Prednisone 組相比,TL 組、TM 組、TH組Caspase-3、Bax 蛋白表達降低,Bcl-2 蛋白表達升高,差異有統計學意義(P<0.05)(見圖8、表8)。

圖7 免疫印跡法檢測腎臟組織中JNK/p38信號通路蛋白表達
表7 各組腎組織中JNK/p38信號通路蛋白表達比較(±s)
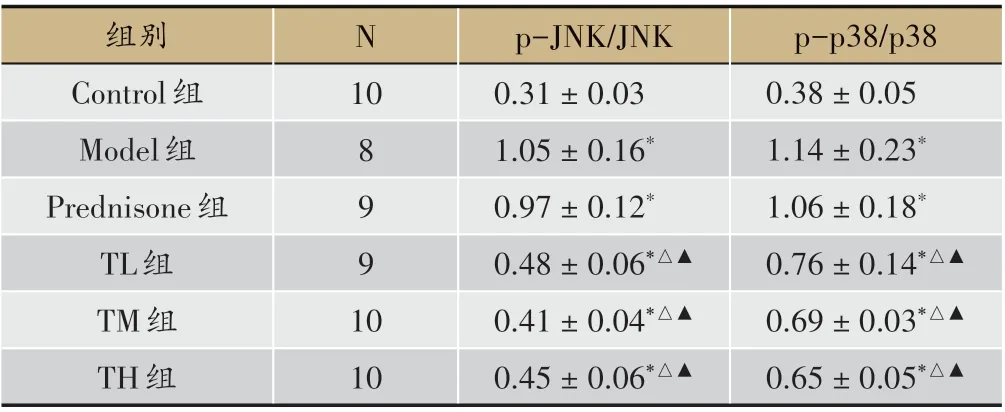
表7 各組腎組織中JNK/p38信號通路蛋白表達比較(±s)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
N 10 p-p38/p38 0.38±0.05 1.14±0.23*1.06±0.18*0.76±0.14*△▲0.69±0.03*△▲0.65±0.05*△▲組別Control組Model組Prednisone組TL組TM組TH組8 9 9 1 0 10 p-JNK/JNK 0.31±0.03 1.05±0.16*0.97±0.12*0.48±0.06*△▲0.41±0.04*△▲0.45±0.06*△▲
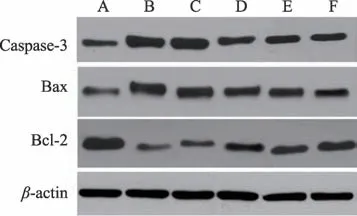
圖8 免疫印跡法檢測腎臟組織中Caspase-3、Bax、Bcl-2蛋白表達情況
表8 各組腎組織凋亡蛋白表達比較(±s)
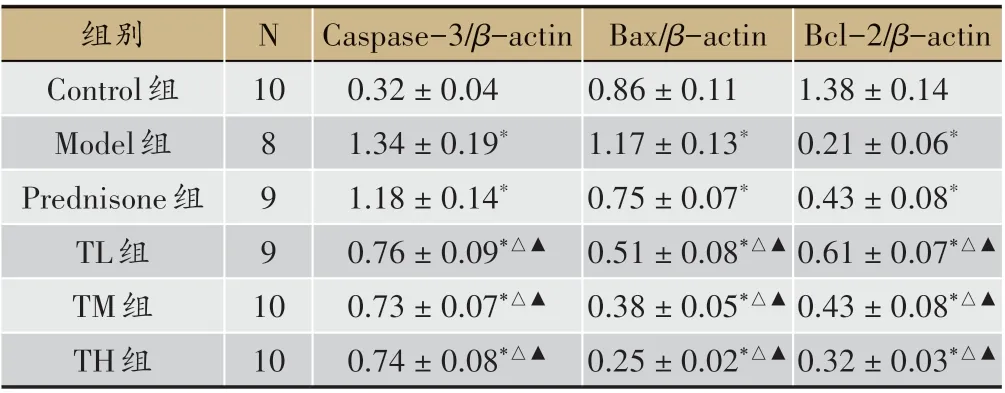
表8 各組腎組織凋亡蛋白表達比較(±s)
注:與Control 組比較,*P < 0.05;與Model 組比較,△P < 0.05;與Predni?sone組比較,▲P<0.05
10組別Control組Model組Prednisone組TL組TM組TH組N Bcl-2/β-actin 1.38±0.14 0.21±0.06*0.43±0.08*0.61±0.07*△▲0.43±0.08*△▲0.32±0.03*△▲10 8 9 9 1 0 Caspase-3/β-actin 0.32±0.04 1.34±0.19*1.18±0.14*0.76±0.09*△▲0.73±0.07*△▲0.74±0.08*△▲Bax/β-actin 0.86±0.11 1.17±0.13*0.75±0.07*0.51±0.08*△▲0.38±0.05*△▲0.25±0.02*△▲
3 討論
阿霉素為癌癥化療藥物,能夠從DNA 水平干預足突細胞DNA 生成,導致足突細胞變異,引發腎細胞損傷;此外,阿霉素還能夠誘發腎小球上皮細胞發生脂質過氧化反應,破壞腎小球濾膜結構,形成蛋白尿,是目前腎病綜合征動物模型常用的化學藥物[6]。既往學者采用阿霉素制備腎病綜合征大鼠發現大鼠出現大量蛋白尿,腎水腫、高血脂等腎病綜合征典型特征[7],與臨床人腎病綜合征臨床表現相似。本研究采用一次性尾靜脈注射阿霉素后,經HE 染色發現與Control組相比,Model 組大鼠腎小球、腎小管發生明顯病理損傷,腎組織損傷評分升高,膠原纖維比例升高,24 h 尿蛋白含量明顯升高,血清學檢測發現大鼠血清TP、ALB 水平降低,TC、TG、Scr、BUN、LDH 水平升高,纖維化蛋白TGF-β1、CTGF 表達升高,進一步表明大鼠蛋白代謝、脂代謝異常、腎功能發生障礙,與腎綜合征大鼠模型制備結果相似[8],提示SRNS 大鼠模型復制成功。
在腎病發生過程中,會發生“溺毒”“腎勞”“腎風”等情況,患者主要表現為正虛邪實,因此中醫認為,脾腎陽虛是腎綜合征疾病的治療目的。右歸丸出自《景岳全書》,屬于補腎代表方,臨床藥理學研究顯示其能夠緩解哮喘、增強機體免疫力,改善大鼠邊緣系統等[9]。熊霞等[10]研究發現,右歸丸能夠降低腎衰竭患者血清中BUN 腎功能指標水平,改善腎功能并提高免疫力,降低炎癥反應,進而緩解病情進展。于化新等[11]研究發現,右歸丸可降低腎衰大鼠血清中Scr、BUN 水平,改善腎損傷,延緩腎衰的發生。上述研究說明,右歸丸對腎病具有一定的緩解作用。本研究顯示,經Prednisone 治療后大鼠腎組織損傷、血清蛋白、脂代謝指標變化并不顯著,而經Prednisone 聯合右歸丸治療后,病理學檢測發現腎小球、腎間質損傷得到一定的改善,血清TP、ALB 水平升高,TC、TG、Scr、BUN、LDH水平、纖維化蛋白TGF-β1、CTGF 表達降低,提示右歸丸能夠緩解SRNS 大鼠腎功能損傷,改善脂代謝、蛋白代謝。
MAPK 信號通路在細胞增殖、分化、應激、炎癥等生理病理過程調控中發揮重要作用,JNK、p38 為通路主要成員,研究發現,在腎纖維化進展中,受到炎癥刺激等可激活p38,使其發生磷酸化,且p38 磷酸化水平與氧化應激程度、纖維化程度密切相關[12-13]。Huang等[14]研究發現,激活Hk-2細胞中JNK信號通路后能夠加速LPS 誘發的急性腎損傷。Yoon 等[15]研究發現,外源性cgrp 通過調控腎近端小管細胞中的cgrp 受體/pkc/jnk 信號通路,進而加速腎小管纖維化的方發生。Wang 等[16]研究發現,抑制JNK/p38 MAPK 信號通路和干擾氧化應激反應減輕大鼠腎缺血再灌注損傷,保護腎功能。本研究發現,與Control組相比,Model組大鼠腎組織中p38、JNK 蛋白磷酸化水平明顯升高,推測JNK/p38 信號通路可能與SRNS 的發生有關。陳葉香等[17]研究發現右歸丸通過抑制TGF-β1 誘導的EMT 過程進而緩解腎間質纖維化。本研究發現,經Prednisone聯合右歸丸治療后,大鼠腎組織中p38、JNK蛋白磷酸化水平明顯降低,提示右歸丸對SRNS 大鼠腎功能的恢復可能是通過對JNK/p38信號通路的抑制來實現的。
腎組織細胞凋亡伴隨著腎病發生發展,存在腎病的損傷及修復過程中。本研究通過采用Tunel 染色檢測SRNS腎組織細胞凋亡情況,結果發現,與Control組相比,Model 組、Prednisone 組大鼠腎組織細胞凋亡率明顯增加,經右歸丸干預后,細胞凋亡率明顯降低,推測右歸丸具有抗腎組織細胞凋亡的作用。Bax、Bcl-2蛋白是研究較多的凋亡蛋白,研究證實Bax/Bcl-2 通路參與腎組織細胞凋亡[18],而Caspase-3是細胞凋亡的最終執行者[19]。本研究發現,與control 組相比,Model組腎組織中Caspase-3、Bax 蛋白表達顯著升高,Bcl-2蛋白表達降低,經右歸丸干預后,腎組織中Caspase-3、Bax 蛋白表達顯著降低,Bcl-2 蛋白表達降低升高,推測右歸丸可通過降低腎細胞凋亡進而發揮對腎臟的保護作用。
綜上所述,右歸丸能夠緩解SRNS 大鼠腎組織損傷,保護腎功能,其可能是通過抑制Jnk/p38 信號通路,降低腎細胞凋亡實現的,然而,SRNS 發病機制較復雜,右歸丸是否還可能通過其他途徑發揮作用,還有待后續深入研究。

