芎歸不忘散對腦缺血大鼠學習記憶障礙及其線粒體、PI3K/Akt信號通路作用機制研究*
付 穎,文 雯,魏江平,陳 歡,文躍強,徐世軍**
(1. 成都中醫藥大學藥學院 成都 611137;2. 成都中醫藥大學中醫腦病藥物整合轉化研究所成都 611137;3. 成都中醫藥大學基礎醫學院 成都 611137)
線粒體作為細胞有氧呼吸的主要場所,在細胞能量代謝中起重要作用。線粒體結構和功能的完整是維持氧化磷酸化及產生ATP 的先決條件[1-2]。線粒體對腦缺血缺氧異常敏感,缺血缺氧會使大腦葡萄糖攝入減少,線粒體呼吸鏈復合物活性下降,功能障礙甚至結構損傷,進而導致腦內產能不足[3-4],可直接誘導神經元凋亡或壞死進而導致。血管性癡呆(vascular dementia,VD)指是由缺血缺氧引起的腦血管病變所致的學習及記憶功能下降[5-6]。線粒體損傷是VD 的重要病理特征,也是加重腦血管損傷和記憶障礙的重要環節。因此,保護線粒體結構和功能完整,維持腦能量供應,增強缺血缺氧受損區域對缺氧條件的耐受力,以維持神經細胞的存活在VD 防治中具有重要地位。磷脂酰肌醇3-激酶/蛋白激酶B(Phosphatidyl alcohol kinases/protein kinase B,PI3K/AKT)信號通路不僅與細胞能量代謝密切相關,而且在線粒體結構和功能完整方面發揮著重要作用[9-10]。芎歸不忘散(XGBWS)是由加味芎歸湯與開心散組合而成,具補心益智,行氣活血的功效,現有研究表明加味芎歸湯和開心散單獨使用對阿爾茨海默癥及VD 均具有一定的治療作用[11-12]。然而,關于加味芎歸湯與開心散進行合方用于治療痰淤釀毒,毒損腦絡所致的VD 還尚未報道,故本研究擬探索兩者合方后對VD 的治療作用及其對PI3K/AKT信號與線粒體保護的影響。
1 材料與儀器
1.1 藥物
川芎、當歸、黃芩、石菖蒲、茯苓、遠志、人參均購于成都中醫藥大學附屬醫院,經成都中醫藥大學馬云桐教授鑒定為符合藥典標準,劑量比例根據中國ZL201310128021.7 加味芎歸湯與《備急千金藥方》開心散確定,藥材用8 倍量的純凈水浸泡1 h 后煎煮3次,每次煎煮1 h,合并煎液,過濾,合并藥液并濃縮至325ML 得率為32.5%濃度即為0.23 g?ml-1,4℃保存。甲磺酸雙氫麥角毒堿片(喜得鎮),天津華津制藥有限公司,批號:7C883T。
1.2 動物
60 只SD 大鼠,雄性,SPF 級,體重180-220 g,于成都達碩實驗動物有限公司購買,實驗動物合格證編號:NO.51203500003215。
1.3 試劑
ATP(1001665433,sigma);ADP(1001726877,sigma);AMP(101606467,sigma);Mitochondrial Membrane Potential DetectionJC-1 Kit(551302,BD);PI3K Rabbit mAb(4257S,Cell Signaling Technology);AKT Rabbit mAb(4685S,Cell Signaling Technology);p-PI3K Antibody(4228S,Cell Signaling Technology);p-AKT Rabbit mAb(4060S,Cell Signaling Technology);PI3K、AKT、p-PI3K、p-AKT抗體稀釋比例均為1∶1000。
1.4 主要儀器
Morris 水迷宮分析系統(WMT-100,成都泰盟科技有限公司),高效液相色譜儀(1260,Agilent),流式細胞儀(ZE5,Bio-Rad 公司),Champchemi 610Plus 全自動多色熒光及化學發光凝膠成像系統(北京賽智創業科技有限公司),ODSHYPERSIL C18色譜柱(thermo)。
2 方法
2.1 模型制備及分組
采用微血栓栓塞法制備VD 大鼠模型[12]。待模型大鼠恢復2 周后,根據“Y”迷宮結果篩選出記憶障礙大鼠隨機分成4 組,每組10 只,分別為模型組(Model)、喜得鎮組(Hydergine,0.7mg/kg)、芎歸不忘散高劑量組(XGBWS H,2.12g?kg-1)、芎 歸 不 忘 散 低 劑 量 組(XGBWS L,1.06 g?kg-1),每組10只。另取10只假手術大鼠作為假手術對照組(Sham),按10 g?kg-1,每日1次,給予對應藥物45 天,其中假手術對照組和模型對照組給予相應量的生理鹽水。本論文的給藥劑量配伍比例是源自于中國ZL201310128021.7 加味芎歸湯與《備急千金藥方》開心散公開的劑量配比,同時參照《中國藥典》藥材使用量確定本論文的大鼠給藥劑量,本論文的給藥時間是結合前期的工作基礎及已發表論文“開心散對多發梗死性癡呆大鼠學習記憶功能及ATP/AMP的影響”確定給藥時間。
2.2 大鼠學習記憶和海馬病理形態學檢測
參考文獻[13]進行定向航行和空間探索實驗,記錄動物逃避潛伏期和穿越平臺次數;空間探索測試結束后于無菌環境處死大鼠,于冰上分離海馬,用4%多聚甲醛固定海馬,常規脫水、包埋、切片、HE 染色、封片,顯微鏡下觀察海馬CA1神經元病理形態學。
2.3 海馬線粒體腫脹度、膜電位和能荷檢測
采用流式細胞儀檢測線粒體腫脹度和膜電位[13]。取適量海馬制成細胞懸液,離心、棄上清、重懸、孵育,清洗、重懸混勻后上機檢測線粒體膜電位及線粒體腫脹;取適量海馬,制樣,采用HPLC 法檢測海馬ATP、ADP、AMP 含量[14],并根據公式計算能荷值:EC =([ATP]+0.5[ADP])/([ATP]+[ADP]+[AMP])。
2.4 大鼠海馬PI3K和AKT表達測定
取適量海馬,制樣、凝膠電泳分離、轉膜、封閉、一抗于4℃孵育過夜,用TBST 洗膜,重復洗3 次,于室溫孵育二抗90 min,重復洗膜3 次。ECL 化學發光顯色,分析各蛋白相對表達量。
2.5 數據處理與統計方法
3 結果
3.1 芎歸不忘散對VD模型大鼠學習記憶能力的影響
如圖1所示,隨著訓練時間,各組動物逃避潛伏期均有不同程度縮短,但模型組相較于假手術組縮短時間較少。在檢測日,與模型組比較,芎歸不忘散高、低劑量組逃避潛伏期顯著縮短,其中高劑量組(F =25.85;P = 0.0071),低劑量組(F = 24.36;P = 0.0078);高低劑量組穿越平臺次數顯著增加(P<0.01)。
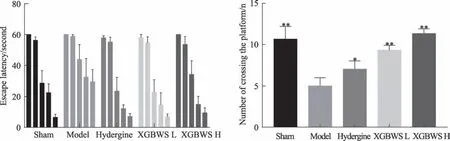
圖1 XGBWS對VD模型大鼠學習記憶能力的影響
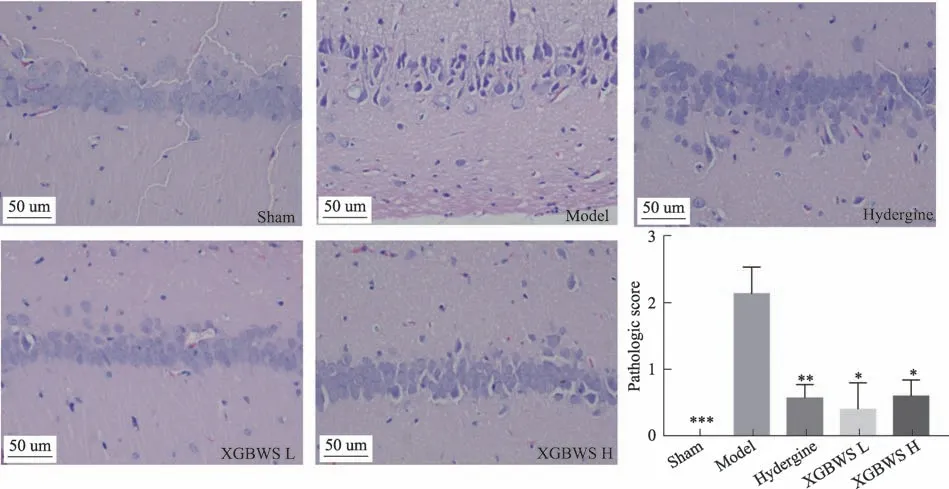
圖2 XGBWS對VD型大鼠海馬CA1區病理形態學影響
3.2 芎歸不忘散對VD模型大鼠海馬CA1區病理形態學影響
如圖2 所示,與模型組相比,經過干預后,芎歸不忘散明顯改善VD 模型大鼠海馬CA1 區神經細胞排列稀疏、神經細胞數量減少和細胞固縮等病理變化(P<0.05)。
3.3 芎歸不忘散對VD模型大鼠海馬線粒體腫脹度及膜電位的影響
如圖3所示,與模型組相比較,芎歸不忘散高劑量組顯著下調線粒體腫脹度(P < 0.05),高、低劑量均能顯著上調線粒體膜電位(P<0.05)。
3.4 芎歸不忘散對VD模型大鼠線粒體功能的影響
由圖4 所示,與模型大鼠比較,芎歸不忘散高、低劑量能顯著提高海馬內能荷及ATP 含量(P < 0.05),AMP和ADP的含量無明顯變化(P>0.05)。
3.5 芎歸不忘散對PI3K/AKT 信號通路相關蛋白的影響
由圖5 可知,與模型組比較,芎歸不忘散高、低劑量均顯著提高VD 模型大鼠p-PI3K 和p-AKT 蛋白表達(P<0.05)。
4 討論

圖3 XGBWS對VD模型大鼠海馬線粒體的影響
VD 是由缺血缺氧性腦血管疾病等腦血管異常引起的一種認知功能損傷綜合征,臨床多表現多為記憶功能衰減或認知功能下降及海馬CA1 區神經元病變[14-18]。本次研究發現,VD 模型大鼠逃避潛伏期明顯延長,穿越平臺次數顯著減少,海馬CA1 區神經元數量減少明顯、神經細胞壞死明顯增多、細胞排列不整齊。經過XGBWS 干預后,VD 模型大鼠逃避潛伏期明顯縮短,穿越平臺次數顯著增多,明顯減緩海馬CA1區不同程度病理變化,說明XGBWS 可顯著改善VD 模型大鼠學習記憶能力和海馬CA1區病理情況。
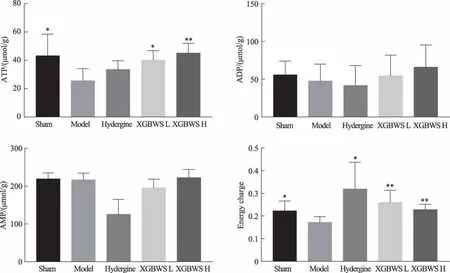
圖4 XGBWS對VD模型大鼠海馬線粒體功能的影響
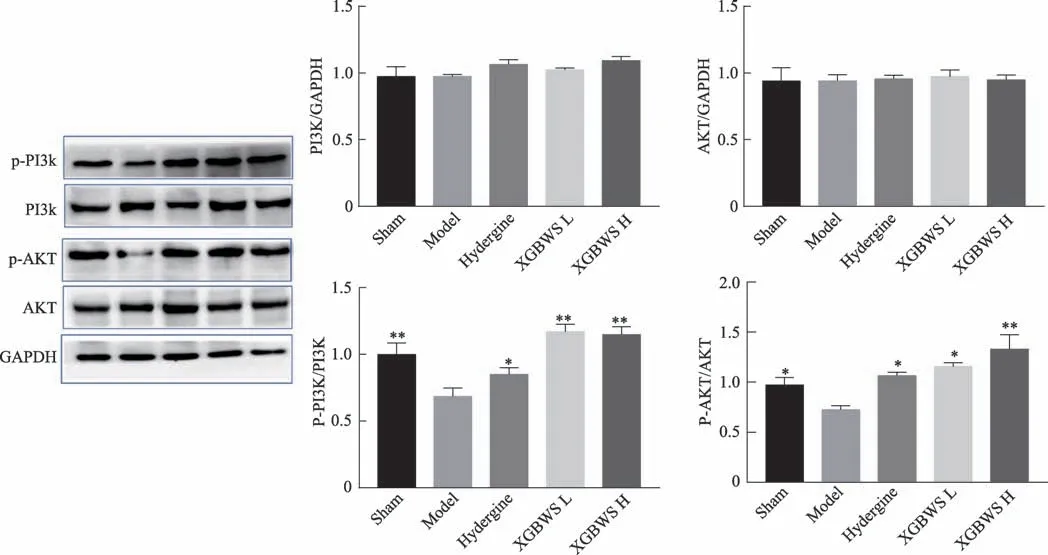
圖5 XGBWS對VD模型大鼠腦PI3K/AKT信號通路的影響
ATP 作為機體直接能源物質,而ADP、AMP 是ATP不完全水解產物,機體通過不斷進行ADP-ATP再循環完成能量的穿梭轉換。能荷則是代表總的腺苷酸系統中所負荷的高磷酸基數量,對代謝起著重要調控作用。因此能荷、ATP、ADP、AMP 含量均能反映線粒體功能。線粒體膜電位與線粒體大小均是反映線粒體結構的重要指標。已有研究表明線粒體功能損傷、能量代謝失常是VD 的發病機制[19-21]。本次研究結果表明,VD 模型大鼠海馬中ATP 含量及能荷值均降低,且線粒體腫脹變性、膜電位下降。經XGBWS 干預后,模型大鼠腦線粒體腫脹度顯著降低,膜電位下降得到改善,能荷、ATP 含量顯著增加,ADP、AMP 含量基本不變。提示XGBWS 修復VD 模型大鼠線粒體結構異常進而達到改善線粒體功能的目的,即XGBWS對線粒體具有保護作用。
然而,線粒體功能由多種因素共同調控,其中PI3K/AKT 信號通路在線粒體保護及能量代謝中扮演著重要角色[22-23]。已有研究表明多種VD 動物模型及細胞模型均顯示PI3K/AKT 信號通路呈抑制狀態[24],這與本研究結果一致,通過XGBWS 干預后,可以激活PI3K/AKT 信號,上調p-PI3K、p-AKT 的表達。綜上,XGBWS 明顯改善VD 模型大鼠學習記憶功能障礙,其作用機制可能是通過激活PI3K/AKT 信號通路達到保護或修復受損的線粒體,進而達到改善腦能量的目的。

