遠(yuǎn)隔缺血處理對腦缺血再灌注大鼠認(rèn)知功能障礙的神經(jīng)保護(hù)作用
徐耀銘,周文靜,2,趙林,山花,趙文博,吉訓(xùn)明
腦缺血再灌注損傷(i s c h e m i c -reperfusion injury,I-RI)可以導(dǎo)致局灶性神經(jīng)功能缺損和血管性認(rèn)知障礙,對患者危害較大。血管性認(rèn)知障礙(vascular cognitive impairment,VCI)病理生理機(jī)制異常復(fù)雜,臨床上發(fā)現(xiàn)多數(shù)卒中患者都出現(xiàn)了不同程度的VCI癥狀,約30%發(fā)展為癡呆[1],目前仍缺乏有效的治療措施。遠(yuǎn)隔缺血處理(remote ischemic conditioning,RIC)通過使器官短暫非損傷性的適度缺血刺激,達(dá)到缺血-再灌注進(jìn)而激活機(jī)體內(nèi)部的保護(hù)機(jī)制,使遠(yuǎn)隔臟器可以耐受較長時間的缺血性損傷,減輕腦組織損傷[2],但能否減輕腦I-RI所致的認(rèn)知障礙仍結(jié)果未知。本研究通過建立血管認(rèn)知功能障礙動物模型,研究RIC是否在腦組織缺血再灌注VCI中發(fā)揮神經(jīng)保護(hù)作用。
1 實驗材料與方法
1.1 實驗動物 清潔級健康雄性SD大鼠,體重220~260 g。所有實驗大鼠均為在入組前進(jìn)行Morris水迷宮實驗并測定為反應(yīng)正常的大鼠。本實驗經(jīng)通遼市醫(yī)院動物倫理委員會批準(zhǔn)進(jìn)行。
1.2 實驗方法 應(yīng)用雙側(cè)頸總動脈閉塞(bilateral common carotid arteries occlusion,BCCAO)方法制備腦缺血再灌注致VCI模型。將SD大鼠分為假手術(shù)組、對照組(VCI組)及RIC組(VCI+RIC組),每組8只SD大鼠,對照組為VCI成功建模的大鼠,RIC組為對VCI模型實施RIC的大鼠。三組分別進(jìn)行Morris水迷宮行為學(xué)測定以評估認(rèn)知功能,并在實驗結(jié)束后每組隨機(jī)選取5只取腦組織進(jìn)行HE染色,電鏡下觀察各組大鼠腦白質(zhì)及海馬病理改變及神經(jīng)元凋亡情況。
1.2.1 實驗?zāi)P偷慕?采用BCCAO方法制備SD大鼠VCI模型[3],具體方法:各組大鼠經(jīng)肛門注入10%水合氯醛(300 mg/kg)麻醉。麻醉后大鼠仰臥位并固定,消毒后行頸部縱向正中切口,依次分離皮下各組織,充分暴露雙側(cè)頸動脈鞘。采用4-0號手術(shù)縫合線做線扣阻斷雙側(cè)頸總動脈血流先進(jìn)行缺血20 min,然后恢復(fù)再灌注10 min;如此重復(fù)3次。在第一次結(jié)扎雙側(cè)頸總動脈20 min內(nèi),在大鼠尾尖約1 cm處斷尾,放血約0.3 mL。3次腦缺血-再灌注結(jié)束后觀察大鼠30 min,狀態(tài)平穩(wěn)后逐層縫合手術(shù)切口。假手術(shù)組大鼠手術(shù)步驟同上,不進(jìn)行雙側(cè)頸總動脈結(jié)扎及斷尾放血。
1.2.2 遠(yuǎn)隔缺血處理 術(shù)后24 h,對RIC組大鼠行雙側(cè)后肢同時RIC處理。彈力繩線加壓捆綁鼠雙后肢根部,阻斷血流,以皮膚發(fā)紫、遠(yuǎn)端肢體皮溫下降、脈搏消失為缺血標(biāo)志,持續(xù)5 min;松開線繩,以皮膚潮紅、遠(yuǎn)端溫度回升、脈搏再現(xiàn)為再灌注標(biāo)志,持續(xù)5 min,4次/日,連續(xù)干預(yù)21 d[4]。
1.2.3 Morris水迷宮的行為學(xué)評定 三組大鼠均于RCI結(jié)束后立即進(jìn)行認(rèn)知功能評估。Morris水迷宮實驗觀察各組大鼠空間學(xué)習(xí)記憶能力,包括逃避潛伏期、穿越平臺次數(shù)和目標(biāo)象限停留時間。本實驗由設(shè)計圓形水池、圖像自動采集處理系統(tǒng)、水下平臺組成。記錄大鼠運動曲線軌跡及分析處理信息,通過記錄觀察大鼠在目標(biāo)象限中停留的相關(guān)軌跡曲線圖判斷其探索運動的規(guī)律性。水池直徑110 cm,高40 cm,水溫(22±2)℃。水下圓形站臺直徑10 cm,高22 cm,距池壁28 cm。將水池人為劃分為4個象限,目標(biāo)象限為第3象限,記錄大鼠找到平臺的時間,將120 s內(nèi)未找到平臺的大鼠引導(dǎo)至平臺停留10 s。定位航行試驗連續(xù)進(jìn)行5 d,第6天在水迷宮中沒有平臺的情況下進(jìn)行空間探索試驗。
(1)定位航行試驗:歷時5 d,觀察大鼠120 s時限在迷宮內(nèi)尋找到平臺的時間。大鼠面壁從第3象限置入池內(nèi)開始計時,到登上站臺終止記錄。記錄各組大鼠第1天、第3天、第5天上臺所需的逃避潛伏期,計算平均時間。
(2)空間探索試驗:檢測大鼠學(xué)會尋找平臺后對平臺空間位置的記憶能力,包括目標(biāo)象限停留時間、穿越原平臺位置次數(shù)。在第6天移除水下平臺,第3象限大鼠面壁入池,記錄120 s內(nèi)的運動曲線軌跡、目標(biāo)象限停留時間以及穿越平臺的次數(shù)。
1.2.4 HE染色 Morris水迷宮實驗完成后切取大鼠腦部白質(zhì)和海馬組織用于檢測,經(jīng)包埋切片、脫蠟、染色等步驟,顯微鏡下觀察,200×鏡下拍照。每個部位選擇5張切片,對每張玻片視野內(nèi)的海馬CA1和CA3區(qū),計數(shù)神經(jīng)元數(shù)量,取平均值。
1.3 統(tǒng)計學(xué)方法 應(yīng)用SPSS 25.0統(tǒng)計軟件進(jìn)行數(shù)據(jù)的分析處理,計量資料進(jìn)行正態(tài)性檢驗,所有數(shù)據(jù)符合正態(tài)分布,以表示,多組間比較采用單因素方差分析及重復(fù)測量方差分析,組間兩兩比較采用t檢驗,P<0.05為差異具有統(tǒng)計學(xué)意義。
2 結(jié)果
2.1 一般情況 假手術(shù)組大鼠術(shù)后反應(yīng)及活動基本正常,在術(shù)后24 h開始進(jìn)食水。對照組大鼠術(shù)后精神狀態(tài)較差,反應(yīng)相對遲鈍,進(jìn)食進(jìn)水較少,5 d后開始逐漸好轉(zhuǎn)。RIC組大鼠術(shù)后2 d后狀態(tài)開始好轉(zhuǎn),介于假手術(shù)組和對照組之間。至術(shù)后4周,對照組大鼠死亡2只;RIC組大鼠死亡1只;假手術(shù)組無死亡。
2.2 Morris水迷宮實驗結(jié)果 第1天、第3天、第5天對照組及RIC組大鼠逃避潛伏期較假手術(shù)組均有延長,差異均具有統(tǒng)計學(xué)意義。除假手術(shù)組外,其他兩組大鼠逃避潛伏期時間隨著訓(xùn)練次數(shù)增加逐漸縮短。第1天、第3天兩組間差異無統(tǒng)計學(xué)意義,第5天RIC組成績好于對照組,兩組間差異具有統(tǒng)計學(xué)意義。第6天空間探索實驗中,目標(biāo)象限停留時間假手術(shù)組與RIC組相近(47.2±10.2 s vs 41.2±9.7 s,P>0.05),均優(yōu)于對照組(33.5±11.3 s),差異均具有統(tǒng)計學(xué)意義;穿越平臺次數(shù)假手術(shù)組與RIC組相近(5.3±1.6 vs 4.7±1.2,P>0.05),均多于對照組(2.8±1.3),差異均具有統(tǒng)計學(xué)意義(表1)。
在空間探索實驗中,與假手術(shù)組相比,對照組大鼠的運動曲線軌跡缺乏目的性而呈現(xiàn)出雜亂無章的平臺搜索軌跡,RIC組較對照組具有明確的目的性呈現(xiàn)出較規(guī)則曲線(圖1)。
2.3 HE染色結(jié)果 假手術(shù)組大鼠腦皮層組織神經(jīng)細(xì)胞無明顯病理改變。對照組可見皮層中錐體細(xì)胞出現(xiàn)明顯的形態(tài)學(xué)改變,細(xì)胞皺縮,細(xì)胞核固縮、深染,細(xì)胞間質(zhì)疏松,神經(jīng)纖維稀疏。RIC組較對照組相比,皮層細(xì)胞間質(zhì)疏松,神經(jīng)纖維變細(xì),破碎細(xì)胞較少,細(xì)胞略皺縮。假手術(shù)組大鼠海馬區(qū)神經(jīng)元排列均勻緊密,核仁著色清晰,無明顯病理改變(圖2)。在對照組中,可見部分海馬區(qū)神經(jīng)細(xì)胞有明顯的空泡樣變性,著色較淺,細(xì)胞體積皺縮。而RIC組較對照組,海馬區(qū)神經(jīng)細(xì)胞可見少量空泡樣變性,細(xì)胞體積輕度皺縮(圖3)。
定量計數(shù)各組大鼠海馬CA1區(qū)和CA3區(qū)錐體神經(jīng)元存活數(shù)目,與假手術(shù)組(CA1:93.53±5.01;CA3:104.63±8.26)相比,對照組CA1區(qū)和CA3區(qū)存活的錐體神經(jīng)元數(shù)目(CA1:51.03±4.95;CA3:78.53±5.31)明顯減少(均P<0.05);而與對照組相比,RIC組大鼠CA1區(qū)和CA3區(qū)錐體神經(jīng)元存活數(shù)目(CA1:80.57±7.30;CA3:92.43±8.16)明顯增加(均P<0.05)。
3 討論
腦I-RI是腦組織缺血區(qū)再灌注導(dǎo)致的二次損傷,其機(jī)制復(fù)雜涉及能量代謝障礙、氧化應(yīng)激反應(yīng)、炎性反應(yīng)、興奮毒性氨基酸、細(xì)胞凋亡等[3]不同機(jī)制,多種機(jī)制共同參了神經(jīng)元超微結(jié)構(gòu)的損傷,特別是涉及線粒體結(jié)構(gòu)[5],最終導(dǎo)致神經(jīng)元凋亡而出現(xiàn)VCI。目前治療VCI尚缺乏有效的方法,在防治領(lǐng)域探索新機(jī)制新方法是本研究的目的所在。
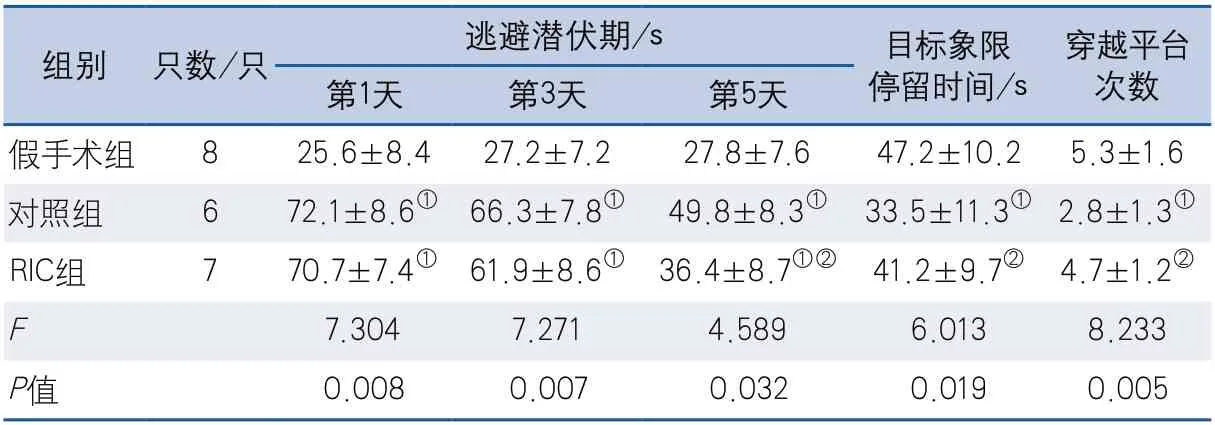
表1 三組大鼠行為學(xué)評定
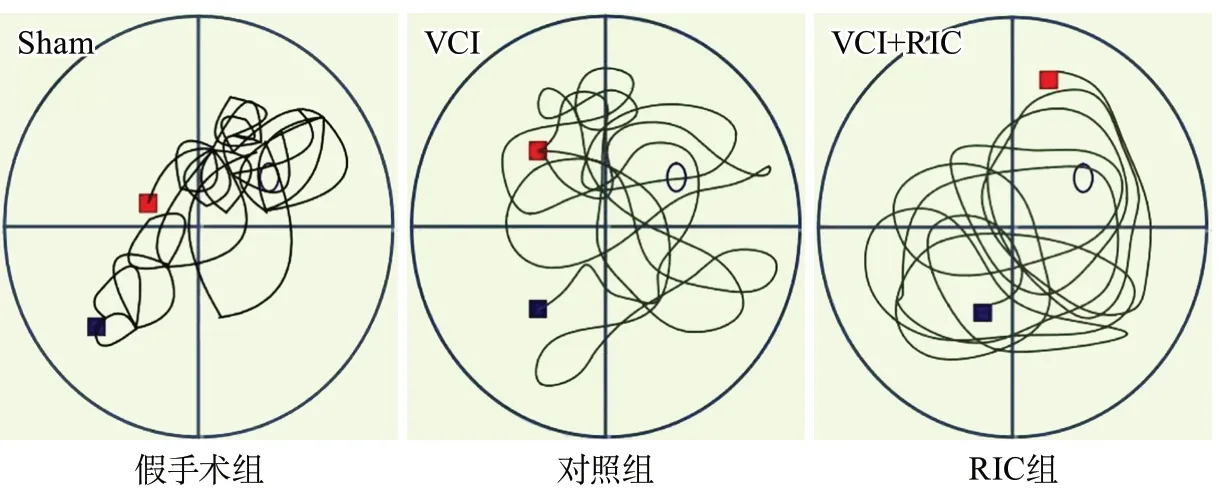
圖1 各組空間探索實驗時的游泳軌跡
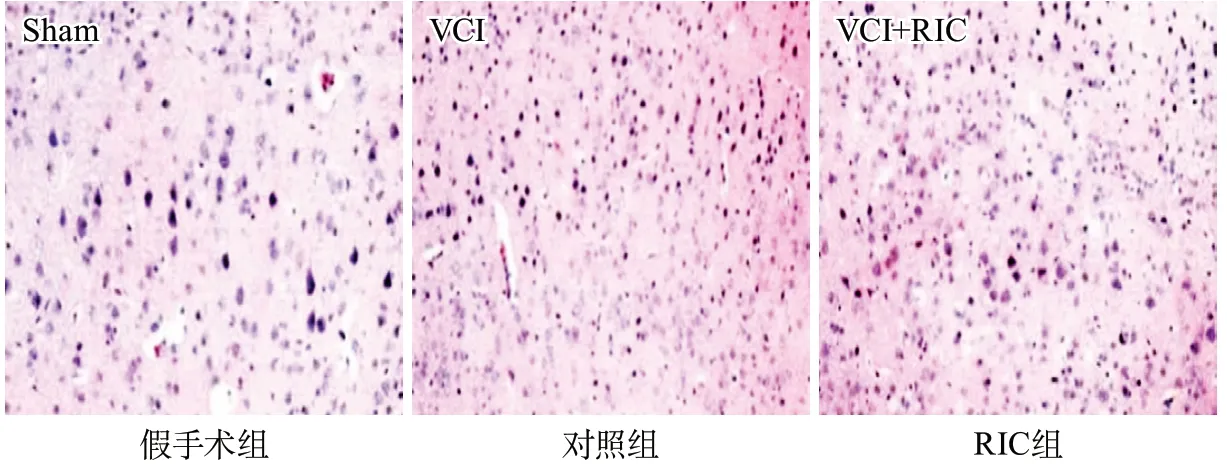
圖2 各組大鼠腦皮層病理變化(HE染色,×200)
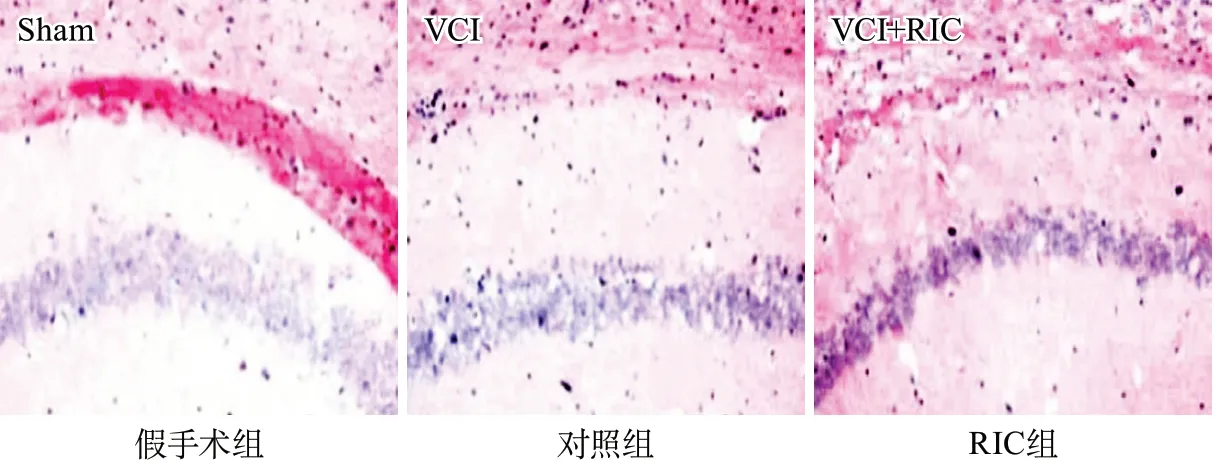
圖3 各組大鼠海馬區(qū)病理變化(HE染色,×200)
建立一個穩(wěn)定的VCI動物模型至關(guān)重要,目前最常用于復(fù)制VCI患者神經(jīng)病理和行為學(xué)改變的是BCCAO模型。夾閉雙側(cè)頸總動脈會引起腦血流量的急劇下降,造成急性腦缺血。鑒于大鼠腦部側(cè)支循環(huán)較豐富,通過剪尾放血降低血壓可以增加模型的穩(wěn)定性。BCCAO法建立的動物模型死亡率低,術(shù)后會出現(xiàn)明顯的學(xué)習(xí)和記憶功能減退等臨床表現(xiàn),組織病理學(xué)研究顯示腦I-RI可以引起海馬神經(jīng)元數(shù)量的減少。這些與人類VCI的臨床表現(xiàn)和病理特點相似,因此BCCAO模型可以作為研究VCI發(fā)病機(jī)制及相應(yīng)治療的可靠模型。術(shù)后大鼠表現(xiàn)出顯著的認(rèn)知功能障礙,已經(jīng)被證實可以作為研究VCI治療較為理想的動物模型[6-7]。Morris水迷宮實驗常用于測試嚙齒類動物空間學(xué)習(xí)和記憶功能情況的裝置之一。反復(fù)訓(xùn)練動物學(xué)習(xí)利用附近的位標(biāo)尋找到水下隱匿的平臺,并測試尋找原來的平臺位置時穿越平臺的次數(shù)以及在平臺所在象限的時長來判斷其記憶力[8-10]。本研究發(fā)現(xiàn),BCCAO術(shù)后的對照組大鼠其逃避潛伏期延長,并出現(xiàn)穿越平臺區(qū)域次數(shù)明顯減少及目標(biāo)象限停留時間明顯縮短的情況,提示腦I-RI可以引起大鼠的記憶力減退,建立了可靠的VCI模型。
RIC對缺血再灌注后遠(yuǎn)隔器官的保護(hù)機(jī)制尚不明確,而且不同形式的缺血處理使腦組織對嚴(yán)重缺血發(fā)生保護(hù)性耐受。目前認(rèn)為RIC的神經(jīng)保護(hù)機(jī)制是多維度的。首先,RIC后可激活細(xì)胞因子、改變基因表達(dá)等多個環(huán)節(jié)產(chǎn)生神經(jīng)保護(hù)作用;另外,RIC可以減輕血腦屏障的破壞,減輕腦I-RI。國內(nèi)外學(xué)者證實,RIC的神經(jīng)保護(hù)機(jī)制在發(fā)病3 h內(nèi)為第一階段(即時相),此階段內(nèi)源性物質(zhì)釋放去甲腎上腺素、緩激肽、腺苷等發(fā)揮神經(jīng)保護(hù)作用;第二階段(延遲相),釋放后的內(nèi)源性物質(zhì)通過調(diào)控基因蛋白表達(dá)或介導(dǎo)細(xì)胞內(nèi)新蛋白合成實現(xiàn)神經(jīng)保護(hù)作用,此階段可持續(xù)48~96 h,甚至數(shù)周[11-12]。
本研究結(jié)果提示RIC可以明顯改善VCI大鼠的認(rèn)知功能障礙。在Morris水迷宮實驗結(jié)果中,RIC后腦I-RI大鼠的逃避潛伏期縮短,穿越平臺區(qū)域次數(shù)增加,在目標(biāo)象限停留時間延長;組織病理學(xué)上RIC減輕了VCI大鼠海馬部位CA1區(qū)和CA3區(qū)結(jié)構(gòu)損傷和海馬神經(jīng)元丟失減少。以上結(jié)果說明RIC可以改善VCI模型大鼠的學(xué)習(xí)及記憶能力,可以減輕腦I-RI引起的海馬神經(jīng)元損傷,這提示了RIC具有神經(jīng)保護(hù)作用。
腦組織特別是海馬組織對血流量的依賴性強,對缺血缺氧性損傷較為敏感。研究發(fā)現(xiàn)腦I-RI會損傷神經(jīng)元,以海馬CA1區(qū)神經(jīng)元損傷最為顯著,因此可導(dǎo)致學(xué)習(xí)和記憶功能障礙[13-15]。腦I-RI導(dǎo)致海馬部位發(fā)生的病理學(xué)損傷,在第2周、第4周以及第6周其神經(jīng)元的排列和數(shù)目發(fā)生明顯改變,以腦I-RI后第4周的神經(jīng)元損傷最為嚴(yán)重[6]。在本研究中,SD大鼠I-RI后海馬組織發(fā)生了類似的改變,與以往的研究結(jié)果一致。
Dave等[2]在2006年首次報道了遠(yuǎn)隔缺血預(yù)處理可減輕腦組織損傷,發(fā)揮神經(jīng)保護(hù)作用,發(fā)現(xiàn)大鼠心臟驟停前48 h,對大鼠實施雙下肢缺血預(yù)處理,組織學(xué)結(jié)果提示處理后腦部損失的神經(jīng)元數(shù)顯著減少。另一研究顯示,RIC可以減少線粒體內(nèi)細(xì)胞凋亡關(guān)鍵物質(zhì)向細(xì)胞質(zhì)的釋放,阻斷了細(xì)胞凋亡從而減輕腦細(xì)胞損傷[16]。研究還發(fā)現(xiàn),RIC治療腦缺血-再灌注大鼠后,醌氧化還原酶-1、組織核因子E2相關(guān)因子2、血紅素加氧酶-1表達(dá)上調(diào),腦組織水腫和梗死體積減小,SOD活性增強。這些結(jié)果顯示RIC通過激活組織核因子E2相關(guān)因子2-抗氧化反應(yīng)元件通路以及通過減少氧化應(yīng)激減輕腦缺血再灌注損傷[17]。缺血處理可以使蛋白激酶B大量活化,蛋白激酶B通路被激活發(fā)揮神經(jīng)元保護(hù)作用。再灌注后海馬CA1區(qū)檢測到磷酸化蛋白激酶B及磷酸化一氧化氮的表達(dá),推測為RIC通過磷酸肌醇3激酶/蛋白激酶B通路上調(diào)了一氧化氮水平,減輕了神經(jīng)元損傷[18]。
本研究顯示RIC可以改善VCI動物模型的學(xué)習(xí)記憶功能,減輕神經(jīng)細(xì)胞的變性壞死,減輕腦白質(zhì)脫髓鞘。但目前RIC對VCI的臨床療效及其具體機(jī)制尚不十分明確。在本實驗中顯示出RIC后腦I-RI大鼠海馬CA1區(qū)和CA3區(qū)神經(jīng)元損傷減輕,存活的錐體神經(jīng)元數(shù)目明顯增多,這表明RIC可以減輕VCI大鼠海馬部位的神經(jīng)元損傷。
綜上所述,RIC可以明顯改善腦I-RI后VCI大鼠的認(rèn)知功能障礙,可以減輕相應(yīng)腦區(qū)或海馬部位的神經(jīng)元損傷。提示RIC具神經(jīng)保護(hù)作用,有望成為VCI有效的治療方法。本實驗不足之處為樣本量較少,其結(jié)果可能存在一定程度的偏倚。另外,本研究只觀察了RIC改善VCI大鼠模型的認(rèn)知功能障礙及腦組織病理變化,未對具體機(jī)制進(jìn)行研究。下一步應(yīng)從加大樣本量及具體機(jī)制方面開展更加深入的研究工作。
《中國卒中雜志》訂閱費用上調(diào)通知
感謝廣大讀者朋友一直以來對我刊的關(guān)注和支持!
我刊自2006年創(chuàng)刊以來,本著質(zhì)量第一、讀者至上的精神,堅持為廣大讀者提供高質(zhì)量的產(chǎn)品和服務(wù)。在眾多學(xué)術(shù)界專家、作者及讀者的支持下,我刊也得以迅速發(fā)展。
為保證期刊產(chǎn)品質(zhì)量,堅持使用銅版紙四色印刷。隨著近年來物價飛漲,我刊的辦刊成本大幅上漲。為保證印刷質(zhì)量,緩解辦刊的經(jīng)濟(jì)壓力,保證刊物的正常運轉(zhuǎn),同時也為了更好地服務(wù)廣大讀者,我刊從2020年第1期起調(diào)整雜志的零售價。每期售價由20元調(diào)整為36元,全年訂價由240元調(diào)整為432元。
我們將一如既往以高質(zhì)量的產(chǎn)品和優(yōu)質(zhì)服務(wù)全力回報讀者的厚愛和支持!
《中國卒中雜志》編輯部
【點睛】遠(yuǎn)隔缺血處理可改善腦缺血再灌注損傷所致血管性認(rèn)知障礙動物模型的認(rèn)知障礙,發(fā)揮神經(jīng)保護(hù)作用。

