基于CRISPR/Cas9的基因分析方法研究進展
田 甜,周小明
(華南師范大學生命科學學院, 分子生物醫學實驗室, 廣州 510631)
1987年,Ishino等[1]在克隆大腸桿菌堿性磷酸酶同工酶(alkaline phosphatase isozyme,iap)基因編碼序列時,發現其編碼區域附近存在間隔串聯重復的DNA片段,但當時未能確定這些保守的重復序列的生物學功能。隨后的1989年,Mojica等[2]在研究地中海嗜鹽菌(Haloferaxmediterranei)限制性內切酶切割微生物基因-Psfl的鹽影響過程中,意外發現該基因的DNA片段里有一些呈回文式對稱的,每段有30個堿基,且片段之間包含36個堿基的間隔序列隔開的多拷貝重復序列的結構,而這個結構與任何已知的微生物的重復序列家族都不相同。Mojica隨后用BLAST等生物信息工具,從一種大腸桿菌測序到的一個基因位點上發現了其中一個spacer與一種P1噬菌體的序列相匹配,而這個噬菌體能感染多種大腸桿菌[3-5]。荷蘭烏得勒支大學的Jansen[6]同樣利用生物信息工具對一系列古細菌和細菌的重復序列進行了分析,并首次將這個重復序列命名為CRISPR(clustered regularly interspaced palindromic repeats),即成簇規律性間隔短回文重復。他在這一研究過程中,還發現了一些與序列功能有關的核酸酶,統稱為CRISPR-associated蛋白, 即Cas蛋白。進一步的研究發現CRISPR中的居間序列并非細菌自身染色體所擁有,而是和很多外源的細菌、病毒和質粒等序列存在很大的相似性。基于這一事實,科學家推測并隨后證實CRISPR-Cas是細菌的一種適應性免疫防御系統[7]。當噬菌體感染細菌時,細菌通過一些特殊方式保留了噬菌體的部分DNA片段,并將其整合到CRISPR序列之中,對外源入侵者的序列信息產生了“記憶”,當下次再次受到噬菌體感染時,就可以利用這些序列信息識別并破壞外源入侵者。
2012年,兩個獨立的小組分別重構了CRISPR/Cas9系統并實現了精確的體外DNA切割[8,9]。他們的試驗證明:成熟的crRNA(CRISPRRNA)可以和反式編碼RNA(tracerRNA)通過堿基互補形成雙鏈RNA結構,該結構可以指導Cas9蛋白對目標雙鏈DNA進行剪切。結構生物學研究表明所有Cas9蛋白都具有保守的由兩個葉組成的結構核心(圖1)[10]:核酸酶葉包含HNH和RuvC的內切核酸酶結構域,這兩者通過橋螺旋相連,分別切割與crRNA序列互補的靶DNA鏈和非互補鏈。識別具有α-螺旋和拓撲異構酶同源的結構域,對于引導RNA(guide RNA)的重復:抗重復RNA雙鏈體以及tracrRNA的莖環1的結合是至關重要的。結果表明,crRNA:tracrRNA可以通過基因工程嵌合成單個指導RNA(sgRNA)。Cas9通過識別并定位原型間隔區相鄰基序(protospacer-adjacent motifs,PAM)來搜索靶標,PAM位點是位于靶dsDNA的非互補鏈下游的短的保守序列(NGG)。識別PAM后啟動dsDNA解旋,使crRNA鏈與靶標鏈配對形成R-環狀復合體。值得注意的是,crRNA和靶DNA之間前8~10個堿基對互補對于靶識別和結合尤為重要,該區域中的錯配會顯著降低Cas9-靶標結合的親和力,而PAM-遠端區域的錯配通常不會影響結合。另外,對Cas9的結構的研究揭示了HNH結構域是可移動的,當Cas9與和crRNA具有完全互補性的靶結合時優先采用催化構象,同時HNH結構域的運動也可變構調節RuvC結構域,確保進行兩條鏈的高保真切割[11,12]。
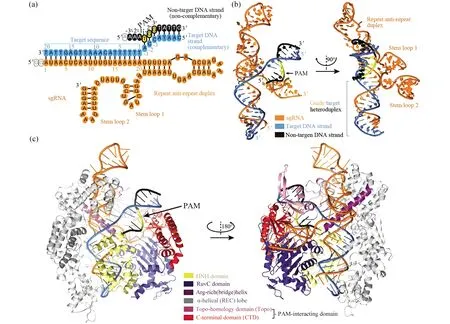
圖1 Cas9識別PAM依賴性靶DNA的結構基礎[10]Fig.1 Structural basis of PAM-dependent target DNA recognition by the Cas9 endonuclease[10](a)指導核酸(sgRNA)和靶核酸的示意圖。空的橢圓表示在電子密度中未觀察到的核苷酸;(b)sgRNA-靶標-DNA四向連接的正交圖;(c)Cas9-sgRNA-DNA復合體的前視圖和后視圖。RNA均為橙色,目標DNA鏈為淺藍色,非目標DNA鏈為黑色。非目標鏈中的5′-NGG-3′PAM三核苷酸以黃色突出顯示(a)Schematic diagram of guide and target nucleic acids. Empty ovals denote nucleotides not observed in the electron density;(b)Orthogonal views of the sgRNA-target-DNA four-way junction;(c)Front and rear views of the Cas9-sgRNA-DNA complex. In all panels guide RNA is coloured orange, target DNA strand in light blue and non-target DNA strand in black. The 5′-NGG-3′ PAM trinucleotide in the non-target strand is highlighted in yellow
II型CRISPR-Cas9系統的發現及后續開發極大的革新了基礎生物學、醫學等學科的發展。通過簡單地設計與鄰近PAM的所需DNA靶向位點配對的sgRNA,可以輕松實現Cas9對目標DNA的靶向。以SpCas9為例,在基因組中每8 bp就可以找到一個NGG,因此CRISPR-Cas9系統幾乎可以靶向任何感興趣的基因。而來自其他物種的Cas9可以識別不同的PAM位點,要求不同的互補堿基數目并包含多種序列組成,這進一步擴展了Cas9可靶向的基因組序列的范圍。因為其程序性、簡易性、高度的特異性,學術界馬上認識到CRISPR/Cas9系統在基因編輯領域的巨大潛力,并于2013年首先實現細胞的基因編輯。由于CRISPR/Cas9的可工程化,近年來,除了應用于基因編輯之外,其在基因表達調控、染色體重組、基因成像、基因檢測等領域也得到了大量的應用[13-15]。在本文中,我們聚焦于綜述CRISPR/Cas9系統在基因檢測中的應用,并展望將來的研究方向。
1 基于Cas9蛋白剪切的基因檢測
第一個將Cas9應用于基因檢測的案例利用了PAM依賴的特異性剪切的功能[16]。像前面述說的,CRISPR/Cas9系統對基因的識別首先依賴于對PAM位點的搜索和定位,所以PAM位點的存在是基因剪切的前提。如果缺失PAM位點,即使sgRNA與靶序列發生完全的互補也將不能使DNA雙鏈發生解鏈及后續的切割反應。Cas9的這一特性曾被用來發展一種鑒別寨卡病毒譜系的新技術[16]。在該方法中,PAM位點僅存在于美洲譜系寨卡序列中,只有美洲型序列能被Cas9切割,這導致截短的RNA的擴增,而非全長的RNA轉錄產物不激活傳感器開關。相反,非洲型序列不含有PAM位點,從而免受Cas9切割,這導致全長RNA的擴增,擴增產物激活RNA傳感器開關。該方法可以在幾個小時內提供精確的基因型信息。
基于CRISPR/Cas9剪切的技術也被應用于HPV病毒分型檢測。HPV16和18型是引起宮頸癌病變的兩種主要病毒亞型。通過設計可以特異性識別HPV16和18型的sgRNA,并對HPV DNA進行切割,切割后的DNA鏈將不能進行擴增,然后采用定量PCR方法來評價切割底物的濃度從而可以判別病毒序列[17]。CRISPR/Cas9剪切也促使發展了一種高信噪比的基因突變檢測方法。循環腫瘤DNA(ctDNA)已成為潛在的腫瘤特異性生物標志物,可用于早期檢測各種癌癥。然而由于血漿中存在的極少量的ctDNA,有效的檢測手段必須依賴高效率的富集技術。基于CRISPR/Cas9剪切,一種名叫CUT-PCR的技術可以在存在大量野生型DNA片段的情況下,通過剪切野生型序列,高效富集和檢測極少量的腫瘤DNA片段[18]。該方法通過使用各種直系同源CRISPR內切核酸酶如SpCas9和FnCpf1來計算,CUT-PCR方法將適用于COSMIC數據庫中登記的80%的已知癌癥相關替代突變。CUT-PCR被證明可以結合深度測序實現更廣泛的癌基因檢測,具有高靈敏度(0.01%)和準確度,優于傳統的靶向深度測序。與此同時,CUT-PCR也被成功應用于檢測結直腸癌患者中血液ctDNA的致癌突變序列,證明該技術可用于早期診斷各種類型的癌癥。我們小組也應用Cas9對單鏈DNA切割的功能,發展了Cas-EXPER技術,實現了單堿基水平的基因檢測和單堿基分辨的甲基化的檢測[19]。
下一代測序技術已經成為一種優勢的分子診斷方法,然而,高豐度的非靶序列對測序結果的深度和靈敏度會產生干擾。在測序之前去除不需要的高豐度的序列對改善測序數據具有廣泛意義。Gu等[20]介紹了一種通過雜交消耗高豐富多余序列(DASH)的方法巧妙的實現這一目的。在該方法中,測序文庫與重組Cas9蛋白、sgRNA文庫混合,其中sgRNA靶向不需要的序列并引導Cas9對其切割,從而防止它們消耗測序空間。該工作在對患者樣品中的病原體序列測序證明可以減少高達99%的HeLa細胞中的線粒體rRNA,并展示了DASH方法在癌癥檢測中的應用。這種簡單的方法可以適用于任何樣品類型,并且無需額外成本即可提高測序產率。
該方法隨后被另一個獨立的課題組應用于小RNA(smRNA)測序研究[21]。在smRNA測序中,高度豐富的分子如銜接子二聚體產物和組織特異性microRNA(miRNA)會抑制低表達序列的準確定量。特別是銜接子二聚體連接產物,除非通過凝膠分離除去,否則非常難以去除。在該研究中,DASH被用于切除miRNA和銜接子二聚體,該方法被稱為MAD-DASH。在MAD-DASH中,Cas9與靶向銜接子二聚體連接產物以及高度表達的組織特異性smRNA的sgRNA結合,用于體外切割。該過程顯著降低了銜接子二聚體和靶向的smRNA序列,并且具有低的脫靶效應,大大改善了人血漿和組織衍生RNA的低表達miRNA的定量和讀取深度,并且不需要凝膠分離,大大提高了樣品通量。此外,該方法可完全根據其他smRNA-seq制備方法進行定制。應用類似的原理,一種名為FLASH技術被用于富集低豐度的病原體抗菌素耐藥性序列[22]。FLASH技術使用一組Cas9的sgRNA,并設計用于將感興趣的序列切割成適合Illumina測序的大小片段。輸入基因組DNA或cDNA首先被磷酸酶處理阻斷,然后用于這組sgRNA混合的Cas9酶切消化(圖2)。因此,所得的切割產物能夠連接通用測序銜接子。通過擴增,靶向序列得到富集并用于流式池測序。這種方法超越了其他基于CRISPR的診斷工具,因為它可實現高水平的多重應用(高達數千個目標)。
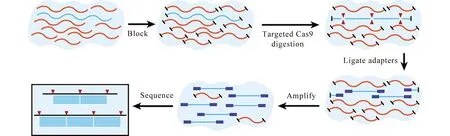
圖2 FLASH方法概述[22]Fig.2 Overview of the FLASH method[22]首先用磷酸酶處理來封閉基因組DNA或cDNA,然后用基于靶向目標基因的指導的Cas9/sgRNA復合物進行消化。 隨后,連接測序適配器,擴增和測序Genomic DNA or cDNA is first blocked with phosphatase treatment and then digested with Cas9 complexed to a set of guide RNAs targeting genes of interest. Ligation of sequencing adaptors, amplification and sequencing follows
2 失活的Cas9蛋白(dCas9)應用于基因檢測
雖然野生型Cas9蛋白是核酸酶,但通過生物工程可以獲得核酸酶缺陷型的Cas9(dCas9)。dCas9是通過在Cas9的RuvC(D10A)和HNH核酸酶(H840A)結構域中分別點突變而獲得。先前的工作已顯示該突變體Cas9在體外缺乏核酸酶活性,因此dCas9可以極大地擴展CRISPR技術的功能庫,包括最初期應用于轉錄調控和成像。近年來,將dCas9應用于基因檢測也獲得了廣泛的興趣和關注。Lou等[23]基于dCas9發展了一種體外DNA檢測系統,該系統使用一對dCas9蛋白連接到半分裂的熒光素酶。當該報告探針對與由sgRNA限定的~44 bp靶序列共定位后誘導生物發光。該系統以高特異性和靈敏度實現了結核分枝桿菌DNA的檢測。隨后,Koo等[24]發展了一種結合dCas9和單微環諧振體生物傳感器的分子診斷技術,實現無標記和實時檢測致病性DNA和RNA。通過使用這種CRISPR/dCas9介導的生物傳感器,實現了單分子靈敏度檢測蜱傳疾病中的恙蟲病(檢測限=0.54 amol/L)和伴有血小板減少癥的嚴重發熱(LOD=0.63 amol/L),這種檢測靈敏度比RT-PCR檢測靈敏度高100倍。基于dCas9與靶基因結合,然后結合非特異性的SBGRI染料應用于金黃色葡萄球菌的檢測,獲得了10 CFU/mL的靈敏度[25]。另一項工作結合dCas9和離子濃度極化(ion concentration polarization,ICP)現象來選擇性預濃縮目標DNA分子從而實現了DNA的直接檢測。該研究通過闡明納米結附近的兩種可區分的堆積和擴散行為,并調節臨界遷移率來改變這些行為,在沒有PCR擴增的情況下實現光學檢測C-C趨化因子受體5型序列[26]。這種基于ICP及dCas9介導的基因檢測方法將為疾病診斷提供快速和準確的微/納米流體活檢平臺。固態納米孔是一種有前景的生物傳感平臺。在納米孔試驗中,作者觀察到CRISPR-dCas9蛋白質結合靶DNA后表現出明顯的電流阻斷信號,這種檢測方式可以方便地識別靶序列。即使在納米孔試驗所需的高鹽條件(1 mol/L LiCl)下,發現dCas9蛋白仍然穩定結合。這種基于納米孔的CRISPR-dCas9生物傳感方法在基于DNA分型的診斷中的應用,例如快速的菌株鑒定,抗生素抗性檢測和基因組分型中具有潛在的應用價值[27]。
大多數檢測核酸的方法仍然需要昂貴的儀器和試劑。近來,Hajian等[28]報道了一種稱作為CRISPR-Chip的生物傳感器,該傳感器利用了dCas9的基因靶向能力,通過與特異性sgRNA復合并固定在晶體管上,產生無標記的核酸檢測裝置。該裝置輸出信號可以用簡單的手持器件測量。CRISPR-Chip分析了從表達藍色熒光蛋白的HEK293T細胞系收集的DNA樣品,以及在具有肌營養不良癥的個體中的DNA臨床樣品。在含有靶基因的基因組DNA存在下,CRISPR-Chip在不需要核酸擴增的前提下獲得了1.7 fmol/L的靈敏度,且檢測過程在15 min內完成。
近來發展的一種CRISPR介導的基因組的特定兆堿基區域的分離技術也是基于dCas9的分離富集功能。該技術能夠對基因組的連續兆堿基區段進行靶向分離。靶向分離純化后的DNA區段的直接測序可以具有>100倍的靶區域富集,因此理論上能夠探索任何物種中復雜基因組區域的DNA序列和結構多樣性。該方法解決了準確評估連續的megabase DNA區域的結構變異所固有的技術和計算挑戰[29]。利用dCas9系統具備的單堿基特異性和通用性,近來發展的一種基于dCas9的等位基因富集方法能夠進行有效的單靶標和多重富集。該方法將dCas9蛋白與靶向目標突變的sgRNA復合,并與含有低豐度突變鏈的cfDNA樣品一起孵育,分離突變結合的dCas9復合物,待解離后,并將捕獲的DNA純化用于下游使用(圖3)。針對非小細胞肺癌中發現的3種最常見的表皮生長因子受體突變(外顯子19缺失,T790M,L858R),該方法實現了等位基因頻率的20倍增加,并通過使用qPCR可檢測到0.1%等位基因頻率。在18個NSCLC患者衍生的cfDNA樣本中,該方法能夠檢測13個突變中的8個,而這些突變未被qPCR檢測到[30]。
3 基于Cas9 Nicking 酶的基因檢測方法
突變Cas9的兩個核酸酶結構域的任意一個,如RuvC(D10A)或HNH核酸酶(H840A),可以獲得Cas9 Nicking酶,也叫Cas9切口核酸內切酶。聚合酶鏈反應(PCR)雖然是最廣泛使用的DNA擴增方法,但熱循環的要求限制了其非實驗室環境的應用。因此,等溫DNA擴增技術對于代替傳統PCR的現場診斷應用是有價值的。在這里,Zhou等[31]描述了基于CRISPR-Cas9觸發的切口核酸內切酶介導的鏈置換擴增方法(即CRISDA)擴增和檢測雙鏈DNA的等溫擴增方法。CRISDA利用CRISPR的高靈敏度/特異性和獨特的構象重排來識別靶DNA,并結合肽核酸(peptide nucleic acid,PNA)侵襲介導的終點測量法。該方法在復雜樣品背景下檢測各種DNA靶標時展現出阿摩爾靈敏度和單核苷酸特異性。此外,通過將該技術與Cas9介導的靶向富集方法相結合,CRISDA可以達到亞阿摩爾靈敏度。
近來,Wang等[32]發展了另一種稱為基于Cas9切口酶的擴增反應(Cas9nAR)。該方法可以在37 ℃的恒定溫度下從基因組DNA中擴增靶片段。Cas9nAR使用具有單鏈切口特性的sgRNA:Cas9復合物,在鏈置換DNA聚合酶作用下,通過引發,延伸,切口和置換的循環過程促進重復的DNA復制(圖4)。Cas9nAR在60 min內獲得zeptomolar檢測限(在20 μL反應體系中2個拷貝)和單堿基鑒別能力。更重要的是,Cas9nAR提供了引物設計的簡單性和應用中的通用性。由于其優異的靈敏度和特異性,以及易于實施,快速和等溫的特征,Cas9nAR具有成為基礎和應用研究中核酸定量檢測的巨大潛力。

圖3 基于dCas9進行等位基因富集的總體工作流程[30]Fig.3 Overall work flow for dCas9 enrichment of rare alleles[30](a)重組6x-His標簽綴合的dCas9蛋白可以與靶向目標突變的sgRNA復合;(b)將它們與突變和野生等位基因以及與抗6x His抗體綴合的磁珠的混合物一起溫育。dCas9復合物與各自的DNA靶標結合;(c)通過磁分離從溶液中提取;(d)解離和純化DNA之后,可以通過下游分析方法(如定量PCR)分析所得的富集DNA(a)Recombinant 6x-His Tag conjugated dCas9 protein can be complexed with sgRNAs targeting mutations of interest;(b)These are incubated with a mixture of both mutant and WT alleles and magnetic beads conjugated with anti-6x His antibodies. dCas9 complexes bind to their respective DNA targets;(c)Extracted from solution by magnetic separation;(d)Following dissociation and DNA purification, resulting enriched DNA can be analyzed by a method of downstream analysis, in this case allele-specific qPCR
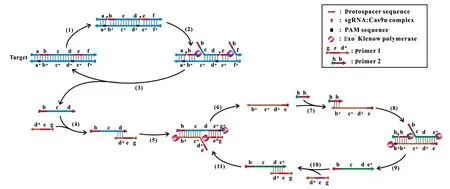
圖4 Cas9nAR方法從基因組DNA擴增目標DNA片段的示意圖[32]Fig.4 Schematic of the proposed Cas9nAR for amplification of a DNA fragment of interest from genomic DNA[32]
4 基于sgRNA和Cas9改造的基因檢測方法
基于對Cas9蛋白進行工程改造,Qiu等[33]發明了一種均相的miRNA檢測策略。該策略使用滾環擴增作為輸入miRNA信號的主放大器,以產生具有重復miRNA互補序列和規則莖環結構的大DNA片段。在RCA中,設計啞鈴狀探針特異性結合靶miRNA以引發鏈置換反應并將其結構改變為phi-29酶介導的RCA的合適底物。隨后,引入基于CRISPR-dCas9的技術靶向來自第一步擴增的產物,從而實現二次擴增和信號輸出。在該方案中,dCas9蛋白預先與半分裂的辣根過氧化酶(HRP)報告片段融合。在特異性sgRNA的指導下,可以在RCA產物的支架樣結構周圍募集分裂HRP-dCas9融合蛋白,從而重構辣根過氧化酶活性。可以使用3,3′,5,5′-四甲基聯苯胺顯色反應來檢測HRP活性,從而實現靶miRNA的檢測。
目前,大多數刺激響應的CRISPR系統是基于Cas9蛋白構建的,并且外部刺激手段仍然主要限于小分子和光。為了構建更精確和易于構建的響應CRISPR系統并拓寬其響應范圍,Li等[34]設計了一種條件性sgRNA而不是Cas9蛋白來介導對應于邏輯操作條件的CRISPR。該方法通過sgRNA重構和立足介導的鏈置換來構建mRNA感應的CRISPR系統,且其中每個靶位點可以獨立控制。該研究表明響應開關可以嵌入到sgRNA中并用作RNA傳感器,能夠正交檢測多個mRNA輸入并提供CRISPR/Cas9響應的輸出。并構造了NOR和NAND邏輯門,展示了其正交性和可編程性。該策略有望用于構建遺傳電路以檢測內源性RNA。
細胞中線粒體DNA(mtDNA)突變的積累與衰老相關疾病密切相關。mtDNA中單核苷酸變異的檢測對于理解具有致病性變化的mtDNA的異質性是至關重要的。Zhang等[35]設計了CRISPR/Cas9介導的鄰近連接測定法(CasPLA),用于直接觀察單細胞mtDNA中的ND4和ND5基因。該方法設計了一對稱為CasPLA的Cas9/sgRNA探針,可識別基因組附近的序列。當配對的CasPLA探針彼此緊密結合時,它們可以引導隨后添加的線性寡核苷酸形成環狀結構,隨后被連接酶共價連接稱環化DNA。通過RCA擴增環化的DNA,然后原位合成的RCA產物與熒光標記的探針雜交,這使得擴增的產物信號能夠與背景區分開。利用CRISPR/Cas9的高特異性,CasPLA可用于以單分子分辨率對ND4基因中的SNV成像。使用CasPLA,也觀察到不同細胞之間的mtDNA轉移過程,這可能解釋了mtDNA異質性的擴散。此外,該方法證明了CasPLA策略可以應用于核基因組中單拷貝基因組位點(KRAS基因)的成像。
5 總結與展望
自實現體外的DNA切割試驗以來,CRISPR/Cas9技術展現其巨大的潛力并應用于很多生物技術領域,比如基因編輯、基因表達與調控、染色體重排、基因成像、基因治療、基因檢測等。特別是CRISPR/Cas9技術現在已經廣泛應用于基因檢測領域,并取得了諸多進展。譬如,CRISPR識別技術可以達到單堿基分辨率水平,實現寨卡病毒譜系檢測。CRISPR技術的這種特異性可以促使在將來的單堿基核苷多態性分析領域大有作為。例如,可以實現一些定點的堿基突變檢測,為腫瘤的早期檢測,細菌的分型提供極其有用的工具。此外,可以預見,通過對DNA進行雙硫轉化也可以實現單堿基分辨率的DNA甲基化檢測。利用Cas9的結合功能,CRISPR技術也可以應用于基因測序前的富集,使得測序深度進一步提高。理論上,CRISPR技術可以實現任何基因的富集,只需要設計相應的sgRNA即可。Cas9和sgRNA也可以被工程化,例如,可以對Cas9蛋白進行生物標記,從而使得其帶有功能化的標簽,為生物傳感技術的開發提供了多樣性。同樣,也可以對sgRNA改造而不影響其功能,從而得以實現新型的探針體系。CRISPR技術對基因的識別是可以在常溫條件下實現的,所以基于CRISPR技術的基因檢測無需嚴格的溫控條件,這一點為將來開發可現場使用的基因檢測奠定了基礎。總之,CRISPR技術正在迅速發展,對現有技術和方法的理解將有助于發展更新一代的基因檢測技術。

