丙戊酸治療老年骨髓增生異常綜合征的療效探究
余敏,江峰錦
1.重慶市渝北區人民醫院血液腫瘤科,重慶 401120;2.重慶市渝北區人民醫院創建辦,重慶 401120
骨髓增生異常綜合征(myelodysplastic syndrome,MDS)屬于髓系克隆性疾病,起源于造血干細胞,其特征為髓系細胞發育、分化異常,臨床表現為無效造血、病態造血、難治性血細胞減少, 晚期患者可出現造血功能衰竭或轉化為急性髓系白血病(AML)。 AML 轉化、骨髓衰竭、并發癥是MDS 患者治療所面臨的主要問題。 MDS 病因不明,免疫因素等導致的細胞凋亡過度、 增殖異常可能在MDS 發病中起重要作用。 組蛋白去乙酰化酶抑制劑 (HDACI)可改變染色體組蛋白結構,促進被抑制基因表達,加快細胞分化成熟,誘導細胞凋亡、周期停滯。丙戊酸鈉具有HDAC抑制活性,可誘導腫瘤細胞分化、凋亡,抑制其生長。 該研究選取2013 年8 月—2017 年12 月就診于重慶市渝北區人民醫院老年MDS 患者54 例, 探究丙戊酸治療老年MDS 的臨床療效。 現報道如下。
1 資料與方法
1.1 一般資料
選取就診于重慶市渝北區人民醫院老年MDS 患者54 例,采用隨機數表法分組,各27 例。 對照組男16 例,女11 例;年齡61~76 歲,平均(68.46±3.58)歲;WHO(2008)分型:難治性貧血(RA)14 例,難治性貧血伴原始細胞增多(RAEB)10 例,難治性貧血伴環形鐵粒幼細胞增多(RAS)3 例。 觀察組男17 例, 女10 例; 年齡62~75 歲, 平均(68.79±3.43)歲;RA15 例,RAEB9 例,RAS3 例。 兩組一般資料對比,差異無統計學意義(P>0.05)。 該研究經該院醫學倫理委員會批準。
1.2 納入及排除標準
①納入標準:符合《血液病診斷與療效標準》中骨髓增生異常綜合征相關診斷標準[1]:持續一系或多系血細胞減少,骨髓涂片中原始細胞達5%~19%,粒細胞系、紅細胞系、巨核細胞系中發育異常細胞比例≥10%,環狀鐵粒幼紅細胞占有核紅細胞比例≥15%;MDS 常見染色體異常;兩組均知情并簽署知情同意書。 ②排除標準:葉酸、維生素B12缺乏;HIV 感染;慢性肝病;重金屬中毒;甲狀腺功能減退;其他可以導致血細胞減少或發育異常的非造血、造血系統疾病。
1.3 方法
①對照組予以常規治療,RA、RAS 采用司坦唑醇等刺激骨髓造血藥物治療,RAEB 采用小劑量阿糖胞苷化療,均加強對癥治療。 觀察組在對照組基礎上予以丙戊酸鈉(國藥準字H32020847)治療,口服丙戊酸鈉0.2 g/次,3 次/d,連續服用24 周。 ②治療后≥1 個月, 每周檢查1 次血常規,每3 個月檢查1 次骨髓象。
1.4 療效判定標準
參照 《骨髓增生異常綜合征診斷與治療中國專家共識(2014 年版)》[2],療效持續時間≥4 周,完全緩解:骨髓:原始細胞≤5%,各系細胞成熟正常,應注明持續存在的發育異常;外周血:血紅蛋白≥110 g/L,中性粒細胞≥1.0×109/L,血小板≥100×109/L,原始細胞為0%。 部分緩解:骨髓原始細胞仍>5%,但較治療前減少≥50%,其他同完全緩解標準。 穩定:未達到部分緩解標準,但疾病無進展時間≥8 周。失敗:治療期間病情進展或患者死亡,表現為骨髓原始細胞比例增高、 血細胞減少加重或出現更高位亞型。 總有效率=(完全緩解+部分緩解+穩定)×100%。
1.5 觀察指標
①臨床療效;②不良反應。
1.6 統計方法
應用SPSS 22.0 統計學軟件進行數據分析, 計數資料用[n(%)]表示,組間比較行χ2檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 臨床療效
兩組治療總有效率對比, 觀察組74.07%高于對照組44.44%,差異有統計學意義(P<0.05),見表1。
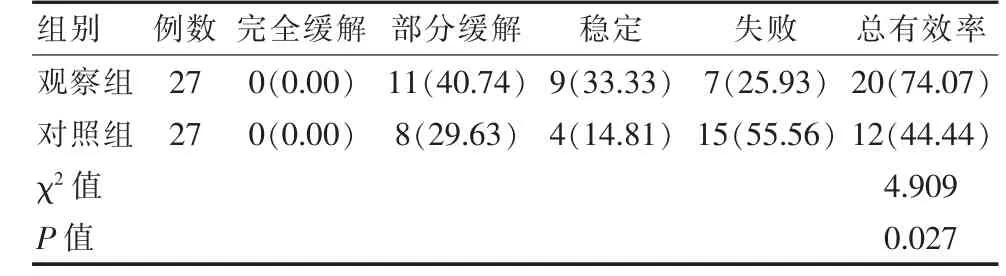
表1 兩組臨床療效對比[n(%)]Comparison of clinical efficacy between the two groups[n(%)]
2.2 不良反應
對照組無明顯不良反應,觀察組出現嗜睡2 例,惡心1 例, 腹瀉1 例, 肝功能損傷1 例, 不良反應發生率為18.52%(5/27),組間對比,差異無統計學意義(χ2=3.527,P=0.060)。
3 討論
MDS 為血液系統常見病,病因不明。 “組蛋白密碼”學說受到廣泛關注,該學說認為,染色體內組蛋白N 端外遺傳學改變, 會影響DNA 與組蛋白親和性, 可調控基因表達。 機體細胞中組蛋白N 端去乙酰化與乙酰化修飾保持動態平衡,組蛋白去乙酰化酶(HDAC)與組蛋白乙酰轉移酶(HAT)可調控該動態平衡[3]。而惡性腫瘤發生、發展多與組蛋白去乙酰化酶(I-IDAC)異常募集有關,局部染色質重塑受到干擾,影響細胞生長、分化、凋亡的基因表達被抑制,進而引發腫瘤。另有研究發現[4],骨髓中T、B、基質細胞等參與的免疫損傷所致造血細胞凋亡過多是MDS 發病的重要原因,減輕免疫損傷可改善MDS 患者病情。 MDS 的原始肝細胞表型與多藥耐藥基因呈高表達, 導致MDS 對一般治療反應較差,療效欠佳。故需尋找治療MDS 的有效方法,以控制病情、增強免疫抑制療效、延長患者生存時間。
研究指出[5],多種短鏈脂肪酸可抑制腫瘤細胞生長,誘導腫瘤細胞分化, 這與短鏈脂肪酸的HDAC 抑制作用有關。 HDAC 與HAT 可調節細胞內染色體組蛋白乙酰化狀態,HAT 可將疏水的乙酰基引入組蛋白N 端賴氨酸殘基,增加組蛋白與DNA 間空間位阻與靜電引力,減弱其相互作用,促進DNA 解聚,增加染色質轉錄活性,促使DNA模板與轉錄因子結合,激活基因轉錄。 而HDAC 促使帶負電的DNA 與去乙酰化后帶正電的組蛋白結合, 染色質呈阻抑結構, 具有抑制基因轉錄的作用。 乙酰化酶可調控DNA 轉錄,調節細胞周期運行,修復DNA 損傷。 而去乙酰化酶與轉錄調控、染色體易位、細胞周期、基因沉默、細胞分化、增殖、凋亡有關。 腫瘤細胞中組蛋白多呈低乙酰化,組蛋白乙酰化狀態失衡會引起染色質重構,激活癌基因,降低抑癌基因表達,導致細胞分化、凋亡異常。 相關研究認為,造血從多克隆轉變為單克隆可能屬于起始步驟,部分癌基因激活、抑癌基因失活及染色體改變可能促進單克隆造血生長、增殖及惡變[6]。MDS 患者外周血細胞數減少而骨髓增生活躍, 其原因可能為造血祖細胞增殖、分化的連續性出現斷裂,導致骨髓內成熟前細胞死亡,即無效造血。
研究發現[7],針對組蛋白改變的靶向治療可能逆轉部分惡性表型表達,具有良好的抑制腫瘤效果。 丙戊酸為短鏈脂肪酸,可抑制HDAC 活性,將組蛋白高度乙酰化,活化轉錄, 誘導人骨髓增生異常綜合征細胞 (MUTZ-1)凋亡, 減少MUTZ-1 細胞增殖, 可選擇性抑制腫瘤細胞生長,誘導其分化、凋亡,對正常造血細胞不具有嚴重毒性,并可與多種化療藥物協同發揮作用[8]。 該研究結果顯示,觀察組治療總有效率74.07%, 高于對照組44.44%(P<0.05﹚,說明丙戊酸治療老年MDS 患者療效顯著,能緩解病情,有助于減少輸血,可能是因為丙戊酸上調了部分調控造血因子基因表達。 丙戊酸常見不良反應有惡心、腹瀉、嗜睡、肝功能損害等,該研究中觀察組出現少量不良反應,但與對照組相比,差異無統計學意義(P>0.05),說明丙戊酸治療老年MDS 患者,安全性高。該次研究的結果表明,觀察組患者的治療總有效率為74.07%,對照組患者的治療總有效率為44.44%,張青宜等[9]報道丙戊酸聯合小劑量化療治療22 例中高危MDS 患者,2 個療程后CR 率為40.9%,總有效率77.2%,優于常規小劑量化療組,且不增加毒副反應,耐受性好。與該研究一致。龔蓉[10]等也報道丙戊酸鈉聯合等地西他濱治療MDS 效果良好,不良反應輕微。
綜上所述,丙戊酸治療老年MDS 患者,療效顯著,能緩解病情,有助于減少輸血,且安全性高,值得推廣。 但本研究樣本量較少,需臨床擴充樣本量進一步驗證,且未對丙戊酸與其他藥物的協同作用及應用時機進行研究。

