黑龍江省稻瘟病菌無毒基因AVR-Pita及其同源基因的檢測與分析
孟峰 張亞玲 靳學慧
黑龍江省稻瘟病菌無毒基因及其同源基因的檢測與分析
孟峰 張亞玲*靳學慧
(黑龍江八一農墾大學, 黑龍江 大慶 163319; *通信聯系人, E-mail: byndzyl@163.com)
【】為了檢測黑龍江省稻瘟病菌無毒基因及其同源基因分布情況與變異機制,了解其變異類型的致病表型。采用3個無毒基因、和的特異性引物,對202個采自黑龍江省各稻區的稻瘟病菌單孢分離菌株的DNA進行PCR擴增,通過瓊脂糖凝膠電泳檢測分析,挑選不同帶型和不同地區代表菌株的PCR產物進行測序。測序結果與相應無毒基因序列進行堿基與氨基酸序列的比較分析,并利用水稻抗性單基因系,對不同變異類型的稻瘟病菌株進行功能驗證。的出現頻率為36.14%,出現頻率為59.41%。在黑龍江省202個菌株DNA中未擴增出目的條帶。對和的部分PCR產物進行序列分析,檢測出有5種變異類型,它們是、、、和。經功能驗證,、、和無毒功能喪失。而無毒基因未檢測出變異菌株。變異能力較強,導致大多數菌株無毒功能喪失,需與其他抗性基因搭配使用。在黑龍江省稻瘟病菌生理小種中未發現基因。基因序列在菌株中比較穩定。
稻瘟病菌;及其同源基因;功能驗證
稻瘟病是由稻瘟病菌引起的,是世界上最重要的水稻病害之一,嚴重威脅水稻高產穩產,每年因該病害引起的水稻產量損失高達10%~30%,嚴重時顆粒無收[1]。實踐證明,利用品種抗性是防治稻瘟病最經濟、安全、有效的途徑。目前定位到的稻瘟病主效抗性基因已達100多個,其中,已克隆的有36個[2]。稻瘟病菌與水稻之間的互作符合經典的基因對基因學說,即致病菌中的無毒()基因在功能上與水稻中的特定抗病基因()相對應。水稻品種的抗性基因與稻瘟病菌的無毒基因相互作用時,表現出抗瘟性[3-4]。目前已報道的無毒基因有70多個,其中,12個被克隆,包括、和等[5-14]。Orbach等[7]成功克隆了稻瘟病菌無毒基因。與水稻抗性基因互作的無毒基因是一個編碼含223個氨基酸的分泌蛋白,含有保守的金屬蛋白酶結構域,是首個被證實編碼蛋白能與相對應的抗病基因產物直接互作的無毒基因。Khang等[15]發現了的兩個新同源體,命名為和,并將重新命名為。甘玉姿等[16]在菲律賓稻瘟病菌生理小種中發現了的新同源序列,將其命名為。其中無毒基因和基因是有功能的,與抗性基因相互作用,而和不具有無毒功能[16,17]。劉殿宇等[18]研究發現2014年和2015年黑龍江省出現頻率分別為23.0%和22.9%;李思博等[19]在2014和2015年遼寧省檢測到的出現頻率為89.91%和76.00%;朱名海等[20]在南繁區檢測到的出現頻率為93.33%。
本研究結合無毒基因家族的基因擴增、測序結果和變異類型的功能驗證,對采集自黑龍江省不同稻區的稻瘟病菌進行分析,從而明確黑龍江省稻瘟病菌基因家族的分布情況及變異類型,以期為黑龍江省抗瘟品種的合理布局與稻瘟病的有效防控提供依據。
1 材料與方法
1.1 供試菌株
2017年在黑龍江省7個市15個縣水稻種植區內采集水稻穗頸瘟標樣,經分離獲得單孢菌株202個,采用濾紙片保存法[21]保存備用。
1.2 供試材料
供試水稻品種為國際水稻研究所選育的含有基因的麗江新團黑谷抗稻瘟病近等基因系IRBtLa-kl,感病對照為麗江新團黑谷。
1.3 稻瘟病菌基因組DNA提取
將分離純化的稻瘟病菌單孢菌株在PDA固體培養基上活化培養,挑取適量菌絲塊接到酵母液體培養基中,于28℃、120 r/min搖床振蕩培養3~5 d,收集菌絲體,分裝于1.5 mL離心管中,–20℃下保存備用。使用真菌DNA提取試劑盒(D3390-01 OmegaBio-Tek公司)提取稻瘟病菌基因組DNA,用微量分光光度計測定DNA濃度,并將DNA原液稀釋成60 ng/μL的工作液備用。原液–20℃下保存。
1.4 引物設計
根據文獻中已克隆的于NCBI上查找其基因序列,利用Primer Premier 5.0設計一對特異性引物,和的特異性引物參照甘玉姿等[16]序列。所有引物均委托上海生工生物工程技術有限公司合成,引物序列見表1。
1.5 PCR擴增及測序分析
PCR體系(20 μL)包括r酶0.1 μL,10×緩沖液(Mg+) 2.0 μL,dNTP混合液1.6 μL,正反向引物各0.3 μL,DNA模板 1 μL,加dd H2O補足20 μL。擴增程序:94℃下預變性4 min;94℃下變性45 s,55℃下退火45 s,72℃下延伸60 s,30個循環;72℃下延伸10 min。擴增產物在1%的瓊脂糖凝膠中電泳檢測并在凝膠電泳成像系統下觀察并拍照,統計無毒基因擴增頻率。
從202個稻瘟病菌菌株中挑選帶型不同和不同地區來源的部分菌株送上海生工生物工程技術有限公司測序,測序結果采用Lasergene 7.0的Seq Man軟件進行比對與拼接;并采用DNAMAN軟件對有差異的核苷酸序列進行比較分析。
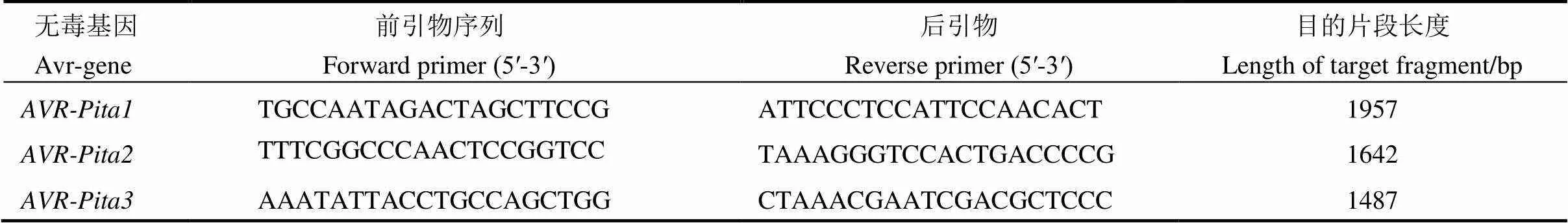
表1 用于擴增稻瘟病菌無毒基因AVR-Pita的引物
1.6 水稻稻瘟病接種與調查
水稻3葉1心時,用無菌水洗下孢子,雙層紗布過濾,調節孢子量為1×105個/mL,將5 mL菌懸液加入5 mL明膠溶液搖勻后噴灑秧苗,25℃下遮光保濕培養24 h后自然條件下培養,接種后5 d調查稻瘟病發病情況,調查標準參照文獻[22]。
2 結果與分析
2.1 AVR-Pita及其同源基因PCR產物擴增檢測
以202個稻瘟病菌菌株的DNA為模板,根據無毒基因及其同源基因序列設計的引物進行PCR擴增(圖1),電泳結果顯示共有5種帶型:無帶、高帶(正常帶型)、低帶、雙帶和三帶。雙帶為非目的條帶[23],三帶為多位點現象。引物在供試的202個菌株中,73個菌株能擴增出目的條帶,出現頻率為36.1%(表2),其中大慶杜蒙、肇源,哈爾濱方正、尚志出現頻率為0%(表2);引物在所有供試菌株DNA中均未擴增出目的條帶;引物電泳結果顯示120個菌株DNA中擴增出目的條帶,出現頻率為59.4%。供試202個菌株中54個菌株DNA同時擴增出和。
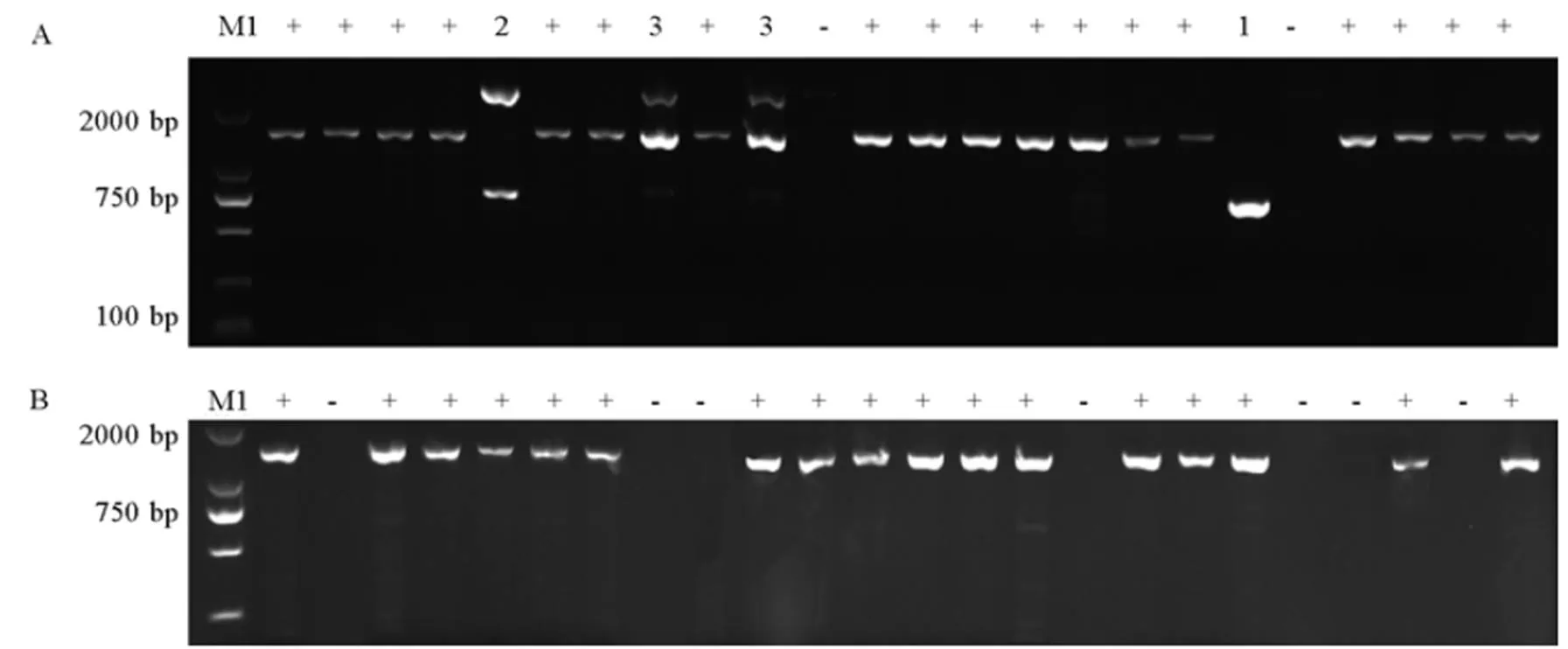
A?AVR-Pita1的部分擴增結果; B?AVR-Pita3的部分擴增結果。M1?分子標記DL2000;+:存在;-:缺失;1:低帶;2:雙帶;3:三帶。
Fig. 1. PCR detection ofand its homologous genesamplification to the tested strains.
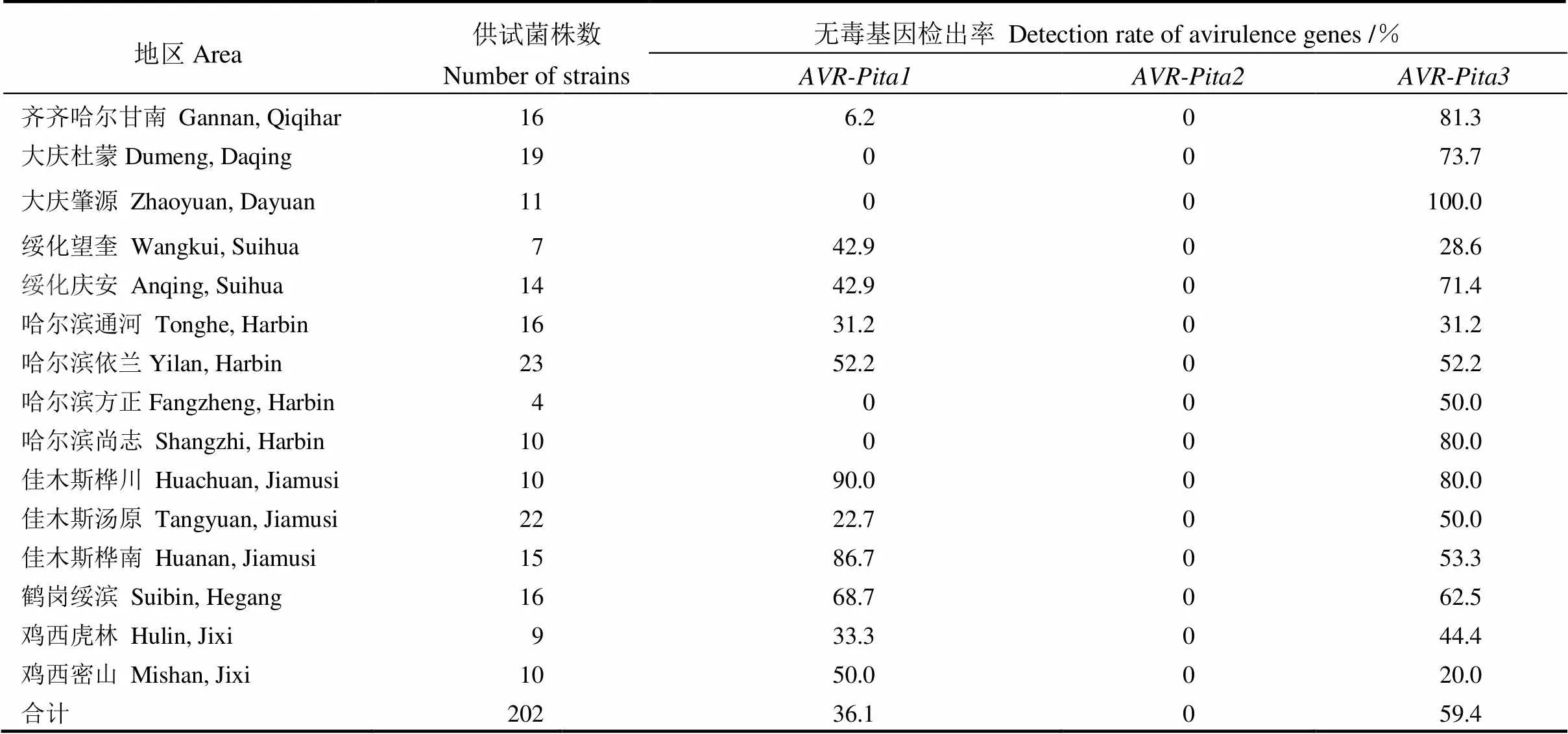
表2 2017年黑龍江省稻瘟病菌無毒基因AVR-Pita1及其同源基因分布情況
2.2 AVR-Pita及其同源基因的序列分析
2.2.1 無毒基因的序列分析
從73個擴增出目的條帶的菌株中挑選不同地區不同帶型的菌株20個進行測序。將測序得到的基因序列與參考序列(AF207841.1)比對。結果顯示(圖2),20個菌株的無毒基因菌株序列可分為5類,一類為存在基因序列1250 bp的缺失,從基因上游1004 bp至下游246 bp處。此變異類型與余歡等[24]研究結果一致,我們將其命名為。其余四類為單堿基的替換、缺失與插入(圖2),我們分別將其命名為和。與Dai等[25]報道的結果序列一致。
的4類堿基序列所翻譯氨基酸序列與已克隆的氨基酸序列比對結果見圖3,除312(T/G)為同義突變外,其余堿基的突變均會導致氨基酸的錯義翻譯。氨基酸序列不僅在6L(Insert)、88(R/K)和104(K/N)存在錯義突變,而且在174位處發生移碼突變導致后面氨基酸發生變化。氨基酸序列存在8處錯義突變:6L(Insert)、82(N/S)、83(D/N)、88(R/K)、104(K/N)、136(G/E)、174(V/I)和192(Y/C),的氨基酸序列存在7處錯義突變:6 L(Insert)、82(N/S)、83(D/N)、88(R/K)、104(K/N)、174(V/I)和192(Y/C)。的氨基酸序列不同于其他4類,它與氨基酸序列比對一致性為25.45%(圖4),氨基酸的缺失與錯義翻譯較多,將進行單獨分析。
20個測序的菌株中,包含2個菌株,占測序菌株的1/10;包含4個菌株,占測序菌株的1/5;類型較多,包含10個菌株,占測序菌株的1/2;包含3個菌株,占測序菌株的3/20;包含1個菌株,占測序總菌株的1/20(圖5)。
2.2.2 無毒基因的序列分析
從120個含有目的條帶的菌株中挑選不同地區的菌株20個進行測序,將測序得到的基因序列與已克隆的基因序列比對后發現,20個菌株的基因序列比對結果完全一致。說明在這20個菌株中沒有出現變異情況。
2.3 AVR-Pita1致病表型分析
對無毒基因型的5種突變類型進行功能驗證,如圖6所示,以麗江新團黑谷(LTH)為對照。結果顯示,、-、和不能被識別表現有毒性,無毒功能喪失。C可以被識別而表現為無毒性。
3 討論
了解家族成員在稻瘟病菌中的分布與變異情況,不僅對研究稻瘟病菌的遺傳多樣性具有重要價值而且可為抗病品種的布局及病情的分子預警提供參考依據。2017年,從黑龍江省各稻區水稻穗頸瘟標樣中分離獲得單孢菌株202個,利用202個單孢菌株對及其同源基因進行PCR擴增檢測,結果發現出現頻率最高,為59.41%,且分布范圍最廣,各稻區均有分布。出現頻率為36.14%,其中,大慶杜蒙、肇源,哈爾濱方正、尚志出現頻率為0。在54個菌株的DNA中同時擴增出和,與序列之間存在71%~72%一致性,驗證了這2個基因可能起源于同一個原始基因的復制事件。在供試202個菌株的DNA中均未擴增出目的條帶,與甘玉姿等[16]對菲律賓稻瘟病菌生理小種研究結果一致。本研究未檢測出目的基因,推測2017年黑龍江省稻瘟病菌生理小種中可能不含或含有少量基因。本研究由于田間分離的菌株已經經過了水稻品種的篩選,不能代表實際的田間群體,所以不能很好地反映田間實際菌株無毒基因的分布情況。
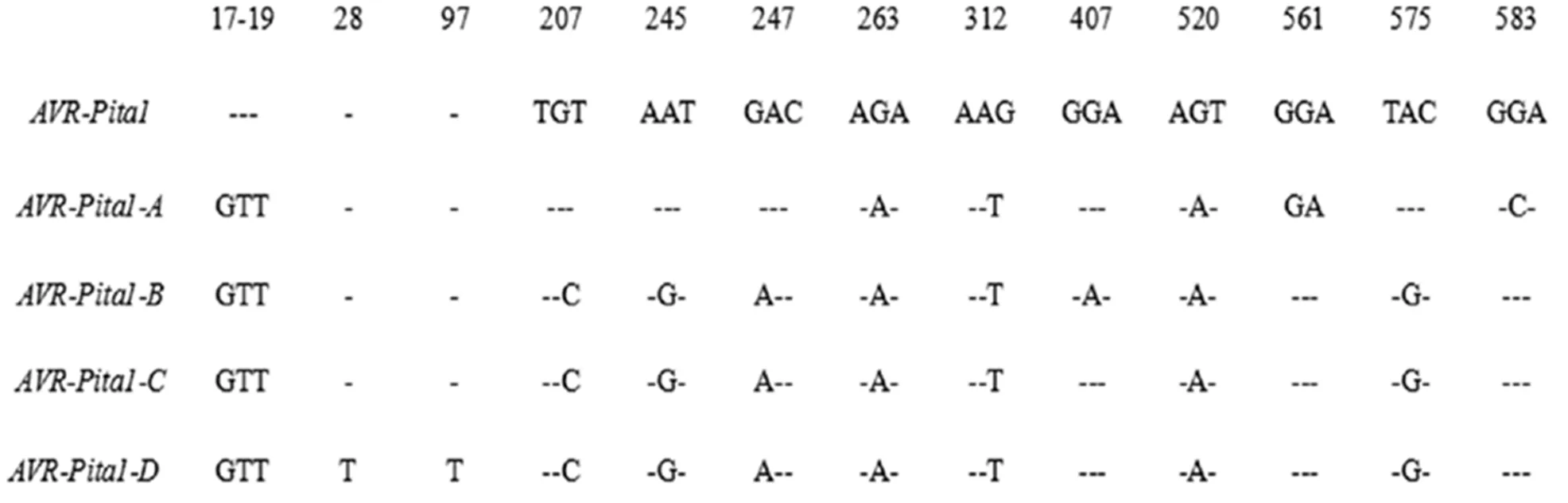
圖2 稻瘟病菌供試菌株AVR-Pita1-A、AVR-Pita1-B、AVR-Pita1-C和AVR-Pita1-D堿基序列比對
Fig. 2. Base sequence comparison ofandof the tested strains.
圖3 稻瘟病菌和氨基酸序列對比分析
Fig. 3. Comparison and analysis of amino acid sequence ofandgenotypes
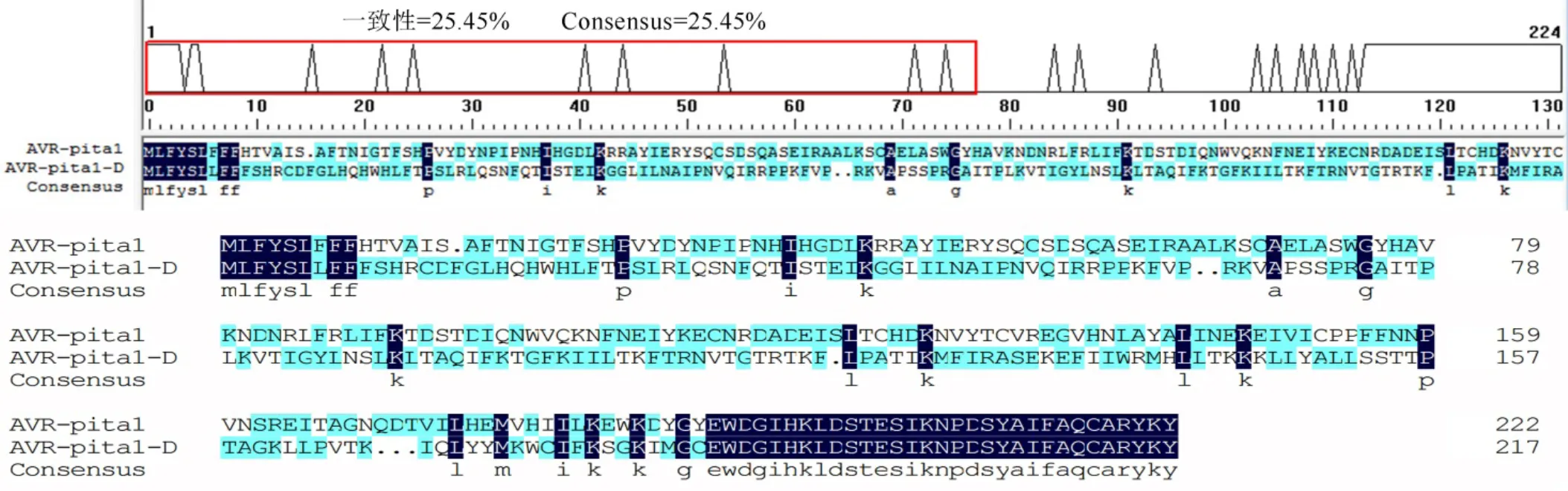
圖4 稻瘟病菌AVR-Pita1-D 氨基酸序列對比分析
Fig. 4. Comparison and analysis of amino acid sequence ofgenotypes of
圖5 稻瘟病菌變異類型比例
Fig. 5. Proportion ofvariant types
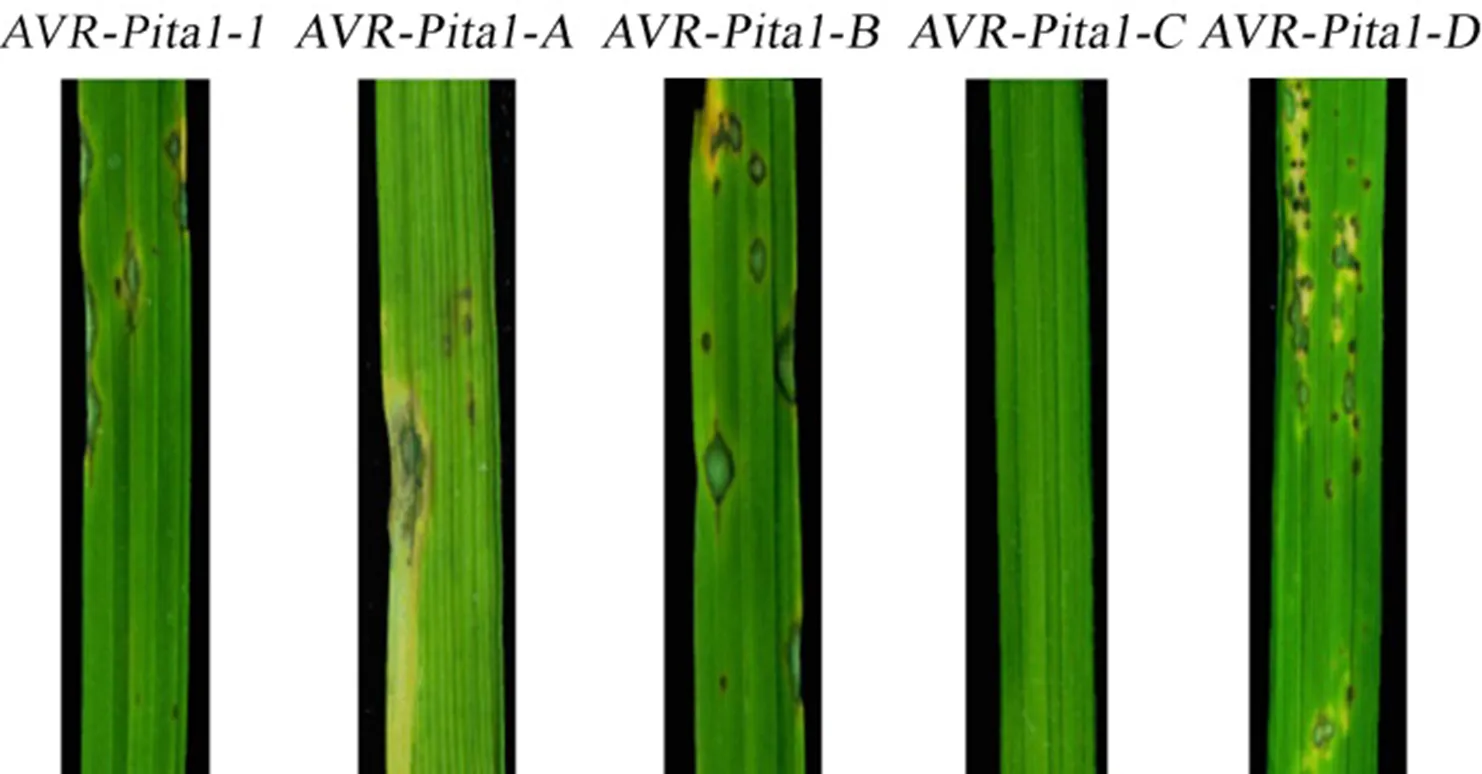
圖6 稻瘟病菌供試菌株AVR-Pita1-1、AVR-Pita1-A、AVR-Pita1-B、AVR-Pita1-C和AVR-Pita1-D致病癥狀
Fig. 6. Symptoms after infected by the strains with,,and
研究者們認為,導致無毒基因不穩定的重要因素為所處的周邊基因環境,和均處于染色體的亞端粒區[15],并且在稻瘟病菌1、3、4、5、6、7等染色體上均有發現[26],具有高度可變性。存在插入、缺失與點突變等多種變異類型。Dai等[25]檢測到27種突變類型,Zhou等[23]在毒性菌株B2中發現了完整的轉座子Pot3,但在黑龍江省202個菌株的DNA中未檢測到Pot3。與和不同,大多數菌株的以比較穩定的形式存在于稻瘟病菌基因組第7染色體上,本研究測序的20個菌株中均未發現變異情況,與前人研究結果相符。
本研究發現存在5種變異類型,其中4種無毒功能喪失,僅可以被識別而表現為無毒性。但-C類型僅占測序菌株數的3/20,大多數菌株已喪失無毒功能。于連鵬[27]在黑龍江省48個水稻品種中檢測到35個品種含有基因,占供試水稻品種的72.92%。周江鴻等[28]報道,在我國稻瘟病菌群體中抗性基因表現為中等至強毒力水平。所以在黑龍江省稻瘟病的抗病育種中不宜單獨使用,需要與含有其他抗性基因的品種搭配使用,才能達到抗病效果。變異能力較強,應同時加強對的田間監測,及時了解的變化規律,以有效地控制病害發生。
[1] Couch B C, Kohn L M. A multilocus gene genealogy concordant with host preference indicates segregation of a new species,, from[J]., 2002, 94(4): 683-693.
[2] 曹妮, 陳淵, 季芝娟, 曾宇翔, 楊長登, 梁燕. 水稻抗稻瘟病分子機制研究進展[J]. 中國水稻科學, 2019, 33(6): 489-498.
Cao N, Chen Y, Ji Z J, Zeng Y X, Yang C D, Liang Y. Recent progress in molecular mechanism of rice blast resistance[J]., 2019, 33(6): 489-498. (in Chinese with English abstract)
[3] Marcel S, Sawers R, Oakeley E, Angliker H,Paszkowski U. Tissue-adapted invasion strategies of the rice blast fungus[J]., 2010, 22(9):3177-3187.
[4] Liu W, Zhou X, Li G, Li L, Kong L, Wang C, Zhang H, Xu J. Multiple plant surface signals are sensed by different mechanisms in the rice blast fungus for appressorium formation [J]., 2011, 7(1): e1001261.
[5] Sweigard J A,Carroll A M, Kang S, Farrall L, Chumley F G, Valent B. Identification, cloning, and character- ization of, a gene for host species specificity in the rice blast fungus[J]., 1995, 7(8):1221-1233.
[6] Kang S, Sweigard J A, Valent B. Thehost specificity gene familyin the blast fungus[J]., 1995, 8(6):939-948.
[7] Orbach M J, Farrall L, Sweigard J A,Chumley F G, Valent B. A telomeric avirulence gene determines efficacy for the rice blast resistance gene[J]., 2000, 12(11):2019-2032.
[8] Collemare J, Pianfetti M, Houlle AE,Morin D, Camborde L, Gagey M J, Barbisan C, Fudal I, Lebrun M H, B?Hnert H U.avirulence genebelongs to an infection-specific gene cluster involved in secondary metabolism[J]., 2010, 179(1):196-208.
[9] Farman M L, Leong S A. Chromosome walking to theavirulence gene ofgrisea: Discrepancy between the physical and genetic maps[J]., 1998, 150(3):1049-1058.
[10] Li W, Wang B, Wu J, Lu G,Hu Y, Zhang X, Zhang Z G, Zhao Q, Zhang H Y, Wang Z Y, Wang G L, Han B, Wang Z H, Zhou B.Theavirulence geneencodes a predicted secreted protein that triggers the immunity in rice mediated by the blast resistance gene[J]., 2009, 22(4):411-420.
[11] Yoshida K, Saitoh H, Fujisawa S, Kanzaki H, Matsumura H, Yoshida K, Tosa Y, Chuma I, Takano Y, Win J, Kamoun S, Terauchi R. Association genetics reveals three novel avirulence genes from the rice blast fungal pathogen[J]., 2009, 21(5):1573-1591.
[12] Wu J, Kou Y, Bao J,Li Y, Tang M, Zhu X, Ponaya A, Xiao G, Li J, Li C, Song M, Cumagun C J, Deng Q, Lu G, Jeon J, Naqvi N I, Zhou B. Comparative genomics identifies theavirulence effectorthat triggers-mediated blast resistance in rice[J]., 2015, 206(4):1463-1475.
[13] Schneider D R, Saraiva A M, Azzoni A R, Miranda H R, Toledo M A, Pelloso A C, Souza A P. Overexpression and purification of, a mutant of the effector proteinfrom[J]., 2010, 74(1):24-31.
[14] Zhang S, Wang L, Wu W, He L,Yang X, Pan X. Function and evolution ofavirulence generesponding to the rice blast resistance gene[J]., 2015, 5:11642.
[15] Khang C H, Berruyer R, Giraldo M C,Kankanala P, Park S Y, Czymmek K, Kang S, Valent B. Translocation ofeffectors into rice cells and their subsequent cell-to-cell movement[J]., 2010, 22(4):1388-1403.
[16] 甘玉姿, 肖貴, 鄧啟云, 吳俊, 柏斌, 盧向陽, 周波. 菲律賓稻瘟病菌生理小種中及其同源基因的序列與功能分析[J].中國生物防治學報,2018,34(3):488-498.
Gan Y Z, Xiao G, Deng Q Y, Wu J, Bai B, Lu X Y, Zhou B. Sequence and functional analysis ofand its homologous genes in physiological races ofin the Philippines[J]., 2018,34(3):488-498. (in Chinese with English abstract)
[17] Chuma I, Isobe C, Hotta Y, Ibaragi K, Futamata N, Kusaba M, Yoshida K, Terauchi R, Fujita Y, Nakayashiki H, Valent B, Tose Y. Multiple translocation of theeffector gene among chromosomes of the rice blast fungusand related species[J]., 2011, 7(7): 395-396.
[18] 劉殿宇. 黑龍江省稻瘟病菌致病性與無毒基因檢測及遺傳多樣性分析[D]. 大慶: 黑龍江八一農墾大學, 2017.
Liu D Y. Pathogenicity avirulent gene detection and genetic diversity analysis ofin Heilongjiang Province[D]. Daqing: Heilongjiang Bayi Agricultural University, 2017. (in Chinese with English abstract)
[19] 李思博. 遼寧省稻瘟菌無毒基因及水稻抗瘟基因鑒定[D]. 沈陽:沈陽農業大學, 2018.
Li S B. Identification of avirulent genes and resistance genes ofin Liaoning Province[D]. Shenyang: Shenyang Agricultural University, 2018. (in Chinese with English abstract)
[20] 朱名海, 趙美, 舒燦偉, 周而勛. 南繁區稻瘟病菌無毒基因的檢測[J]. 華中農業大學學報,2017,36(4):21-25.
Zhu M H,Zhao M,Shu C W,Zhou E X. Detection of avirulence genes infrom South China Crop Breeding Area[J]., 2017,36(4):21-25.(in Chinese with English abstract)
[21] 蔣金芬, 韓紅萍, 梁友方. 濾紙片法低溫冷凍保存菌種的實驗室應用[J]. 中國公共衛生, 2006, 22(3):310.
Jiang J F, Han H P, Liang Y F. Laboratory application of filter paper method for cryopreservation[J]., 2006, 22(3):310-310. (in Chinese)
[22] 靳學慧. 農業植物病理學[M]. 赤峰: 內蒙古科學技術出版社,1999.
Jin X H. Agricultural Plant Pathology[M]. Chifeng: Inner Mongolia Science and Technology Press, 1999. (in Chinese)
[23] Zhou E, Jia Y, Singh P, Correll J C, Lee F N. Instability of theavirulence genealters virulence[J]., 2007, 44(10):1034.
[24] 余歡, 姜華, 王艷麗, 孫國昌. 無毒基因在不同寄主梨孢菌中的變異研究[J]. 浙江農業學報, 2015, 27(8):1414-1421.
Yu H, Jiang H, Wang Y L, Sun G C. Study on the variation of avirulence genes in different host Phasporium[J]., 2015, 27(8): 1414-1421.(in Chinese with English abstract)
[25] Dai Y, Jia Y, Correll J, Wang X, Wang Y. Diversification and evolution of the avirulence genein field isolates of[J]., 2010, 47(12):973-980.
[26] Chuma I, Isobe C, Hotta Y, Ibaragi K, Kusaba M, Yoshida K, Terauchi R, Fujita Y, Nakayashiki H, Valent B, Tosa Y. Multiple Translocation of theeffector gene among chromosomes of the rice blast fungusand related species[J]., 2011, 7(7):395-396.
[27] 于連鵬. 黑龍江省主栽水稻品種、和抗瘟基因檢測和抗性評價[D]. 大慶: 黑龍江八一農墾大學,2017.
Yu L P.,andgenes detection and blast resistance evaluation of main rice varieties in Heilongjiang Province[D]. Daqing: Heilongjiang Bayi Agricultural University,2017.(in Chinese with English abstract)
[28] 周江鴻, 王久林, 蔣琬如, 雷財林, 凌忠專.我國稻瘟病菌毒力基因的組成及其地理分布[J]. 作物學報, 2003(5):646-651.
Zhou J H, Wang J L, Jiang W R, Lei C L, Ling Z Z. Composition and geographical distribution of virulence genes of rice blast fungus in China[J]., 2003(5):646-651.(in Chinese with English abstract)
Detection and Analysis ofAvirulent Geneand Its Homologous Genes in Heilongjiang Province
MENG Feng, ZHANG Yaling*, JIN Xuehui
(Heilongjiang Bayi Agricultural University, Daqing 163319, China;*Corresponding author, E-mail: byndzyl@163.com)
【】We aimto investigate the distribution and variation of avirulentfamily offrom Heilongjiang Province, and to understand the pathogenic phenotypes ofavirulencealleles.【】Specific primers of the three avirulent genes,andwere used. 202single-spore isolates were obtained from different regions of Heilongjiang Province, their DNA were PCR-amplified by using avirulent genes primers in 2017. PCR products of representative strains falling into different types and from different aresa were selected and sequenced by using agarose gel electrophoresis detection. The base and amino acid sequences were compared with those of the corresponding avirulent genes, and the rice resistant single gene line was used to verify the function of different strains of.【】The frequency ofis 36.14%, and that ofis 59.41%. The target band ofcould not be amplified from the DNA of202 strains from Heilongjiang Province. Sequence analysis of some PCR products ofandwere carried out. Five variation types ofwere detected; they were-,-,,and. Functional verification showed that,,and-lost their function. No mutant strain was detected in the virulent gene. 【】had strong mutation ability, which led to the loss of avirulent function of most strains, this should be used in conjunction with other resistant genes.was not found inHeilongjiang Province. The sequence ofgene was stable in the strain.
;gene family; functional verification
S435.111.4+1
A
1001-7216(2020)02-0143-07
10.16819/j.1001-7216.2020.9085
2019-07-21;
2019-11-21。
黑龍江省自然科學基金資助項目(QC2011C046);黑龍江省農墾總局科技攻關計劃資助項目(HNK125A-08-06, HNKXIV-01-04-02, HKKYZD190205);黑龍江省教育廳項目(12521376);黑龍江八一農墾大學學成、引進人才科研啟動計劃資助項目(XDB201605, XDB201802)。

