谷子SiHd3a基因的克隆及表達分析
賈小平,桑璐曼,王振山,趙 淵,張小梅,李劍峰,張 博,周俊超
(河南科技大學 農學院,河南 洛陽 471023)
植物的生長發育過程受到很多環境因素的影響,在其進化過程中逐漸形成了對環境信號做出敏銳反應的能力[1]。光照是植物生長發育過程中不可或缺的環境信號。植物會通過獨特的光合作用(Photosynthesis)與周圍環境進行著物質和能量的交換,以維持其正常的生長發育[2]。光周期(Photoperiod)即晝/夜交替周期,在地球上各緯度地帶季節性交替循環,植物對這種規律性變化的日照時間長短往往會表現出有規律的生長發育現象,稱為光周期現象(Photoperiodism),不同的植物對光周期的敏感性是不同的[3-4]。抽穗開花是植物生長發育過程中非常重要的階段,主要是由植物的感光性、感溫性和基本營養生長性所決定,近些年相關研究者提出了光周期途徑、自主調節途徑、赤霉素途徑和春化途徑這4種開花調控途徑[5]。其中光周期是植物開花的主要環境決定因素,一些熱帶種質在長日照條件下可以顯著延遲生殖生長的開始,因此,光周期現象也被視為一種重要的生理特征[6-7]。目前對光周期途徑的研究較徹底,如通過水稻抽穗期的遺傳學分析、QTL定位及相關基因克隆等基礎研究發現,抽穗期受多個基因調控,而Hd3a(Heading date 3a)基因是所有調控路徑的末端基因,其表達量的高低直接與抽穗期早晚緊密相關,并且受光周期調控,在短日照條件下表達量增加,而在長日照條件下表達量較低,Hd3a基因表現出一定的晝夜節律性表達特點,同時植物的生理過程也表現出晝夜節律,從而能夠適應環境的晝夜循環[8-9]。
谷子是短日照喜溫作物,其中光周期是影響其生態適應性的關鍵因素,這種生態適應性主要是通過調節抽穗期來實現的。作為一種C4作物,谷子中關于光周期調控開花的基因極少報道[10],目前谷子全基因組測序已經完成,這為克隆光周期途徑抽穗、開花控制基因提供了基礎。鑒于成花素基因Hd3a是水稻抽穗期的直接調控者,本研究利用RT-PCR技術克隆谷子成花素基因SiHd3a,在進行生物信息學分析的基礎上,研究該基因在長、短日照條件下的晝夜表達規律,揭示其在調控谷子抽穗過程中所起的作用,為進一步深入研究谷子光周期敏感性的分子機制奠定基礎。
1 材料和方法
1.1 試驗材料
供試材料為谷子地方品種黃毛谷,來源于河北,具有對光周期非常敏感的特性。
1.2 試驗方法
1.2.1 谷子的種植和取樣 選取籽粒飽滿的黃毛谷種子點播于營養土中,置于光照培養箱,晝夜溫度30 ℃/25 ℃,待長至四葉期分別進行2種不同光周期處理:短日照處理(9 h光/15 h暗)、長日照處理(15 h光/9 h暗)。統一早上6:00開始光照,分別于15:00和21:00進入黑暗培養。培養21 d,在晝夜24 h內從晚上21:00開始取樣,每隔3 h取1次,共取9次樣(21:00取樣2次),每次均取頂端第1片幼葉,所取葉片均在液氮速凍后置-70 ℃保存,用于總 RNA 的提取。
1.2.2 谷子總RNA的提取與第一鏈cDNA 的合成 用康為世紀生物技術有限公司的OmniPlant RNA Kit提取葉片總RNA。用寶生物公司(TaKaRa)的DNase 處理各樣品總RNA,去除殘留的基因組DNA,參照寶生物公司的PrimeScript Ⅱ1st Strand cDNA Synthesis Kit說明書以總RNA為模板,用 Oligo(dT18)及6堿基隨機引物(Random hexamers)合成第一鏈 cDNA,于-20 ℃保存。
1.2.3 引物設計及PCR擴增 利用生物信息學方法以水稻Hd3a基因(登錄號:AB052941)編碼蛋白質序列為查詢序列,對基因組數據庫phtozome(https://phytozome.jgi.doe.gov/pz/portal.html)中的谷子基因組數據進行 Blast同源搜索,獲得谷子4號染色體的成花素基因序列(Seita.4G067600),命名為SiHd3a。根據此序列,用軟件Primer Premier 5.0設計1對特異引物:正向引物為5′-CCAAGCAAGGCTACAGGT-3′,反向引物為5′-GTGGCTAGTGTGTCGTACT-3′;預期擴增片段大小為792 bp,包含完整的CDS區域。
PCR擴增體系為:ddH2O 10.5 μL,2×TaqPCR Green Mix 12.5 μL,上游引物0.5 μL,下游引物0.5 μL,cDNA模板1.0 μL。擴增循環程序為:94 ℃預變性4 min;94 ℃變性40 s,55 ℃退火40 s,72 ℃延伸1 min,共35個循環;最后72 ℃延伸5 min。
1.2.4 擴增產物的回收純化 PCR擴增產物經l%瓊脂糖凝膠電泳分離,使用全式金生物技術有限公司的EasyPure Quick Gel Extraction Kit回收純化目標片段。
1.2.5 擴增產物的克隆及測序 將回收純化的基因片段連接到pMD18-T載體(寶生物公司),轉化大腸桿菌DH5α感受態細胞(天根生化有限公司)。挑取陽性菌落,移入裝有1 mL無菌液體 LB 培養基(含Amp 50 mg/L)的1.5 mL滅菌離心管中,37 ℃、200 r/min 振蕩培養8 h后,用M13引物進行菌液PCR檢測。菌液PCR擴增體系為20 μL,含2 μL 10×Buffer、1.6 μL 2.5 mmol/L的dNTPs、1.6 μL 25 mmol/L MgCl2、0.6 μL 10 pmol/μL的正反向引物、1 μL菌液、0.4 μLTaq酶、12.2 μL ddH2O。PCR擴增程序為:95 ℃預變性4 min;隨后94 ℃ 30 s,56 ℃ 30 s,72 ℃ 90 s,共34個循環;最后72 ℃延伸5 min。菌液PCR擴增產物經1.2% 瓊脂糖凝膠電泳檢測后拍照,將檢測正確的陽性克隆菌液送往生工(上海)有限公司測序部測序。
1.2.6SiHd3a基因生物信息學分析 用ProtParam在線工具(https://web.expasy.org/protparam/)預測蛋白質的基本物理化學性質;用 SOPMA和Swiss-model在線分析軟件(http://www.sopma.org/,https://swissmodel.expasy.org/)預測蛋白質的二級結構;用CELLO在線工具(http://cello.life.nctu.edu.tw/)進行亞細胞定位預測;將SiHd3a蛋白序列作為查詢序列,通過Blast(http://blast.ncbi.nlm.nih.gov/Blast.cgi)程序同源搜索NCBI數據庫,獲得部分物種Hd3a蛋白同源序列,用Mega 5.0軟件構建系統進化樹。
1.2.7SiHd3a基因半定量PCR分析 設計SiHd3a基因半定量擴增引物:SiHd3aRT-F為5′-AAGTTGCGACGAGATGGC-3′,SiHd3aRT-R為5′-GCGAAGTCCCTGGTGTTGA-3′;擴增產物459 bp。以谷子SiActin基因作為對照,引物序列:SiActin-F為5′-GGCAAACAGGGAGAAGATGA-3′,SiActin-R為5′-GAGGTTGTCGGTAAGGTCACG-3′;產物大小為228 bp[11]。
通過摸索得到半定量 PCR 反應最佳循環程序: 94 ℃ 3 min;94 ℃ 30 s,58 ℃ 40 s,72 ℃ 50 s,28 個循環;72 ℃ 5 min。反應產物經1.2%瓊脂糖凝膠電泳分離后,采用凝膠成像系統拍照并進行分析。
2 結果與分析
2.1 谷子總RNA的提取
分別在長日照、短日照條件下培養谷苗,取21 d的頂端幼嫩葉片提取總RNA,結果見圖1,可以看出,所提取的RNA完整性較好。以總RNA為模板,反轉錄合成第一鏈cDNA,并用作模板擴增內參基因,結果擴增出與預期一致的228 bp的條帶,證明cDNA合成成功(圖2)。
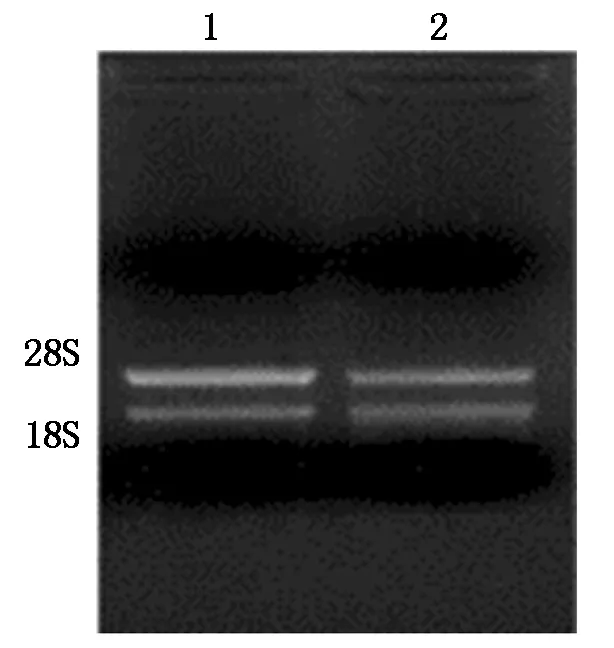
1,2.提取的2管RNA。
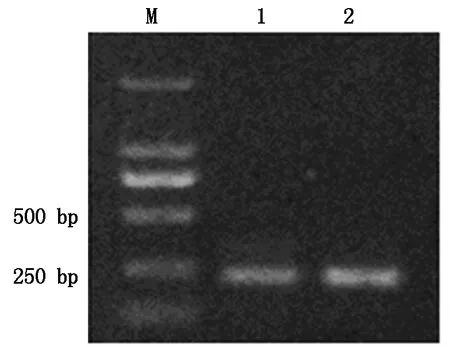
M.Marker DL2000;1,2.內參基因擴增產物。
2.2 谷子SiHd3a基因擴增與菌液PCR檢測
以 cDNA為模板擴增SiHd3a基因,結果見圖3,可以看出,在靠近750 bp處擴增出一條特異性條帶,與預期的792 bp接近。通過連接、轉化得到單克隆,挑取陽性克隆經培養后進行菌液PCR檢測,獲得了與預期條帶一致的目的片段(圖4),將檢測成功的陽性克隆菌液送生工上海生物技術公司測序。
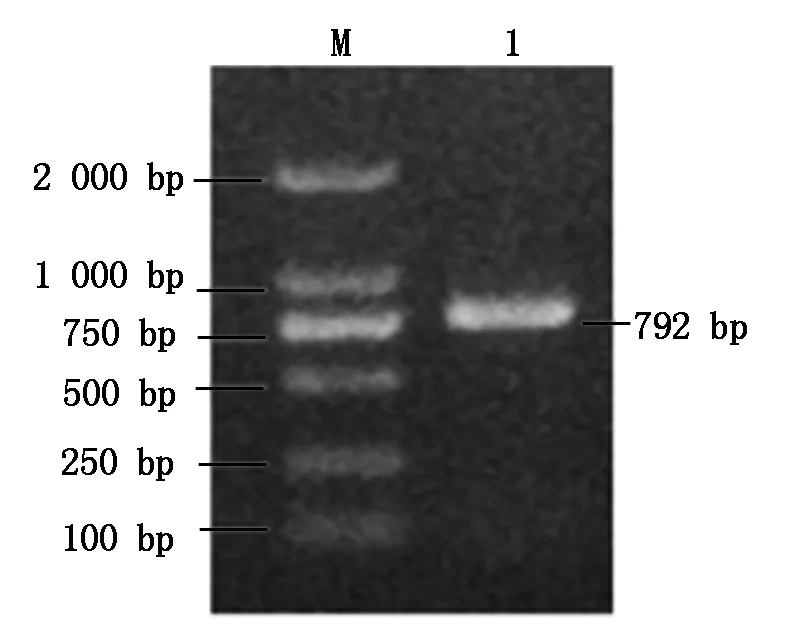
M.Marker DL2000;1.RT-PCR產物。
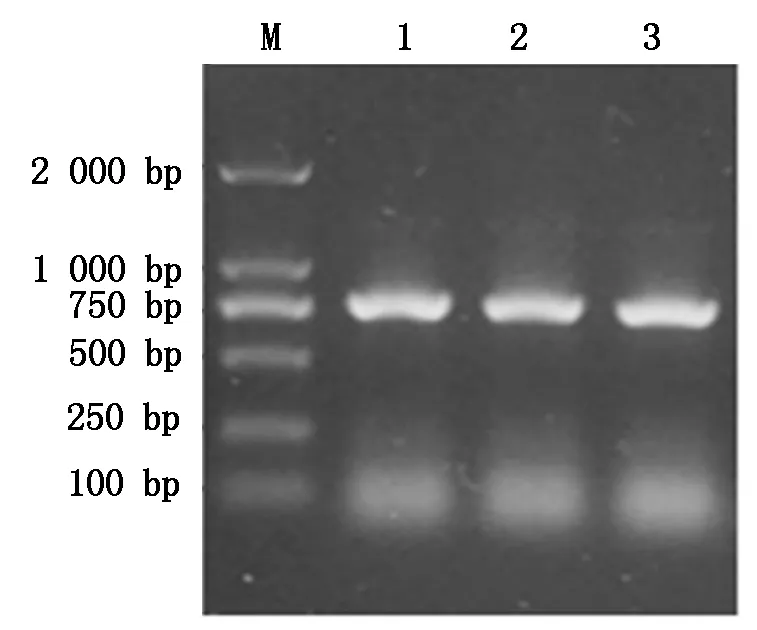
M.Marker DL2000;1-3.3管菌液。
2.3 谷子SiHd3a基因的序列分析
通過測序得到谷子SiHd3a的cDNA序列,如圖5所示。序列分析表明,該基因cDNA序列大小為792 bp,包含完整的CDS序列537 bp,編碼178個氨基酸。將測序結果與數據庫豫谷1號基因序列進行比對,只有3個堿基突變,分別位于豫谷1號SiHd3a基因序列的38,144,218 bp處,對應黃毛谷SiHd3a基因cDNA序列的32,138,212 bp處(圖6)。其中第1處突變位于編碼區外,第2處突變使豫谷1號SiHd3a蛋白第14位的精氨酸突變為黃毛谷SiHd3a蛋白的甘氨酸,第3處突變為同義突變,未造成所編碼氨基酸的改變(圖7)。

粗體下劃線.起始密碼子和終止密碼子;下劃線.引物序列。

圖6 黃毛谷與豫谷1號SiHd3a基因序列比對結果

圖7 黃毛谷與豫谷1號SiHd3a蛋白序列比對結果
2.4 谷子SiHd3a蛋白的理化性質分析
生物信息學分析發現,SiHd3a蛋白分子質量為19.74 ku,等電點(pI)為6.82。其一級結構中氨基酸豐度依次為甘氨酸(Gly,19個,10.70%)、纈氨酸(Val,18個,10.10%)、脯氨酸(Pro,16個,9.00%)、精氨酸(Arg,16個,9.00%)、亮氨酸(Leu,12個,6.70%)、丙氨酸(Ala,11個,6.02%)、天冬氨酸(Asp,11個,6.02%)、蘇氨酸(Thr,11個,6.02%)、苯丙氨酸(Phe,10個,5.60%)、天冬酰胺(Asn,8個,4.50%)、谷氨酰胺(Gln,7個,3.90%)、蛋氨酸(Met,7個,3.90%)、絲氨酸(Ser,7個,3.90%)、絡氨酸(Tyr,7個,3.90%)、谷氨酸(Glu,6個,3.40%)、半胱氨酸(Cys,3個,1.70%)、組氨酸(His,3個,1.70%)、異亮氨酸(Ile,3個,1.70%)、色氨酸(Trp,2個,1.10%)、賴氨酸(Lys,1個,0.60%)。帶負電荷的氨基酸有Asp、Glu,共17個,帶正電荷的氨基酸有Arg、Lys,共17個。對SiHd3a蛋白的親/疏水性進行分析表明,多肽鏈的第143位氨基酸分值最低,為-2.422,第13位氨基酸分值最高,為1.978。從整體上看,SiHd3a的親水氨基酸多于疏水氨基酸,可初步判斷SiHd3a為親水蛋白。
2.5 谷子SiHd3a蛋白的二級結構預測與亞細胞定位
SiHd3a蛋白的二級結構分析結果見表1,可以看出,谷子SiHd3a蛋白的二級結構中α螺旋29個,所占比例為16.29%;延伸鏈52個,所占比例為29.21%;β轉角20個,所占比例為11.24%;無規則卷曲77個,所占比例為43.26%。亞細胞定位分析發現,谷子SiHd3a蛋白定位在細胞質和細胞間質。
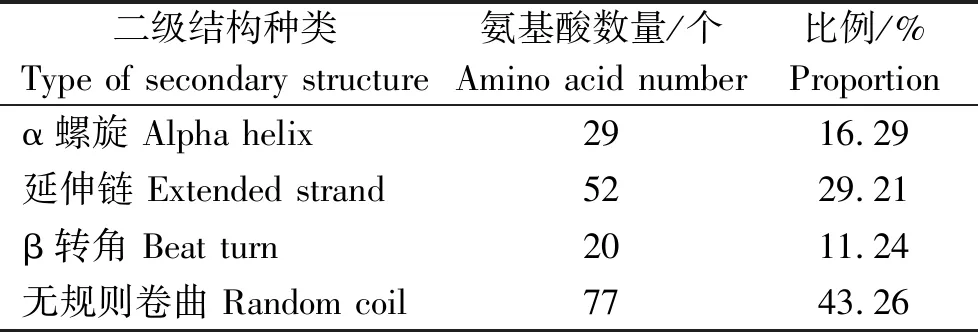
表1 SiHd3a蛋白的二級結構組成
2.6 谷子SiHd3a蛋白進化樹分析
從 NCBI 獲取與谷子SiHd3a蛋白相似性高的8種植物Hd3a蛋白氨基酸序列,構建的進化樹結果見圖8,可以看出,谷子與野生黍(Panicumhallii)、玉米(Zeamays)、高粱(Sorghumbicolor)親緣關系最近,4個物種聚為一個組,其次與節節麥(Aegilopstauschii)、二穗短柄草(Brachypodiumdistachyon)親緣關系較近,與3種稻類親緣關系最遠。
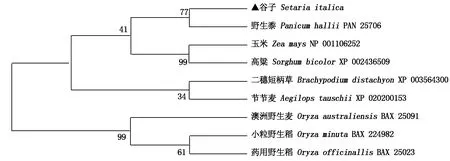
圖8 基于Hd3a蛋白氨基酸序列的9個物種進化樹
2.7 谷子SiHd3a基因表達半定量分析
SiHd3a基因在長、短日照條件下晝夜表達情況見圖9。從圖9可以看出,在短日照條件下SiHd3a基因呈24 h晝夜節律性表達特點:從下午15:00黑暗開始至凌晨3:00整個暗夜期,除凌晨3:00有少量表達外其余時間基因表達量均較低,早晨6:00開始光照,基因表達量最高,達到第1個峰值,早晨9:00至中午12:00 光照期間SiHd3a基因表達量有所下降,但仍維持較高表達水平,12:00達到1個小高峰。在長日照條件下SiHd3a基因表達并沒有出現明顯的晝夜節律性,從早晨6:00光照開始至凌晨3:00,無論光照期還是黑暗期SiHd3a基因均具有較強的表達活性,各時間點表達量差異不明顯,這與水稻中Hd3a基因長日照下表達規律不同。

A.短日照條件下;B.長日照條件下。
3 結論與討論
利用RT-PCR技術從黃毛谷克隆得到SiHd3a基因cDNA序列,包含1個537 bp的開放讀碼框,編碼178個氨基酸;生物信息學分析發現,SiHd3a為親水蛋白,定位在細胞質和細胞間質,谷子與野生黍、玉米、高粱的Hd3a蛋白進化關系較近,而與稻類進化關系較遠;SiHd3a基因在短日照條件下呈晝夜節律性表達,早晨6:00見光時達到最高峰,長日照條件下SiHd3a基因在晝夜24 h內表現穩定高表達。
Hd3a屬于水稻FT-like基因家族,該家族包括13個成員[12-13],其中Hd3a/FT-L2與RFT1(RICEFLOWERINGLOCUST1)/FT-L3同源性最高。在不同植物間Hd3a基因具有很高的保守性[14-15]。本研究表明,Hd3a蛋白在谷子、野生黍、玉米、高粱之間的進化關系比較近,而與水稻進化關系較遠,說明Hd3a進化過程中在C3與C4作物間可能產生了功能上的分化。
在野生型水稻中引入Hd3a可以導致早花表型,而利用RNAi(RNA interference)抑制Hd3a的表達會推遲開花,說明Hd3a具有促進水稻開花的功能[16-17]。將在大腸桿菌中表達的Hd3a重組蛋白分離純化后,對大花蕙蘭和蝴蝶蘭的葉和葉基部莖進行不同濃度蛋白注射,結果發現,注射的植株和未注射的植株在開花進程中未產生顯著差異[18]。事實上,Hd3a蛋白在葉片維管組織中合成,然后通過韌皮部維管組織運輸到頂端分生組織,證明Hd3a 蛋白可以長距離運輸[19]。Hd3a基因是水稻開花調控途徑的信息整合基因,負責將來自各種途徑的開花信號匯總起來,繼而誘導下游的花器官決定基因表達,從而誘導開花[20]。作為短日照植物,水稻的成花包括短日照促進途徑和長日照抑制途徑。短日照條件下水稻主要通過2條途徑即Hd1(Heading date 1)途徑和Ehd1(Early heading date 1)途徑促進開花,Hd1和Ehd1基因在短日照條件下表達能夠促進Hd3a的表達,從而加速水稻開花[21-22]。Hd1對Hd3a的調控并不像擬南芥CO(CONSTANS)調控FT那樣簡單,Hd1在長日照、短日照條件下均能正常表達,但是長日照條件下對開花起抑制作用,與短日照相反。Ehd1僅在短日照條件下誘導表達,且表達具有節律性,在Hd1基因失活的條件下仍能通過促進Hd3a的表達來誘導開花,且表達模式與Hd3a一致[23]。本研究發現,SiHd3a基因在短日照條件下表現晝夜節律表達特性,早晨6:00開始光照表達量最高,這與水稻Hd3a基因短日照條件下在黎明表達量最高是一致的[24],這種節律性表達可能是受Ehd1調控的結果。長日照條件下,水稻Hd3a基因表達量在各個階段都較低,因為Hd1在長日照條件下抑制Hd3a的表達,同時Ehd1基因表達量較低[25]。本研究發現,長日照條件下SiHd3a基因晝夜24 h內均有較強的表達活性,與水稻Hd3a長日照條件下低表達相反,產生這種結果的原因可能是本研究獲得的SiHd3a基因在長日照條件下對谷子開花沒有作用,谷子中可能存在著另一個成花素基因專門負責長日照條件下促進抽穗開花。因為本研究所使用的谷子材料黃毛谷對光周期敏感,長日照條件下抽穗期嚴重推遲,這與SiHd3a基因長日照條件下的高表達量存在矛盾。

