棉花色素腺體發育相關基因GhNAC201的克隆與表達分析
張 曦,錢玉源,劉 祎,王廣恩,宋世佳,李曉飛,米換房,崔淑芳,李俊蘭
(1.河北省農林科學院 棉花研究所,農業部黃淮海半干旱區棉花生物學與遺傳育種重點實驗室,國家棉花改良中心河北分中心,河北 石家莊 050051;2.河北省農林科學院,河北 石家莊 050051;3.河北工程大學,河北 邯鄲 056038;4.邯鄲市農業科學院,河北 邯鄲 056001)
棉花色素腺體(Pigment gland)又稱棉酚腺體,通常呈褐色或黑褐色點狀,是積累棉酚及其衍生物質的溶生腔隙,分布于棉屬(Gossypium)植物各主要器官[1-2]。棉花種子富含蛋白質、優質脂肪、碳水化合物、維生素、礦物質等,具有巨大的食用、保健、飼用和工業應用潛力。但由于棉酚對單胃動物和人類有毒害作用,嚴重限制了棉籽的綜合利用[3-4]。棉酚含量通常與腺體數量正相關[5]。研究棉花色素腺體發育和棉酚代謝的調控機制,發掘和利用關鍵基因開展低酚棉分子育種,具有重要理論意義和應用價值。

NAC(NAM/ATAF/CUC)轉錄因子屬于植物特有的基因超家族,參與植物生長發育、物質代謝、脅迫應答、信號轉導等生命過程[11-12]。通常NAC蛋白具有N端的DNA結合域和C端的轉錄調控區2個功能域,一些NAC蛋白的C端還含有跨膜基序[13]。Sun等[13]鑒定了4個棉種的NAC轉錄因子,分別為陸地棉(G.hirsutum)283個、海島棉(G.barbadense)267個、亞洲棉(G.arboreum)147個和雷蒙德氏棉(G.raimondii)149個。一些NAC轉錄因子已證實在棉花生長發育、脅迫應答等方面發揮重要作用。陸地棉GhXND1基因負調控植物木質部形成,在擬南芥(Arabidopsis)中超表達GhXND1后,木質部導管細胞減少,維管束間細胞的細胞壁變薄[14]。GhNAC12自棉花子葉開始衰老時(子葉展開后35 d)顯著上調表達,超表達GhNAC12引起擬南芥早衰[15]。陸地棉GhFSN1能夠正調控次生壁加厚和負調控纖維伸長[16]。棉花中超表達水稻SNAC1基因,可以促進根系生長和降低呼吸速率,從而增強植株耐鹽、耐旱性[17]。海島棉GbNAC1基因正調控擬南芥黃萎病抗性并參與多種非生物脅迫應答[18]。草棉GhNAC2基因在非脅迫條件下可以促進擬南芥和棉花生長。甘露醇和NaCl脅迫下,GhNAC2仍能促進擬南芥根系發育;水分脅迫下可減少轉基因棉花葉片的萎蔫和脫落[19]。GhNAC79超表達植株的抗旱性得到了提高[20]。棉花中超表達GhATAF1可以增強耐鹽性,但也提高了棉花對黃萎病和灰霉病病菌的敏感性[21]。
河北省農林科學院棉花研究所品種資源研究室對有腺體陸地棉品種中棉所12(以下簡稱中12)和其顯性無腺體近等基因系中棉所12顯性無腺體(以下簡稱中12顯無)幼胚進行轉錄組測序,篩選到1個在兩材料間顯著差異表達的NAC轉錄因子Gh-D06G2096。Gh-D06G2096在中12顯無幼胚發育過程中幾乎不表達,但在中12幼胚發育至花后35 d(腺體發育后期)時顯著上調表達,表明其可能與腺體形成密切相關[22]。本研究利用RT-PCR技術克隆了Gh-D06G2096編碼區(Coding sequence,CDS)序列,命名為GhNAC201,并對其進行了基因序列和時空表達模式分析,為NAC轉錄因子在棉花腺體發育中的功能研究和低酚棉育種提供理論基礎和可利用的基因資源。
1 材料和方法
1.1 植物材料與處理
本研究的試驗材料有腺體棉花品種中12和顯性無腺體材料中12顯無由國家棉花種質資源中期庫和國家棉花種質資源平臺提供,隱性無腺體品種邯無198由邯鄲市農業科學院提供。對3個棉花材料于種子萌發期、苗期、開花期和花后26 d分別取樣,每個樣品取2份,1份液氮速凍用于基因時空表達模式分析,1份用于觀察和計數腺體數量。種子萌發期:種子胚根伸長1 cm左右時剝殼。苗期:參照Zhang等[23]的方法種植水培苗,第2片真葉完全展開時分別取根、莖、葉、子葉。開花期:田間種植的植株取倒四葉、當天上午盛開的花和1 cm左右的幼蕾。花后26 d:田間種植的植株取倒四葉和花后26 d幼胚。激素處理:光照培養室中種植的中12幼苗第2片真葉完全展開時分別噴施脫落酸(Abscisic acid,ABA,100 μmol/L)、茉莉酸甲酯(Methyl jasmonate,MeJA,400 μmol/L)、赤霉素(Gibberellin,GA3,150 μmol/L)和油菜素內脂(Brassinosteroid,BR,1 μmol/L),于處理后0,3,6 h分別取葉片,用于基因激素應答分析。
1.2 棉花RNA提取和cDNA合成
使用RNAprep Pure Plant Kit(DP441,天根生化科技(北京)有限公司)提取樣品總RNA,并檢測其質量。參照FastQuant cDNA第一鏈合成試劑盒(KR106,天根生化科技(北京)有限公司)說明書合成cDNA,然后置于-20 ℃保存備用。
1.3 基因時空表達分析
用Primer Premier 5軟件設計GhNAC201的熒光定量PCR引物(表1),以Histone3為內參基因[2]。qRT-PCR使用SuperReal熒光定量試劑盒(FP205,天根生化科技(北京)有限公司),反應體系為20 μL:2×SuperReal PreMix Plus 10 μL,正向和反向引物(10 μmol/L)各0.6 μL,cDNA模板1 μL,RNase-free ddH2O 7.8 μL。采用Bio-rad熒光定量PCR儀,反應參數參照試劑盒說明書:95 ℃ 15 min;95 ℃ 10 s,60 ℃ 20 s,72 ℃ 30 s,40個循環,最后進行溶解曲線分析。每個樣品3次重復,采用2-ΔΔCT法計算基因的相對表達量。

表1 試驗中所使用的引物
1.4 基因克隆和序列分析
根據公布的TM-1(NAU-NBI_v1.1)Gh-D06G2096側翼序列,使用Primer Premier 5軟件設計基因克隆引物。以中12 cDNA為模板進行PCR擴增。PCR產物TA克隆后轉化大腸桿菌DH5α菌株,經菌液PCR鑒定的單克隆送蘇州金唯智生物科技有限公司測序。利用BlastX進行基因的同源性比對,用Mega 7.0進行序列比對和構建進化樹。利用ProtParam(http://www.expasy.org/tools/protparam.html)分析蛋白的理化性質;SMART(http://smart.embl-heidelberg.de/)預測蛋白功能域;TargetP 1.1(http://www.cbs.dtu.dk/services/TargetP/)預測蛋白的亞細胞定位;NetPhos 3.1(http://www.cbs.dtu.dk/services/NetPhos/)預測蛋白磷酸化位點;SOMPA和Phyre分別預測蛋白的二級和三級結構;MEME(http://meme-suite.org)預測蛋白氨基酸序列的保守motif,并用TBtools重新繪制motif圖。
1.5 棉花色素腺體數量的統計與分析
體視顯微鏡(LEICA DFC550)觀察和計數不同組織樣品腺體數量,并換算成腺體密度(個/cm2),分析棉花色素腺體的時空分布規律。
2 結果與分析
2.1 GhNAC201基因克隆及序列分析
利用RT-PCR技術克隆了中12中Gh-D06G2096的CDS序列(圖1),經測序驗證,與TM-1中參考序列(https://www.ncbi.nlm.nih.gov/)完全一致,參考Sun等[13]對陸地棉NAC基因的編號,命名為GhNAC201(GenBank登錄號:MN232001)。GhNAC201CDS區為948 bp,編碼315 aa。GhNAC201蛋白的分子量為36.8 ku,理論pI 5.97。SOPMA預測GhNAC201的二級結構包括27.94%的α-螺旋,18.10%的延伸鏈,5.40%的β-轉角和48.57%的無規則卷曲。三維結構預測表明,GhNAC201 26-190 aa序列與水稻(OryzasativaL. ssp.japonica)stress-responsive NAC1(SNAC1)蛋白序列高度匹配(100%置信度)。根據SNAC1晶體結構預測GhNAC201的三維結構(圖2)。GhNAC201蛋白在30-163 aa存在1個NAM結構域。用NetPhos 3.1預測潛在磷酸化位點,表明GhNAC201有16個絲氨酸、9個蘇氨酸和5個酪氨酸潛在修飾位點。其中第66,85,111,137,145 aa處的蘇氨酸磷酸化位點,第106,109,110,130,139,161 aa處的絲氨酸磷酸化位點和第118,127,152,157 aa處的酪氨酸磷酸化位點位于NAM結構域內(圖3)。用TargetP 1.1工具對GhNAC201的亞細胞定位進行預測(表2),表明GhNAC201定位于分泌通路(0.536)和其他亞細胞結構(0.721)的概率較高。
M.DL2000 DNA Marker;1.GhNAC201編碼區。

彩色箭頭方向為N→C末端。模型維度(?):X.55.229;Y.36.150;Z.46.112。

圖3 GhNAC201磷酸化位點預測

表2 GhNAC201亞細胞定位預測
2.2 GhNAC201同源蛋白進化及保守基序分析
將GhNAC201與棉屬及其他物種中代表性同源蛋白構建系統進化樹,結果表明,棉屬不同棉種中的GhNAC201同源序列的相似度很高,且與擬南芥和油菜(Brassicanapus)同源蛋白最為相似。GhNAC201在雙子葉植物中的同源性高于單子葉植物(圖4-A)。進一步分析GhNAC201及其同源蛋白的保守基序,可以發現基序1、基序2、基序3、基序4和基序7在不同物種中高度保守,GhNAC201與XP 017614396.1(G.arboreum)、XP 012452555.1(G.raimondii)基序組成模式完全一致(圖4-B)。
2.3 GhNAC201的時空表達模式與腺體密度的時空分布
GhNAC201在有腺體棉各個組織的表達均極顯著高于無腺體棉,且有腺體棉的種子、苗期根、苗期莖、苗期葉和花后26 d幼胚中GhNAC201豐度較高。2個無腺體棉材料中,GhNAC201僅在苗期根中表達量較高,在其他組織部位不表達或表達量很低(圖5-A)。在有腺體棉中12中,GhNAC201的時空表達模式與腺體密度時空分布規律趨于一致(圖5-B),且受ABA、BR、GA和MeJA誘導極顯著上調表達(圖5-C)。
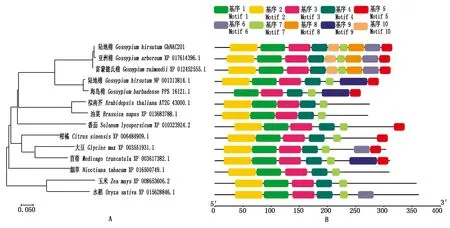
圖4 GhNAC201同源蛋白的進化(A)及保守基序(B)分析

A.3個棉花材料不同組織中GhNAC201的表達模式;B.中棉所12中GhNAC201表達模式與腺體密度的關聯;C.中棉所12中GhNAC201受激素誘導的表達模式。不同大寫字母表示1%水平差異顯著(P<0.01)。
A.Expression patterns ofGhNAC201in different tissues of 3 cotton germplasms; B.Correlationship between gland density and expression pattern ofGhNAC201in Zhongmiansuo 12;C.Expression patterns ofGhNAC201under hormone treatment in Zhongmiansuo 12.Different capital letters are significantly different at the 1% level(P<0.01).
圖5GhNAC201的時空表達模式及與腺體密度的關聯
Fig.5 Expression patterns ofGhNAC201and its correlationship with gland density
3 結論與討論
棉酚對人畜的毒害作用限制了棉株和棉籽的綜合利用[4]。棉花色素腺體發育與棉酚的合成與代謝密切相關[2,5],研究腺體發育及其對棉酚合成的調控機制,開展低酚棉分子育種,對于增加棉花產業附加值具有重要意義。
本研究克隆的GhNAC201基因在有腺體棉中的表達極顯著高于無腺體棉,且在有腺體棉中的時空表達模式與腺體密度的時空分布規律趨于一致,表明其與腺體形成存在較高相關性。棉花色素腺體是棉屬植物體內儲藏棉酚的囊狀內分泌結構[24],一般認為,棉酚及其衍生物由根尖合成,之后向植株地上部分輸送并貯藏于色素腺體內[25]。低酚棉全株無色素腺體,但在各器官中仍能檢測到少量游離棉酚[5]。本研究克隆的GhNAC201基因,通過生物信息學手段預測其可能定位于分泌通路,且其在無腺體棉中,僅在苗期根中的表達較高,在其他組織中幾乎不表達,推測其可能直接或間接調控棉酚代謝。
NAC轉錄因子廣泛參與植物生長發育、脅迫應答等生命過程[13]。對不同腺體類型材料進行轉錄組測序,可以檢測到NAC基因差異表達[2,26-27]。本研究室中12和中12顯無幼胚轉錄組測序結果表明,差異表達轉錄因子中,NAC數量最多。澳洲野生棉和亞洲棉萌發期種子轉錄組測序也得到了類似結果,差異表達的轉錄因子中,NAC數量僅次于MYB/MYB-related基因[26]。上述研究表明,NAC轉錄因子很可能參與了棉花腺體形成或棉酚代謝。進化樹和基序分析表明,GhNAC201及其同源蛋白在不同物種中序列相似性較高,其中有5個基序高度保守。故可以參考其他物種中同源基因的功能研究,分析GhNAC201在腺體發育或棉酚代謝中的作用。GhNAC201在擬南芥中的同源基因AT2G43000.1(又稱ANAC042、ATJUB1、NAC042等),可能通過調控P450基因,進而誘導擬南芥植保素的生物合成。但ANAC042是直接還是間接調控這些P450基因尚不明確[28]。P450也是棉酚合成的關鍵基因[29]。解析NAC轉錄因子調控P450的機制,為腺體發育及棉酚代謝提供了可參考的研究方向。擬南芥和番茄(Solanumlycopersicum)中,JUB1參與調控GA和BR代謝及信號通路[12,30]。NAC轉錄因子在依賴于ABA的信號轉導通路發揮重要作用[11]。本研究中,GhNAC201受GA、BR和ABA誘導表達,可能參與GA、BR和ABA信號通路。在生物脅迫下,NAC基因通過茉莉酸(Jasmonic acid,JA)通路參與應答[31]。棉花中,控制顯性無腺體性狀的基因GoPGF可能通過JA通路調控色素腺體形成及棉酚代謝[2]。GhNAC201在中12和中12顯無間差異表達,且受MeJA誘導,可能參與GoPGF調控的JA信號通路,影響色素腺體形成及棉酚代謝。綜上所述,GhNAC201與棉花色素腺體發育密切相關,可能通過ABA、BR、GA和JA通路調控腺體發育或棉酚代謝。

