血液惡性腫瘤患者中MTHFR基因多態性與大劑量甲氨蝶呤血液毒性相關性的Meta分析
劉爽 宋再偉 易湛苗 趙榮生

摘 要 目的:系統評價血液惡性腫瘤患者中亞甲基四氫葉酸還原酶(MTHFR) C677T及A1298C多態性與大劑量甲氨蝶呤(HDMTX)血液系統不良事件的相關性。方法:系統檢索Medline、Embase、Clinical Trials.gov、中國學術期刊網絡出版總庫、萬方數據庫、中國生物醫學文獻數據庫,收集采用HDMTX治療血液惡性腫瘤涉及MTHFR C677T及A1298C基因多態性的隊列研究,時限均為自建庫起至2018年3月。對符合納入標準的文獻進行資料提取,并采用紐卡斯爾-渥太華量表進行質量評價后,應用Rev Man 5.3軟件對不同遺傳模型下HDMTX血液系統不良事件進行Meta分析。結果:共納入25項隊列研究,其中23項研究關注MTHFR C677T位點(1 858例患者)、16項研究關注MTHFR A1298C位點(1 088例患者)。Meta分析結果表明,MTHFR C677T突變型顯著增加了血液毒性[TT/CT vs. CC:OR=1.57,95%CI(1.12,2.20),P=0.009;TT vs. CT/CC:OR=2.19,95%CI(1.49,3.23),P<0.001;T vs. C:OR=1.34,95%CI(1.03,1.74),P=0.03]、嚴重血液毒性[TT/CT vs. CC:OR=2.33,95%CI(1.43,3.81),P<0.001]的發生風險,具體包括增加了白細胞減少[TT/CT vs. CC:OR=1.37,95%CI(1.02,1.82),P=0.03]、嚴重白細胞減少[TT/CT vs. CC:OR=1.63,95%CI(1.03,2.56),P=0.04]、嚴重粒細胞減少[TT/CT vs. CC:OR=2.26,95%CI(1.50,3.39),P<0.001]的發生風險;MTHFR A1298C突變型顯著降低了嚴重血液毒性[CC/AC vs. AA:OR=0.17,95%CI(0.04,0.76),P=0.02]的發生風險,具體包括降低了白細胞減少[CC/AC vs. AA:OR=0.68,95%CI(0.48,0.97),P=0.03; CC vs. AC/AA:OR=0.28,95%CI(0.14,0.59),P<0.001]、嚴重白細胞減少[CC/AC vs. AA:OR=0.43,95%CI(0.19,0.97),P=0.04]的發生風險。結論:在血液惡性腫瘤患者中,MTHFR C677T突變型可能增加HDMTX血液毒性發生風險,包括白細胞減少以及粒細胞減少;而MTHFR A1298C突變型則可能降低HDMTX血液毒性發生風險,包括白細胞減少。
關鍵詞 亞甲基四氫葉酸還原酶;基因多態性;大劑量甲氨蝶呤;血液惡性腫瘤;安全性;Meta分析
ABSTRACT? ?OBJECTIVE: To systematically evaluate the correlation of methylenetetrahydrofolate reductase (MTHFR) C677T and A1298C gene polymorphisms with blood system adverse events induced by high-dose of methotrexate (HDMTX). METHODS: Retrieved from Medline, Embase, Clinical Trials.gov, CNKI, Wanfang database, CBM, cohort studies about MTHFR gene polymorphism in hematological neoplasm treated by HDMTX were collected from inceptions to March 2018. After data extraction of included literatures, quality evaluation with Newcastle Ottawa scale, Meta-analysis was performed for adverse events of blood system induced by HDMTX in different genetic models with Rev Man 5.3 software. RESULTS: Totally 25 cohort studies were included, 23 studies of which were related to MTHFR C677T site (including 1 858 patients) and 16 studies related to MTHFR A1298C site (including 1 088 patients). Results of Meta-analysis showed that MTHFR C677T mutation type significantly increased the risk of hematotoxicity [TT/CT vs. CC: OR=1.57, 95%CI(1.12,2.20), P=0.009;TT vs. CT/CC: OR=2.19, 95%CI(1.49,3.23), P<0.001;T vs. C: OR=1.34, 95%CI(1.03,1.74), P=0.03] and severe hematotoxicity [TT/CT vs. CC: OR=2.33, 95%CI(1.43,3.81), P<0.001], including leukopenia [TT/CT vs. CC: OR=1.37, 95%CI(1.02,1.82), P=0.03], severe leukopenia [TT/CT vs. CC: OR=1.63, 95%CI(1.03,2.56), P=0.04], severe granulopenia [TT/CT vs. CC: OR=2.26, 95%CI(1.50,3.39), P<0.001]. The mutation genotypes of MTHFR A1298C significantly decreased the risk of severe hematotoxicity [CC/AC vs. AA: OR=0.17, 95%CI(0.04,0.76), P=0.02], including leukopenia [CC/AC vs. AA: OR=0.68, 95%CI(0.48,0.97), P=0.03; CC vs. AC/AA: OR=0.28, 95%CI(0.14,0.59), P<0.001] and severe leukopenia [CC/AC vs. AA: OR=0.43, 95%CI(0.19,0.97), P=0.04]. CONCLUSIONS: Among patients with hematological neoplasms, MTHFR C677T mutation may significantly increase the risk of hematotoxicity by HDMTX including the risk of leukopenia and granulopenia; while MTHFR A1298C may reduce the risk of hematotoxicity by HDMTX, including the risk of leukopenia.
KEYWORDS? ?Methylenetetrahydrofolate reductase; Gene polymorphisms; High-dose methotrexate; Hematological neoplasms; Safety; Meta-analysis
甲氨蝶呤(Methotrexate,MTX)是臨床上重要的葉酸拮抗藥,屬于周期特異性細胞毒藥物,對增殖旺盛的細胞,尤其是處于S期的細胞具有較強的殺傷作用,可使細胞的DNA和RNA合成中斷,進而發揮阻斷腫瘤細胞增殖的作用[1]。MTX在非靶向性抑制腫瘤細胞增殖的同時,也會使正常細胞的代謝受阻,從而引起不同程度的不良事件,包括血液毒性、肝毒性、腎毒性、口腔黏膜炎、消化道毒性、皮膚毒性及神經毒性等[2]。目前臨床常用大劑量MTX(High-dose methotrexate,HDMTX,>500 mg/m2)[3]治療急性淋巴細胞白血病(ALL)、非霍奇金淋巴瘤(NHL)等血液系統腫瘤。HDMTX在提高血藥濃度、改善預后的同時,也增加了不良事件的發生風險。其中,骨髓抑制是HDMTX最嚴重的不良事件之一,主要表現為白細胞下降,也可見血小板減少,嚴重時可出現全血細胞下降、皮膚或內臟出血,臨床常根據患者化療后的白細胞、粒細胞、血小板及血紅蛋白等監測值對骨髓抑制進行嚴重程度分級[4-5]。
亞甲基四氫葉酸還原酶(Methylenetetrahydrofolate reductase,MTHFR)是葉酸代謝的關鍵酶之一,對DNA的合成、活化、修復等起調控作用,其中,C677T、A1298C是其常見的基因多態性位點[6]。目前多項研究結果表明,C677T、A1298C兩個位點的不同基因型對HDMTX血液系統不良事件發生風險的影響不盡相同,如樊春艷[7]研究表明,MTHFR C677T野生型患者發生骨髓抑制的風險顯著降低;Chiusolo P等[8]研究表明,MTHFR C677T多態性與血液毒性的發生風險無顯著相關性,MTHFR A1298C突變型降低了血液毒性的發生風險;而Kantar M等[9]研究則表明,MTHFR A1298C突變型增加了貧血及血小板減少的發生風險。因此,本研究納入并整合相關臨床證據,系統評價血液惡性腫瘤患者的MTHFR C677T、A1298C多態性對其HDMTX血液系統不良事件發生風險的影響,從而為臨床決策提供循證依據。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型 隊列研究。
1.1.2 研究對象 接受HDMTX治療的血液惡性腫瘤患者,包括ALL、NHL等患者。年齡、性別及種族均不限。
1.1.3 干預措施 MTHFR C677T與A1298C基因型患者分別按照野生型與突變型分組。
1.1.4 結局指標 ①血液毒性/骨髓抑制率;②嚴重血液毒性/骨髓抑制率;③白細胞減少率;④嚴重白細胞減少率;⑤粒細胞減少率;⑥嚴重粒細胞減少率;⑦血小板減少率;⑧嚴重血小板減少率;⑨貧血發生率;⑩嚴重貧血發生率;11淋巴細胞減少率;12嚴重淋巴細胞減少率。不良反應分級標準參照世界衛生組織(WHO)抗癌藥物毒副作用分級(嚴重程度:0級為正常或輕微,3~4級為重度)[1]、美國國家癌癥研究所常見不良反應評價標準(CTCAE,嚴重程度:1級為正常或輕微,3~4級為重度)[1]或其他通用標準。
1.1.5 排除標準 結局指標為非血液毒性或血藥濃度/排泄延遲的研究;不符合哈迪-溫伯格平衡定律(HWE)[10]的研究;無法定量合并的研究;非中英文研究;重復文獻(樣本重復的文獻則僅納入最新發表的文獻);聯系原文作者后仍無法獲取全文的文獻;數據有誤或缺失的文獻。
1.2 檢索策略
英文以“Methotrexate”及其同義詞和“Acute lymphoblastic leukemia”“B cell lymphoma”“Polymorphim”“Methylenetetrahydrofolate reductase”“MTHFR”等為關鍵詞,中文以“甲氨蝶呤”及其同義詞和“急性淋巴細胞白血病”“B細胞淋巴瘤”“亞甲基四氫葉酸還原酶”“基因多態性”等為關鍵詞,檢索英文數據庫包括Medline、Embase,中文數據庫包括中國學術期刊網絡出版總庫、萬方數據庫、中國生物醫學文獻數據庫,并補充檢索Clinical Trials.gov,時限均為自建庫起至2018年3月。此外,利用Google等搜索引擎手工補充檢索綜述和納入文獻的參考文獻。
1.3 文獻篩選和數據提取
兩位研究者獨立篩選文獻,按照題目、摘要、全文的逐級順序確定符合納排標準的研究,交叉核對后如有分歧,通過與第三人討論解決。兩位研究者閱讀全文后獨立提取納入研究的基本信息,主要包括第一作者、發表年份、血液腫瘤類型、患者數、性別和年齡構成、結局指標及不良反應分級標準。若納入研究中數據缺失,則嘗試通過郵件等方式聯系原文作者。提取過程如遇分歧,則通過討論或咨詢第三人裁決。
1.4 質量評價
兩位研究者采用Cochrane協作網推薦的紐卡斯爾-渥太華量表(NOS)[11]獨立評價,量表包括研究人群選擇(4個條目)、組間可比性(1個條目)、結果測量(3個條目)3個部分,滿分為9分,其中7~9分為高質量研究,5~6分為中等質量研究,1~4分為低質量研究。綜合評價后如有分歧,則通過討論或咨詢第三人裁決。
1.5 統計分析方法
應用Microsoft Excel 2016軟件建立數據庫,對納入研究的基因型分布頻率進行χ2檢驗,P>0.05表明樣本符合HWE,說明具有群體代表性。采用Rev Man 5.3軟件進行定量分析(Meta分析)。Meta分析時,采用比值比(OR)作為計數資料的分析統計量,效應量以95%置信區間(CI)表示,分別計算顯性遺傳模型(MM/Mm vs. mm)、隱性遺傳模型(MM vs. Mm/mm)、等位基因遺傳模型(M vs. m)下的OR值及95%CI(“M”在MTHFR C677T中表示T,在MTHFR A1298C中表示C)。用Z檢驗分析OR值是否具有統計學意義(P<0.05表示具有統計學意義),所有分析均采用固定效應模型合并OR值。采用q檢驗分析各研究間的異質性(檢驗水平α=0.1),并根據I 2評價研究間的異質性大小,Phet>0.1(Phet為異質性的P值)或I 2≤50%表明異質性尚可;Phet≤0.1且I 2>50%表明異質性顯著,應進一步分析異質性來源[12]。各研究結果存在統計學異質性時,首先排除數據提取錯誤,其次當文獻數量足夠時,按照不同種族、年齡(兒童或成人)等進行亞組分析,進而判斷是否可以解釋異質性來源。采用敏感性分析判斷Meta分析結果的穩定性及可靠性,逐篇剔除納入Meta分析的研究,去除低質量研究后與原合并結果進行比較,若未使原結果發生逆轉,則合并結果可能較為可靠;若最終未明確異質性來源,則換用隨機效應模型,或只行定性分析。如果研究數量大于10,則采用漏斗圖評估納入研究是否存在發表偏倚[13]。
2 結果
2.1 文獻篩選流程及結果
共檢索到1 901項相關原始研究,經除重和閱讀題目、摘要及全文后,最終納入25項隊列研究[7-8,14-36],其中與MTHFR C677T有關的隊列研究有23項[7-8,14-29,31-33,35-36],共1 858例患者;與MTHFR A1298C有關的隊列研究有16項[7-8,16-18,20-22,27-28,30-31,33-36],共1 088例患者;同時涉及MTHFR C677T和MTHFR A1298C的研究有14項[7-8,16-18,20-22,27-28,31,33,35-36]。25項研究中,中文研究有9項[7,23-27,29,35-36],英文研究有16項[8,14-22,28,30-34]。文獻篩選的具體流程圖詳見圖1。
2.2 納入研究的基本特征及質量評價
納入人群均為ALL或NHL等血液系統惡性腫瘤患者,其中17項研究[7,14,16-18,20-23,26,28-29,31-32,34-36]限定患兒,5項研究[15,19,27,30,33]限定成人,3項研究[8,24-25]同時納入了患兒與成人。大部分研究中不良事件的定義采用了WHO標準或CTCAE。報告MTHFR C677T多態性的23項研究的NOS平均分為7.52分,報告MTHFR A1298C多態性的16項研究的NOS平均分為7.75分,可見納入研究均為高質量研究。其中,8項研究[14,16-19,21,30,34]滿足NOS的所有條目,均充分考慮了納入人群的選擇性與隊列間的可比性,但多數研究未報道隨訪情況。納入研究的基本特征及質量評價結果詳見表1。
2.3 MTHFR C677T多態性對HDMTX血液毒性的影響
共有11項研究[7-8,16,23-25,28-29,31-33]報告了MTHFR C677T與骨髓抑制的相關性,Meta分析結果詳見表2。結果顯示,在3種遺傳模型下,突變型均顯著增加了骨髓抑制的發生風險[TT/CT vs. CC:OR=1.57,95%CI(1.12,2.20),P=0.009(見圖2); TT vs. CT/CC:OR=2.19,95%CI(1.49,3.23),P<0.001; T vs. C:OR=1.34,95%CI(1.03,1.74),P=0.03](受文章篇幅限制,部分森林圖略,下同)。
上述Meta分析納入的研究間均無顯著異質性(Phet>0.10)。基于年齡與種族分層的亞組分析表明,一方面,在顯性遺傳模型中,突變型顯著增加了成人骨髓抑制的發生風險(Psub=0.03,Psub為亞組間的P值),而在隱性遺傳模型及等位基因模型中,不同年齡亞組間的差異無統計學意義(Psub>0.05);另一方面,各種族間的差異無統計學意義(Psub>0.05)。
共有4項研究[15,27,29,32]報告了MTHFR C677T與嚴重骨髓抑制的相關性。在顯性遺傳模型下,突變型增加了嚴重骨髓抑制的發生風險,且差異有統計學意義[TT/CT vs. CC:OR=2.33,95%CI(1.43,3.81),P<0.001]。在隱性遺傳模型下,伴隨顯著異質性(Phet<0.10,I 2=75%)。對異質性來源進行分析,首先排除了數據提取錯誤,亞組分析提示亞洲人群與高加索人群之間存在顯著差異(Psub=0.03),故異質性可能源于種族差異。
2.3.1 MTHFR C677T與白細胞減少的相關性 共有7項研究[17-18,20-22,25-26]報告了MTHFR C677T與白細胞減少的相關性。在顯性遺傳模型下,突變型顯著增加了白細胞減少的發生風險[TT/CT vs. CC:OR=1.37,95%CI(1.02,1.82),P=0.03(見圖3)]。而在隱性及等位基因遺傳模型下,未觀察到顯著相關性。但在等位基因遺傳模型下,伴隨顯著異質性(Phet<0.10,I 2=61%)。對異質性來源進行分析,首先排除了數據提取錯誤,亞組分析提示亞洲人群與高加索人群之間存在顯著差異(Psub=0.03),故異質性可能源于種族差異。
共有3項研究[14-15,20]報告了MTHFR C677T與嚴重白細胞減少的相關性。在顯性遺傳模型下,突變型顯著增加了嚴重白細胞減少的發生風險[TT/CT vs. CC:OR=1.63,95%CI(1.03,2.56),P=0.04],但伴隨顯著異質性(Phet<0.10,I 2=56%),基于年齡及種族的亞組分析均未觀察到顯著相關性。
2.3.2 MTHFR C677T與粒細胞減少的相關性 共有5項研究[16,25,28,35-36]報告了MTHFR C677T與粒細胞減少的相關性。在3種遺傳模型下,MTHFR C677T與粒細胞減少發生風險無顯著相關性,但均伴隨顯著異質性(Phet<0.10,I 2>50%)。對異質性來源進行分析,排除數據提取錯誤,針對年齡與種族分層的亞組分析提示患兒、成人及混合人群之間,亞洲人與非洲人之間的差異均有統計學意義(Psub<0.05),故異質性可能源于納入患者的年齡及種族差異。
共有2項研究[14-15]報告了MTHFR C677T與嚴重粒細胞減少的相關性。在顯性遺傳模型下,突變型顯著增加了嚴重粒細胞減少的發生風險[TT/CT vs. CC:OR=2.26,95%CI(1.50,3.39),P<0.001]。
2.3.3 MTHFR C677T與血小板減少、貧血及淋巴細胞減少的相關性 分別有11項研究[17-22,25-26,28,35-36]、10項研究[17-21,25-26,28,35-36]、2項研究[19,25]報告了MTHFR C677T與血小板減少、貧血及淋巴細胞減少的相關性。在3種遺傳模型下,均無顯著相關性,且納入的各研究間均無顯著異質性(Phet>0.10,I 2≤30%)。
分別有3項研究[15,20,28]、2項研究[15,20]、1項研究[15]報告了MTHFR C677T與嚴重血小板減少、嚴重貧血及嚴重淋巴細胞減少的相關性。在3種遺傳模型下,均無顯著相關性。
2.4 MTHFR A1298C多態性對HDMTX血液毒性的影響
共有6項研究[7-8,16,27,31,33]報告了MTHFR A1298C與骨髓抑制的相關性,Meta分析結果詳見表3。在3種遺傳模型下,均無顯著相關性,且納入的各研究間無顯著異質性(Phet>0.10)。基于1項研究[27]的結果表明,在顯性遺傳模型下,突變型顯著降低了嚴重骨髓抑制的發生風險[CC/AC vs. AA:OR=0.17,95%CI(0.04,0.76),P=0.02]。
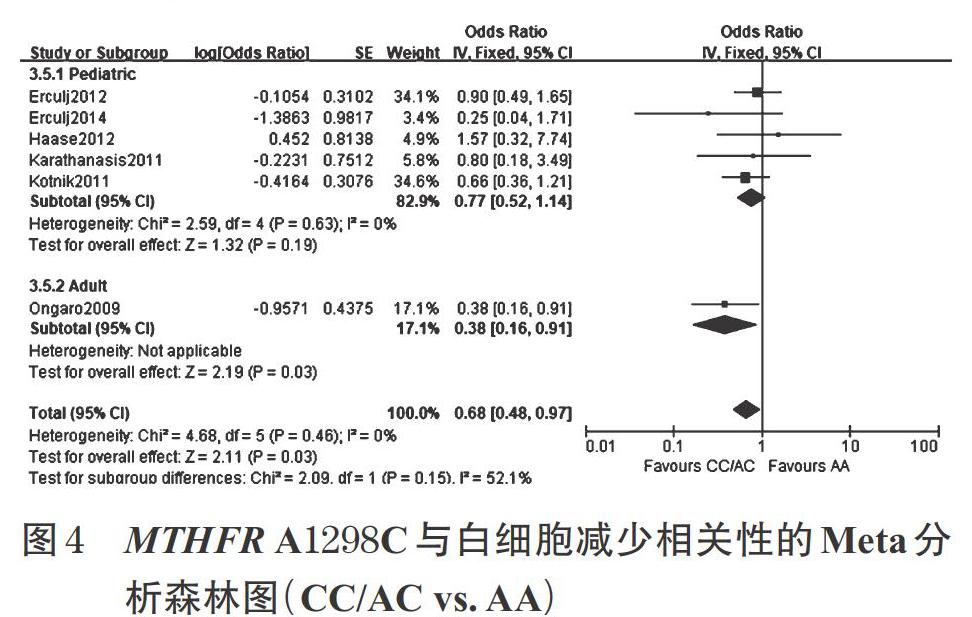
2.4.1 MTHFR A1298C與白細胞減少的相關性 共有6項研究[17-18,20-22,30]報告了MTHFR A1298C與白細胞減少的相關性。在顯性遺傳模型及隱性遺傳模型下,突變型降低了白細胞減少的發生風險,差異有統計學意義[CC/AC vs. AA:OR=0.68,95%CI(0.48,0.97),P=0.03(見圖4)]; CC vs. AC/AA:OR=0.28,95%CI(0.14,0.59),P<0.001],且納入的各研究間無顯著異質性(Phet>0.10)。
共有2項研究[20,30]報告了MTHFR A1298C與嚴重白細胞減少的相關性。在顯性遺傳模型下,突變型降低了嚴重白細胞減少的發生風險,差異有統計學意義[CC/AC vs. AA:OR=0.43,95%CI(0.19,0.97),P=0.04],且2項研究間無顯著異質性(Phet>0.10)。
2.4.2 MTHFR A1298C與粒細胞減少的相關性 共有4項研究[16,28,35-36]報告了MTHFR A1298C與粒細胞減少的相關性。在3種遺傳模型下,MTHFR A1298C與粒細胞減少的發生風險無顯著相關性,但顯性遺傳模型納入的各研究間伴隨顯著異質性(Phet<0.10,I 2=53%)。對異質性來源進行分析,排除數據提取錯誤,針對年齡與種族分層的亞組分析提示患兒及成人之間、亞洲人與非洲人之間的差異均有統計學意義(Psub<0.05),故異質性可能源于各研究間納入患者的年齡及種族差異。1項研究[30]表明,MTHFR A1298C與嚴重粒細胞減少的發生風險無顯著相關性。
2.4.3 MTHFR A1298C與血小板減少、貧血的相關性 分別有8項研究[17-18,20-22,28,35-36]、2項研究[20,28]、7項研究[17-18,20-21,28,35-36]、1項研究[20]報告了MTHFR A1298C與血小板減少、嚴重血小板減少、貧血及嚴重貧血的相關性。在3種遺傳模型下,MTHFR A1298C與上述不良事件的發生風險均無顯著相關性,僅在隱性遺傳模型下的血小板減少、嚴重血小板減少伴有顯著異質性(Phet<0.10,I 2=52%、57%)。基于年齡及種族的亞組分析均未觀察到顯著差異(Psub>0.05)。
2.5 敏感性分析與發表偏倚
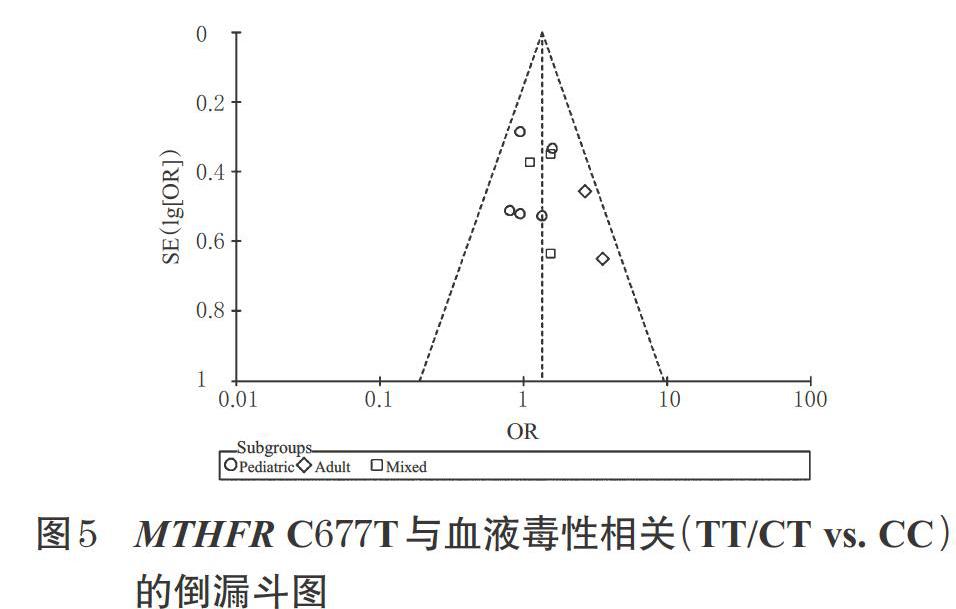
對表2中MTHFR C677T與HDMTX血液系統不良事件相關性的31項Meta結果進行敏感性分析,21項Meta結果在逐篇剔除納入研究后合并效應量均未發生顯著改變;對表3中MTHFR A1298C與HDMTX血液系統不良事件相關性的21項Meta結果進行敏感性分析,15項Meta結果在逐篇剔除納入研究后合并效應量均未發生顯著改變,這表明上述Meta結果整體均較穩定。上述各結局指標漏斗圖基本對稱,呈近似倒漏斗狀,未觀察到明顯的發表偏倚,詳見圖5(僅列出TT/CT vs. CC的倒漏斗圖,余圖略)。
3 討論
MTX對增殖速度快的細胞抑制強度大,主要抑制已經定向分化的骨髓幼稚細胞,對未定向分化的骨髓多能造血干細胞的損傷較輕,故骨髓抑制是MTX常見的不良事件[37]。MTX通過抑制MTHFR發揮抗葉酸代謝的作用。MTHFR是葉酸代謝途徑中的關鍵酶,催化5,10-亞甲基四氫葉酸還原為5-甲基四氫葉酸,其正常的活性能夠保證葉酸代謝、DNA合成和甲基化的正常進行,而MTHFR基因發生突變將會影響酶的催化活性,干擾DNA的合成及損傷修復,從而導致MTX給藥后不良事件的發生風險增加[38]。
本系統評價整合現有的原始研究,在嚴格評價納入研究質量的基礎上對結局指標進行定量合并,綜合23項關于MTHFR C677T和16項關于MTHFR A1298C的研究的Meta分析結果,發現MTHFR C677T突變型與更高風險的(嚴重)血液毒性/骨髓抑制相關,具體包括(嚴重)白細胞減少、嚴重粒細胞減少及嚴重貧血,不良反應嚴重程度可能是導致血液系統不良事件發生風險差異的影響因素;MTHFR A1298C突變型則與更低風險的嚴重血液毒性/骨髓抑制相關,包括(嚴重)白細胞減少。亞組分析結果表明,年齡因素可能會影響MTHFR C677T與血液毒性(包括粒細胞減少)的相關性,種族因素可能會影響MTHFR C677T與嚴重血液毒性(包括白細胞減少及粒細胞減少)的相關性;年齡及種族因素可能均會影響MTHFR A1298C與粒細胞減少的相關性。敏感性分析結果表明,大部分研究結果穩健性較好,信度尚可。
對比既往已發表的系統評價[39-40],大多在單一遺傳模型下進行定量分析,或納入研究未限制MTX的給藥劑量及患者病種類型,或未依據血液系統不良事件的嚴重程度進行亞組分析以及未充分評估原始研究質量。本研究考慮到HDMTX用于不同病種(如骨肉瘤)在給藥劑量與輸注時間等用藥方案方面存在差異,故僅關注HDMTX在血液惡性腫瘤患者中的應用,并結合3種遺傳模型合并效應量,因此更全面集中地評價了MTHFR C677T及A1298C兩個位點的多態性對HDMTX血液系統不良事件發生風險的影響;其次,納入的原始研究總體質量較高,均滿足HWE,因此具有較好的群體代表性。但本研究尚存在一定局限性,如部分合并結果受納入原始研究數目限制(小于10項),發表偏倚不能完全除外;此外,部分研究未提及不良事件分級標準,且不同研究間HDMTX具體輸注方案存在差異,故臨床異質性無法完全除外。因此,本文所得結論仍需更高質量、更大樣本量的原始研究進一步驗證。
參考文獻
[ 1 ] RADTKE S,ZOLK O,RENNER B,et al. Germline genetic variations in methotrexate candidate genes are associated with pharmacokinetics,toxicity,and outcome in childhood acute lymphoblastic leukemia[J]. Blood,2013,121(26):5145-5153.
[ 2 ] SCHMIEGELOW K. Advances in individual prediction of methotrexate toxicity:a review[J]. Brit J Haematol,2009,146(5):489-503.
[ 3 ] HOWARD SC,MCCORMICK J,PUI CH,et al. Preventing and managing toxicities of high-dose methotrexate[J]. Oncologist,2016,21(12):1471-1482.
[ 4 ] 汪洋,葉琦,張華年,等.應用群體藥動學-藥效學結合模型評估大劑量甲氨蝶呤化療后的骨髓抑制[J].中國新藥雜志,2017,26(19):70-78.
[ 5 ] 裔照國,劉洪月,丁哲,等.甲氨蝶呤臨床常見不良反應及其應對方法[J].中國藥物與臨床,2014,14(11):1529- 1530.
[ 6 ] MATTIA ED,TOFFOLI G. C677T and A1298C MTHFR polymorphisms,a challenge for antifolate and fluoropyrimidine-based therapy personalisation[J]. Eur J Cancer,2009,45(8):1333-1351.
[ 7 ] 樊春艷. MTHFR、ABCB1基因多態性與急性淋巴細胞白血病患兒甲氨蝶呤化療毒副反應的關系[D].烏魯木齊:新疆醫科大學,2017.
[ 8 ] CHIUSOLO P,GIAMMARCO S,BELLESI S,et al. The role of MTHFR and RFC1 polymorphisms on toxicity and outcome of adult patients with hematological malignancies treated with high-dose methotrexate followed by leucovorin rescue[J]. Cancer Chemother Pharmacol,2012,69(3):691-696.
[ 9 ] KANTAR M,KOSOVA B,CETINGUL N,et al. Methylenetetrahydrofolate reductase C677T and A1298C gene polymorphisms and therapy-related toxicity in children treated for acute lymphoblastic leukemia and non-hodgkin lymphoma[J]. Leuk Lymphoma,2009,50(6):912-917.
[10] 翁鴻,江梅,仇成鳳,等.遺傳關聯性研究Meta分析中的Hardy-Weinberg平衡[J].中國循證心血管醫學雜志,2016,8(11):1281-1283.
[11] STANG A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses[J]. Eur J Epidem,2010,25(9):603-605.
[12] SEDGWICK P. Meta-analyses:what is heterogeneity? [J]. BMJ,2015.DOI:10.1136/bmj.h1435.
[13] SEDGWICK P,MARSTON L. How to read a funnel plot in a Meta-analysis[J]. BMJ,2015.DOI:10.1136/bmj.h4718.
[14] AR?OZ HV,DALOI K,FONCUBERTA ME,et al. Pharmacogenetic studies in children with acute lymphoblastic leukemia in Argentina[J]. Leuk Lymphoma,2015,56(5):1370-1378.
[15] CHOI YJ,PARK H,LEE JS,et al. Methotrexate elimination and toxicity:MTHFR 677C>T polymorphism in patients with primary CNS lymphoma treated with high- dose methotrexate[J]. Hematol Oncol,2016,35(4):504- 509.
[16] EISSA DS,AHMED TM. C677T and A1298C polymorphisms of the methylenetetrahydrofolate reductase gene:effect on methotrexate-related toxicity in adult acute lymphoblastic leukaemia[J]. Blood Coagul Fibrinol,2013,24(2):181-188.
[17] ER?ULJ N,KOTNIK BF,DEBELJAK M,et al. Influence of folate pathway polymorphisms on high-dose methotrexate-related toxicity and survival in childhood acute lymphoblastic leukemia[J]. Leuk Lymphoma,2012,53(6):1096-1104.
[18] ER?ULJ N,DEBELJAK M,JAZBEC J,et al. The influence of folate pathway polymorphisms on high-dose methotrexaterelated toxicity and survival in children with non-Hodgkin malignant lymphoma[J]. Radiol Oncol,2014,48(3):289-292.
[19] GEMMATI D,ONGARO A,TOGNAZZO S,et al. Methylenetetrahydrofolate reductase C677T and A1298C gene variants in adult non-Hodgkins lymphoma patients:association with toxicity and survival[J]. Haematologica,2007,92(4):478-485.
[20] HAASE R,ELSNER K,MERKEL N,et al. High dose methotrexate treatment in childhood ALL:pilot study on the impact of the MTHFR 677C>T and 1298A>C polymorphisms on MTX-related toxicity[J]. Klinische Padiatrie,2012,224(3):156-159.
[21] KARATHANASIS NV,STIAKAKI E,GOULIELMOS GN,et al. The role of the methylenetetrahydrofolate reductase 677 and 1298 polymorphisms in Cretan children with acute lymphoblastic leukemia[J]. Genetic Testing and Molecular Biomarkers,2011,15(1/2):5-10.
[22] KOTNIK BF,GRABNAR I,GRABAR PB,et al. Association of genetic polymorphism in the folate metabolic pathway with methotrexate pharmacokinetics and toxicity in childhood acute lymphoblastic leukaemia and malignant lymphoma[J]. Eur J Clin Pharmacol,2011,67(10):993- 1006.
[23] 李天媛,王斌,徐康康,等.急性淋巴細胞白血病患兒亞甲基四氫葉酸還原酶基因C677T多態性與甲氨蝶呤毒副反應的研究[J].南京醫科大學學報(自然科學版),2010,30(3):386-389.
[24] 李靜,王捷,趙軍,等.亞甲基四氫葉酸還原酶基因多態性與甲氨蝶呤不良反應的相關性[J].中國臨床藥理學雜志,2014,30(12):1086-1088.
[25] 李靜,王捷,郁長治,等.亞甲基四氫葉酸還原酶基因多態性與急性淋巴細胞白血病患者甲氨蝶呤化療藥物不良反應的相關性研究[J].中國臨床藥理學雜志,2017,33(17):1634-1636.
[26] 廖清船,李曉蕾,劉思婷,等. MTHFR基因多態性及單體型與大劑量甲氨蝶呤化療毒性反應的相關性研究[J].中華流行病學雜志,2012,33(7):735-739.
[27] 劉晶霞,陳潔平,譚文,等.亞甲基四氫葉酸還原酶基因多態性與急性淋巴細胞白血病患者甲氨蝶呤化療毒副反應的研究[J].中國實驗血液學雜志,2008,16(3):488- 492.
[28] LIU SG,LI ZG,CUI L,et al. Effects of methylenetetrahydrofolate reductase gene polymorphisms on toxicities during consolidation therapy in pediatric acute lymphoblastic leukemia in a Chinese population[J]. Leuk Lymphoma,2011,52(6):1030-1040.
[29] 聶朝霞,劉嵐,崔巍. MTHRF基因C677T多態性與ALL患兒MTX血藥濃度和毒副反應的相關性[J].醫學臨床研究,2012,29(2):295-298.
[30] ONGARO A,DE MATTEI M,DELLA PORTA MG,et al. Gene polymorphisms in folate metabolizing enzymes in adult acute lymphoblastic leukemia:effects on methotrexate-related toxicity and survival[J]. Haematologica,2009,94(10):1391-1398.
[31] PAKAKASAMA S,KANCHANAKAMHAENG K,KAJANACHUMPOL S,et al. Genetic polymorphisms of folate metabolic enzymes and toxicities of high dose methotrexate in children with acute lymphoblastic leukemia[J]. Ann Hematol,2007,86(8):609-611.
[32] SHIMASAKI N,MORI T,SAMEJIMA H,et al. Effects of methylenetetrahydrofolate reductase and reduced folate carrier 1 polymorphisms on high-dose methotrexate-induced toxicities in children with acute lymphoblastic leukemia or lymphoma[J]. Int J Pediatr Hematol Oncol,2006,28(2):64-68.
[33] SUTHANDIRAM S,GAN GG,ZAIN SM,et al. Effect of polymorphisms within methotrexate pathway genes on methotrexate toxicity and plasma levels in adults with hematological malignancies[J]. Pharmacogenomics,2014,15(11):1479-1494.
[34] TANTAWY AA,EL-BOSTANY EA,ADLY AA,et al. Methylene tetrahydrofolate reductase gene polymorphism in Egyptian children with acute lymphoblastic leukemia[J]. Blood Coagul Fibrinol,2010,21(1):28-34.
[35] 伍艷鵬,賀湘玲,鄒潤英,等.急性淋巴細胞白血病患兒 MTHFR基因多態性與大劑量甲氨蝶呤化療后不良反應的關系[J].廣東醫學,2015,36(3):413-416.
[36] 鄭苗苗,岳麗杰,陳小文,等.急性淋巴細胞白血病患兒MTHFR基因多態性與大劑量甲氨蝶呤毒副反應的關系[J].中國當代兒科雜志,2013,15(3):201-206.
[37] 焦力,周道斌,王書杰,等.血藥濃度監測在大劑量甲氨蝶呤治療中的應用價值[J].中國醫學科學院學報,2009,31(5):564-566.
[38] KODIDELA S,SURESH CP,DUBASHI B. Pharmacogenetics of methotrexate in acute lymphoblastic leukaemia:why still at the bench level?[J]. Eur J Clin Pharmacol,2014,70(3):253-260.
[39] YAO P,HE X,ZHANG R,et al. The influence of MTHFR genetic polymorphisms on adverse reactions after methotrexate in patients with hematological malignancies:a meta-analysis[J]. Hematology,2018,24(1):10-19.
[40] 黃琳,于芝穎,顧群,等.亞甲基四氫葉酸還原酶基因多態性與甲氨蝶呤不良反應關系的Meta分析[J].中國臨床藥理學雜志,2016,32(2):183-185.
(收稿日期:2019-10-21 修回日期:2019-12-21)
(編輯:劉明偉)

