中歐藥物警戒制度的比較研究
胡歆雅,梁玉清,曾亞莉,王 剛,梁 毅*
(1 中國藥科大學國際醫藥商學院,南京 210000;2 科睿唯安,倫敦 SE18EZ)
藥物警戒(pharmacovigilance,PV)一詞的詞根來源于希臘語Pharmakon(“藥用物質”的意思)和拉丁語Vigilia(“保持警惕”的意思)。世界衛生組織(WHO)將其定義為“與發現、評估、理解和預防各種不良反應或與其他任何可能的藥物問題有關的科學研究和活動[1]”。1961年,“沙利度胺海豹胎兒事件”的發生,反映出藥品安全性監管方面的諸多問題,引起世界各國對動實驗的可靠性以及藥品上市后監測的重要性的關注與思考。1970年,WHO成立了藥物監測中心(WHO Drug Monitoring Centre),1978年遷移至烏普薩拉,并更名為世界衛生組織國際藥物監測合作中心,簡稱烏普薩拉監測中心(Uppsala Monitoring Centre,UMC)。自此,國際藥品監管制度發生了巨大變化,藥品安全性監測活動變得系統化、組織化和規范化。歐盟自2012年7月執行新版藥物警戒法規,至今已形成了相當完備的藥物警戒制度。而我國于2019年8月頒布新修訂的《中華人民共和國藥品管理法》(簡稱“新《藥品管理法》”,下同),將藥物警戒制度寫入法律。目前來講,我國藥物警戒制度建設仍在探索階段,需要借鑒先進的藥物警戒理念與方法。因此,本文將中歐藥物警戒制度進行比較,通過法律框架、監管范圍、機構設置和數據庫建設方面的比較分析,剖析我國藥物警戒制度現狀,為其進一步發展提出建議。
1 法律框架
1998年,中國開始建立藥品不良反應監測與報告制度,鼓勵企業自主上報藥品不良反應。2004年3月原國家食品藥品監督管理局和衛生部共同頒布《藥品不良反應報告和監測管理辦法》(局令第7號)。2011年,《藥品不良反應報告和監測管理辦法》(簡稱“81號令”,下同)發布,正式規定了藥品生產企業、藥品經營企業、醫療機構應報告藥品不良反應以及藥品監管部門在藥品不良反應監管中所承擔的責任和義務,詳細說明了藥品不良反應報告、定期安全性更新報告(PSUR)和重點監測的要求[2]。2017年,中國正式加入人用藥品注冊技術要求國際協調會議(ICH),開始逐步適用ICH指導原則,藥物不良反應的報告和電子傳輸開始與國際接軌。2018年,《關于藥品上市許可持有人直接報告不良反應事宜的公告》(簡稱“66號公告”,下同)正式發布,明確藥品上市許可持有人(簡稱“持有人”,下同)建立藥品不良反應監測體系、及時報告藥品不良反應、加強不良反應監測數據的分析評價及采取有效的風險控制措施的主體責任,進一步完善了我國藥品不良反應監測制度。2019年,新《藥品管理法》正式將藥物警戒制度立法,規定“國家建立藥物警戒制度,對藥品不良反應及其他與用藥有關的有害反應進行監測、識別、評估和控制”,我國對藥物警戒工作的重視程度進一步提升,藥物警戒制度的建設與發展開始進入新篇章。中國藥物警戒制度相關的主要文件見表1。
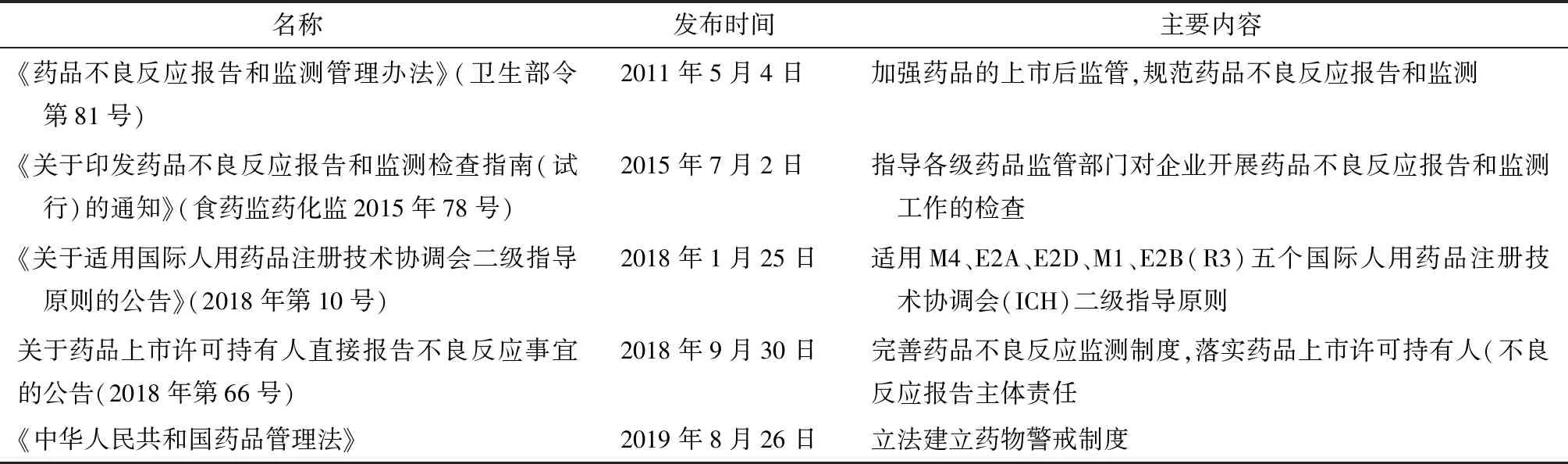
表1 中國藥物警戒制度相關的主要文件
資料來源:科睿唯安Cortellis RI全球藥政法規情報數據庫
1965年1月,歐盟理事會頒布第65/65號(EEC)指令,標志歐盟藥事立法的開始。2001年,歐盟頒布第2001/83號(EC)指令,統一了人用藥品相關的規定,專門設置第9章規定藥物警戒的總體要求。2010年通過的第2010/84號(EU)指令和第1235/2010號(EU)法規,于2012年7月正式生效,修訂后的藥物警戒法規對歐盟藥物警戒制度進行了實質性的更新,完善了關于藥品上市后監測的法律體系,明確了藥品主管機構和持有人的分工和責任[3]。2012年,歐盟頒布了第2012/26號(EU)指令和第1027/2012號(EU)法規,提高了藥物警戒制度的執行要求,特別是對藥品安全性問題的及時通知和評估。同年,為支持新法的實施,歐盟制定了《藥物警戒實踐指南》(Good Pharmacovigilance Practices,GVP),為藥物警戒工作的開展提供了一整套的指南。歐盟藥物警戒制度立法的主要文件見表2。GVP共包括16個模塊(見表3),涵蓋藥物警戒的主要方面,目前已制定完成,其中模塊編號Ⅺ、Ⅻ、和因有其他指導文件替代而保持無效狀態[4]。

表2 歐盟藥物警戒制度立法的主要文件
資料來源:科睿唯安Cortellis RI全球藥政法規情報數據庫
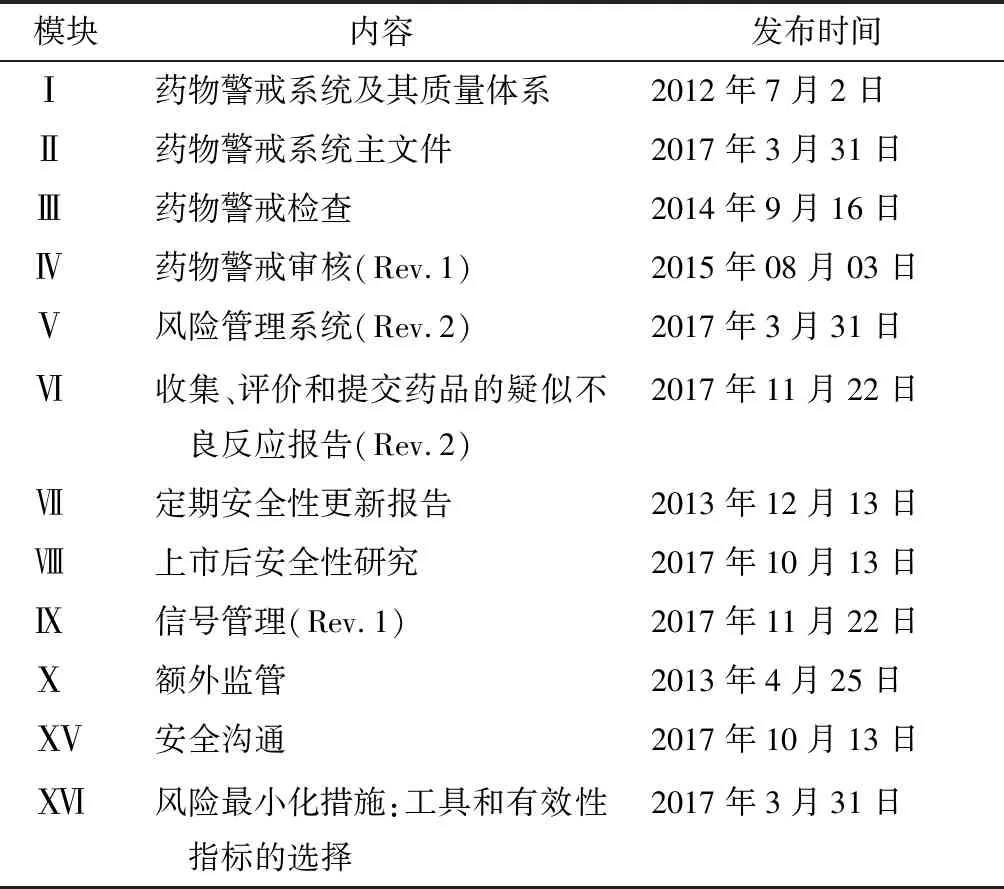
表3 歐盟GVP模塊介紹
資料來源:科睿唯安Cortellis RI全球藥政法規情報數據庫
2 監管范圍
第81號令規定了我國藥品不良反應的報告范圍,即合格藥品在正常用法用量下出現的與用藥目的無關的有害反應。2018年,66號公告的發布擴大了報告范圍,規定按照可疑即報的原則,上報患者使用藥品出現的與用藥目的無關且無法排除與藥品存在相關性的所有有害反應。因此,我國藥物警戒的監管范圍也隨之擴大,包括藥品上市后研究、風險管理計劃、藥品不良反應信息收集和反饋、監測數據定期分析評價等方面[5]。我國無菌藥品警戒監測范圍的擴大,一方面了擴大藥品不良反應的收集規模,提升了藥品安全性方面的監管質量;另一方面也讓持有人從被動方轉為主動方,通過建立自身的藥物警戒體系,自發向藥監部門報告,提高了藥監部門處理藥品風險的效率。
歐盟在2010年發布了第2010/84號(EU)指令,將藥品不良反應的定義擴大為用藥后出現的有害和非預期反應。這一舉措不僅擴大了藥品不良反應的上報范圍,增加了藥品不良反應的報告數量,也提高了藥物警戒數據分析結果的質量。目前,歐盟藥物警戒的監管范圍涉及藥品關鍵信息的收集、數據和信息的分析理解、維護公眾健康的監管活動以及與利益相關方的溝通4個領域,包括風險管理計劃、PSUR、患者和醫護人員的不良反應報告、藥物警戒系統主文件(PSMF)、藥品信號檢測等一系列行為[6]。這種嚴密的藥品監測,能夠讓主管部門及時干預并盡可能減少與使用藥物相關的不良反應或潛在風險的發生。
3 機構設置
我國藥品不良反應監測機構是國家藥品不良反應監測中心(NCADRM),該機構承擔了國家藥品不良反應報告和監測資料的收集、評價、反饋和上報,以及全國藥品不良反應監測信息網絡的建設和維護等職責。截至2011年末,我國已經建立34個省級藥品不良反應監測中心和333個地市級藥品不良反應監測中心,形成了從國家到縣級的四級藥品不良反應監測中心。由于我國國土遼闊,人口眾多,醫療機構和藥品生產企業遍布各地,因此這種層級分明,層層上傳信息的機構設置能夠適應我國的基本國情[7]。
歐盟的藥物警戒工作機構是藥物警戒風險評估委員會(PRAC)。2010年,歐洲藥品管理局(European Medicines Agency, EMA)為加強歐洲藥品的安全性監測,根據藥物警戒立法正式成立了PRAC。PRAC是EMA負責評估及監測人用藥物安全事務的科學委員會。它由成員國監管機構的藥物安全專家、歐洲委員會提名的科學專家以及患者和醫療保健專業人員的代表組成[8],主要負責與不良反應風險相關的檢測、評估、建議和溝通,在藥品安全性評價方面發揮關鍵作用[9]。PRAC的獨立設置既使自身成為藥品監管系統中最先進的部分,也保證了歐洲藥品的安全性和有效性。
4 數據庫建設
國家藥品不良反應監測系統,作為我國的藥物警戒數據庫,目前設有持有人報告、醫療機構/經營企業報告、監測機構管理3個入口。2018年,全國藥品不良反應監測網絡共收到149.9萬份《藥品不良反應/事件報告表》。1999~2018年累計收到1368萬份《藥品不良反應/事件報告表》,其中86.8%的報告來自醫療機構,來自藥品生產企業的報告僅占5.1%。該系統目前僅持有人、醫療機構和監管機構能夠查詢使用;公眾沒有訪問權限,因此無法獲取藥品不良反應相關的信息。目前,公眾僅能通過《藥品不良反應信息通報》獲知我國上報的藥品不良反應信息,但該通報發布時間無規律且自2010年后每年發布的期數明顯減少[10]。
EudraVigilance,作為歐盟藥物警戒數據庫,是EMA用于監測所有已上市藥品和臨床試驗中研究藥品安全性的工具。根據第726/2004號(EU)法規,與EudraVigilance相關的活動主要包括:藥品不良反應報告的收集與處理(包括醫學文獻檢索到的報告)、歐盟所有批準藥品信息數據庫的維護和更新、風險信號的識別[11]。2017年11月12日,EMA發布新的EudraVigilance系統,增強了疑似不良反應報告和分析功能。2018年,EudraVigilance共收集201.6萬份上市后疑似不良反應報告,擁有超過1450萬份個例藥品不良反應報告(ICSRs)。目前,歐洲地區公眾可以訪問EudraVigilance數據庫,并查詢和下載病例列表和病例報告表格。其他利益相關方,包括上市許可持有人、監管機構、醫療機構等都可以在一定權限內訪問該數據庫,獲得各自需要的信息。
人工智能,作為近年新興技術,針對來自藥物警戒遇到的挑戰,目前已經有相關解決方案。主要挑戰包括:信息及時跟蹤、管理和監控所有利益相關者、縮短上報監管機構時間、制定行動方案優先級、把控安全趨勢、全面的審計準備工作等。
5 中歐藥物警戒制度的比較
通過比較上述中國和歐盟的藥物警戒制度現狀,可以發現:第一,在法律框架方面,中國藥物警戒相關的法律法規正處于快速更新的節奏中,特別是在66號公布發布之后;但相關法規過于碎片化,缺乏系統的藥物警戒指導文件。第二,在監管范圍方面,中國從之前的“狹義”藥品不良反應擴大為使用藥品出現的與用藥目的無關且無法排除與藥品存在相關性的所有有害反應,依然側重于上市后監測,與歐盟覆蓋藥品全生命周期的藥物警戒還存在差距。第三,在機構設置方面,基于中國國情的“地方模式”缺乏地方與地方的信息交流以及中央與地方的聯系和有效溝通。第四,在數據庫建設方面,我國藥品不良反應監測系統,除了收集不良反應報告的基礎功能,缺乏進一步的數據分析、預警功能和相應的風險防控,同時沒有足夠公開的訪問權限設置。
6 對我國藥物警戒制度建設的建議
6.1 建立系統的藥物警戒制度框架
歐盟GVP為藥物警戒的開展提供了一整套的指南,我國66號公告可以看做是建立該指南的探索,要求持有人建立藥物警戒系統,設立專門的人員負責執行和管理。在此,建議我國參照歐盟GVP,結合現有法律法規,從藥物警戒體系建設、藥物警戒人員要求和培訓、藥物警戒文件管理、藥物警戒審核等方面,制定一部既與國際接軌又符合中國實際的藥物警戒實踐指南。除了指導上市許可持有人之外,該指南還應明確藥監部門及其下屬部門的職責,明確醫療機構、藥品經營企業和個人在藥物警戒活動中的輔助作用。
6.2 形成覆蓋藥品全生命周期的藥物警戒制度
藥物警戒貫穿藥品發展的始終,涵蓋從藥品上市前研究、上市后安全性監測及評價、直至最后的撤市或淘汰的整個藥品生命周期。目前,國家藥品監督管理局藥品審評中心(CDE)負責藥品上市前研究,包括藥品注冊、臨床試驗登記等;國家藥品不良反應監測中心負責藥品不良反應的收集和報告、上市后藥品安全性監測及評價。也就是說,我國臨床試驗和上市后監測存在斷層現象。一方面,建議我國制定關于藥品上市前安全性研究的指南,開通藥品風險的上報渠道,及時發現藥品的潛在風險。另一方面,建議我國加強藥品上市前研究和上市后監測的安全性方面的數據交流,實現數據互通;同時,適當調整機構職能,實現覆蓋藥品全生命周期的藥物警戒制度。
6.3 完善我國藥物警戒數據庫
建議我國借鑒歐盟EudraVigilance數據庫的先進功能,以及應用人工智能等先進技術,通過收集藥品全生命周期的安全性信息,加強監測藥品安全問題的能力,提高數據分析效率,優化不良反應報告程序。該數據庫為藥監部門、企業及其他利益相關者提供更有效的系統的同時,也要求解決藥監部門地方與地方的信息交流以及中央與地方的聯系和有效溝通問題。藥品收集數據的全面性和完整性有助于藥監部門早期發現并及時評估新的藥物不良反應或已知藥物不良反應的新變化(如頻率或嚴重程度的改變),及時通知相關利益者,將藥品安全性的風險降到最低。在權限訪問方面,建議我國不良反應監測系統適當開放數據庫的權限,供公眾查詢信息,而不是讓藥品安全數據和信息僅僅面向醫療機構、企業和監管部門。

