土壤有效鉛與全鉛線性規律研究
肖自昌

摘要 本文以尤溪縣的部分瓜類、豆類蔬菜相應的表層土壤為材料,通過原子吸收分光光度法測定土壤有效鉛與全鉛的濃度狀況,通過實驗數據表明土壤有效鉛與全鉛呈極顯著的直線關系。
關鍵詞 土壤;鉛;有效鉛
中圖分類號:X8 文獻標識碼:A 文章編號:2095–3305(2020)07–0–03
DOI:10.19383/j.cnki.nyzhyj.2020.07.049
Study on the Linear Law of Available Lead and Total Lead in Soil
XIAO Zi-chang (Youxi environmental monitoring station of Sanming City, Sanming, Fujian 365100)
Abstract This article take Youxi County's partial melons class, the legumes vegetables corresponding surface layer soil as a material, through the atomic absorption spectrophotometric method determination soil effective lead and the entire lead density condition, through the empirical datum indicated the soil effective lead and the entire lead assume the extremely remarkable linear relation.
Key words Soil; Lead; Effective lead
1 土壤鉛污染
1.1 土壤鉛污染源
土壤中的鉛污染主要來源于大氣含鉛塵粒的降落、含鉛廢渣的堆放、含鉛污水灌溉農田、含鉛污泥作肥料使用等,來自于礦山、冶煉、蓄電池廠、電鍍廠、合金廠、涂料等工廠排放的“三廢”,也是非常重要的鉛污染源。
1.2 土壤鉛對人體和植物的危害
鉛中毒對人體危害很大,鉛中毒會引起腎功能不全,表現為血清尿素和尿酸的升高,過量鉛還對心肌線粒體產生破壞,從而導致心臟功能障礙。鉛影響腦組織乙酰膽堿代謝,抑制了神經突觸的傳導,導致精神運動的協調功能減退。鉛使大腦皮層興奮和抑制功能紊亂,引起一系列神經系統癥狀,當人體吸收過量鉛時,產生精神障礙,出現記憶衰退、疲勞、頭昏等癥狀,鉛過量使兒童心不在焉、表達能力差、智力較低,鉛中毒還會引起高血壓,并且兒童比成人更容易遭受鉛的毒害。鉛的毒性還表現在生殖毒性、致癌性、致突變性等[1]。
鉛進入土壤后,會產生明顯的生物效應,可導致植物特別是其根部中毒,葉色不一致變化、抽穗期和成熟期推遲、籽實畸形、植株枯萎,甚至死亡,產量降低等。匡少平等[2]研究表明,土壤環境激素鉛不會對玉米、水稻等作物產生明顯的宏觀毒害效應,但可直接被作物吸收,殘留在作物的各個部位。
1.3 影響植物對鉛吸收的因素
影響植物吸收鉛的因素很多。就土壤因素而言,土壤pH、有機質含量、陽離子交換量、氧化還原電位、土壤機械組成等都可能影響植物的吸收。植物因素也影響其對鉛的吸收,如植物品種、植物生長狀況和生長期、植物其他元素的吸收情況等。此外,環境因素也會通過影響植物的生長狀況而影響植物對鉛的吸收。
2 材料與方法
2.1 土壤樣品的采集
此次樣品采自尤溪縣管前鎮南華村、坂面鎮坂面村、洋中鎮后樓村、新陽鎮雙鯉村、梅仙鎮梅營村等各蔬菜區土壤,樣品數58個。采樣時,先用竹片刮去表層土,再借用輔助工具鐵鏟挖成直角三角形狀,用竹片刮去表層土后在直角邊取足夠土樣。樣品裝入潔凈聚乙烯塑料袋,寫上標簽,盡快運回實驗室處理。
2.2 土壤樣品前處理與測定方法
土壤鉛全量測定前處理:準確稱取0.2~0.5 g(精確至0.0 002 g)試樣(<0.149 mm)于50 ml聚四氟乙烯坩鍋中,用水潤濕后加入10 ml鹽酸,于通風廚內的電熱板上低溫加熱,使樣品初步分解,蒸發至約剩3 ml左右時,取下稍冷,然后加入5 ml硝酸、5 ml氫氟酸、3 ml高氯酸,加蓋后電熱板上中溫加熱。1 h后,開蓋,繼續加熱除硅,為了達到良好的飛硅效果,應經常搖動坩鍋,當加熱至冒濃厚白煙時,加蓋,使黑色的有機碳化物分解。待坩鍋壁上的黑色有機物消失后,開蓋驅趕高氯酸白煙并蒸至內容物呈粘稠狀,視消解情況可再加入3 ml硝酸、3 ml氫氟酸和1 ml高氯酸,重復上述消解過程。當白煙再次冒盡且坩鍋內容物呈粘稠狀時,取下稍冷,用水沖洗坩鍋和內壁,并加入1 ml鹽酸溶液溫熱溶解殘渣,然后將溶液轉至50 ml容量瓶中,定容到標線搖勻待測。
土壤鉛全量測定:鉛元素用石墨爐原子吸收分光光度法(GB/T,17141-1997)測定。測定原理是,采用鹽酸硝酸—氫氟酸—高氯酸全消解方法,徹底破壞土壤的礦物晶格,使試樣中的待測元素全部進入試液。然后,將試液注入石墨爐中。經過預先設定的干燥、灰化、原子化等升溫程序使共存基體蒸發出去,同時在原子化階段的高溫下;鉛化合物離解為基態原子蒸汽,并對空心陰極燈發射的特征譜線產生選擇性吸收。在選擇的最佳測定條件下,通過背景扣除,測定試液中鉛的吸光度。本次測定的儀器參數:測定波長283.3 nm、通帶寬度1.3 nm、燈電流7.5 mA、干燥溫度85℃、灰化溫度700℃、原子化溫度2 000℃、清除溫度2 600℃。氬氣流量200 ml/min。
土壤有效鉛測定前處理:采用DTPA法提取測定。準確稱取5.0 g左右通過2 mm篩孔(尼龍篩)的風干土樣放于100 ml具塞錐形瓶中,加入25 ml DTPA浸提劑,稱取二乙三胺五乙酸{[(CHOCOCH2)2CH2]NCH2COOH,優級純}置于1 L容量瓶中,加TEA(三乙醇胺)13.3 ml,加二次去離子水950 ml,再加1.47 g無水氯化鈣(CaCl2,優級純),用鹽酸溶液[c(HCl)=6 mol/L]調節pH值至7.3,然后定容至刻度,加蓋,防止振蕩時溶液飛濺,而后在室溫下,塑料瓶放于振蕩機振蕩120 min,速度為210轉/min,注意把塑料瓶放在振蕩網時要盡量緊,以防振蕩時脫落。振蕩完后取下,過濾到小塑料瓶中待測。
樣品的測定:本次測定有效鉛方法是火焰原子吸收分光光度法測定(GB/T,23739-2009)。采用的儀器:原子吸收光譜儀-島津AA-6300C。儀器參數:測定波長283.3 nm、通帶寬度0.7 nm、燈電流10 mA、乙炔流量2 L/min、空氣流量15 L/min。
3 質量保證與質量控制
3.1 標準曲線的制作
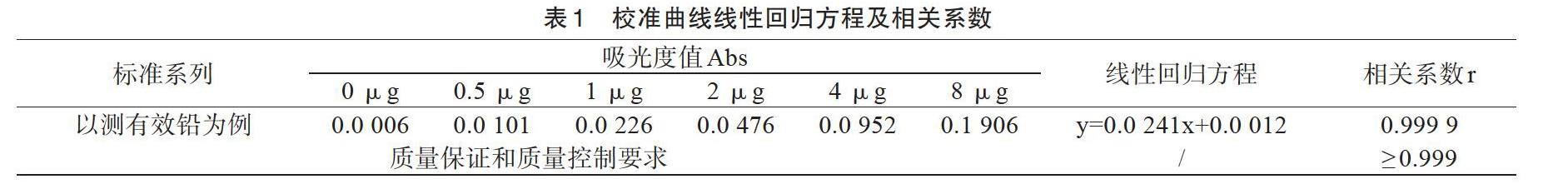
校準曲線線性回歸方程及相關系數(表1)。
3.2 精密度檢驗
樣品平行測定結果(表2)。
3.3 準確度檢驗
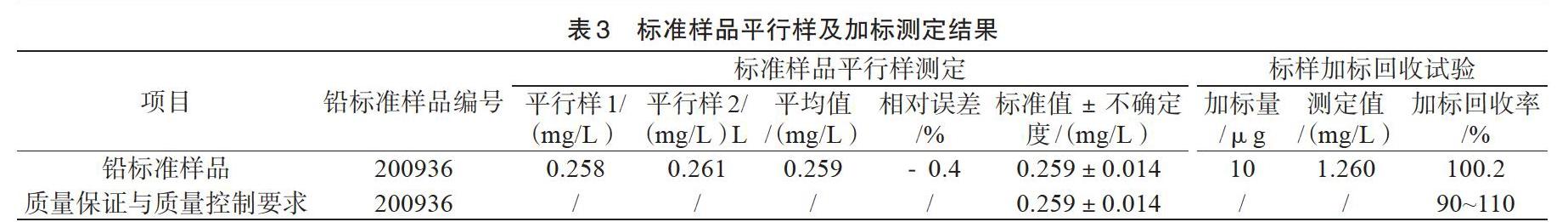
標準樣品平行樣及加標測定結果(表3)。
4 結果與討論
4.1 各蔬菜品種采樣區土壤含鉛狀況
分別列出了不同蔬菜采樣區土壤全鉛量和不同蔬菜采樣區土壤有效鉛含量(表4、5),總體低于國家土壤污染風險篩查值(農用地鉛=80 mg/kg1),只有個別樣品超標,這可能與采樣區的周圍環境有關,因為個別樣品的鉛土壤背景值較高,且周圍有鉛礦和生產鉛的工廠,造成其土壤含鉛量較高。
從所有土壤采樣區的有效鉛與全鉛的關系(圖1)可以看出:土壤有效鉛的含量隨著土壤全鉛含量的升高而升高,R2=0.819**(n=58),得出R=0.9050,土壤有效鉛量與全鉛量呈極顯著的直線相關,即土壤全鉛量可以解釋土壤有效鉛量變化的81.9%。
5 小結
(1)不同蔬菜采樣區土壤全鉛含量和有效鉛含量總體低于國家土壤污染風險篩查值(農用地鉛=80 mg/kg1),只有個別樣品超標,這可能與采樣區的周圍環境有關,因為個別樣品的鉛土壤背景值較高,且周圍有鉛礦和生產鉛的工廠,造成其土壤含鉛量較高。
(2)土壤有效鉛量與全鉛量呈極顯著的直線相關,即土壤全鉛量可以解釋土壤有效鉛量變化的81.9%。考慮到有效鉛測定比全鉛測定更容易,所以用土壤有效鉛來指示土壤鉛向蔬菜的轉移傾向更合理。
參考文獻
[1] 陳懷滿.環境土壤學[M].北京:科學出版社,2005.
[2] 匡少平,張書圣.作物對土壤中環境激素鉛的吸收效應及污染防治[J].農業環境保護,2002,21(6):481–484.
責任編輯:黃艷飛

