基于納米材料改良酶聯免疫吸附法的研究進展
張光胤 - 魯 迨 鄧放明 - 趙 倩 石星波 -
(1.食品科學與生物技術湖南省重點實驗室,湖南 長沙 410128;2.湖南農業大學食品科學技術學院,湖南 長沙 410128)
酶聯免疫吸附(ELISA)是一種基于抗原與抗體的特異性相結合,以及酶催化反應建立的方法,通過酶與抗體或抗原偶聯形成酶偶聯物,當抗原與抗體特異結合時,酶偶聯物催化無色底物分子轉化為易于檢測的產物(例如有色產物)[1]。通過底物信號的變化可以判斷免疫反應是否發生,進而分析目標物(抗原、抗體)的濃度[2]。由于操作簡便,檢測成本低,高速通量且可以目測預判等優點,ELISA已成為臨床診斷、食品質量控制和環境監測等領域公認的標準方法[3]。但這種傳統的ELISA檢測性能在很大程度上取決于酶的催化活性和負載量。而傳統的生物酶耐熱性差、保質期短、容易失活等,并且酶負載量有限,導致其檢測穩定性與靈敏度較差[4]。
近年來,具有特殊的光、電、磁以及催化性質的新型納米材料的成功合成為開發新型ELISA法帶來了新的機遇。目前,關于改良型ELISA的研究較多[5-6],如利用金納米顆粒(AuNPs)作為比色信號底物與金納米棒(AuNRs)酶載體的改良型ELISA。但是,隨著基于納米材料構建的改良型ELISA的迅速發展,相關綜述總結其進展尚未見報道。
文章擬聚焦基于納米材料構建的改良型ELISA,總結其在信號檢測模式(如比色法、熒光法、電化學和光熱傳感)方面的研究進展,對其發展方向以及所面臨的挑戰進行展望與分析,為ELISA在生物分子檢測方面提供新思路。
1 改良型比色ELISA
1.1 基于納米材料改良信號輸出比色ELISA
傳統酶底物的顏色響應能力可以滿足高濃度目標物的檢測需求,但不適用于痕量目標物的高靈敏度檢測。納米材料特殊的光、電、磁以及催化性質,使其可以作為信號底物的替代物,以改善肉眼的視覺感知,適合超靈敏檢測。
由于具有較大的摩爾消光系數和很強的局部表面等離子體共振(LSPR)效應,AuNPs可以作為信號底物。其信號的產生主要基于AuNPs的聚集及原位生長。表面修飾的抗體、核酸以及化學配體可以觸發金納米顆粒的聚集。Jiang等[7]構建了辣根過氧化物酶(HRP)介導的碘化物催化的級聯反應,以調節AuNPs的分散/聚集。由圖1可知,在過氧化氫(H2O2)存在下,通過在抗體上修飾的HRP將碘化物氧化為碘單質,從而發生半胱氨酸誘導的金納米粒子聚集,使溶液由紅色變為藍色。與基于3,3′,5,5′-四甲基聯苯胺(TMB)的ELISA相比,這種級聯反應可使肉眼讀出的靈敏度提高20倍。此外,Huang等[8]通過氧化氫酶(CAT)調節H2O2濃度介導的AuNPs生長開發的改良型ELISA對赭曲霉毒素A(OTA)表現出極高的靈敏度,檢測限為5×10-20g/mL,比常規ELISA(10-11g/mL)低8個數量級。
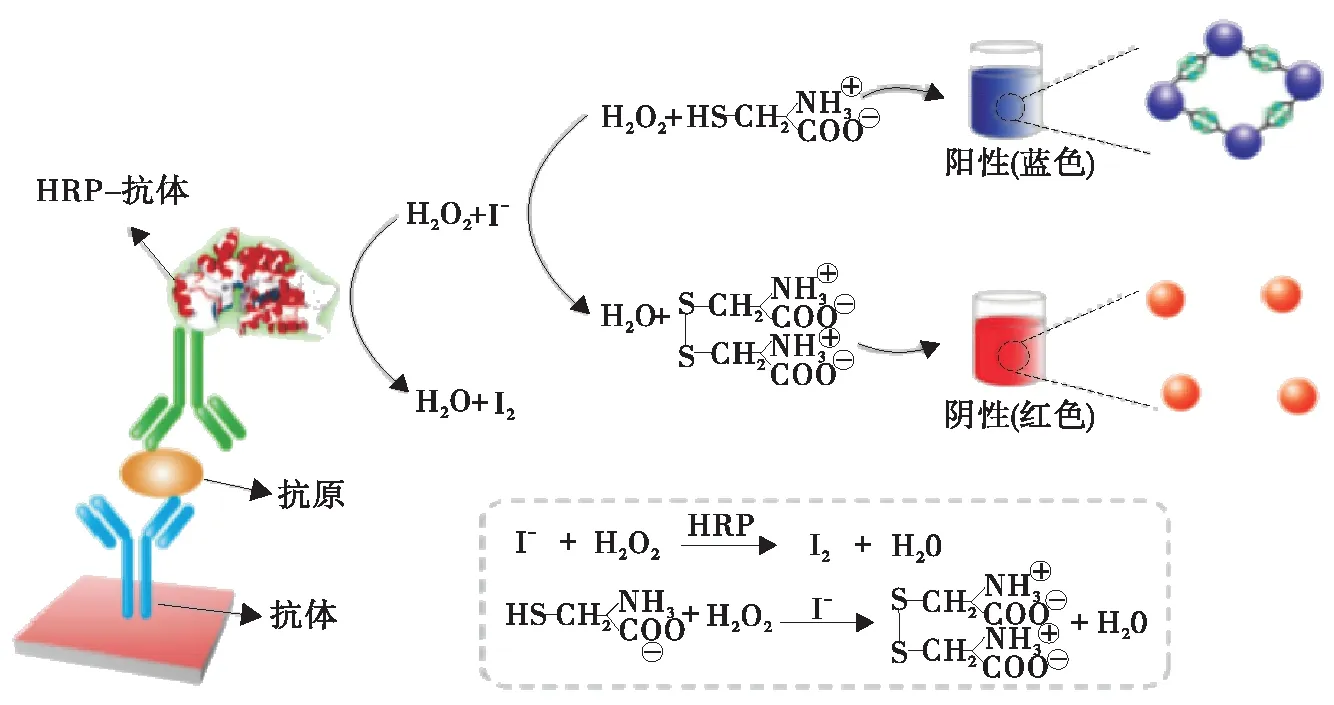
圖1 基于HRP介導的AuNPs可視ELISA示意圖[7]
與球形AuNPs相比,AuNRs對周圍電介質環境的變化反應更加靈敏,且具有更好的呈色性能[9-10]。研究[11]表明,一些氧化劑從AuNRs的末端開始刻蝕,使AuNRs出現不同長寬比以呈現不同的顏色。根據這一現象,AuNRs作為信號輸出底物廣受研究者的青睞[12]。Ma等[13]利用Fe2+離子充當催化劑,催化H2O2歧化以產生羥基自由基(·OH),進而刻蝕AuNRs,開發了一種用于檢測甲胎蛋白(AFP)的改良型ELISA。利用固定在96孔板表面的單克隆抗體捕獲抗原(靶分子/蛋白質),過氧化氫酶標記的多克隆抗體與抗原結合,在平板表面形成“抗體—抗原—第二抗體”夾心復合物[圖2(a)]。附著在板表面的過氧化氫酶起催化劑作用,催化H2O2分解為水和氧氣。在沒有AFP的情況下,Fe2+催化H2O2歧化產生·OH刻蝕AuNRs使溶液的顏色為黃色,隨著AFP濃度的增加,溶液顏色逐漸由黃色變為無色,再變為粉色、綠色、橙色[圖2(b)]。AFP的可視檢查動態范圍為0~120 ng/mL,可視檢測限為5.0 ng/mL。
由于其良好的光學性能,AuNPs、AuNRs、金納米星(AuNS)[14]、金納米雙錐體(Au NBP)[15]、銀納米顆粒(AgNPs)[16]、三角銀納米棱鏡(AgNPR)[17]被作為信號底物以改良比色ELISA。這類納米材料用于顯色底物,其顏色信號輸出豐富改善了比色ELISA的可視檢測能力和檢測靈敏度。
1.2 基于納米酶的改良型比色ELISA
納米酶具有易于制備,堅固耐用,穩定性好,可調節催化特性,增強夾心比色法的檢測靈敏度和效率等多種優勢。這些基于納米酶的夾心比色法不僅可以檢測蛋白質,還有檢測其他生物分子的潛在應用空間。基于納米酶的過氧化物酶活性,Huang等[18]以金納米簇(AuNCs)作為納米酶,以AuNPs作為顯色底物,設計了一種用于T3甲狀腺激素檢測的改良型ELISA(圖3)。利用AuNCs催化H2O2分解,在HAuCl4存在的情況下,得到不同顏色的AuNPs。該傳感器擁有超高的靈敏度,實現了T3甲狀腺激素的痕量檢測,檢測限為2.0×10-15mg/mL。此類改良型ELISA不但簡化了系統,還降低了成本,利于實際應用。

圖2 基于AuNRs構建的改良型ELISA示意圖[13]
Figure 2 Schematic diagram of improved ELISA based on AuNRs
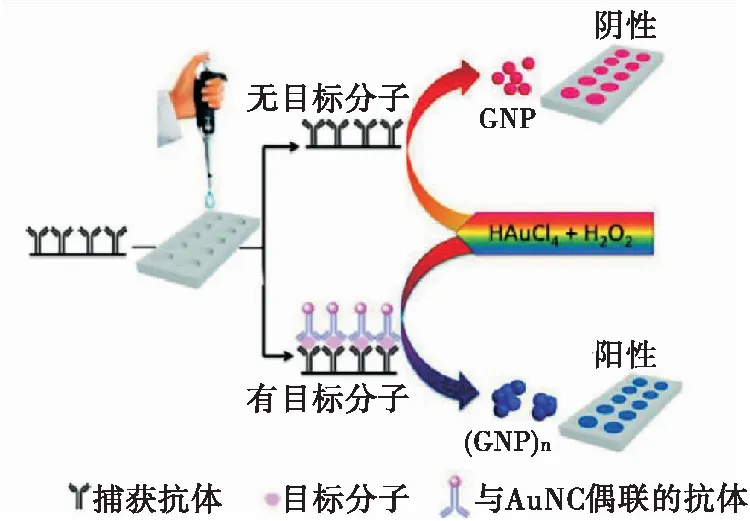
圖3 T3甲狀腺激素檢測示意圖[18]
Figure 3 Schematic diagram of T3 thyroid hormone detection
此外,基于AgNPs的比色傳感器具有更高的消光系數和更低的價格等優勢[19-20],已被廣泛用于生物分子的比色測定。Chen等[21]利用3D-MnO2-PEG納米花和4-巰基苯甲酸與三聚氰胺改性的銀納米顆粒(4-MBA-MA-AgNPs)設計了一種改良型ELISA,用于檢測腸道病毒71型(EV71)(圖4)。采用3D-MnO2-PEG代替酶,并修飾抗體;捕獲目標物后,利用VC還原3D-MnO2-PEG,釋放Mn2+;加入4-MBA-MA-AgNPs,通過Mn2+聚集AgNPs,溶液顏色和紫外—可見光譜發生變化,通過還原反應釋放Mn2+以提高檢測靈敏度。
2 改良型熒光ELISA
Albert等[22-23]提出了熒光免疫概念,并應用于肺炎球菌的檢測。近年來,基于新型熒光納米材料的改良型ELISA和熒光免疫測定(FELISA)引起了研究人員的廣泛關注。由于量子點(QD)特有的光學特性、高光穩定性以及尺寸和形狀可調等優點,引起了研究人員對提高FELISA靈敏度的關注[24-26]。Xu等[27]基于CAT調控的CdTe QD熒光轉換,開發了一種競爭型FELISA,用于檢測伏馬毒素B1(FB1)(圖5)。巰基丙酸修飾的CdTe量子點(MPA-QD)的熒光被H2O2淬滅,CAT作為競爭性抗原的載體,調節H2O2的濃度實現對目標物的檢測。若體系中不存在FB1,CdTe QD的熒光被H2O2猝滅;若樣品中存在FB1,則體系中存在CAT,H2O2被分解,CdTe QD的熒光不會被猝滅。檢測限為0.33 ng/mL,為基于HRP的傳統ELISA的1/15。
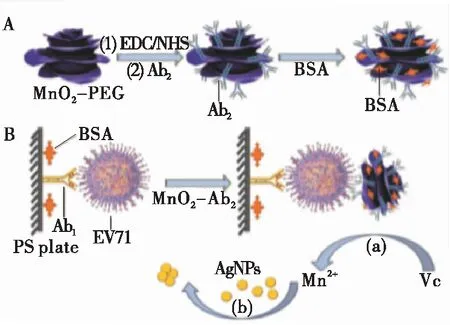
圖4 EV71的免疫測定示意圖[21]
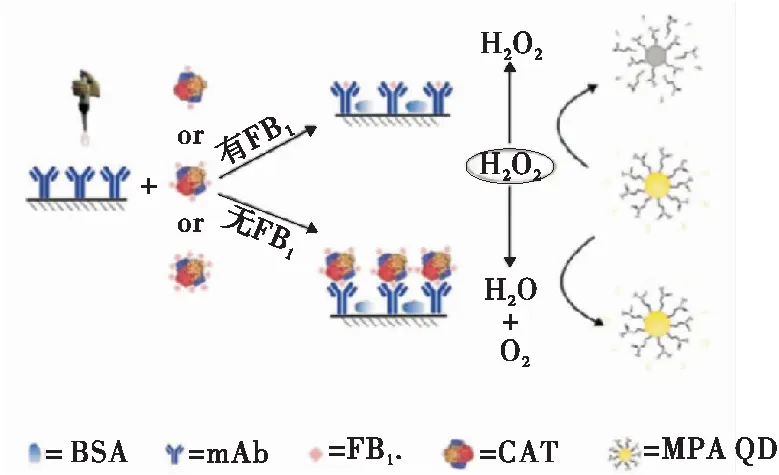
圖5 ELISA檢測FB1示意圖[27]
作為新興材料,碳點(CDs)具有易于合成、成本低、無毒和良好的生物相容性等優點,其熒光特性和過氧化物酶特性被廣泛用于免疫測定[28-31]。Dong等[32]利用CDs的熒光特性和MnO2NSs的淬滅特性,建立了一種新型的FELISA。該方法中熒光CDs和MnO2NSs通過靜電吸附結合,由于CDs和MnO2NSs之間的熒光能量轉移(FRET),CDs的熒光被淬滅。堿性磷酸酶(ALP)催化抗壞血酸2-磷酸酯(AAP)水解產生的AA可將MnO2NSs還原為Mn2+,釋放CDs。基于這種熒光“開啟”機制,FELISA實現了金剛烷胺的檢測,檢測限達0.035 ng/mL。此外,利用CDs的熒光特性與過氧化物酶特性,開發了一種結合熒光與比色的改良型ELISA法用于檢測AFP[29](圖6)。將CDs與抗AFP抗體(Ab2)通過戊二醛胺—胺偶聯,當AFP存在時,加入Ab2后形成夾心復合物。基于CDs的熒光特性,夾心免疫復合物的熒光強度與AFP濃度呈正相關,檢測范圍為0~350 ng/mL,R2為0.995。而傳統免疫分析使用HRP的R2為0.964,熒光素異硫氰酸酯(FITC)的R2為0.973,表明CDs具有很大的潛力,可用于免疫分析的生物標記。
Tan等[33]將Pd-Ir納米立方體作為納米酶及CDs信號讀出底物有機結合,開發了檢測心肌肌鈣蛋白I(cTnI)的FELISA(圖7)。在H2O2存在的情況下,納米酶催化鄰苯二胺(OPD)轉化為其氧化物(Ox-OPD),在400 nm激發波長下,570 nm處有發射峰,Ox-OPD可吸附于CDs表面上,猝滅CDs的熒光。在cTnI存在的情況下,Ox-OPD在570 nm處的熒光峰增加,同時CDs在450 nm處的熒光峰減少,從而形成比例熒光信號用于cTnI的定量,FELISA的檢測限為0.31 pg/mL。同理,Zhu等[34]利用Au@Pt納米材料作為OPD氧化的納米酶,Ox-OPD的顏色變化實現了比色檢測,而雙發射峰的熒光變化實現了cTnI的熒光檢測。因此,納米酶和納米底物共同構建的FELISA可為生物分子檢測提供準確、靈敏的免疫測定。
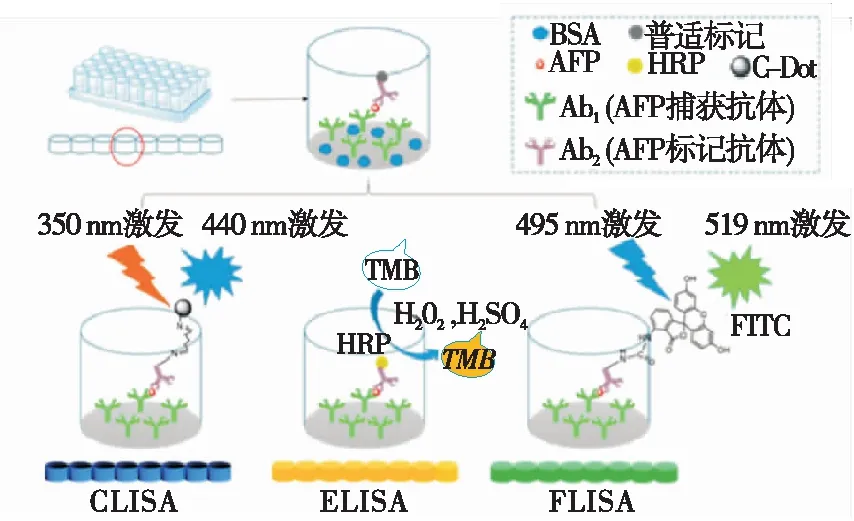
圖6 免疫吸附示意圖[29]
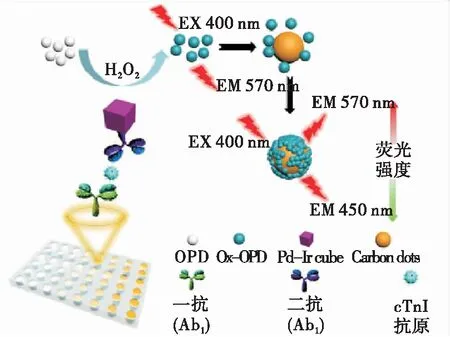
圖7 基于Pd-Ir納米酶與CDs的熒光免疫測定示意圖[33]
Figure 7 Schematic diagram of fluorescent immunoassay based on Pd-Ir nanozyme and CDs
3 其他改良型ELISA
近年來,除比色法和熒光法外,還探索了其他方法來改良ELISA,如電化學免疫測定(ECLISA)、光熱效應技術(PTE)、表面增強拉曼散射技術(SERS)和化學發光免疫測定(CLIA)。這些技術與ELISA結合可得到更加靈敏和便捷的方法,滿足痕量檢測與降低成本的要求。
3.1 基于電化學免疫分析的改良型ELISA
作為快速現場檢測中最有前途的方法,電化學免疫測定法既具有電化學傳感器價格低廉、攜帶方便、靈敏度高,又具有免疫分析工具便于操作和高選擇性,彌補了傳統ELISA靈敏度不足、背景高和成本高的缺陷[35-37]。納米級PbS膠體(PbS CSs)被成功應用于新型ECL ELISA的構建,實現了人附睪蛋白4(HE4)的超靈敏檢測[38]。將修飾了抗體的富勒烯—殼聚糖(C60-Chit)納米復合物固定于玻璃碳電極(GCE),擴大了Pb2+的檢測靈敏度;夾層結構形成后,可從PbS CSs釋放的Pb2+側面反映HE4的濃度,其檢測限為3.4 fg/mL。Knopp等[39-41]開發了一種基于氣體的非接觸式電化學生物傳感器,實現了傳感器的重復使用,還提高了精度、穩定性和可重復性。將氫(H2)和鈀(Pd)納米材料結合,構建了基于氣體的電化學生物傳感器,H2與Pd反應形成PdHx,增加Pd電阻。氧氣的干擾是傳感器的固有局限性,為了減輕氧對靈敏度的影響,Knopp等[42]構建了一種改良的ELISA傳感平臺。以包裹在Pd納米線表面的沸石咪唑鹽骨架(ZIFs-67)作為檢測探針,與抗AFP抗體偶聯用于AFP檢測,由于氧不能透過ZIFs-67,其檢測限達0.04 ng/mL[43]。
3.2 基于光熱效應的改良型ELISA
近年來,光熱納米材料的光熱效應(PTEs)是改良型ELISA的研究熱點之一[44-45],以光熱納米材料為基礎已開發了使用普通溫度計對目標進行定量讀取的光熱免疫測定法(PTIA)[46]。同時,使用溫度計作為信號讀出系統的改良型ELISA也得到了廣泛發展,如將Fe3O4NP錨定在功能化的氧化石墨烯上并偶聯DNA制備成檢測探針,無目標物PSA時,DNA與PSA適配體之間的雜交反應捕獲信號探針,Fe3O4NP轉化為普魯士藍納米顆粒(PB),通過808 nm激光輻照將生物信號轉化為熱信號,實現PSA定量檢測,檢測限為0.31 ng/mL[47]。Jiao等[48]利用Au@Pt納米枝晶介導的多模信號輸出,開發了一種改良型ELISA。基于其過氧化物酶活性實現了比色及熒光信號讀出,同時因Au@Pt較強的光熱效應,實現了808 nm照射下的熱信號讀出,完成了cTnI的定量免疫分析
3.3 基于表面增強拉曼散射的改良型ELISA
基于表面增強拉曼散射(SERS)的技術具有抗光漂白、較少的背景干擾、高靈敏度以及較好的穩定性[49]。這些優勢使SERS在生物學分析中具有潛在的應用前景[50-53]。近年來,Yang等[54]將SERS技術與ELISA結合,開發了一種改良型ELISA檢測PSA。該方法利用Cu2-xSySe1-y納米顆粒作為納米酶,催化C≡C—PEG2CH2CH2NH2和N3—PEG3—CH2CH2NH2的點擊化學反應,有效避免了光漂白以及背景對結果的影響。Su等[55]利用結合了AuNPs的共價有機骨架(COF)復合材料作為納米酶,催化4-硝基苯硫酚(4-NTP)還原轉化為4-氨基硫酚(4-ATP),構建了一種新型SERS-ELISA。在NaBH4存在的情況下,新產生的4-ATP與AuNS觸發了拉曼信號“開啟”實現了β-乳球蛋白的高靈敏檢測,其檢測限達0.01 ng/mL。
3.4 基于化學發光免疫分析的改良型ELISA
化學發光免疫測定(CLIA)是基于底物吸收化學反應產生的能量轉化為化學發光的方法[56-57]。由于其背景干擾小,能有效避免背景光和光漂白,具有高靈敏度和寬線性范圍的優點,已廣泛應用于生物傳感器和生物醫學檢測領域[58-59]。Yang等[60]利用親和素化的磁納米顆粒(SA-MNP)開發了一種CLIA方法。在兔免疫球蛋白(rIgG)存在的情況下,加入K4Fe(CN)6使磁顆粒表面生成PB,提高了PB過氧化物酶樣活性,使魯米諾的CL信號增強,且CL強度與rIgG的濃度呈正相關,其檢測限分別為0.28 ng/mL,0.044 pmol。
4 總結與展望
文章簡要分析了傳統ELISA作為檢測手段的局限性,重點總結了近年來基于納米材料開發的改良型ELISA方法。其中,以貴金屬納米材料(如金納米顆粒、金納米棒、銀納米顆粒等)作為底物輸出多色信號的策略已在很大程度上提高了比色ELISA的肉眼檢測能力和檢測靈敏度。以納米酶替代傳統生物酶為特點的新型ELISA不僅彌補了傳統ELISA中酶的耐熱性差、保質期短、容易失活的缺陷,也為提高測定靈敏度和穩定性,縮短測定時間等方面提供了解決思路,且檢測策略相對簡單、價格便宜,展現出了較大的應用前景。
雖然各種改良型ELISA在臨床醫學、環境測量和食品行業中廣泛應用,但對改良型ELISA的研究還存在以下不足:
(1)納米底物的引入很大程度上提高了比色ELISA的檢測靈敏度,但對于分析物濃度的微小變化導致的色度變化還難以區分。因此,提高納米底物對微小濃度變化的響應能力,制備出響應性能更佳,選擇性更好的納米底物,將是未來一個重要的研究方向。
(2)基于熒光的ELISA已被廣泛應用于改良型ELISA,且具有較高的靈敏度,但在如何克服其他基質背景干擾,熒光探針的光漂白現象,以及熒光漲落及淬滅現象方面需進一步開發研究。
(3)新興的信號(電化學信號、光熱效應、表面增強拉曼和化學發光)有足夠的穩定性、準確性、較高的靈敏度以及低背景信號的優點,但其策略相對復雜,需要特定的設備與專業人員的操作,不能滿足現場快速檢測的要求。若能與智能手機,便攜式、高分辨率檢測器結合使用,有望實現便攜式信號讀取,進而滿足現場即時檢測需求。

