SelectSecure 3830電極房間隔起搏的有效性和可行性
張新才,孫波文,邱立彬,蘇亮,邵靜波
1濰坊市人民醫院,山東濰坊261041;2濰坊市濱海經濟開發區人民醫院
目前人工心臟起搏器仍是治療慢性心律失常及多種離子通道病的首選方法[1]。隨著起搏器置入數量的不斷激增,我們發現起搏器能否有效運轉主要取決于電極導線與心臟是否接觸良好,而起搏電極頭端的形態、構造與之關系密切。同時,傳統翼狀電極起搏導致的心臟激動順序異常對心功能造成的不利影響,也被越來越多的學者關注。現代科技不斷發展,各種新型主動起搏電極相繼問世,如何根據患者病情置入適宜的電極,成為當下許多心內科醫生需要思考和解決的關鍵問題。本研究采用目前世界上最細主動電極——3830電極,應用SelectSecure選擇部位起搏,旨在探討3830電極在心房起搏應用中的安全性和有效性。
1 資料與方法
1.1 臨床資料 選擇濰坊市人民醫院2015年11月~2017年11月行人工心臟雙腔起搏器置入56例患者,均符合《埋置心臟起搏器及抗心律失常器指南(修訂版)》[2]Ⅰ、Ⅱa指征,心室電極均采用3830螺旋電極。56例患者根據心房電極選擇分為兩組。觀察組30例,男13 例、女17例,年齡47~82(66.4±15.4)歲,置入3830心房螺旋電極。對照組26例,男12例、女14例,年齡45~78(64.5±16.1)歲,置入4574心房翼狀電極。術前所有患者均完善心電圖、超聲心動圖、胸部正位片等檢查,兩組患者性別、年齡、術前超聲心動圖測得左房內徑大小等資料無統計學差異(P均>0.05)。
1.2 手術方法 兩組患者均取仰臥位行局部麻醉,兩次穿刺左鎖骨下靜脈,放置兩個8F可撕開鞘管,分別置入心室、心房電極。采用3830螺旋電極(Medtronic公司,美國,69 cm)置入右室室間隔或右室流出道,在泥鰍導絲引導下,將C315-S10鞘管通過三尖瓣送入右心室,后送達右室高位流出道。調整鞘管位置至右室間隔部或右室流出道,正位及左前斜45°透視下確定鞘管位置,使其指向中高位室間隔。沿鞘管送入3830心室電極,心腔內心電圖示損傷電流,則將3830電極旋出4圈。測試電極起搏閾值電壓、感知電壓及阻抗,直至各參數在正常范圍內,切開鞘管,調整電極張力并固定。觀察組患者心房電極采用3830螺旋電極(Medtronic公司,美國,59 cm)置入右心房房間隔,在泥鰍導絲引導下,將C315-S4鞘管送達右心房。正位及左前斜位45°透視下確定鞘管位置,使其指向房間隔,沿鞘管送入3830心房電極。心腔內心電圖示損傷電流,則將3830電極旋出4圈,測試電極起搏閾值電壓、感知電壓及阻抗,直至各參數在正常范圍,切開鞘管,調整電極張力并固定。對照組應用4574翼狀電極(Medtronic公司,美國,52 cm)常規方法置入右心耳。
1.3 心臟起搏器程控參數觀察 3830心房螺旋電極置入即刻測試起搏閾值電壓0.6~1.5 V,最高未超過1.5 V,感知電壓3.5~1.9 mV,電極阻抗360~550 Ω。4574心房翼狀電極置入即刻測試起搏閾值電壓0.5~1.2 V,感知電壓5.0~2.0 mV,電極阻抗435~640 Ω。隨訪期間內上述3項指標均穩定可靠,在正常允許范圍內,分別記錄兩組置入即刻、術后1個月、術后3個月、術后6個月心房電極起搏閾值電壓、感知電壓、阻抗,術后臥床時間,術前及術后6個月左房內徑大小等各項指標。

2 結果
2.1 兩組電極置入不同時點心房起搏閾值電壓、感知電壓、阻抗變化 置入即刻,觀察組心房電極起搏閾值電壓高于對照組(P<0.05),術后1、3、6個月兩組起搏閾值電壓無統計學差異(P均>0.05);觀察組術后1、3、6個月心房電極起搏閾值電壓均低于置入即刻(P均<0.05)。觀察組置入即刻、術后1個月、3個月、6個月測得阻抗明顯低于對照組,(P均<0.05)。兩組置入即刻、術后1個月、3個月、6個月心房電極感知電壓無統計學差異(P均>0.05)。見表1。
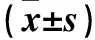
表1 兩組電極置入不同時點心房起搏閾值電壓、感知電壓、阻抗比較
注:與對照組同期相比,aP<0.05;與本組置入即刻相比,bP<0.05 。
2.2 兩組術后臥床時間及心功能變化 術后臥床時間觀察組(23.4±2.5)h,對照組(61.2±7.8)h,觀察組術后臥床時間較對照組明顯縮短(P<0.05)。觀察組術后6個月左房內徑小于同期對照組(P<0.05);對照組術后6個月左房內徑大于術前(P<0.05)。
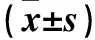
表2 兩組術前及術后6個月超聲心動圖檢測結果比較
注:與對照組同期相比,*P<0.05;與本組術前相比,#P<0.05 。
3 討論
經歷60年的發展,心臟起搏器由最初的單腔起搏模式發展到目前的雙腔、三腔起搏模式[3,4],起搏電極也由被動電極逐漸過渡到了主動電極,特別是心室起搏電極,現已基本進入了主動電極時代。傳統翼狀電極勾掛右心耳法操作簡單、到位便捷、固定可靠、價格便宜,因此翼狀電極目前仍是許多心內科醫生心房起搏的首選電極。近年來許多研究發現,與起搏心房其他部位相比,傳統的右心耳起搏,有效不應期較短,房內傳導時間延長,p波離散度增加[5],由此推斷右心耳起搏可能是誘發此類患者心房顫動的原因之一[6,7]。同時也有相關研究證實右心耳起搏會增加電刺激信號至左房的傳導時間,導致左房電-機械活動延遲加劇,從而影響左右房整體的同步協調收縮功能[8]。本研究兩組患者術前超聲心動圖測得左房內徑無統計學差異,術后6個月左房內徑3830電極組明顯小于同期對照組。對照組術后6個月左房內徑大于術前。因此我們認為,3830心房螺旋電極選擇部位起搏的起搏方式更符合心房電傳導的生理學特性,能有效減少因心房起搏而導致的心房擴大。
當今世界老齡化進程不斷加快,起搏器置入日趨傾向老齡化,而高齡患者的心臟往往存在心房擴大、心內膜纖維化、肌小梁平滑、松弛等,這些特點使翼狀電極的嵌頓困難,即使勉強到位也易發生電極脫位[9]。同時,起搏器感染、電極磨損等所致的電極拔出病例越來越多,相比主動螺旋電極,被動翼狀電極拔出時對右室心內膜、三尖瓣瓣膜及右心耳損傷造成的嚴重后果也不容忽視[10]。另外相關研究報道顯示,對于診斷永存左上腔的患者通過永存左上腔選擇主動電極可成功置入,而選用被動電極則難以成功[11]。
本研究發現,觀察組在置入心房即刻起搏閾值電壓明顯高于對照組,觀察組術后1、3、6個月起搏閾值電壓明顯下降。已有研究表明,主動電極旋入心肌后會損傷細胞,造成局部水腫,因而導致閾值電壓暫時性增高;隨著局部損傷的修復,閾值電壓會有明顯下降[12],這也與本研究結論相一致。本研究觀察組同期電極阻抗明顯低于對照組,這可能是由于主動電極頭端的螺旋結構能使其更好地與心房肌接觸所致;而被動電極頭端為錨狀,近乎倒掛于右心耳的梳狀肌之間,電極需要時間與心內膜黏連[13]。本研究還顯示,觀察組術后臥床時間明顯較對照組縮短,這主要是因為對照組被動電極置入右心耳內,鉤掛于梳狀肌之間,而心房梳狀肌相比心室更為薄弱,易發生電極移位或脫位,同時電極末端和右心耳內膜粘連愈合有一過程,期間體位變換可能影響電極的固定。而觀察組主動電極由于其頭端螺旋結構,可旋入心肌,脫位率更低[14]。這不僅可以提高患者舒適度,更能有效降低圍手術期尿潴留、腸脹氣、腸麻痹、下肢靜脈血栓的發生率[13]。觀察組3830電極為目前世界上最細的主動電極,搭配C315S4(心房)/C315S10(心室)預塑形鞘管,操作簡單,固定可靠,且其良好的通過性及柔順性可大大降低三尖瓣反流、鎖骨下擠壓綜合征的發生率。
綜上所述, SelectSecure 3830電極用于心房起搏具有良好的安全性和可行性,值得在臨床工作中進一步推廣。

