運用網絡藥理學探討開心散治療抑郁癥的作用機制
吳源陶 鄒譯嫻 王理槐
〔摘要〕 目的 本研究旨在運用網絡藥理學方法,預測開心散活性成分的抗抑郁藥理作用機制。方法 通過TCMSP、ETCM獲取開心散的成分和靶點,運用Genecard、OMIM篩選抑郁癥相關的蛋白,通過STRING構建蛋白相互作用網絡,使用 Cytoscape進行靶點的拓撲分析、MCODE聚類分析,使用R語言進行GO和KEGG通路富集分析,最后使用MOE軟件進行分子對接驗證。結果 網絡分析表明,開心散中25個活性成分與其發揮抗抑郁作用密切相關,該機制涉及到51個靶點(包括ACHE、HTR3A、DRD2等)以及24條通路;分子對接結果顯示化合物aposcopolamine、 perlolyrine、 hederagenin與PPARG、ACHE、SLC6A4、DRD2靶點均具有較好的結合能力。結論 開心散可能主要通過神經活性受體配體相互作用、羥色胺突觸、cAMP通路等相關靶標起到抗抑郁的功效,該研究為一步揭示開心散治療抑郁癥的潛在活性成分及其可能的作用機制提供了思路。
〔關鍵詞〕 開心散;抑郁癥;網絡藥理學
〔中圖分類號〕R277.7? ? ? ?〔文獻標志碼〕A? ? ? ?〔文章編號〕doi:10.3969/j.issn.1674-070X.2020.04.012
Using Network Pharmacology Model to Explore the Mechanism of Kai-Xin-San in
Treating Depression
WU Yuantao, ZOU Yixian, WANG Lihuai*
(The First Affiliated Hospital of Hunan University of Chines Medicine, Changsha, Hunan 410007, China)
〔Abstract〕 Objective To predict the anti-depressant pharmacological mechanism of Kai-Xin-San (KXS) active ingredients by network pharmacology. Methods The components and targets of KXS were obtained by TCMSP and ETCM, and the proteins related to depression were screened by Genecard and OMIM. The protein interaction network (PPI) was constructed by STRING. Topological attribute analysis and MCODE cluster analysis of the target were performed by Cytoscape. R language was performed to conduct GO and KEGG path enrichment analysis. Finally, MOE software was applied for molecular docking verification. Results Network analysis showed that the 25 active ingredients in KXS were closely related to its anti-depressant effect. The mechanism involved 51 targets (ACHE, HTR3A, and DRD2, etc.) and 24 pathways. The molecular docking showed that aposcopolamine, perlolyrine, and hederagenin had good docking activity with PPARG, ACHE, SLC6A4, and DRD2, respectively. Conclusion KXS may exert anti-depressant effects through pathway-related targets such as neuroactive receptor-ligand interactions, serotonin synapses, and cAMP pathways efficacy. This study provides an idea for the study of the potential active components of KXS in the treatment of depression and its possible mechanism of action.
〔Keywords〕 Kai-Xin-San; depression; network pharmacology
抑郁癥又稱抑郁障礙,是各種原因導致的一種心理障礙的精神疾病,臨床表現為情緒低落,興趣減低,精神不振,悲觀,思維遲緩,嚴重者甚至出現自殺行為,嚴重影響著人類的健康[1]。據世界衛生組織統計,截止到2017年,全球范圍的抑郁癥患者高達3億多。有研究顯示,我國約20%人群出現抑郁癥狀,在疾病負擔排名第2位[1]。目前針對抑郁癥的治療主要是依靠氟西汀、文法拉辛等藥物,但這些藥物不良反應以及單一成分發揮藥效使其應用受到限制。而近年來,通過對中草藥的深入研究,發現了許多具有抗抑郁的天然藥物,中草藥憑借自身效果好、副作用少,越來越受到人們的青睞[2]。
在唐代孫思邈的《備急千金要方》中,記載著開心散(人參、遠志、茯苓、石菖蒲)主治悲憂不樂、神志不寧、善忘等癥,而這些與現代醫學的抑郁癥狀相一致[3]。動物研究發現,開心散可增加神經遞質與神經的營養因子,從而緩解抑郁樣癥狀,在細胞中可以促進星型膠質細胞合成與神經營養因子分泌[4]。但中藥復方成分復雜,研究作用機制困難,而基于系統生物學和藥理學的網絡藥理學的興起,以更省時省力的方式從整體水平上探討中藥與疾病之間的關系,為解釋中藥復方多成分、多靶點、多途徑的整體機制提供了新的研究方式[5-6]。
本研究主要通過網絡藥理學的方法,探究其治療抑郁癥的關鍵靶點和潛在作用機制,為闡釋中藥復方作用機制提供新的研究思路。
1 材料和方法
1.1? 構建開心散化學成分和預測靶點
從數據庫TCMSP(http://lsp.nwu.edu.cn/tcmsp.php)[7]、ETCM(http://www.nrc.ac.cn:9090/ETCM/index.php/Home/Index/index.html )收集開心散各單味藥的化學成分,并在TCMSP進行篩選。
ADME指機體對外源化學物的吸收(absorption)、分布(distribution)、代謝(metabolism)及排泄(excretion)一系列過程[8]。在這項研究中,我們選取ADME的3個相關的指標:口服生物利用度(OB),血-腦屏障(BBB),和類藥性(DL),設置OB≥30%,BBB≥-0.3、DL≥0.18進行化合物篩選。
1.2? 抑郁癥靶點的收集及蛋白質互作網絡構建
在OMIM(http://omim.org/)[9]、Gencards(http://www.
genecards.org/)[10]中輸入“Depression”,獲得相關的抑郁癥靶點;同時將潛在治療靶基因輸入STRING(http://stringdb.org/cgi/input.pl)[11-13]網站,設置物種為“人”和置信度分數>0.4,獲得蛋白相互作用關系圖。
1.3? GO、KEGG富集
使用R語言對靶點進行基因本體論(GO)和京都基因與基因組百科全書(KEGG)途徑富集分析。
1.4? 網絡分析
運用Cytoscape(3.7.1)[13]的Network Analyzer分析中介中心度和節點度2個拓撲參數、MCODE聚類分析。此外,通過Cytoscape構建PPI網絡圖,抑郁癥的成分-靶點-通路圖。
1.5? 分子對接
運用Molecular Operating Environment(MOE 2015.10軟件)來驗證化合物(aposcopolamine, perlolyrine, hederagenin)與部分靶蛋白之間的關系[13]。從蛋白數據庫-PDB數據庫(http://www.RCSB.org/)獲取靶點PPARG(PDB ID: 6k0t)、ACHE(PDB ID: 1DX4)、SLC6A4(PDB ID: 5i6x)、DRD2(PDB ID: 3PBL)的3D結構,經過對靶點原始結構的預處理,最后保留靶點的活性區域。用MOE軟件中MOE-Dock模塊,將配體(化合物)與受體(靶點)進行半柔性對接,通過得分值的高低和與氨基酸殘基結合的數目評價化合物與靶點的結合活性。
2 結果
2.1? 開心散成分分析
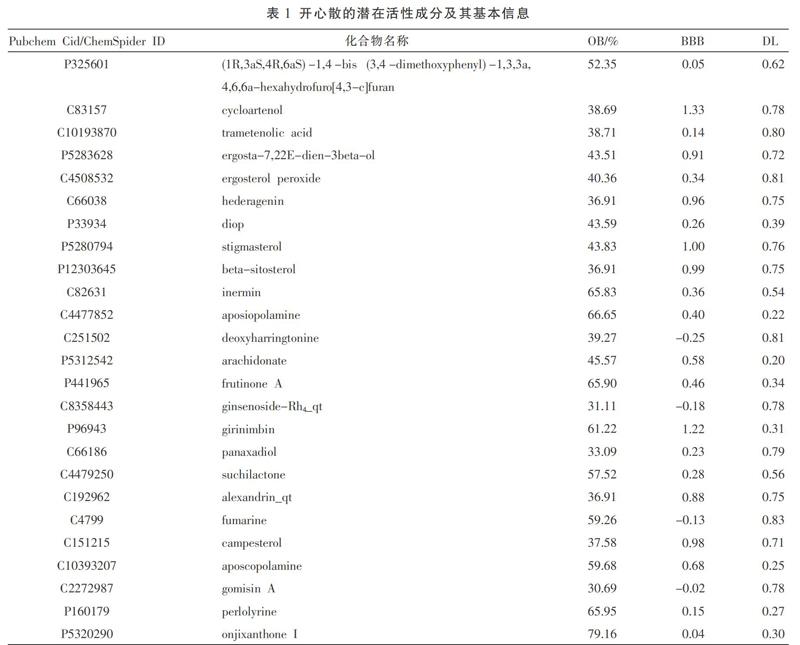
根據OB≥30%、BBB≥-0.3、DL≥0.18,我們共獲得開心散化合物31種,去除沒有靶點的成分后,得到25種活性成分(表1),其中2種源于石菖蒲,4種源于茯苓,17種源于人參,2種源于遠志,并且基于TCMSP,得到53個開心散預測的靶點。
2.2? 開心散治療抑郁癥靶點的預測和PPI網絡的構建
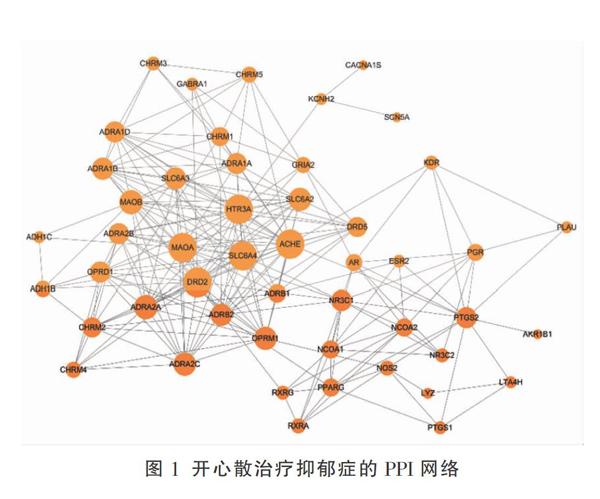
對OMIM和GeneGard收集的抑郁癥相關靶點去重,獲得9 274個相關的靶點。通過與開心散預測的靶點匹配,獲得51個潛在治療抑郁癥靶點。將51個潛在治療靶點輸入STRING,得到由49個節點和228條邊構成的PPI網絡圖(圖1)。根據介度中心性(BC)確定關鍵分子,其中ACHE(BC=0.160)、PTGS2(BC=0.144)、HTR3A(BC=0.141)、NR3C1(BC=0.124)、DRD2(BC=0.099)排名靠前。
2.3? GO和KEGG富集分析
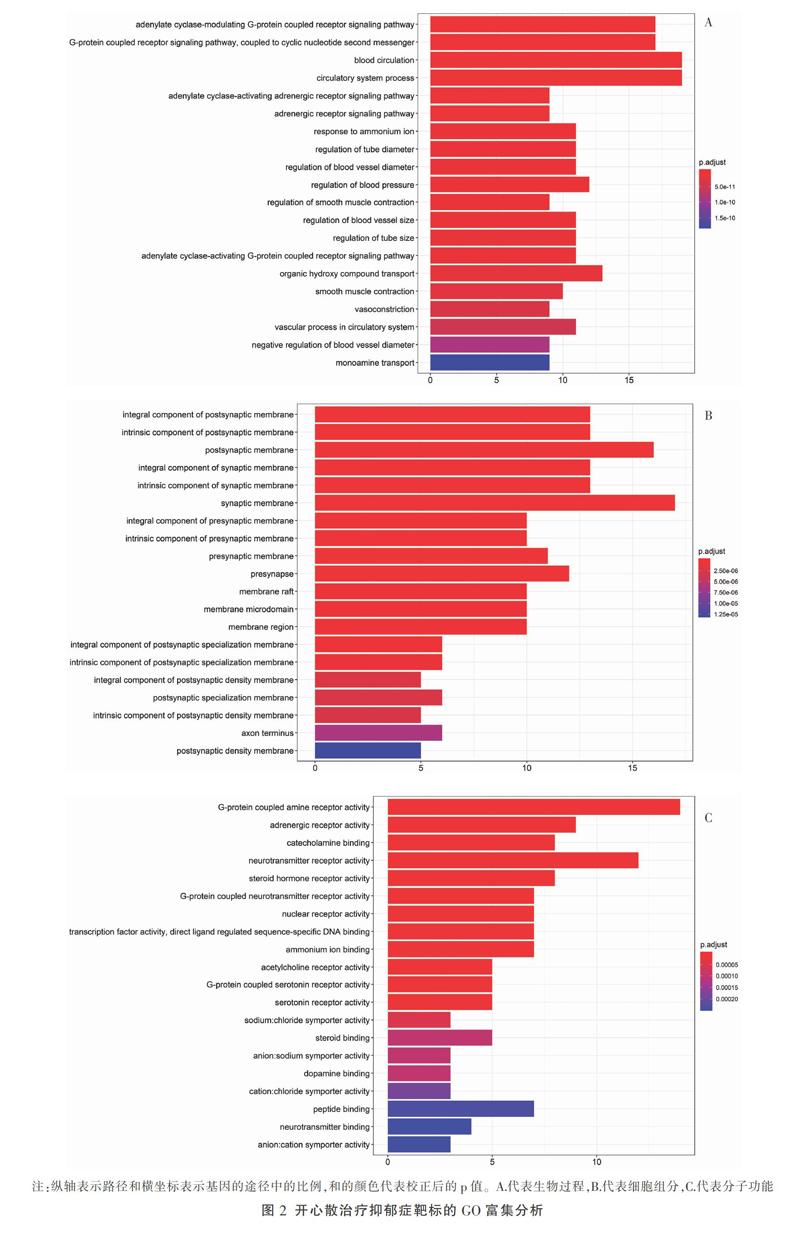
GO分析中,生物過程(BP)得到 405 個條目,細胞組成(CC)得到56個條目,分子功能(MF)有 88個條目,分別取前20個繪制柱狀圖(圖2)。在生物過程分析中,排名前五的是腺苷酸環化酶調節G蛋白偶聯受體信號通路(GO:0007188),G蛋白偶聯受體信號途徑與環核苷酸第二信使偶聯(GO:0007187), 腺苷酸環化酶激活腎上腺素能受體信號通路(GO:0071880),血液循環(GO:0008015),循環過程(GO:0003013);在細胞組成分析中,主要涉及突觸后膜、突觸前膜、突觸等;在分子功能中,主要有G-蛋白偶聯胺受體、腎上腺素受體、兒茶酚胺、神經遞質受體、類固醇激素受體等參與。KEGG通路富集分析顯示共24條通路,取前20條通路繪制 KEGG氣泡圖(圖3)。從圖中可看出治療抑郁癥的常見的通路:神經活性配體-受體相互作用、cAMP信號通路、5-羥色胺能神經突觸、鈣信號通路和膽堿能突觸、多巴胺能突觸等。
2.4? 網絡分析
開心散治療抑郁癥的“成分-靶點-通路”相互作用網絡如圖4所示。該網絡有102個節點,374條邊,密集的連線顯示開心散的多個成分通過多個目標與治療抑郁癥途徑相關聯,揭示開心散多成分、多靶點、多途徑的治療作用。
2.5? 分子對接
如圖5所示,開心散3種潛在活性化合物(aposcopolamine、perlolyrine、hederagenin)與靶點PPARG、ACHE、SLC6A4、DRD2中的氨基酸殘基結合主要以分子間的氫鍵為主,分子間的氫鍵是較為重要的穩定作用力,可使得配體與受體之間結合更加穩定,進而發揮調控蛋白的作用[14]。由此說明,開心散的主要特征性化學成分與PPARG、ACHE、SLC6A4、DRD2靶點均具有較好的結合能力。
3 討論
開心散中人參補益元氣,是為君藥;臣藥茯苓養心安神;佐藥遠志,寧心化痰;使藥石菖蒲,具有益智醒神和引藥入經功效[8]。劉麗琴等[15]發現人參中的主要成分人參皂苷能改善慢性應激所致的大鼠抑郁行為;此外,人參皂苷 Rg1、Rb1、Re、Rg3等都具有一定的抗抑郁作用[16]。遠志中的皂苷類、寡糖酯類化合物具有抗氧化、抗抑郁作用[17]。胡霜等[18]通過懸尾實驗和強迫游泳實驗發現石菖蒲具有一定的抗抑郁作用;茯苓具有鎮靜、抗氧化、調節免疫等作用[19]。這些研究表明,開心散活性成分具有抗抑郁,抗氧化、保護神經等作用,而且該方可能主要通過人參中而且該方的人參皂苷可能是主要發揮療效的成分。發揮其抗抑郁療效。
預測結果顯示ACHE、HTR3A、DRD2可能是潛在的核心靶點。分子對接結果亦證實,開心散可能作用于 ACHE、DRD2靶點。乙酰膽堿酯酶(AChE)在神經元發育和神經再生起到重要作用。張曉杰等[20]發現抑郁癥模型中AChE活性升高,并且隨著年齡的增長而升高。在一項前瞻性縱向研究中,色胺(5-HT)轉運蛋白基因可以緩解應激性生活事件對抑郁的影響[21]。多巴胺(DA)參與神經內分泌系統功能的調節,研究發現,抑郁動物體內多巴胺能神經元的放電頻率明顯增加[22]。綜合分析表明,開心散可能通過調節這些靶點發揮神經保護作用。
KEGG分析發現,羥色胺突觸有7個靶點,分別是PTGS2、PTGS1、MAOB、MAOA、HTR3A、SLC6A4、CACNA1S,其中SLC6A4靶基因經分子對接證實與開心散有靶向關系。Dong等[23]發現,開心散可以通過增加關鍵酶TPH的蛋白質mRNA的表達,從而使5-HT在大腦和突觸間隙的含量升高,發揮抗抑郁作用。王石等[24]發現開心散對體外MAOA和MAOB的活性均有一定的抑制作用。PTGS2、PTGS1調節抑郁癥中的炎癥介質,而cAMP通路可以促進NGF與BDNF表達。臨床研究表明,抑郁癥患者血清中神經營養因子NGF與BDNF 均有均顯著下降[25]。此外,神經活性受體-配體相互作用通路、鈣信號通路、膽堿能突出通路等通過調節多巴胺受體、γ-氨基丁酸受體、谷氨酸受體、乙酰膽堿受體、5-HT受體、糖皮質受體等靶點發揮抗抑郁的功效。
綜上所述,本文通過構建“活性成分-靶標-通路”的網絡藥理研究模式進行開心散抗抑郁的研究。分析發現,開心散中有潛在25個藥物活性成分共涉及51個靶標,24條通路,預測結果表明開心散可能通過作用于羥色胺突觸、cAMP通路、神經活性受體配體相互作用等通路發揮抗抑郁作用。本研究雖然采用網絡藥理學及分子對接方法對開心散抗抑郁的活性成分、關鍵靶點、作用機制做了預測分析,但是其進一步的機制研究還需要通過實驗技術來進行驗證。
參考文獻
[1] 周芯蕾,閆? 芳.1999-2017年抑郁癥領域科技成果項目分析[J]. 預防醫學情報雜志,2019,35(7):777-782.
[2] 姚? 媛,周? 藝,周婷婷.抑郁癥致病機制及中藥治療抑郁癥的機制研究[J].藥學實踐雜志,2018,36(3):193-197.
[3] ZHU Y, DUAN X, CHENG X, et al. Kai-Xin-San, a standardized traditional Chinese medicine formula, up-regulates the expressions of synaptic proteins on hippocampus of chronic mild stress induced depressive rats and primary cultured rat hippocampal neuron[J]. Journal of Ethnopharmacology, 2016,193:423-432.
[4] 曹? 程,肖鈞元,劉夢秋,等.中藥復方開心散調控神經營養因子抗抑郁物質基礎與作用機制研究[J].世界科學技術-中醫藥現代化, 2018,20(6):847-855.
[5] 高? 耀,吳? 丹,田俊生,等.逍遙散和開心散“同病異治”抑郁癥的網絡藥理學作用機制研究[J].中草藥,2018,49(15):3483-3492.
[6] LI X J, ZHANG H Y. Synergy in natural medicines: implications for drug discovery[J]. Trends in Pharmacol Sciences, 2008,29(7):331-332.
[7] RU J, LI P, WANG J, et al. TCMSP: a database of systems pharmacology for drug discovery from herbal medicines[J]. Journal of Cheminformatics, 2014,6:13.
[8] 時? 悅,姚瓔珈,藺? 瑩,等.基于網絡藥理學的開心散治療阿爾茨海默病的作用機制分析[J].藥學學報,2018,53(9):1458-1466.
[9] AMBERGER J S, HAMOSH A. Searching Online Mendelian Inheritance in Man (OMIM): A Knowledgebase of Human Genes and Genetic Phenotypes[J]. Current Protocols in Bioinformatics, 2017,58:1-2.
[10] STELZER G, ROSEN N, PLASCHKES I, et al. The GeneCards Suite: From Gene Data Mining to Disease Genome Sequence Analyses[J]. Current Protocols in Bioinformatics, 2016,54:1-30.
[11] SZKLARCZYK D, FRANCESCHINI A, WYDER S, et al. STRING v10: protein-protein interaction networks, integrated over the tree of life[J]. Nucleic Acids Research, 43(D1):D447-D452.
[12] 周? 鵬,楊建澳,許繼公,等.基于分子對接技術預測苓桂術甘湯防治慢性心力衰竭的作用機制[J].云南中醫學院學報,2018,41(4):82-87.
[13] SHANNON P, MARKIEL A, OZIER O, et al. Cytoscape: a software environment for integrated models of biomolecular interaction networks[J]. Genome Research, 2003,13(11):2498-2504.
[14] HE D, HUANG J H, ZHANG Z Y, et al. A Network Pharmacology-Based Strategy For Predicting Active Ingredients And Potential Targets Of LiuWei DiHuang Pill In Treating Type 2 Diabetes Mellitus[J]. Drug Design Development and Therapy, 2019,
13:3989-4005.
[15] 劉麗琴,羅? 艷,張瑞睿,等.人參皂苷對慢性應激抑郁模型大鼠行為學及HPA軸、BDNF的影響[J].中國中藥雜志,2011,36(10):1342-1347.
[16] 任思宇,王真真,陳乃宏.人參皂苷抗抑郁作用研究進展[J].藥學學報,2019,54(12):2204-2208.
[17] 章主恒,王? 靜,付? 宇,等.中藥遠志抗抑郁有效成分及其作用機制研究進展[J].中國中醫基礎醫學雜志,2018,24(12):1797-1801.
[18] 胡? 霜,馬義澤.石菖蒲等五味中藥抗抑郁作用的實驗研究[J]. 山東中醫雜志,2009,28(11):799-800.
[19] 溫智林,王真真,賀文彬,等.開心散及其有效成分抗抑郁作用的研究進展[J].中藥新藥與臨床藥理,2015,26(3):420-423.
[20] 張曉杰,興桂華,董海影,等.不同年齡組抑郁癥模型大鼠腦乙酰膽堿酯酶及乙酰膽堿轉移酶活性的變化[J].中國老年學雜志,2012,
32(6):1191-1193.
[21] CASPI A, SUGDEN K, MOFFITT T E, et al. Influence of life stress on depression: moderation by a polymorphism in the 5-HTT gene[J]. Science, 2003,301(5631):386-389.
[22] LI Z, HE Y, TANG J, et al. Molecular imaging of striatal dopamine transporters in major depression-a meta-analysis[J]. Journal of Affective Disorders, 2015,174:137-143.
[23] DONG X Z, LI Z L, ZHENG X L, et al. A representative prescription for emotional disease, Ding-Zhi-Xiao-Wan restores 5-HT system deficit through interfering the synthesis and transshipment in chronic mild stress-induced depressive rats[J]. Journal of Ethnopharmacology, 2013,150(3):1053-1061.
[24] 王? 石,董憲喆,譚? 瀟,等.開心散對單胺氧化酶活性的影響[J]. 中國中藥雜志,2016,41(10):1898-1902.
[25] ALFONSO J, FRICK L R, SILBERMAN D M, et al. Regulation of hippocampal gene expression is conserved in two species subjected to different stressors and antidepressant treatments[J]. Biological Psychiatry, 2006,59(3):244-251.
〔收稿日期〕2019-10-17
〔基金項目〕湖南省教育廳科學研究項目(18C0373);湖南省衛生健康委科研課題(20191304)。
〔作者簡介〕吳源陶,女,碩士,主治醫師,研究方向:中西醫結合防治內分泌疾病。
〔通訊作者〕*王理槐,男,主治醫師,E-mail:510236274@qq.com。

