硫辛酸-香豆素偶聯(lián)物合成及抗腫瘤活性研究
戴 一,馮 艷,陳天芹
1安徽新華學(xué)院藥學(xué)院,合肥 230088;2中國(guó)科學(xué)技術(shù)大學(xué)化學(xué)系,合肥 230036
1 材料與方法
1.1 儀器與試劑
BruckerACF-300型核磁共振儀(布魯克(北京)科技有限公司);CytoFLEX流式細(xì)胞儀(美國(guó)貝克曼庫(kù)爾特公司);奧林巴斯IX71熒光顯微鏡(日本奧林巴斯公司);API3000質(zhì)譜儀(美國(guó)PE公司);bio-rad mode680酶標(biāo)儀(美國(guó)伯樂(lè)生命醫(yī)學(xué)產(chǎn)品有限公司);硫辛酸、7-羥基-4-甲基香豆素(阿拉丁試劑有限公司)。DEME培養(yǎng)基(hyclone公司),胎牛血清FBS(Lonsera公司),MTT、活性氧檢測(cè)試劑盒及細(xì)胞凋亡檢測(cè)試劑盒(碧云天公司),其他試劑均為分析純。
1.2 受試細(xì)胞株
受試細(xì)胞株人肝癌HepG2細(xì)胞、人宮頸癌細(xì)胞HeLa細(xì)胞、人卵巢癌A2780細(xì)胞及人肺癌A549細(xì)胞來(lái)自于美國(guó)ATCC公司。
1.3 硫辛酸-香豆素偶聯(lián)物及正辛酸-香豆素偶聯(lián)物合成路線
以硫辛酸為起始原料,二氯亞砜作為酰氯化試劑合成硫辛酰氯,所得酰氯在縛酸劑三乙胺存在的條件下與7-羥基-4-甲基香豆素發(fā)生酯化反應(yīng)即得硫辛酸-香豆素偶聯(lián)物,同法合成正辛酸-香豆素偶聯(lián)物,合成路線見(jiàn)圖1。

圖1 硫辛酸-香豆素偶聯(lián)物及正辛酸-香豆素偶聯(lián)物的合成路線Fig.1 Synthesis route of lipoic acid-coumarin conjugate and n-caprylic acid-coumarin conjugate
1.4 化學(xué)合成
1.4.1 硫辛酰氯的制備[20]
取二氯亞砜(2.04 mL,28.0 mmol)溶于30 mL 二氯甲烷中,在0 ℃ 緩慢滴入硫辛酸(3.88 g,18.72 mmol)的50 mL二氯甲烷溶液中,滴加完畢,室溫反應(yīng)4 h,減壓除去溶劑,得淺黃色固體,即為硫辛酰氯,保存?zhèn)溆谩?/p>
1.4.2 硫辛酸-香豆素偶聯(lián)物的合成
7-羥基-4-甲基香豆素(1.76 g,10 mmol)溶于50 mL無(wú)水四氫呋喃中,加入三乙胺(1.39 mL,10 mmol)。另取硫辛酸酰氯(2.25 g,10 mmol),溶于50 mL 無(wú)水四氫呋喃中,冰水浴條件下緩慢滴入上述溶液中,滴加完畢,室溫?cái)嚢璺磻?yīng),TLC跟蹤反應(yīng)(展開(kāi)劑為石油醚:乙酸乙酯=2∶1)。反應(yīng)完畢,減壓除去溶劑,以乙酸乙酯溶解,分別以稀鹽酸、飽和食鹽水洗滌,無(wú)水硫酸鈉干燥,過(guò)濾,粗產(chǎn)物過(guò)硅膠柱,以石油醚:乙酸乙酯=4∶1洗脫,得黃色固體。
1.4.3 正辛酰氯的制備
事實(shí)上,許沁想錯(cuò)了。許沁在葛局長(zhǎng)的心中,早已沒(méi)有任何位置了。當(dāng)然這并不是位置的問(wèn)題,而是為官之道。在葛局長(zhǎng)看來(lái),許沁是條狗,是條隨時(shí)會(huì)咬人的狗,是條翻臉不認(rèn)人的狗。一旦受到威脅或傷害,她會(huì)逮誰(shuí)咬誰(shuí)。葛局長(zhǎng)不能不嚴(yán)加提防,因而斷然割斷了和許沁的任何聯(lián)系。
取正辛酸(2.88 g,20.00 mmol) 溶于100 mL 二氯甲烷中,0 ℃ 條件下緩慢滴入草酰氯(3.06 g,24.00 mmol),滴加完畢,加入2滴DMF作為催化劑,逐漸升溫至室溫反應(yīng)4 h,減壓除去溶劑,得無(wú)色油狀物,即為正辛酰氯,保存?zhèn)溆谩?/p>
1.4.4 正辛酸-香豆素偶聯(lián)物的合成
7-羥基-4-甲基香豆素(1.76 g,10 mmol)溶于50 mL二氯甲烷中,加入三乙胺 (1.39 mL,10 mmol)。另取正辛酸酰氯(2.25 g,10 mmol)溶于30 mL 二氯甲烷中,冰水浴條件下緩慢滴入上述溶液中,滴加完畢,室溫?cái)嚢璺磻?yīng),TLC跟蹤反應(yīng)(展開(kāi)劑為石油醚∶乙酸乙酯=3∶1)。反應(yīng)完畢,分別以稀鹽酸、飽和食鹽水洗滌,無(wú)水硫酸鈉干燥,過(guò)濾,粗產(chǎn)物過(guò)硅膠柱,以石油醚∶乙酸乙酯=5∶1洗脫,得無(wú)色油狀物。
1.5 硫辛酸-香豆素偶聯(lián)物抗腫瘤活性研究
于96孔板中接種對(duì)數(shù)生長(zhǎng)期腫瘤細(xì)胞培養(yǎng),每孔加5 000個(gè)細(xì)胞、培養(yǎng)基為100 μL,于37 ℃、5%CO2的條件下培養(yǎng)。培養(yǎng)過(guò)夜后給予不同濃度的待測(cè)化合物,平行設(shè)3個(gè)孔,陰性對(duì)照組加與給藥組等體積的培養(yǎng)基,以DEME 培養(yǎng)基作為空白對(duì)照組,給藥后繼續(xù)培養(yǎng)48 h,棄去培養(yǎng)液,每孔加5 mg/mL的MTT溶液20 μL,繼續(xù)孵育4 h,棄去上清液,每孔加入DMSO 150 μL,震蕩10 min,酶標(biāo)儀570 nm測(cè)定吸光度OD值,計(jì)算抑制率及IC50值。抑制率=[1-(A實(shí)驗(yàn)組-A空白組)/(A對(duì)照組-A空白組)]×100%。
1.6 硫辛酸-香豆素偶聯(lián)物與正辛酸-香豆素偶聯(lián)物抗腫瘤活性比較
于96孔板中接種對(duì)數(shù)生長(zhǎng)期肝癌HepG2細(xì)胞培養(yǎng),每孔5 000個(gè)細(xì)胞,37 ℃、5%CO2、100 μL培養(yǎng)基培養(yǎng)。次日給予高低濃度(250和125 μM)的硫辛酸-香豆素偶聯(lián)物、正辛酸-香豆素偶聯(lián)物或香豆素與酸的相應(yīng)混合物,平行設(shè)3個(gè)孔,陰性對(duì)照組加給藥組等體積的培養(yǎng)基,以DEME 培養(yǎng)基作為空白對(duì)照組,給藥后繼續(xù)培養(yǎng)48 h,棄去培養(yǎng)液,每孔加5 mg/mL的MTT溶液20 μL,繼續(xù)孵育4 h,棄去上清液,每孔加入DMSO 150 μL,震蕩10 min,酶標(biāo)儀570 nm測(cè)定吸光度OD值,計(jì)算抑制率。抑制率=[1-(A實(shí)驗(yàn)組-A空白組)/(A對(duì)照組-A空白組)]×100%。
1.7 硫辛酸-香豆素偶聯(lián)物對(duì)活性氧的清除
于6孔板中接種HepG2細(xì)胞,每孔10萬(wàn)個(gè)細(xì)胞,2 mL完全培養(yǎng)基在37 ℃、5%CO2培養(yǎng)箱培養(yǎng)過(guò)夜,于次日分別用含藥培養(yǎng)基進(jìn)行替換繼續(xù)培養(yǎng)24 h,所加藥物的濃度硫辛酸-香豆素偶聯(lián)物、硫辛酸、硫辛酸與香豆素混合物(摩爾比1∶1)、正辛酸-香豆素偶聯(lián)物、正辛酸、正辛酸與香豆素混合物(摩爾比1∶1)及香豆素以硫辛酸或正辛酸計(jì)均為500 μM。24 h 后按活性氧檢測(cè)試劑盒(DCFH-DA)(購(gòu)于碧云天生物)原位處理,經(jīng)PBS 洗滌后用熒光顯微鏡觀察[21]。
1.8 硫辛酸-香豆素偶聯(lián)物誘導(dǎo)細(xì)胞凋亡
對(duì)于硫辛酸-香豆素偶聯(lián)物誘導(dǎo)的細(xì)胞凋亡,本實(shí)驗(yàn)于12孔板中接種HepG2細(xì)胞,每孔20萬(wàn)個(gè)細(xì)胞,1 mL完全培養(yǎng)基在37 ℃、5%CO2培養(yǎng)箱培養(yǎng)過(guò)夜,于次日分別用含藥培養(yǎng)基進(jìn)行替換繼續(xù)培養(yǎng)48 h,所加藥物的濃度硫辛酸-香豆素偶聯(lián)物、硫辛酸、硫辛酸與香豆素混合物(摩爾比1∶1)及香豆素均為500 μM。48 h后按Annexin V-FITC 凋亡試劑盒說(shuō)明書(shū)(購(gòu)于碧云天生物)收集所有細(xì)胞,經(jīng)PBS洗滌后加Annexin V-FITC及PI 進(jìn)行染色,流式細(xì)胞儀檢測(cè)。
1.9 硫辛酸-香豆素偶聯(lián)物細(xì)胞內(nèi)水解釋放
于6孔板中接種HepG2細(xì)胞,每孔10萬(wàn)個(gè)細(xì)胞,2 mL完全培養(yǎng)基在37 ℃、5%CO2培養(yǎng)箱培養(yǎng)過(guò)夜,于次日分別用含藥培養(yǎng)基進(jìn)行替換繼續(xù)培養(yǎng),所加藥物的濃度硫辛酸-香豆素偶聯(lián)物為1 mM。在0、1、2、4、6、8 h分別取樣,經(jīng)PBS 洗滌后用熒光顯微鏡觀察。
2 結(jié)果與分析
2.1 化合物表征
硫辛酸-香豆素偶聯(lián)物為黃色固體,收率為73%,TLC的Rf約0.6(展開(kāi)劑為石油醚∶乙酸乙酯=2∶1);1H NMR(300 MHz,CDCl3)δ:1.45~1.75(m,2H),1.70~2.09(m,5H),2.45(s,3H),2.44~2.59(m,1H),2.64(t,J= 7.4 Hz,2H),3.07~3.29(m,2H),3.55~3.70(m,1H),6.28(s,1H),7.03~7.16(m,2H),7.62(d,J= 8.6 Hz,1H);13C NMR(75 MHz,CDCl3)δ:18.77(4-CH3),24.50(C-3′),28.69 (C-4′),34.10(C-2′),34.59(C-5′),38.55(C-8′),40.27(C-7′),56.28(C-6′),110.45(C-8),114.52(C-2),117.83(C-4a),118.10(C-6),125.40(C-5),151.93(C-7),153.08(C-4),154.18(C-8a),160.50(C-2),171.31(C-1′);IR(KBr)vmax:3 091,2 930,2 859,1 732,1 613,1 568,1 501,1 413,1 384,1 328,1 263,1 227,1 014,981,879 cm-1;ESI-MS:m/z365.2 [M+H]+,387.1 [M+Na]+,729.5 [2M+H]+,746.4 [2M+H2O]+,751.3 [2M+Na]+。
正辛酸-香豆素偶聯(lián)物為無(wú)色油狀液體,收率為87%,TLC的Rf約0.7(展開(kāi)劑為石油醚∶乙酸乙酯=2∶1);1H NMR(400 MHz,CDCl3)δ:0.83~0.94(t,J= 7.9 Hz,3H),1.25~1.43(m,8H),1.71~1.82(q,J= 7.6,7.1 Hz,2H),2.38~2.43(s,3H),2.55~2.64(t,J= 7.5Hz,2H),6.19~6.24(s,1H),7.01~7.09(m,2H),7.55~7.63(dd,J= 8.5,2.1 Hz,1H);13C NMR(100 MHz,CDCl3)δ:13.98(C-8′),18.56(4-CH3),22.52(C-7′),24.68(C-3′),28.83(C-4′),28.92(C-5′),31.56(C-6′),34.18(C-2′),110.16(C-8),114.16(C-2),117.53(C-4a),118.04(C-6),125.40(C-5),152.05(C-7),153.11(C-4),153.93(C-8a),160.28(C-2),171.44(C-1′)。
2.2 硫辛酸-香豆素偶聯(lián)物抗腫瘤活性研究
通過(guò)MTT法評(píng)價(jià)所得偶聯(lián)物細(xì)胞毒性,結(jié)果見(jiàn)表1。除HepG2細(xì)胞外,對(duì)A2780細(xì)胞、A549細(xì)胞及Hela細(xì)胞,硫辛酸與香豆素的混合物抑制活性均高于單個(gè)的母體化合物香豆素或硫辛酸,顯示出硫辛酸與香豆素具有一定的協(xié)同效果,且硫辛酸-香豆素偶聯(lián)物的抑制活性明顯高于硫辛酸與香豆素的混合物以及單個(gè)的母體化合物香豆素、硫辛酸,尤其相比于硫辛酸,活性提高了一個(gè)數(shù)量級(jí),可見(jiàn)硫辛酸與香豆素的偶聯(lián)組合提高了硫辛酸抗癌活性。
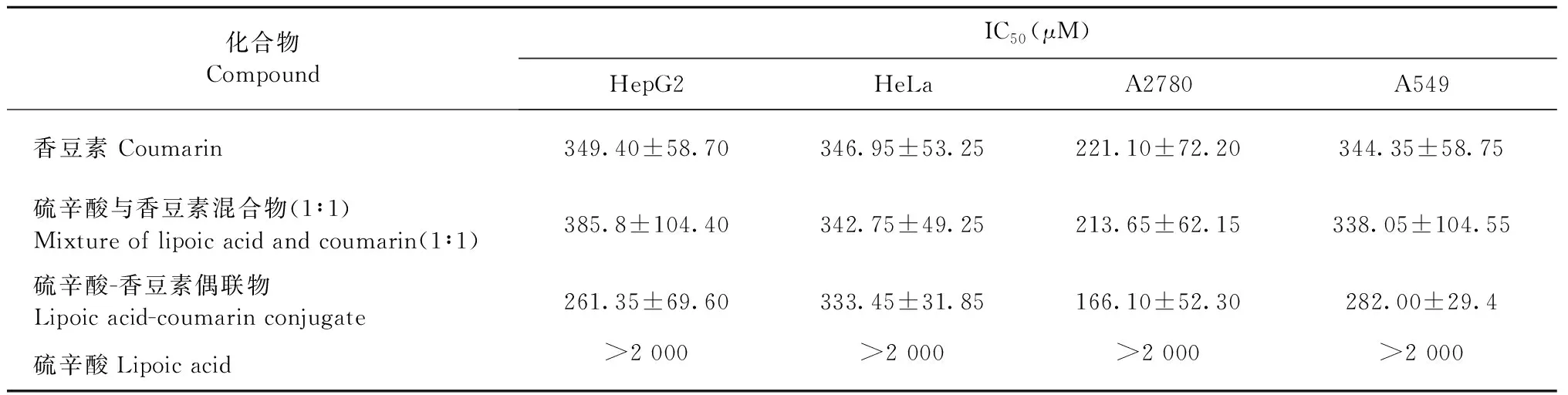
表1 硫辛酸與香豆素偶聯(lián)物體外抗腫瘤活性結(jié)果
2.3 硫辛酸-香豆素偶聯(lián)物與正辛酸-香豆素偶聯(lián)物抗腫瘤活性比較
為確定硫辛酸-香豆素偶聯(lián)物抗腫瘤活性提高的原因是否由于其本身脂溶性提高增加了攝取所導(dǎo)致,本實(shí)驗(yàn)進(jìn)一步合成了一個(gè)脂溶性更大的正辛酸-香豆素偶聯(lián)物。通過(guò)考察在高濃度(250 μM)和低濃度(125 μM)對(duì)HepG2細(xì)胞的抑制作用,由圖2可見(jiàn),無(wú)論在高低濃度,硫辛酸與香豆素的混合物相比于正辛酸與香豆素的混合物,腫瘤抑制活性沒(méi)有明顯的差別,可能因?yàn)榛旌衔镏辛蛐了帷⒄了峄蛳愣顾鼐鶠閱误w,而單獨(dú)的硫辛酸、正辛酸腫瘤抑制作用較弱,主要表現(xiàn)為香豆素的作用。而高低濃度給藥組硫辛酸-香豆素偶聯(lián)物的腫瘤抑制活性均高于正辛酸-香豆素偶聯(lián)物,說(shuō)明硫辛酸-香豆素偶聯(lián)物抗腫瘤活性提高除了脂溶性提高所致較高攝取因素外,硫辛酸本身也表現(xiàn)出了一種其他方式的抗腫瘤作用,文獻(xiàn)報(bào)道硫辛酸可以清除ROS而產(chǎn)生腫瘤抑制作用[7,8]。本實(shí)驗(yàn)進(jìn)一步考察了兩種偶聯(lián)物對(duì)ROS的清除作用。
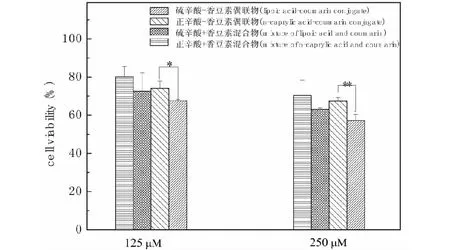
圖2 硫辛酸-香豆素偶聯(lián)物與正辛酸-香豆素偶聯(lián)物抗腫瘤活性比較Fig.2 Comparison of antitumor activity between lipoic acid-coumarin conjugate and n-caprylic acid-coumarin conjugate 注:*P<0.05,**P<0.01。
2.4 硫辛酸-香豆素偶聯(lián)物對(duì)活性氧的清除
低濃度活性氧對(duì)腫瘤細(xì)胞的增殖、分化及轉(zhuǎn)移等具有重要的促進(jìn)作用,硫辛酸清除活性氧對(duì)于抑制腫瘤細(xì)胞的增殖、轉(zhuǎn)移等具有重要價(jià)值。采用活性氧檢測(cè)試劑盒(DCFH-DA)(購(gòu)于碧云天生物)原位處理,活性氧與DCFH-DA反應(yīng)可產(chǎn)生綠色熒光。在一定曝光時(shí)間條件下,由圖A1可見(jiàn)HepG2腫瘤細(xì)胞本身可以產(chǎn)生低濃度活性氧,從圖B1-D1可見(jiàn),硫辛酸的參與可以降低ROS的濃度,尤其是硫辛酸-香豆素偶聯(lián)物可降低效果更為顯著,顯示出該偶聯(lián)物顯著的活性氧清除功能。由圖A2-D2可見(jiàn),香豆素、正辛酸組成的偶聯(lián)物或混合物及它們各自的單體,均不能有效地清除腫瘤中的ROS,說(shuō)明清除ROS可能是硫辛酸-香豆素偶聯(lián)物產(chǎn)生更強(qiáng)抗腫瘤活性的一個(gè)重要原因。
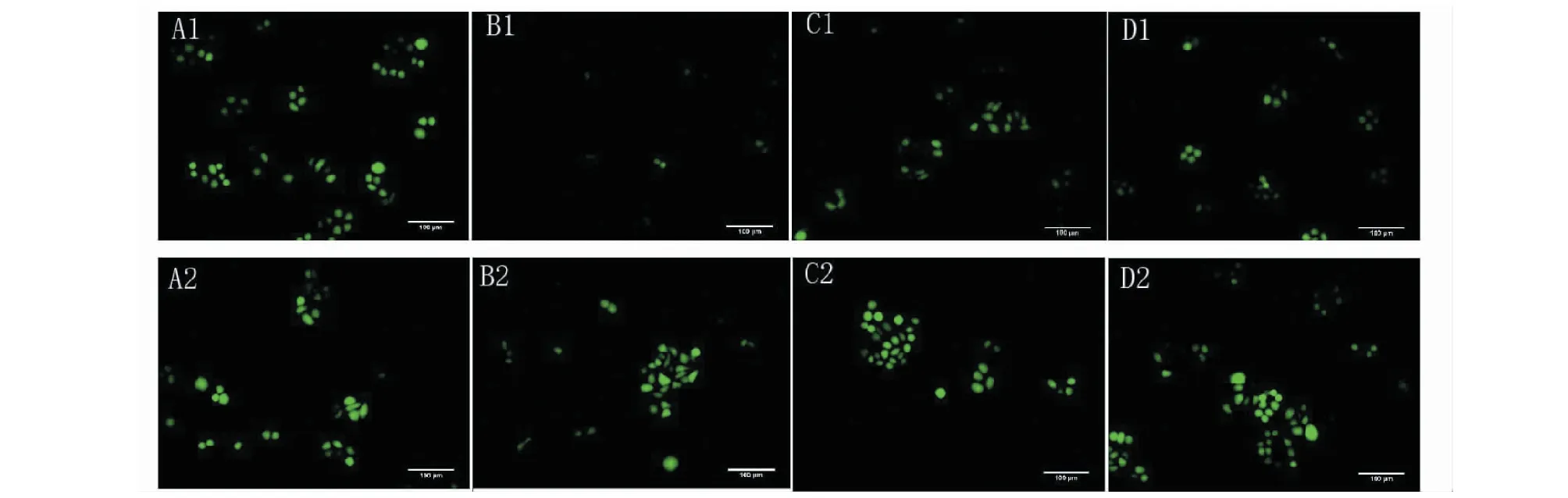
圖3 硫辛酸-香豆素偶聯(lián)物對(duì)活性氧的清除Fig.3 Scavenging of reactive oxygen by lipoic acid coumarin conjugate注:HepG2細(xì)胞孵育24 h后給藥濃度均為500 μM,A1為對(duì)照組;A2為香豆素組;B1為硫辛酸-香豆素偶聯(lián)物組;B2為正辛酸-香豆素偶聯(lián)物組;C1為硫辛酸與香豆素混合物組;C2為正辛酸與香豆素混合物組;D1為硫辛酸組;D2為正辛酸組。Note:HepG2 cells were pre-incubated for 24 h with drugs at dose of 500 μM,A1:control group;A2:coumarin group;B1:lipoic acid-coumarin conjugate group;B2:n-caprylic acid -coumarin conjugate group;C1:mixture of lipoic acid and coumarin group;C2:mixture of n-caprylic acid and coumarin group;D1:lipoic acid group;D2:n-caprylic acid group.
2.5 硫辛酸-香豆素偶聯(lián)物誘導(dǎo)細(xì)胞凋亡
對(duì)于硫辛酸-香豆素偶聯(lián)物誘導(dǎo)的細(xì)胞凋亡,流式細(xì)胞儀檢測(cè)如圖4顯示,相比于對(duì)照組4.94%的凋亡率,單純硫辛酸對(duì)凋亡幾乎沒(méi)有影響,單純香豆素組可見(jiàn)凋亡率提高到7.28%,但遠(yuǎn)低于硫辛酸與香豆素混合物組的16.78%及硫辛酸-香豆素偶聯(lián)物的17.49%,可見(jiàn)硫辛酸與香豆素有明顯的協(xié)同作用,同時(shí)可以發(fā)現(xiàn)硫辛酸與香豆素的混合物誘導(dǎo)的凋亡早晚期幾乎相等,而硫辛酸-香豆素偶聯(lián)物誘導(dǎo)的凋亡主要集中在晚期。

圖4 硫辛酸-香豆素偶聯(lián)物誘導(dǎo)細(xì)胞凋亡Fig.4 Effect of lipoic acid-coumarin conjugate on the apoptosis注:HepG2細(xì)胞孵育24 h后給藥濃度均為500 μM,A為對(duì)照組;B為硫辛酸組;C為香豆素組; D為硫辛酸與香豆素混合物組;E為硫辛酸與香豆素偶聯(lián)物組。Note:HepG2 cells were pre-incubated for 24 h with drugs at dose of 500 μM,A:Control group;B:Lipoic acid group;C:Coumarin group;D:The mixture of lipoic acid and coumarin group;E:Lipoic acid-coumarin conjugate group.
2.6 硫辛酸-香豆素偶聯(lián)物細(xì)胞內(nèi)水解釋放
硫辛酸-香豆素偶聯(lián)物除具有抑制腫瘤細(xì)胞生長(zhǎng)的活性外,同時(shí)具有細(xì)胞示蹤藥物水解釋放功能,本實(shí)驗(yàn)設(shè)計(jì)的硫辛酸-香豆素偶聯(lián)物具有“turn-on”功能,由圖5中 A、B圖可見(jiàn),硫辛酸-香豆素偶聯(lián)物在PBS中用365 nm光激發(fā)無(wú)藍(lán)色熒光,而當(dāng)用堿液水解后可以觀察到強(qiáng)烈的藍(lán)色熒光,這是因?yàn)樗夂笤撆悸?lián)物釋放出香豆素母體,產(chǎn)生了熒光。在細(xì)胞體內(nèi),存在著豐富的酯水解酶,可以把硫辛酸-香豆素偶聯(lián)物同樣水解,起到在細(xì)胞內(nèi)示蹤藥物水解釋放的效果。實(shí)驗(yàn)進(jìn)一步研究了該偶聯(lián)物不同時(shí)間細(xì)胞內(nèi)藥物水解釋放,由圖5可見(jiàn),該偶聯(lián)物與癌細(xì)胞共孵育1 h,基本觀察不到藍(lán)色熒光,從2 h開(kāi)始,藍(lán)色熒光逐漸增強(qiáng),6 h時(shí)達(dá)到最強(qiáng),在8 h時(shí)熒光變?nèi)酰ㄟ^(guò)該實(shí)驗(yàn)實(shí)時(shí)檢測(cè)到藥物的水解釋放。體現(xiàn)了該偶聯(lián)物具有示蹤藥物水解釋放的功能。
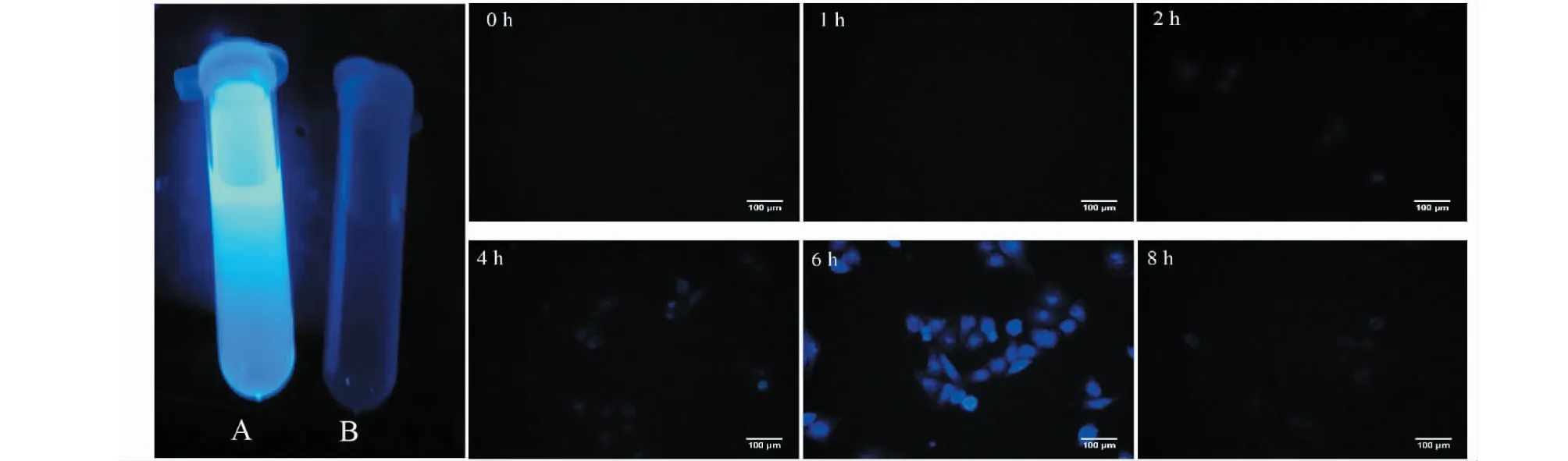
圖5 硫辛酸-香豆素偶聯(lián)物的細(xì)胞內(nèi)水解釋放Fig.5 The release of lipoic acid coumarin conjugate in cancer cells注:A為硫辛酸-香豆素偶聯(lián)物的氫氧化鈉溶液;B為硫辛酸-香豆素偶聯(lián)物PBS溶液;0、1、2、4、6、8 h 為給藥1 mM后各時(shí)間點(diǎn)細(xì)胞內(nèi)熒光強(qiáng)度。Note:A:Sodium hydroxide solution of lipoic acid-coumarin conjugate;B:PBS solution of lipoic acid-coumarin conjugate;Fluorescence intensity in cancer cells treated with 1 mM drug at 0,1,2,4,6,8 h.
3 結(jié)論
硫辛酸作為一個(gè)內(nèi)源性維生素類(lèi)分子,具有多種生物功能。近年來(lái)在對(duì)抗癌治療方面的研究較為活躍,因單獨(dú)的硫辛酸治療效果有限,多對(duì)硫辛酸進(jìn)行結(jié)構(gòu)改造。改造主要在兩個(gè)位點(diǎn)展開(kāi),如本研究采取的方式,利用硫辛酸本身具有的羧基,另一個(gè)位點(diǎn)就是打開(kāi)二硫鍵形成巰基后進(jìn)行改造,其中引起較大關(guān)注的為CPI-613,已完成臨床I期研究[22]。藥物可示蹤化持續(xù)受到廣泛的關(guān)注,對(duì)于個(gè)體化給藥具有重要的意義。本實(shí)驗(yàn)通過(guò)硫辛酸與7-羥基-4-甲基香豆素成酯制成了具有可示蹤功能的硫辛酸-香豆素偶聯(lián)物,通過(guò)細(xì)胞體內(nèi)酯水解酶的作用釋放出硫辛酸及香豆素達(dá)到治療及示蹤的一體化。細(xì)胞實(shí)驗(yàn)顯示,該偶聯(lián)物對(duì)腫瘤細(xì)胞的增殖抑制活性是硫辛酸的10倍以上,可以有效地清除腫瘤細(xì)胞增殖轉(zhuǎn)移賴(lài)以生存的低濃度活性氧,其誘導(dǎo)的凋亡為硫辛酸的3.5倍,體現(xiàn)出硫辛酸與香豆素的協(xié)同作用,另外給藥6 h,可見(jiàn)到強(qiáng)烈的藍(lán)色熒光產(chǎn)生。總之,本實(shí)驗(yàn)合成了一種可示蹤藥物水解釋放的硫辛酸-香豆素偶聯(lián)物,為硫辛酸衍生物的開(kāi)發(fā)提供了一種新的思考。

