載萬古霉素骨水泥與人工骨人體局部釋放對比分析
毛 璐,張伯松,董 迪,姜 璐,齊文淵
0 引言
創傷后骨感染由于局部血運差,全身使用抗生素在感染局部往往不能達到有效的治療濃度,治療過程漫長、并發癥多,是困擾骨科醫生的難題[1]。目前,骨科感染耐甲氧西林的金黃色葡萄球菌及表皮葡萄球菌檢出率較高,而萬古霉素對于上述細菌普遍敏感[2],治療骨感染推薦萬古霉素血藥濃度為15~20 mg/L[3],長期大劑量靜脈使用萬古霉素可能出現白細胞減少[4]、腎毒性等很多不良反應。既往研究發現,在徹底清創的前提下局部植入抗感染藥物骨水泥鏈珠可以提高骨感染的治愈率[5]。萬古霉素骨水泥治療骨關節感染取得了滿意的療效[6]。研究發現,不同患者雖植入相同劑量的萬古霉素人工骨或骨水泥,但是局部引流液藥物濃度差別較大,可達數十倍,局部藥物濃度及釋放量的影響因素包括:病灶大小及部位、引流量等[7],因此,我們對同一患者分別植入萬古霉素骨水泥和人工骨后的局部藥物及全身藥物濃度進行檢測,可以最大限度地減少患者局部植入部位不同對于藥物釋放的影響,以客觀評價對比2種材料局部緩釋萬古霉素的差異,為臨床選擇提供參考。
1 一般資料
1.1 研究對象 選擇2017年6月至2018年4月創傷骨科骨感染患者,第1次手術植入萬古霉素骨水泥,第2次手術植入萬古霉素人工骨,兩次手術間隔1周。患者進行第1次手術主要目的在于清創病灶刮除,留取局部組織進行細菌學培養,清創后植入萬古霉素骨水泥鏈珠作為經驗用藥,之后等待藥敏結果及觀察患者一次清創后的反應,待藥敏結果回報,行二次清創并根據術中情況選擇是否植入人工骨,如果患者藥敏結果提示為G+菌感染且對萬古霉素敏感,植入萬古霉素人工骨進行治療。最終共納入患者16例,男14例,女2例,患者平均年齡(45.63±15.14)歲,感染部位:股骨干8例,脛腓骨4例,粗隆間1例,髖關節1例,尺橈骨1例,踝關節1例(本試驗方案及知情同意書經過我院倫理委員會批準,倫理批件號:積倫科審字第201706-05號)。
1.2 試劑和材料 骨水泥(Palacos R,生產廠家:Heraeus Medical GmbH),硫酸鈣人工骨(OSTEOSET-RBK 8400-0611快干型5 ml),注射用鹽酸萬古霉素[VIANEX S.A.(PLANT C),希臘],萬古霉素檢測試劑(酶放大免疫法)。
1.3 儀器 ViVa-E全自動藥物濃度分析系統(德國西門子公司),自動平衡離心機(長沙湘儀離心機儀器有限公司)。
2 方法
2.1 樣本采集及處理 所有16例患者第1次手術時植入手工制成的萬古霉素骨水泥鏈珠(萬古霉素2 g +骨水泥40 g),間隔1周后行第2次手術時將萬古霉素骨水泥鏈珠取出,局部徹底沖洗后植入自制硫酸鈣人工骨微球(萬古霉素2 g+人工骨5 ml)。植入骨水泥或人工骨后局部留置引流管。于術后2 h及術后次日清晨分別留取靜脈血及引流液,此后每日清晨量取前一日引流量,混勻后留取其中2 ml做濃度檢測,直至臨床拔除引流管。靜脈血及引流液用離心機4 000 r/min,離心5 min后取上清,每次取樣300 μl,使用ViVa-E全自動藥物濃度分析系統進行萬古霉素濃度測定[6]。
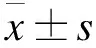
3 結果
3.1 引流液測定結果對比
3.1.1 引流量 術后總體引流量符合正態分布,但每日引流量不符合正態分布。骨水泥組總體引流量為(504.50±306.52)ml,人工骨組為(278.68±136.18)ml,骨水泥組明顯多于人工骨組(t=3.21,P<0.01),進一步對比發現,骨水泥組的第1天引流量明顯多于人工骨組(Z=2.90,P<0.01),但此后兩組引流量比較差異無統計學意義。見表1。

表1 萬古霉素骨水泥及人工骨局部引流量對比[ml,M(P25,P75)]
3.1.2 引流液藥物濃度 人工骨組藥物濃度明顯高于骨水泥組。以手術后次日清晨采集點為例,人工骨組引流液濃度中位數為2 985.00 mg/L,骨水泥組為259.00 mg/L,人工骨組顯著高于骨水泥組(Z=-3.41,P<0.01);對每日引流液濃度進行比較,人工骨組局部濃度均高于骨水泥組。見表2。
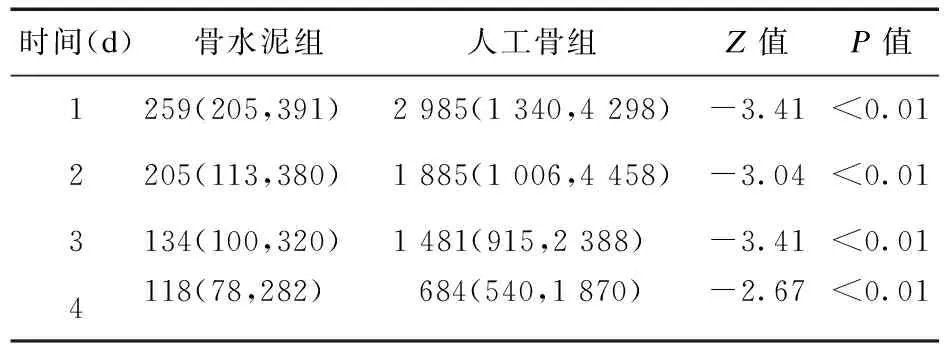
表2 萬古霉素骨水泥及人工骨的局部引流液濃度對比[mg/L,M(P25,P75)]
3.2 藥物動力學參數對比 利用Phoenix WinNonlin 6.4計算萬古霉素骨水泥和人工骨的藥動學參數,采用非房室模型,并對兩組數據及其差值分別進行Shapiro-Wilk檢驗。
3.2.1 局部釋藥性能結果比較 骨水泥組、人工骨組的局部最大釋放速率出現時間中位數均為10.5 h (Z=1.34,P=0.18),人工骨組局部釋放速率、釋放量、累計釋放率均大于骨水泥組。見表3。
3.2.2 局部植入后全身藥物動力學參數比較 骨水泥組、人工骨組Tmax、MRTlast比較差異無統計學意義,但人工骨組Cmax、AUClast高于骨水泥組。全身藥代動力學參數比較見表4。
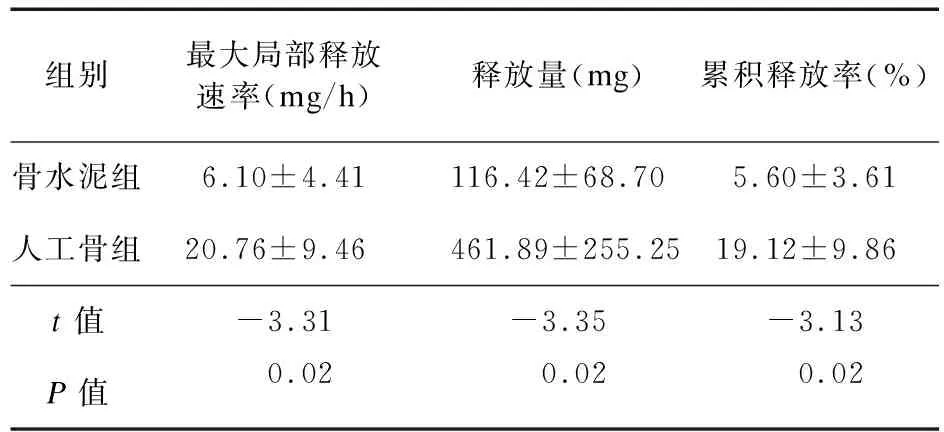
表3 萬古霉素骨水泥及人工骨的局部釋藥參數比較

表4 萬古霉素骨水泥及人工骨植入后全身的藥代動力學參數比較
4 討論
治療骨感染需要在感染局部達到有效的治療濃度,而骨組織標本難于獲取,因此,既往研究通過測定局部引流液的濃度,反映藥物在局部的濃度變化[8]。骨水泥及人工骨局部釋放藥物的影響包括骨感染病灶的大小及部位,血運豐富的部位藥物局部吸收入血的藥量多[9],造成局部藥物濃度降低,促進藥物釋放,因此,整體藥物釋放量會增加。而感染灶比較狹小,血運欠佳的部位感染則恰好相反,這會造成較大的個體差異[7]。本次研究收集了同一患者分別植入萬古霉素骨水泥及人工骨的局部引流液,進行對比分析,以消除不同感染灶大小對于藥物釋放造成的影響,更客觀地反映骨水泥及人工骨2種材料對于藥物緩釋的差異。
既往研究發現,硫酸鈣人工骨降解造成傷口滲液。由于人工骨降解過程中會產生水[10],而骨水泥由于不可生物降解而無此現象,據此推論,植入人工骨后的局部引流液應多于骨水泥。然而,本次試驗顯示,骨水泥總體引流量多于人工骨,此差異集中在術后1 d,這可能是因為骨水泥植入手術為大多數患者的第1次清創術,手術創傷較大,因為只有將內置物、死骨、瘢痕、肉芽等可能存在細菌生物膜的病灶全部移除,傷口才能愈合,一旦懷疑髓腔內存在感染,需要通過擴髓進行清創,若感染發生在骨干遠端或近端,擴髓腔長度不夠,則需要在病灶部位的皮質骨表面直接打開[11]。因此,手術創傷較大,術后局部出血多,引流量多,而人工骨手術是在第1次清創術后進行,無需進一步擴髓,僅需將第1次手術植入的鏈珠取出,植入抗生素人工骨即可,因此,創傷較第1次手術小,引流量總體小于第1次手術。由于臨床治療限制,無法進行交叉實驗,造成同一患者2次手術創傷大小可能存在差異,萬古霉素骨水泥治療手術創傷更大,因此引流量更多。
雖然萬古霉素骨水泥手術后的引流量明顯多于人工骨植入術,而既往研究顯示,引流量更大則藥物釋放量會更多[7],但本研究結果顯示,人工骨組藥物局部濃度、釋放率、釋放量、最大局部釋放速率、藥物植入后的全身濃度Cmax、AUClast均顯著高于骨水泥,說明除去局部引流量的因素,人工骨在術后1周內的釋藥性能高于骨水泥。
總之,萬古霉素人工骨和骨水泥植入人體后均能獲得很高的局部藥物治療濃度,全身藥物濃度均很低,安全性較好。人工骨作為藥物釋放載體,局部藥物濃度更高,總體釋放量、釋放率、釋放速度及植入后全身的藥物濃度均高于萬古霉素骨水泥。

