藥物臨床試驗倫理審查質量風險的管理研究
于浩 潘巖 武志昂 薛薇 李可欣


中圖分類號 R969.4;R-052 文獻標志碼 A 文章編號 1001-0408(2020)10-1153-05
DOI 10.6039/j.issn.1001-0408.2020.10.01
摘 要 目的:為提高我國藥物臨床試驗倫理審查質量、保障受試者權益提供參考。方法:以風險管理理論為指導,運用文獻研究法、專家意見法和層次分析法對藥物臨床試驗倫理審查流程進行梳理,提取并確定影響倫理審查質量的風險因素及其權重,并對我國藥物臨床試驗倫理審查工作提出改進建議。結果與結論:構建的藥物臨床試驗倫理審查風險指標體系包括5個方面共31個影響因素,其中影響藥物臨床試驗倫理審查質量的5個方面的重要性(權重)排序依次為醫學倫理委員會的自身建設(0.263 5)、審查會議的管理(0.251 4)、跟蹤審查(0.194 5)、審查申請的受理與處理(0.189 2)、文件檔案的管理(0.101 4);權重較高的影響因素包括“討論投票過程利益沖突人員回避(0.078 7)”“對方案修改、知情同意修改、嚴重不良事件等情形及時審查或召開會議討論(0.070 5)”“明確倫理審查工作流程及時間并對外公示(0.059 8)”“統一、規范的審查標準與批準標準(0.052 1)”等。建議可通過討論投票環節利益沖突人員予以回避,對方案修改、知情同意修改、嚴重不良事件等情形及時審查或召開倫理會議討論,明確倫理審查工作流程及時間,建立統一、規范的審查標準和批準標準等方式提高藥物臨床試驗倫理審查的質量。
關鍵詞 藥物臨床試驗;倫理審查;風險管理;層次分析法;專家意見法
Study on Quality Risk Management of Ethical Review of Drug Clinical Trials
YU Hao1,PAN Yan1,WU Zhiang1,2,XUE Wei3,LI Kexin3(1. School of Business Administration, Shenyang Pharmaceutical University, Shenyang 110016, China; 2. Beijing Yidu Zhengkang Health Technology Co., Ltd., Beijing 100055, China;3. Beijing Hospital Clinical Trial Center, Beijing 100083, China)
ABSTRACT? ?OBJECTIVE: To provide suggestions for improving the quality of ethical review of drug clinical trials in China and protecting the rights and interests of subjects. METHODS: Guided by risk management theory, the literature research method, expert opinion method and analytic hierarchy process method were used to sort out the ethical review process of drug clinical trials, extract and determine the risk factors that affect the quality of ethical review, and determine the weight of each risk factor. Suggestions were put forward improving the ethical review of drug clinical trials in China. RESULTS & CONCLUSIONS: Established ethical review risk index system of drug clinical trials included 31 influential factors of 5 aspects; the order of importance (weights) of 5 aspects affecting the quality of ethical review of drug clinical trials was as follows: the construction of the medical ethics committee (0.263 5), the management of review meetings (0.251 4), follow-up review (0.194 5), the acceptance and processing of review applications (0.189 2), and the management of documents and files (0.101 4). The influential factors with high weight included “withdrawal of people with conflict of interest in the discussion and voting process (0.078 7)”“timely review or conference discussion of scheme modification, informed consent modification, serious adverse events, etc. (0.070 5)”“clarification and external exhibition of the work process and time of ethical review (0.059 8)”“unified and standardized review standards and approval standards (0.052 1)”, etc. The quality of ethical review can be improved by avoiding people with conflict of interest in the discussion and voting process, timely reviewing or holding ethics meetings on scheme modification, informed consent modification, serious adverse events, etc., clarifying the working process and time of ethical review, and establishing unified and standardized review standards and approval standards.
KEYWORDS? ?Drug clinical trials; Ethical review; Risk management; Analytic hierarchy process; Expert opinion method
藥物臨床試驗是驗證新藥安全性和有效性必不可少的步驟,也是新藥研發和注冊的關鍵環節。為了證明某種新藥的療效和安全,在經動物實驗、機制研究證明有效后,必須要進行人體試驗來進一步驗證,因此需要相關人員來承擔臨床試驗所造成的風險。為保護臨床試驗中受試者的安全和權益,我國《藥物臨床試驗質量管理規范》明確指出,需成立獨立的醫學倫理委員會,試驗方案需經該委員會審核通過并簽署批準意見后方可實施[1]。由此可見,醫學倫理委員會的工作對于保障受試者權益具有重要意義。目前,由于各醫學倫理委員會對法規、指導文件的理解不一,缺乏標準的操作規程,審查的尺度和質量存在較大差異[2]。因此,本研究擬在風險管理理論的指導下,通過對醫學倫理委員會的倫理審查流程進行梳理,總結提取影響倫理審查質量的風險因素,以期對提高我國藥物臨床試驗倫理審查質量、保障受試者權益提供參考。
1 基本理論、概念與研究方法
1.1 基本理論、概念
1.1.1 基本理論 風險管理始于美國,于1930年由美國管理協會首次在保險相關問題的研討會上正式提出。之后,美國多所大學開始設立風險管理課程,風險管理遂逐步在全球范圍內流行并迅速發展,目前已被廣泛應用到政府部門和多個商業領域中,包括保險領域、財務管理領域、藥物警戒領域、公共健康領域等。2016年,人用藥物注冊技術要求指導委員會(ICH)頒布了新版《藥物臨床試驗質量管理規范E6(R2)》,并推薦了采用基于風險管理理論開展臨床試驗[3]。
風險是指在一定條件下,某個不良事件的預期發生概率與實際結果之間不同的頻率分布[4]。風險管理的目的在于識別潛在的風險因素并采取相應措施進行有效控制,降低損失發生的可能性和(或)嚴重性,其基本過程為風險識別、風險評估和風險控制[5]。其中,風險識別是指運用風險管理工具對風險因素進行系統和全面的識別;風險評估是在對風險識別定性分析的基礎上,運用統計分析等技術手段對風險主體發生的風險及概率進行定量分析;風險控制是對可能面臨的風險按照其風險發生概率的大小制定相應的風險應對策略,對風險進行防范和控制。
1.1.2 主要概念 本研究涉及的主要概念界定如下——倫理審查質量:倫理審查保障受試者安全和權益的程度;倫理審查質量風險:使得倫理審查質量受損的各種因素。
1.2 研究方法
以風險管理理論為指導,通過文獻研究和專家意見法識別影響倫理審查質量的風險,構建風險指標體系;采用Yaahp V12.4軟件,應用層次分析法對各風險指標進行評估,結合專家問卷咨詢結果,計算各風險指標的權重,進而提出提升倫理審查質量風險管理水平的具體建議。
采用SPSS 22.0軟件對調查問卷結果進行數據統計分析,主要包括描述性統計分析、信度分析以及效度分析。
2 臨床試驗倫理審查風險因素的提取
以“臨床試驗倫理審查” “質量管理”“風險管理”“Clinical trial ethics review”“Quality management”“Risk management”等為中英文關鍵詞,在中國知網、萬方數據、PubMed等數據庫進行交叉檢索,檢索時限均為2009年1月-2019年12月,共檢索到相關文獻43篇。排除與倫理審查質量相關度不高或無關的文獻后獲得中文文獻12篇、英文文獻2篇。運用風險識別分析方法中的流程圖分析法,通過文獻研讀梳理倫理審查工作流程,從醫學倫理委員會的自身建設[6-9]、審查申請的受理與處理[10-11]、審查會議的管理[12-14]、跟蹤審查[15-16]和文件檔案的管理[17-19]等5個方面初步提取影響藥物臨床試驗倫理審查質量的影響因素,結果見表1。
3 藥物臨床試驗倫理審查風險因素及權重的確定
3.1 問卷調查方案
本研究共開展兩輪問卷調查,均通過問卷星平臺發放。第1輪采用李克特量表法設計調查問卷,將初步擬定的各風險因素的回答設計為“非常重要”“重要”“一般”“不重要”“非常不重要”等5個選項,并分別以“5、4、3、2、1分”為上述5個選項計分。通過對影響倫理審查質量的風險因素進行專家論證,確定風險因素。第2輪運用風險評估方法中的層次分析法,將專家論證過的各因素進行兩兩比較,以確定各風險因素的權重。
3.1.1 調查對象 本研究主要選取藥品監管部門、醫療機構、醫藥企業、合同研究組織、臨床機構管理組織等從事倫理審查或藥物臨床試驗工作、本科及以上學歷并對倫理審查比較了解或非常了解的專家為調查對象。主要包括醫學倫理委員會委員、研究者、臨床監察員、臨床協調員、稽查員等。
3.1.2 問卷樣本量的確定 為確保問卷調查具有統計學意義,需要確定問卷調查的樣本量大小。樣本容量(N)的計算公式為:N=[Z 2P(1-P)]/E 2。式中,Z為統計量,P為概率值,E為采樣誤差值[20]。
為保證結果的有效性,令P=0.5,則P(1-P)=0.25。設定樣本置信區間為90%,抽樣誤差范圍在±15%以內,查詢Z統計分布表可得Z=1.65,帶入公式得N=30.25,因此本研究需要31份問卷,方可使樣本置信度達90%,誤差范圍小于15%。
3.2 應用專家意見法對風險指標進行確認
第1輪調查共發放問卷79份,回收有效問卷70份,問卷回收率為88.6%。其中,合同研究組織30人(42.9%),醫療機構16人(22.9%),醫藥企業13人(18.6%),臨床機構管理組織7人(10.0%),藥品監管部門及其他機構4人(5.7%);本科學歷41人(58.6%),碩士學歷28人(40.0%),博士及以上學歷1人(1.4%)。運用SPSS 22.0軟件對問卷進行描述性分析及信效度分析。描述性分析結果顯示,所有風險指標的評分均值均大于4,變異系數均小于0.25,說明各風險指標均是影響倫理審查質量的重要風險因素,且各專家對風險指標重要性評價的分歧較小[21]。信度分析結果顯示,問卷的Cronbachs α系數為0.956,說明問卷信度良好,具有較高的穩定性和一致性[22]。經分析,刪除“參與倫理審查認證體系項目,如美國人體研究保護項目認證協會認證、醫學倫理審查委員會能力拓展戰略方案認證、中醫藥研究受試者保護體系評估認證”這項風險指標,問卷的信度得到顯著提高,故刪除該指標。采用因子分析法計算問卷的效度,結果KMO值為0.824,表明本研究問卷有效性和準確度良好[23]。后又根據專家意見對風險指標進行修正,得到藥物臨床試驗倫理審查質量風險指標體系,詳見表2。
3.3 應用層次分析法對風險指標的權重進行分析
3.3.1 層次結構模型構建 采用Yaahp V12.4軟件對上述風險指標構建層次結構模型。其中,目標層為藥物臨床試驗倫理審查質量風險,準則層共計5項風險指標,方案層共計31個風險要素。
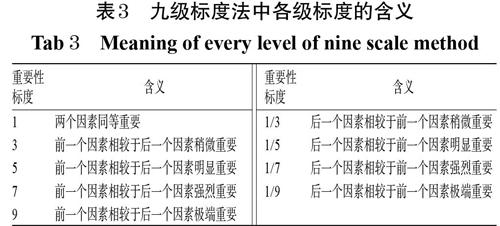
3.3.2 構造判斷矩陣 以建立的層次結構模型為依據構造判斷矩陣,采用九級標度法,取1、3、5、7、9、1/3、1/5、1/7、1/9共9個等級標度[24],詳見表3。邀請專家對上述風險指標的相對重要程度進行評估,計算各風險指標的權重。
3.3.3 各風險因素權重的確定 第2輪調查共發放問卷41份,回收有效問卷33份,問卷回收率為80.5%。其中,合同研究組織 12人(36.4%),醫療機構9人(27.3%),臨床機構管理組織5人(15.2%),醫藥企業4人(12.1%),藥品監管部門及其他3人(9.1%);本科學歷15人(45.5%),碩士學歷17人(51.5%),博士及以上學歷1人(3.0%)。將33份專家問卷結果錄入到Yaahp V12.4軟件中,經軟件自動調整一致性后,所有專家問卷均通過了一致性檢驗。將通過一致性檢驗的專家問卷輸入層次結構模型中,得到各風險因素對總目標的權重,詳見表2。
4 分析與討論
4.1 準則層因素對目標層的權重
藥物臨床試驗倫理審查質量風險各影響因素的重要程度依次為:醫學倫理委員會的自身建設>審查會議的管理>跟蹤審查>審查申請的受理與處理>文件檔案的管理。由此可見,醫學倫理委員會的自身建設環節對倫理審查質量具有重要的影響,值得重點關注;文件檔案的管理相對其他環節的風險權重最低,反映出目前的倫理審查流程在文件檔案管理方面做得相對較好。
4.2 方案層因素對目標層的權重
方案層共31個風險因素,取權重前40%的因素共計12個,重要程度依次為:討論投票過程利益沖突人員回避>對方案修改、知情同意修改、嚴重不良事件等情形及時審查或召開會議討論>明確倫理審查工作流程及時間并對外公示>統一、規范的審查標準與批準標準>制定醫學倫理委員會培訓制度,定期接受倫理審查知識及相關法律法規培訓>確保送審文件的完整性、有效性>加強與受試者交流,重視受試者反饋,建立反饋機制>對倫理審查意見進行充分討論>制定醫學倫理委員會委員及倫理秘書的準入制度以及根據項目類別和風險大小合理選擇倫理審查方式>醫學倫理委員會委員的獨立性>對倫理審查申請的相關事宜作出明確規定,明確送審渠道及送審文件。其中,屬于醫學倫理委員會自身建設環節的因素有4個,屬于審查申請的受理與處理環節的有3個,屬于審查會議的管理環節的有3個,屬于跟蹤審查環節的有2個。這些均為影響倫理審查質量的重要因素,應予以高度重視。此外,文件檔案的管理環節各因素風險雖然相對較低,但也不容忽視。
5 建議
5.1 醫學倫理委員會的自身建設環節
醫學倫理委員會是倫理審查的主體機構,其成功組建是確保倫理審查能夠有效開展的基本保障,其中,應特別關注以下問題:(1)規范醫學倫理委員會工作流程及時間并對外公示。規范的醫學倫理委員會工作流程及時間將有助于倫理審查工作的有序進行并提高審查效率,便于申請人能夠及時掌握倫理審查動態,如建立醫療機構醫學倫理委員會官方網站,明確告知審查流程及倫理審查文件受理時間、審查時間、審查后發放批件時間等。(2)制定醫學倫理委員會培訓制度。倫理知識以及倫理審查評價方法都是與時俱進的,醫學倫理委員會可根據國際相關指南標準,結合國內實際情況,制定倫理委員的入職培訓與繼續教育培訓相結合的多樣化、多層次的培訓體系,并在培訓完成后進行考核,以了解委員掌握知識的真實狀況。(3)制定倫理委員及倫理秘書的準入制度。通過建立統一的任職資格標準,對倫理委員進行資格認證,資質未達要求的人員不予聘任。(4)確保倫理委員的獨立性。利益沖突有時無法避免,但可通過優化倫理委員的構成確保委員獨立性的最大化。例如,可聘請退休資深專家或機構外權威專業人員擔任委員會主席,并保證委員組成比例適當,應既包括本機構的醫學專家,也包括機構外醫學倫理學、社會學、心理學、法學等相關專家以及社區代表[25]。
5.2 審查申請的受理與處理環節
倫理審查申請的受理與處理是倫理委員對研究項目開展審查的初始階段,倫理秘書或相關工作人員需確保文件質量并合理選擇審查方式,應注意以下幾個方面:(1)確保送審文件完整有效。申請人將倫理審核文件送審后,秘書或相關工作人員應依照審查清單逐一核對文件,檢查文件的完整性、有效性、合法性;若需補充修改,應立即告知申請人修改內容并明確送審截止日期。(2)合理選擇審查方式。倫理審查方式主要包括會議審查、快速審查和緊急會議審查,倫理委員需根據項目類別和風險大小選擇會議審查或快速審查的方式,而對于研究過程中出現危及受試者安全的嚴重問題或其他需緊急處理和決定的情況則需采取緊急會議審查。(3)對倫理審查申請的相關事宜作出明確規定。醫學倫理委員會應在事前制定申請人送審操作須知,明確申請文件類型、文件格式要求、送審渠道等,避免申請人因文件準備不充分或格式不符合要求等而反復修改。
5.3 審查會議的管理環節
審查會議時間有限且任務繁重,如何管理好審查會議至關重要。在審查會議過程中需注意以下幾個問題:(1)參會委員若與審查項目存在利益沖突應提前聲明,討論投票過程中利益沖突人員應主動回避,保證投票過程的民主與公正。(2)建立統一、規范的審查標準和批準標準。目前我國雖已頒布了一系列法規及指導原則,但如何將其應用到具體的實踐操作中,各個醫學倫理委員會都有不同的標準。建議應制定研究項目啟動前、進行中和結題后各環節的統一、規范的審查標準,使倫理審查過程有據可依,盡量避免因不同醫學倫理委員會標準不一所致的審查結果不同的現象。(3)對倫理審查意見進行充分討論。申請人在匯報研究項目后,會議主持人應組織各委員積極發言;當出現審查意見不一致時,與會委員應積極發表自己的意見,必要時可向相關研究方面的專家進行咨詢,確保所提意見被及時討論解決。
5.4 跟蹤審查環節
跟蹤審查是指醫學倫理委員會根據一定的標準操作規程對通過初始審查的研究項目所進行的持續的監督、審查及評價。跟蹤審查需注意以下問題:(1)當出現方案修改、知情同意修改、嚴重不良事件等情形時,應及時審查或召開倫理審查會議討論。在臨床試驗過程中,受多方因素影響,可能會出現試驗方案修改、知情同意修改、嚴重不良事件、受試者退組等情況,醫學倫理委員會需建立標準操作規程,及時進行審查,對試驗的進展、風險與受益進行持續性評估,保證研究項目安全、有效地開展,并確保受試者的利益不受侵害。(2)建立受試者反饋機制。在美國,醫學倫理委員會的一項重要工作任務就是傾聽受試者的抱怨、疑惑、擔憂等[16]。建議我國可借鑒其經驗,構建受試者反饋機制,指派專人負責與受試者溝通交流,了解受試者現狀,及時協助其解決問題。
5.5 文件檔案的管理環節
檔案歸檔的過程真實地反映了醫學倫理委員會的運行情況和倫理審查的經過,檔案不僅是試驗過程中最真實、最可靠的依據資料,而且也包括受試者的個人信息和隱私。因此,需健全檔案資料管理制度,統一規范文件的收集、整理、歸檔、保存、查閱、銷毀等步驟,確保文件安全完整,符合規范。本研究中,該環節總體權重較低,反映了當前文檔管理的總體狀態良好、風險較低,但從長遠來看,該項工作仍應予以持續關注。
6 結語
本研究運用文獻研究法和專家意見法確立了藥物臨床試驗倫理審查質量的風險因素,運用層次分析法確定了各風險因素的權重,并對權重較高的因素提出針對性的風險防控建議。本研究所建立的風險指標體系有助于明確倫理審查工作質量的改進重點,有助于風險管理效果的提升。但因筆者調查時間以及人脈資源有限,調查問卷數量相對較少,較難向更多權威專家進行咨詢,可能對調研結果造成一定影響,因此所建風險指標體系有待后續實踐進一步驗證。
參考文獻
[ 1 ] 國家食品藥品監督管理局.藥物臨床試驗質量管理規范[S].2003-09-01.
[ 2 ] 呂麗娜,熊楠楠,常運立,等.完善醫學倫理委員會工作機制的思考[J].醫學與社會,2012,25(2):26-28.
[ 3 ] 肖亮,鄭高哲,黃瑜敏.臨床試驗基于風險的管理研究進展[J].中國臨床藥理學與治療學,2017,22(8):955-960.
[ 4 ] 王周偉.風險管理[M].北京:機械工業出版社,2012:3.
[ 5 ] 任佳偉,張若明,張象麟.藥物臨床試驗機構備案制對藥物Ⅰ期臨床試驗質量影響的風險管理研究[J].中國新藥雜志,2019,28(3):319-324.
[ 6 ] RAVINDRA BG. Institutional review boards:challenges and opportunities[J]. Perspect Clin Res,2014,5(2):60-65.
[ 7 ] 余中光,馮力,李素娟,等.醫學倫理審查管理中存在的問題及發展建議[J].中國醫學倫理學,2017,30(2):158- 161.
[ 8 ] 武敏,高敬龍.藥物臨床試驗倫理質量管理持續改進實踐[J].中國醫學倫理學,2015,28(5):769-771.
[ 9 ] 王晨,姚鐵男,白彩珍.藥物臨床試驗倫理審查中的風險與防范[J].中華醫院管理雜志,2011,27(9):684-688.
[10] 白樺,孫燕,宋亞京,等.影響倫理審查速度的因素分析[J].中國醫學倫理學,2016,29(3):465-468.
[11] 胡晉紅.醫院倫理委員會標準操作規程[M].北京:化學工業出版社,2015:54-57.
[12] 訾明杰,翁維良,高蕊,等.試析倫理審查會議中的常見問題[J].中國醫學倫理學,2013,26(5):562-564.
[13] 師明陽,閆冬,任萍.醫院倫理委員會會議審查工作實踐和啟示[J].醫學與哲學(A),2018,39(11):15-16、31.
[14] IVOR AP. How do IRB members make decisions: a review and research agenda[J]. J Empir Res Hum Res,2011,6(2):31-46.
[15] 吳柳娟,周建國,柳龔堡.戴明環循環法在醫學倫理跟蹤審查工作中的應用[J].醫學與社會,2018,31(6):43- 45、48.
[16] 張雪,尹梅,劉丹茹.倫理審查委員會跟蹤審查制度探析[J].醫學與哲學(A),2012,33(4):26-27、51.
[17] 郜翀,李紅英.機構倫理委員會文件材料“檔案化”管理探討[J].醫學與哲學(A),2018,39(2):32-34、76.
[18] 柴怡,張馥敏,孫寧生,等.淺談藥物臨床試驗倫理審查中的文件管理[J].中國藥物警戒,2011,8(7):413-415.
[19] 蘇勃.淺析如何加強倫理審查工作中檔案材料的管理[J].蘭臺世界,2015(17):78-79.
[20] 劉晶晶,武志昂.建立我國藥品專利鏈接制度的專家調查研究[J].中國新藥雜志,2016,25(11):1206-1211.
[21] 張丁丁.描述性統計分析及SPSS實現[J].協和醫學雜志,2018,9(5):447.
[22] 楊再運.信度分析在環境問卷中的應用研究[J].現代工業經濟和信息化,2015,5(21):101-103.
[23] 黃薇,張瀾.高中心理健康教育課的實施現狀調查量表的編寫及應用[J].科技創新導報,2015,12(19):218-220.
[24] 王雷.商業銀行操作風險影響性評級模型研究[J].經濟問題,2011(7):100-104、126.
[25] 邵蓉,樓洪剛,楊丹丹,等.臨床研究倫理審查現狀及其問題探討[J].中國腫瘤,2015,24(10):830-833.
(收稿日期:2020-01-09 修回日期:2020-04-13)
(編輯:孫 冰)

