合肥地區2型糖尿病患者尿微量白蛋白肌酐比值與DR的關系
魏 科,李永蓉,王志敏
0引言
糖尿病視網膜病變(diabetic retinopathy,DR)是嚴重威脅視功能的眼底病變,隨著人均壽命的延長及人民生活水平的不斷改善,我國糖尿病患病率由1980年的0.67%飆升至2013年的10.4%[1],已成為全球糖尿病患者人口最多的國家[2]。DR是糖尿病常見并發癥之一[3],我國DR患者占糖尿病患者的21.87%[4],DR成為目前工作年齡人群第一位致盲性眼病。DR的早期干預對疾病的轉歸影響頗大。目前DR的診斷主要依賴于眼底攝片及眼底造影等影像學方法[5],基層普查存在難度,尋找一些較為簡便經濟的篩查指標具有一定臨床價值。
表1 兩組患者基本資料的比較

基本資料NDR組(n=169)DR組(n=112)t/χ2/UP男/女(例)105/6463/490.9690.325年齡[M(P25,P75),歲]54(25,62)57(50,66)7258.5000.001高血壓(例)68531.3790.240糖尿病病程[M(P25,P75),a]5.00 (1.00,10.00)10.00(4.25,13.00)6321.500<0.001BMI( x±s,kg/m2)25.22±3.9724.95±3.480.5740.566FBG[M(P25,P75),mmol/L]8.71(6.54,10.95)7.98(6.65,10.30)8755.0000.288HbA1c[M(P25,P75),%]8.90(7.40,10.70)8.65(7.43,10.98)9404.0000.928TB[M(P25,P75),mmol/L]16.30(11.55,20.95)14.00(11.20,20.18)8701.5000.253TC[M(P25,P75),mmol/L]4.26(3.55,4.96)4.10(3.41,4.95)9155.5000.644TG[M(P25,P75),mmol/L]1.57(1.11,2.47)1.56(1.04,2.25)9219.9000.713BUN[M(P25,P75),mmol/L]5.02(4.24,5.97)5.36(4.43,6.55)8315.0000.085UACR[M(P25,P75),mg/g·Cr]4.10(2.40,10.65)14.20(4.70,70.23)5352.500<0.001
1對象和方法
1.2方法采集患者性別、年齡、糖尿病病程、高血壓史、體質量指數(body mass index,BMI)、尿微量白蛋白肌酐比值(urine microalbumin creatinine ratio,UACR)、空腹血糖(FBG)、糖化血紅蛋白(HbA1c)、總膽紅素(TB)、總膽固醇(TC)、甘油三酯(TG)、血尿素(BUN)等資料。血液標本采集時間為晨起空腹,尿液標本采集時間為首次晨尿,所有標本均送檢檢驗中心并出具檢測結果。眼底攝片采用OPTOMED Smartscope PRO眼底照相機,拍攝以黃斑中心凹為中心的45°后極部彩色眼底像,根據ETDRS診斷標準[6]對DR進行診斷,由2名眼科主治醫師分別進行閱片和診斷,對于診斷存疑者交由第3名眼科副主任醫師進行判讀。DR患者定義為至少1眼發生DR,非DR(NDR)患者定義為雙眼均未發生DR。
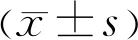
表2 Logistic回歸分析結果
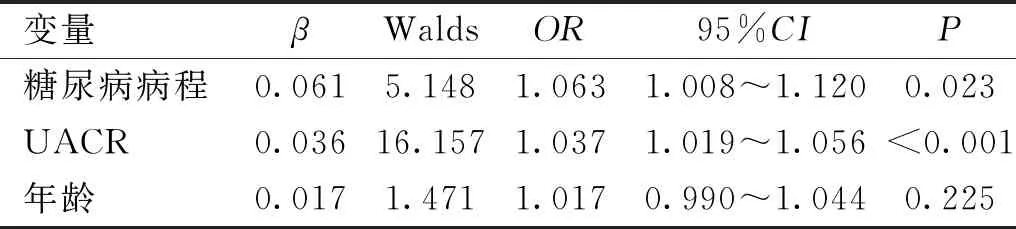
變量βWaldsOR95%CIP糖尿病病程0.0615.1481.0631.008~1.1200.023UACR0.03616.1571.0371.019~1.056<0.001年齡0.0171.4711.0170.990~1.0440.225
表3 DR危險因素ROC曲線特征參數
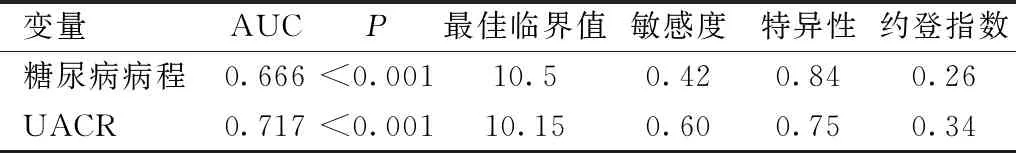
變量AUCP最佳臨界值敏感度特異性約登指數糖尿病病程0.666<0.00110.50.420.840.26UACR0.717<0.00110.150.600.750.34
2結果
2.1基本資料根據眼底檢查結果,本研究納入的281例患者中,檢出DR患者112例(39.9%,DR組),NDR患者169例(60.1%,NDR組),兩組患者年齡、糖尿病病程、UACR比較,差異均有統計學意義(P<0.05),其余各指標差異均無統計學意義(P>0.05),見表1。
2.2二元Logistic回歸分析DR發生的危險因素將糖尿病病程、年齡、UACR作為自變量納入二元Logistic回歸分析,結果顯示糖尿病病程及UACR為DR發生的危險因素,見表2。Hosmer-Lemeshow擬合優度檢驗結果滿意(χ2=5.981,df=8,P=0.649)。
2.3危險因素ROC曲線分析繪制危險因素ROC曲線,見圖1。計算曲線特征參數,見表3。DR危險因素的最佳臨界值為糖尿病病程10.5a,UACR為10.15mg/g·Cr。
3討論
糖尿病患者持續的高血糖狀態通過激活多元醇通路、氨基己糖通路等代謝途徑,介導氧化應激,對包括視網膜在內富含外周血管的組織造成損傷[7-8],同時糖化后的血紅蛋白攜氧能力下降,導致末梢組織缺氧,也可引起外周組織受損[9]。腎小球富含毛細血管,可作為觀測外周毛細血管系統損害程度的窗口之一,臨床上常選取微量蛋白尿為內皮系統損傷標志物[10-11],UACR是尿微量白蛋白與尿肌酐的比值,選取UACR評估腎功能可避免單一指標觀測的片面性。研究證實,UACR與24h尿微量白蛋白間具有很好的相關性[12-13],且因其便于取材,UACR已廣泛用于糖尿病患者腎功能的評估及心血管類疾病風險預測[14-17]。視網膜同為富含外周微血管系統的組織,有學者報道,糖尿病患者中,腎臟病變與DR高度相關[3,18-21]。Boelter等[22]對巴西地區1 214名2型糖尿病患者研究發現,微量白蛋白尿是2型糖尿病患者DR發生的危險因素。王養忠等[23]對295例2型糖尿病患者研究發現,DR患者與NDR患者間UACR存在顯著差異。李梅芳等[24]對上海地區595例2型糖尿病患者的橫斷面研究結果表明,即使修正糖尿病病程等因素后,UACR與DR發生仍顯著相關。本研究結果顯示,UACR是DR發生的危險因素,與國內外類似研究結果一致,根據ROC曲線,本研究將UACR臨界點定義在10.15mg/g·Cr,當糖尿病患者UACR維持在較高狀態時,應關注視網膜微循環系統,警惕DR發生。
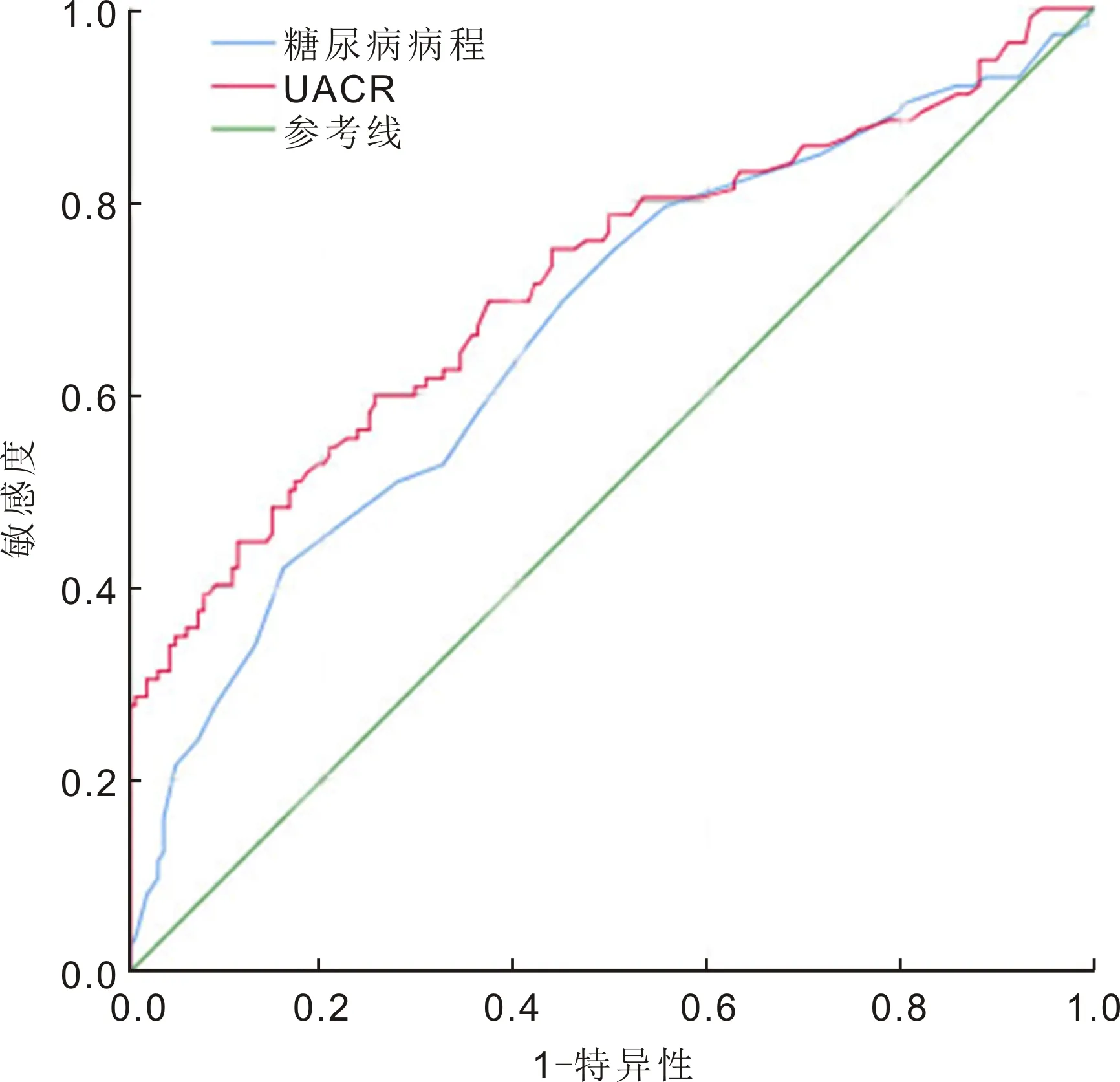
圖1危險因素ROC曲線。
糖尿病病程是目前較為公認的DR發生的獨立危險因素[25],高血糖狀態對于靶器官的損害是一個不斷累積的過程,糖尿病病程越長,意味著風險暴露時間越長,DR發生率越高。段春文等[26]通過回顧性分析2型糖尿病患者753例,將糖尿病病程≥4.5a作為DR的獨立危險因素。本研究亦發現糖尿病病程為DR風險相關因素,糖尿病病程≥10.5a為DR發生的高危因素,樣本量及患者不同的文化程度、生活習慣和醫療依從性等可能引起細節差異,尚需進一步研究。
本研究未發現HbA1c、高血壓史等與DR發生存在顯著相關,與國內外部分相似研究存在一定差異,分析原因可能包括:(1)本研究樣本量偏小,結果可能存在一定程度的偏差;(2)DR病因復雜,部分指標與DR的相關性可能需要進一步研究,如HbA1c為最近8~12wk平均血糖水平的評估指標[27],有國內外學者報道HbA1c只能部分解釋糖尿病并發癥的發病風險,單純控制HbA1c不能有效降低糖尿病血管并發癥發生風險[28-29];糖尿病心血管并發癥防控研究(ACCORD)發現控制收縮壓在DR防控方面并無顯著作用[30],英國前瞻性糖尿病研究 (UKPDS)指出嚴格控制血壓并不能完全阻止DR[31]。
本研究結果提示UACR及糖尿病病程為DR風險相關因素,對于DR患者的篩查及病情監控具有一定參考價值。但本研究仍存在不足之處:(1)本研究為回顧性研究,樣本量較小且有地域限制,若能設計多中心及前瞻性研究,所得結果將更加可靠;(2)本研究中自變量類別較少,尚可能存在其它與DR顯著相關的風險因素未被發現;(3)受設備條件及實際操作等因素影響,本研究主要依賴醫師通過眼底攝片判斷DR,對于部分只存在少量微血管瘤的輕度DR患者可能漏診,今后需進一步完善。
3劉家燕, 樊映川. 糖尿病視網膜病變的流行病學研究現狀. 實用醫院臨床雜志 2015; 2: 137-138, 139

