重癥患者腸內營養期間的血糖管理研究進展
農慧瓊,劉遠金,文藝,張理
(廣西柳州市人民醫院重癥醫學科,廣西 柳州)
0 引言
有研究表明,重癥患者處于高分解代謝狀態,并且機械通氣會極大增加患者機體能量消耗,使得74%左右的患者會出現營養不良[1]。近年來,在危重患者的支持治療中,營養支持與機械通氣、腎臟替代療法具有同等重要的地位[2]。目前,重癥患者治療方案中營養支持治療為不可或缺的一部分[3]。
危重患者受到創傷、感染、中毒等特殊的病理生理學改變,使得常出現明顯的內分泌紊亂情況,發生應激性血糖升高,而血糖升高程度又和患者的住院時間、死亡率等具有直接關聯[4,5]。諸多研究均證實危重患者血糖波動越大,則患者的死亡率越高,二者關系密切[6]。血糖波動性是指非穩態波動血糖在峰值和谷值之間波動的幅度,其可以作為預測危重患者預后的一項重要指標,如重癥肺炎、嚴重多發傷、膿毒癥等[7]。很多專家學者通過研究,認為重癥患者的血糖波動幅度越大,則炎癥反應、氧化應激損傷會越嚴重,這可能是使得重癥患者死亡率升高的一項重要原因[8]。
鐘春苗等人研究的早期腸內營養支持標準化治療流程管理可降低機械通氣患者血糖波動水平,從而改善預后[9]。
因此將血糖控制在合理范圍,在適度放松對血糖控制目標值的同時,避免血糖波動。本文旨在綜述重癥患者糖代謝紊亂的原因、影響、腸內營養的供給、血糖的控制等,為臨床重癥患者腸內營養期間的血糖管理提供參考。
1 危重患者血糖的變化
很多因素都會導致患者血糖發生變化,如營養支持治療、藥物使用等,會使糖代謝紊亂情況加重,血糖過高或過低及血糖的波動對患者的預后有很重要的影響。
1.1 高血糖發生原因及機制
1.1.1 機體應激反應
重癥患者受到創傷、感染、手術、疾病導致的器官功能損傷等,會使患者發生較大的機體應激反應,使得機體處于高能量代謝狀態以及高炎癥狀態,導致機體內環境穩定性遭到破壞,從而使病情加重,嚴重影響預后甚至導致死亡[10]。在應激狀態下,下丘腦- 垂體- 腎上腺素興奮,升糖激素如糖皮質激素、兒茶酚胺、胰高血糖素、生長激素等分泌增加,分解代謝和糖異生,并對胰島素產生拮抗作用,對胰島素分泌進行抑制,使得發生胰島素抵抗,影響機體血糖調節功能;多種細胞因子作用,已知YNF-α 主要通過調節胰島素受體后信號的傳導,使得肝臟、骨骼肌出現胰島素耐受情況,從而促進血糖水平提升。
1.1.2 醫源性高血糖
危重患者需要接受較多的治療,受到諸多醫源性因素,如腸內營養、靜脈輸入含糖液體、皮質激素和血管升壓藥等的影響,也會導致血糖升高。
1.1.3 其他
重癥患者臥床時間長,骨骼肌胰島素敏感性會逐漸降低,另外年齡也是發生高血糖的一個重要影響因素。
1.2 低血糖發生原因
與禁食、不合理應用胰島素、多器官功能障礙有直接關聯。
2 高血糖對機體重要器官的影響
2.1 對心功能的影響
高血糖引起血管內炎癥反應,氧化應激會導致內皮細胞和微血管功能障礙。而炎癥細胞因子大量增加,會使氧化應激反應進一步加劇,從而使血管內皮功能受到損害,促進了血管病變[11]。高血糖還會產生血栓前期狀態,降低血漿纖維蛋白的溶解活性與組織纖溶原的活性,并對患者心肌細胞造成進一步損傷,影響心功能。
2.2 對腦功能的影響
要想使大腦功能正常運轉,需要有穩定且持續的血糖、血氧供應。而低血糖狀態會使患者大腦正常能量代謝受到影響,使神經元損傷情況加重,而高血糖狀態持續時間長短則直接關系預后。研究顯示,血糖異常波動會增加患者腦梗死面積,使患者療效和神經系統自我修復均出現不良影響[12]。
2.3 對腎臟功能的影響
唐之韻等[13]研究發現,相比于血糖正常的重癥患者,高血糖患者尿量明顯更少。經分析,認為血糖波動致使患者預后不良,其原因可能是血糖異常波動使得產生較多的細胞氧化應激物質,激活了炎癥反應因子,對內皮細胞、胰腺細胞造成損傷,激活了凝血系統而增加了血栓形成風險等。
2.4 對肺功能的影響
研究[14]發現,COPD 患者如果存在高血糖情況,患者的血漿D-D、FIB 濃度會明顯增加,與正常血糖組患者之間存在明顯差異。而伴有高血糖狀態的AECOPD 患者,機體凝血機制反應會被明顯激活,增加患者發生血管內微血栓形成與肺栓塞的風險。
2.5 對肝臟功能的影響
高血糖狀態產生的毒性反應會增加氧化應激、線粒體應激,并造成DNA 損傷等,并進而對肝臟、胰腺等臟器造成損傷[15]。
3 腸內營養的供給
目前對于重癥患者,營養支持治療為一項研究重點,而采取的營養支持治療方案直接決定了治療效果,其影響因素主要有如下幾種。
3.1 時機
若重癥患者存在高營養風險,入院后24-48h 內需要開展營養支持治療,對于無明顯禁忌的患者,腸內營養支持方法為首選。
3.2 供給方式
對危重患者使用鼻飼泵進行持續少量的腸內營養供給是目前臨床上所提倡的,有助于降低并發癥風險,但仍有待更多更高質量的研究證據支持。間歇大劑量給予腸內營養便捷性更好,成本更低,對多數使用胃管且情況穩定的患者適用。腸內營養可通過鼻腸管、鼻胃管方式進行營養供給,兩種方法的療效有一定差異。重癥患者接受鼻腸營養支持,有助于避免發生營養液返流、誤吸等情況,降低肺炎風險,這是因為重癥患者的胃賁門更易處于開放狀態,通過鼻胃管供給營養會增加營養液反流和誤吸的概率[16]。
3.3 熱量與蛋白質供給量
危重患者因為應激或炎癥反應導致營養吸收和利用障礙,早期若營養供給量較多,會增加機體負擔,降低疾病恢復效果,在這種情況下,滋養型喂養方式應運而生。該喂養方式提出每天給予的熱量為10-20kcal/kg或<500 kcal,這樣可以降低胃腸道不耐受情況的發生概率,逐漸在1周后達到目標量的80%是最優的方案[17]。多研究顯示,機械通氣患者早期(3-12d)提供70%的目標量及≥1.3g/kg/d的蛋白質,病死率最低[18]。由此美國重癥醫學會與美國腸外腸內營養治療學會及歐洲腸外腸內營養學會2016、2018年頒布的成年重癥營養治療指南指出蛋白質供給量保持在1.2-1.5g/kg/d或>1.3g/kg/d的水平較為適宜[19]。但需要明確一點,在未過度喂養的情況下,增加蛋白質供給量會有明顯收益。
4 血糖控制方案
4.1 血糖的監測
快速血糖儀在臨床有普遍應用,其通過采集末梢血測量血糖,但是測量結果容易受到采血部位、采血量、靜脈輸液、消毒劑等因素的影響。另外有學者認為有水腫情況的重癥患者,末梢血糖標本反應的為組織間隙血糖濃度,而非末梢血糖水平[20]。ICU患者外周組織水腫、微循環障礙、血壓異常、HCT下降很容易,加之血管活性藥物的使用,末梢血糖測量結果容易產生誤差,從而影響接下來的治療。近年來國外研究[21]顯示動脈血實驗室血糖值更能準確反映休克患者的真實血糖水平。
4.2 動脈血糖的控制方案
周亞敏等[22]對ICU患者采用的血糖控制新方案,取得比較滿意的效果。將動脈血糖值作為控制血糖的指導標準,即連續2次動脈血糖≥10.1mmol/L,開始輸注胰島素(胰島素40u+生理鹽水40ml微量泵輸入),使其血糖維持在6-10mmol/L。胰島素劑量動態調整方案見表1。
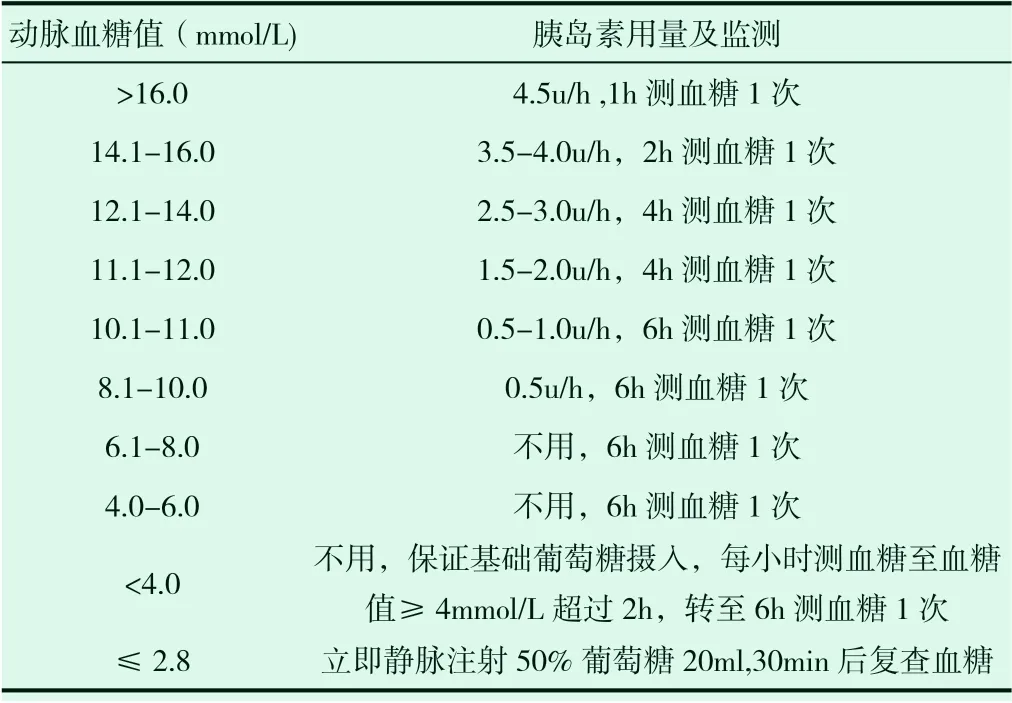
表1 動脈血糖的控制方案
總之,若重癥患者胃腸道功能良好,腸內營養可起到較好效果;然而,對于腸道不耐受者則需要在早期腸外營養的基礎上盡快改善腸功能,盡早啟動腸內營養,使患者受益,但重癥患者極易出現血糖異常,因此應當加強血糖檢測,制定控制血糖方案,合理應用胰島素,使患者血糖平穩降低,改善預后。

