鐵酸鋅配碳選擇性還原的熱力學分析和試驗研究
汪鑫,鄧寅祥,許繼芳,魯菊
(蘇州大學沙鋼鋼鐵學院,江蘇 蘇州 215021)
電爐煉鋼粉塵中含有大量的有價元素,如鐵,鋅等[1]。我國電爐粉塵中鋅含量約10% ~ 15%,主要以鐵酸鋅和氧化鋅的形式存在。大量的電爐粉塵堆積不僅造成金屬資源的浪費,還造成環境污染[2-3]。因此,電爐粉塵中鐵和鋅的回收利用的研究具有重要意義。
電爐粉塵處理工藝中,填埋處理法工藝簡單,但無法利用有價金屬資源[4];循環利用進入鋼鐵生產流程,可回收其中的鐵資源,但鉛鋅的富集對后續高爐煉鐵以及煉鋼生產造成影響;火法工藝則受設備投資大,能耗大等問題限制[5];濕法工藝處理過程中,氧化鋅中的鋅較易浸出,不易浸取鐵酸鋅中的鋅,導致鋅浸出率低[6-7]。此外還有真空冶金法[8]、鋁浴熔融法[9]、焙燒轉化-分離[10]等方法。其中焙燒轉化-分離方法是通過焙燒把它變成易溶解的化學相(如氧化鋅以及鋅的氯化物或硫酸鹽等),再浸出回收鋅,關鍵是提高電爐粉塵鐵酸鋅的轉化率[11-12]。
鐵酸鋅的焙燒轉化的關鍵在于鐵酸鋅的高效分解和焙燒產物的有效調控。本文為研究鐵酸鋅配碳選擇性還原分解過程,通過Factsage計算和試驗研究相結合,分析鐵酸鋅配碳還原分解的熱力學,討論反應溫度和配碳量對鐵酸鋅分解行為的影響,獲得鐵酸鋅選擇性還原和抑制還原產物過還原的條件,為鐵酸鋅選擇性還原、鐵和鋅等資源的綜合利用提供依據。
1 試驗原料
將ZnO粉末試劑(AR)和Fe2O3粉末試劑(AR)按摩爾比1:1球磨混勻,高溫馬弗爐內在1200℃下固相反應2 h,期間發生的主要反應為ZnO+Fe2O3→ZnFe2O4,隨后采取自然冷卻至室溫,隨后進行研磨(小于74 μm)、篩分和干燥保存,用于后續配碳還原試驗。X射線衍射儀物相分析結果見圖1。由圖1可知,衍射峰峰型尖銳,晶型完好,與鐵酸鋅標準衍射峰一一對應,表明固相反應產物為鐵酸鋅(JCPD #22-1012),且產物結晶度好、純度較高[13]。

圖1 固相合成鐵酸鋅的XRD圖譜Fig. 1 XRD pattern of synthetic zinc ferrite by solid-state synthesis
將固相反應合成的鐵酸鋅和活性炭粉(AR)按10:1質量比(C/O摩爾比為0.50)稱量后,球磨混勻。然后壓塊、干燥后裝入剛玉坩堝,高溫馬弗爐內進行不同溫度下2 h的還原反應,隨后自然冷卻至室溫,研磨、篩分和干燥保存。
2 研究方法
為研究鐵酸鋅配碳選擇性還原分解過程,采用Factsage計算和分析鐵酸鋅配碳還原分解的熱力學,主要計算的各反應的標準吉布斯自由能變化(ΔGθ)隨溫度的變化關系,分析配碳還原鐵酸鋅在不同反應溫度和氣體組成條件下的物質平衡關系,討論反應溫度和配碳量對鐵酸鋅分解行為的影響。通過固相反應法制備鐵酸鋅,進行鐵酸鋅配碳還原試驗,驗證計算結果,獲得鐵酸鋅選擇性還原和抑制還原產物過還原的條件。
3 鐵酸鋅配碳還原的熱力學研究
3.1 鐵酸鋅配碳還原過程ΔGθ的變化
鐵酸鋅配碳還原過程中固體碳是主要還原劑,可能發生的主要反應如式(1)~(5)所示。計算的各反應的標準吉布斯自由能變化(ΔGθ)隨溫度的變化關系見圖2。
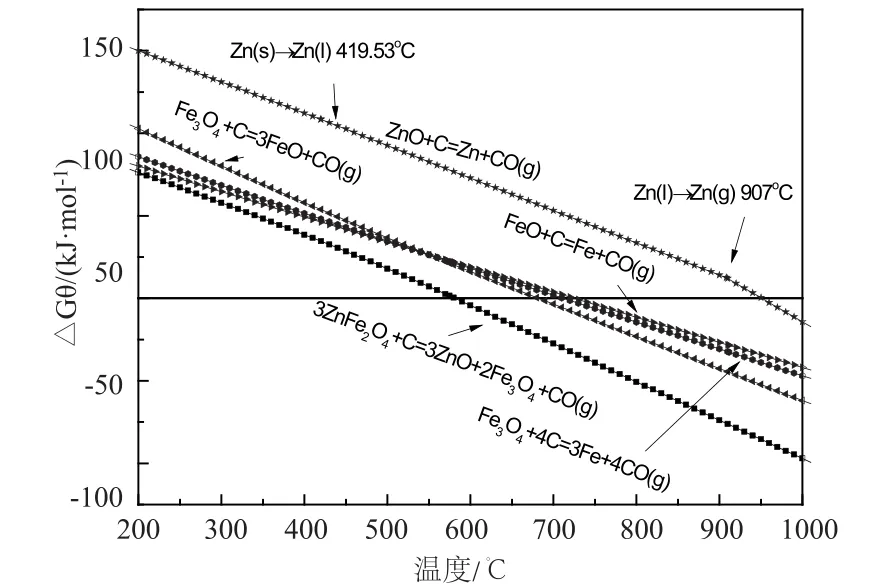
圖2 鐵酸鋅配碳還原過程的ΔGΘ隨溫度的變化關系Fig. 2 ΔGΘ changes with temperature for reduction of zinc ferrite by carbon
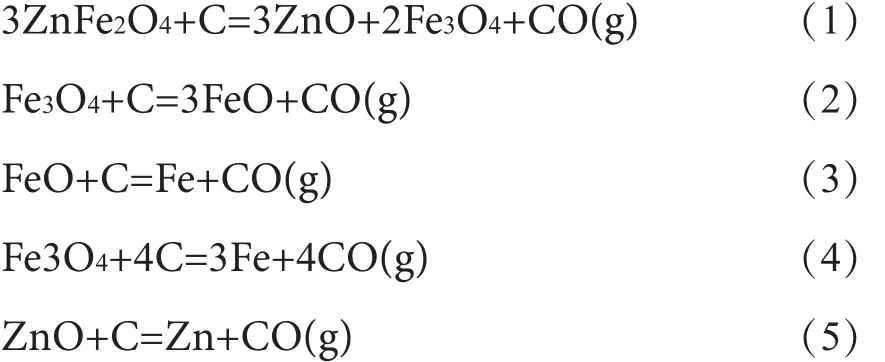
結果顯示,上述反應的ΔGθ隨著溫度的增加,呈下降趨勢,在計算溫度范圍內由正轉為負,說明固體碳可將鐵酸鋅進行還原,提高溫度可以促進反應的發生。鐵酸鋅配碳還原過程,鐵酸鋅和鐵氧化物較易被還原,還原過程遵循逐級還原規律;鐵酸鋅在582℃時被還原為Fe3O4和ZnO。隨著溫度的升高,鐵氧化物被過還原,在682℃時Fe3O4可被還原為FeO,在712℃時就可還原出金屬鐵;ZnO雖然比Fe2O3難以還原,但由于Zn的沸點較低,在標準狀態下約907℃形成鋅蒸氣[14],ZnO在941℃時被還原為鋅蒸氣。由此可見,鐵酸鋅配碳擇性還原為ZnO而抑制氧化鋅的過還原在熱力學上是可行的,合適的溫度范圍為582 ~941℃之間,溫度過低不利于鐵酸鋅的分解,溫度過高則存在氧化鋅的過還原。
3.2 鐵酸鋅配碳還原條件下的物質平衡關系
采用Factsage分析配碳還原鐵酸鋅在不同反應溫度和氣體組成條件下的物質平衡關系。計算初始條件為1 mol 鐵酸鋅,配碳量按照不同的C/O摩爾比(O為鐵酸鋅中所有的氧)添加,假定反應體系總壓為1 atm(約為101 kPa)。鐵酸鋅配碳還原過程中不同條件的計算結果見圖3、4。
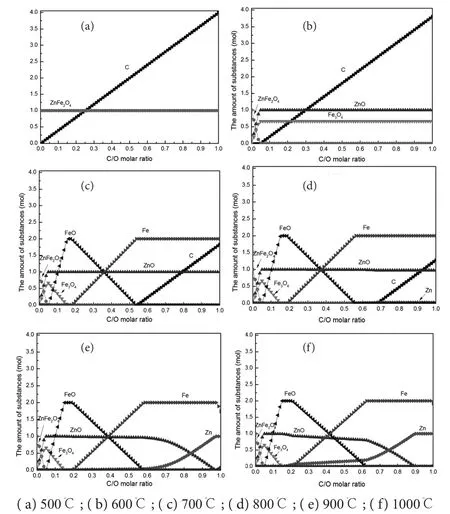
圖3 不同恒溫條件下各物質的量與配碳量的關系Fig. 3 Relationships between substances and the C/O molar ratio at different temperatures
由圖可見,當溫度為500℃時,鐵酸鋅質量保持不變,未發生還原分解,調節C/O摩爾比均不能還原鐵酸鋅。當溫度高于600℃時,鐵酸鋅能夠被還原為Fe3O4和ZnO,當C/O摩爾比超過0.04時,鐵酸鋅完全分解轉化為Fe3O4和ZnO,且提高C/O摩爾比也不會發生鐵氧化物的過還原。隨著溫度的升高,鐵酸鋅完全分解的C/O摩爾比略有降低。隨著溫度的升高,還原產物為Fe3O4、FeO和Fe,即發生鐵氧化物的過還原。在700℃時,當C/O摩爾比為0.06時,鐵酸鋅分解的Fe3O4開始被還原為FeO,當C/O摩爾比為0.18時,完全分解轉化為FeO和ZnO,同時部分的FeO被還原為Fe,當C/O摩爾比為0.54時,FeO完全轉化為Fe。隨著溫度的增加,鐵氧化過還原的C/O摩爾比也略有降低。
當溫度低于800℃時,鐵酸鋅分解的鋅以氧化鋅形式存在,生成的氧化鋅并未明顯被進一步還原為金屬鋅;800℃時,在高C/O摩爾比的情況下(C/O摩爾比>0.6),才會有少量的金屬鋅(0.01 mol~0.02 mol)產生;隨著溫度繼續升高,鋅完全還原所需要的C/O摩爾比逐漸減少;當溫度為900℃時,在低C/O比例的情況下就會產生金屬鋅,隨著C/O摩爾比的增加,更多的氧化鋅轉化為金屬鋅,當C/O摩爾比超過0.97時,體系中的鋅將完全轉化為金屬鋅;1000℃時,當C/O摩爾比超過0.89時,體系中的鋅將完全轉化為鋅蒸氣。
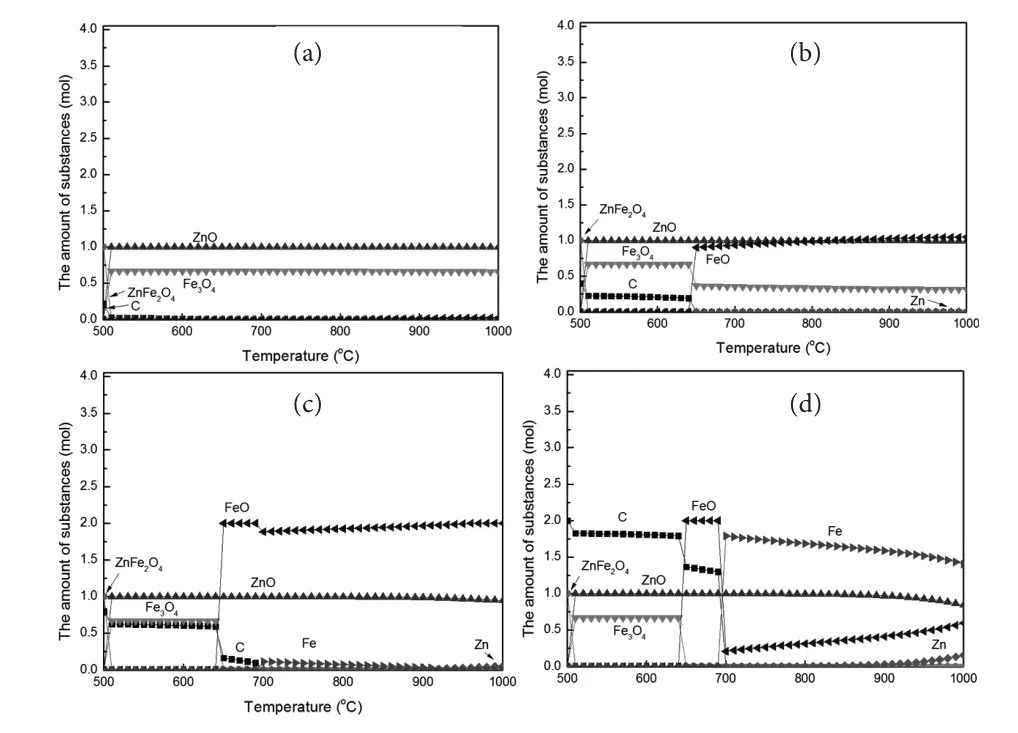
圖4為恒定C/O摩爾比條件下各物質的量與反應溫度的關系(C/O摩爾比分別為0.05、0.10、0.20、0.50、0.80和1.00)。結果表明,當C/O摩爾比為0.05時,鐵酸鋅在溫度超過500℃時被碳還原為Fe3O4和ZnO,隨著溫度的增加,還原產物并未發生改變;當C/O摩爾比為0.10時,鐵酸鋅首先被還原為Fe3O4和ZnO,過量的碳在650℃左右將部分Fe3O4進一步還原為FeO。隨著C/O摩爾比的增加,過量的碳將Fe3O4還原為FeO,同時部分的FeO在700℃左右被進一步還原為Fe。當C/O摩爾比為0.80時,過量的碳將FeO還原為Fe。
當C/O摩爾比小于0.50時,鐵酸鋅中分解的鋅以ZnO形式存在,生成的ZnO并未明顯被還原為金屬鋅,只發生了鐵氧化物的逐級還原;當C/O摩爾比超過0.50時,隨著溫度的增加,部分鐵酸鋅分解的ZnO在高溫條件下還原為金屬鋅,當溫度為850℃時,還原產物中會有少量的金屬鋅(0.02 mol),當溫度超過850℃時,還原產物中出現明顯的金屬鋅(0.15 mol);當C/O摩爾比為1.00時,體系中的鋅在900℃左右將完全轉化為金屬鋅。
計算結果中碳含量的變化體現碳還原的歷程,如C/O摩爾比為1.00時,隨著溫度的升高,體現中碳含量逐漸減少,出現4個明顯的降低階段,分別對應著鐵酸鋅還原為Fe3O4和ZnO、Fe3O4還原為FeO、FeO還原為Fe、以及ZnO還原為Zn,每個階段反映出各個還原過程中消耗的碳含量,即控制反應歷程所需要的配碳量。
綜上所述,為了抑制氧化鋅的過還原,必須保持適宜的C/O摩爾比和溫度條件,控制C/O摩爾比0.6以下,溫度低于900℃時,還原產物中會有少量的金屬鋅(0.04 mol)出現,鐵酸鋅分解的鋅主要以氧化鋅的形式存在,生成的氧化鋅并未明顯被進一步還原為金屬鋅,滿足后續處理過程對鋅存在形式的要求,從而實現鐵酸鋅的有效分解、ZnO過還原的抑制。
4 鐵酸鋅配碳選擇性還原試驗
4.1 鐵酸鋅配碳選擇性還原
結果顯示,在650℃時,產物中出現Fe3O4和ZnO衍射峰,鐵酸鋅還原分解為Fe3O4和ZnO,由于鐵酸鋅和Fe3O4均為尖晶石結構,故圖譜中有衍射峰的重疊。在800℃時,產物中出現明顯的FeO和ZnO衍射峰,還存在少量的Fe衍射峰,鐵酸鋅和Fe3O4衍射峰不明顯,鐵酸鋅分解出的Fe3O4進一步還原為FeO,少量的FeO被還原為Fe。在950℃時,產物中存在較為明顯的中FeO和ZnO衍射峰,但ZnO衍射峰明顯被800℃產物中ZnO衍射峰弱,還存在Zn和Fe衍射峰,鐵酸鋅分解出的Fe3O4進一步還原為FeO,同時FeO部分被還原分解Fe,ZnO部分被還原為Zn。雖然Zn的沸點為907℃,部分ZnO被還原為鋅蒸氣而揮發,但仍有少量的鋅殘留在粉末顆粒中;不同溫度下的產物中均存在碳的衍射峰,產物中還有過量的碳存在。由此可見,XRD分析的試驗結果與上述熱力學計算結果基本一致。
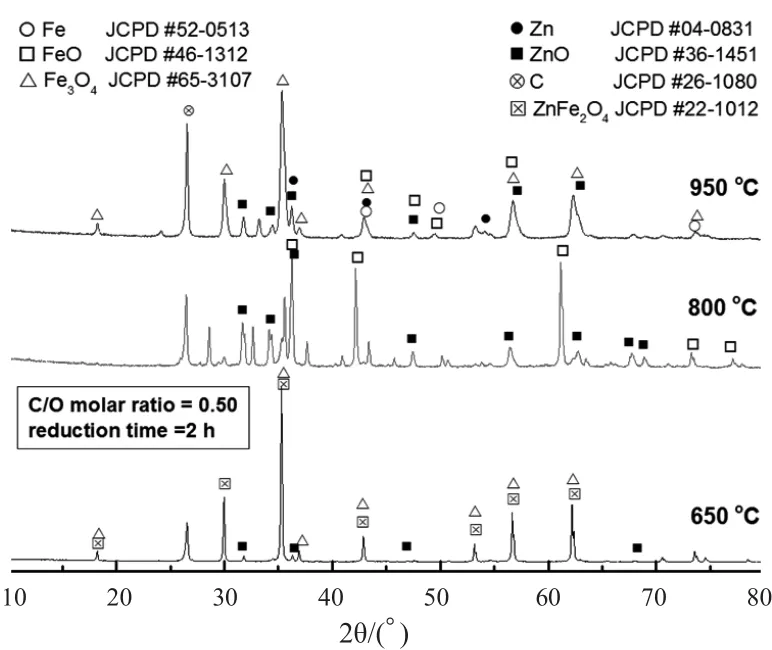
圖5 不同溫度下鐵酸鋅配碳還原的XRDFig. 5 XRD pattern of reduction of zinc ferrite with carbon at different temperatures
4.2 還原過程中鋅的揮發
Zn的沸點為907℃,部分ZnO被還原為鋅蒸氣而揮發,將導致產物中鋅含量降低,為研究反應產物中鋅含量隨反應溫度的變化,對還原產物中鋅含量進行了測量,結果見圖6。

圖6 鐵酸鋅配碳還原過程中鋅含量變化Fig .6 The Zn content of reduction of zinc ferrite with carbon
結果表明,當溫度為650℃和800℃時,隨著反應溫度的增加,產物中的鋅含量略有下降;在950℃時,由于ZnO被還原為鋅蒸氣而揮發,產物中鋅含量明顯降低。
5 結 論
(1)鐵酸鋅配碳選擇性還原熱力學計算結果表明,鐵酸鋅配碳擇性還原為ZnO而抑制氧化鋅的過還原在熱力學上是可行的。
(2)鐵酸鋅配碳還原過程遵循逐級還原規律,控制C/O摩爾比0.6以下,溫度低于900℃時,可實現鐵酸鋅的有效分解、ZnO過還原的抑制,有利于后續鐵鋅資源的有效分離。
(3)采用固相反應法合成了結晶度好、純度較高的鐵酸鋅;650℃時,鐵酸鋅配碳還原分解為Fe3O4和ZnO,隨著溫度的升高,鐵氧化物的逐級還原為Fe3O4、FeO和Fe,ZnO被還原為Zn。試驗結果與熱力學計算結果基本一致。

