基于Calpain-ERK信號通路研究Calpeptin對雌激素誘導人乳腺上皮細胞MCF-10A轉化及干性標志物表達的影響
張艷 王旭東 金愛 何艷 詹云惠 沈敬堃 董宇華 宛蕾
摘 要 目的:研究鈣激活中性蛋白酶(Calpain)抑制劑Calpeptin對雌二醇(E2)誘導人乳腺上皮細胞MCF-10A轉化及干性標志物表達的影響,并探討其作用機制。方法:以人乳腺上皮細胞MCF-10A為研究對象,采用E2誘導制備轉化細胞模型。將細胞分為對照組[0.1%二甲基亞砜(DMSO)]、E2轉化組(50 nmol/L)、E2轉化+Calpeptin組(50 nmol/L E2+1 μmol/L Calpeptin),以相應含藥培養基連續培養15代。然后采用MTT法檢測細胞的增殖率(24、48 h),采用平板克隆試驗檢測細胞的克隆形成率,采用懸浮成球試驗檢測細胞的成球數;采用實時熒光定量-聚合酶鏈式反應法檢測細胞中干性標志物(CD44、Nanog、OCT4)和細胞外信號調節激酶(ERK)mRNA表達水平,并采用Western blotting法檢測細胞中CD44、Nanog、OCT4、ERK和磷酸化ERK(p-ERK)蛋白表達水平。另取E2轉化細胞分為對照組(0.1%DMSO)和U0126(ERK抑制劑)組(10 μmol/L),按上述方法測定細胞的克隆形成率、成球數以及細胞中CD44、Nanog、OCT4、p-ERK蛋白表達水平,以驗證ERK表達抑制與轉化細胞生物學行為及干性標志物表達之間的關系。結果:與對照組比較,E2轉化組細胞的增殖率(24、48 h)、克隆形成率均顯著升高(P<0.01),細胞成球數均顯著增加(P<0.01),細胞中CD44、Nanog、OCT4、p-ERK mRNA表達水平及CD44、Nanog、OCT4、p-ERK蛋白表達水平均顯著升高(P<0.01)。與E2轉化組比較,E2轉化+Calpeptin組細胞的增殖率(24、48 h)、克隆形成率均顯著降低(P<0.01),細胞成球數顯著減少(P<0.05),細胞中CD44、Nanog、OCT4、ERK mRNA表達水平及CD44、Nanog、OCT4、p-ERK蛋白表達水平均顯著降低(P<0.05或P<0.01)。加入ERK抑制劑U0126后,E2轉化細胞的克隆形成率、成球數以及細胞中p-ERK、CD44、Nanog、OCT4蛋白表達水平均顯著增加或升高(P<0.05或P<0.01)。結論:Calpeptin可抑制E2誘導的人乳腺上皮細胞MCF-10A轉化及干性標志物表達,其機制可能與抑制Calpain-ERK信號通路的激活有關。
關鍵詞 Calpeptin;雌二醇;人乳腺上皮細胞MCF-10A;細胞轉化;干性標志物;細胞外信號調節激酶;機制
ABSTRACT? ?OBJECTIVE: To study the effects of Calpeptin inhibitor Calpeptin on the transformation and stemness markers expression induced by estradiol (E2), and to investigate its mechanism. METHODS: Taking human mammary epithelial cells MCF-10A as research object, transformed cells were induced by E2 treatment. Cells were divided into control group(0.1%DMSO), E2-transformed group (50 nmol/L), E2-transformed+Calpeptin group (50 nmol/L E2+1 μmol/L Calpeptin), then continuously treated with corresponding drug-containing culture medium for 15 generations. Then, MTT assay was used to determine the proliferation rate of cells (24,48 h); plate colony test was used to detect the Clone formation rate of cells; the number of sphere-forming cells was measured by suspension spheroidization test;mRNA expressions of stemness marker (CD44, Nanog, OCT4) and extracellular sigal-regulated kinase (ERK) were detected by RT-qPCR,and protein expressions of CD44, Nanog, OCT4 , ERK and p-ERK were detected by Western blotting assay. Another E2-transformed cells were divided into control group (0.1%DMSO) and U0126 (ERK inhibitor) group (10 μmol/L). Clone formation rate, the number of sphere-forming, protein expressions of CD44, Nanog, OCT4,ERK and p-ERK were determined with above methods, and to validate the relationship of ERK inhibition with transformed cell behavior and the expression of stemness markers. RESULTS:Compared with control group, proliferation rate and clone formation rate of E2 transformed group were increased significantly (P<0.01), and the number of sphere-forming was increased significantly (P<0.01); mRNA expression levels of CD44, Nanog, OCT4,ERK and protein expression levels of CD44, Nanog, OCT4 and p-ERK in cells were increased significantly (P<0.01). Compared with E2-transformed group, proliferation rate (24, 48 h) and clone formation rate of E2-transformed+Calpeptin group were decreased significantly (P<0.01), and the number of sphere-forming was decreased significantly (P<0.05); mRNA expression levels of CD44, Nanog, OCT4 , ERK and protein expression levels of CD44, Nanog, OCT4, p-ERK in cells were decreased significantly (P<0.05 or P<0.01). After treated with ERK inhibitor U0126, clone formation rate of E2-transformed cells, the number of sphere-forming, protein expression levels of CD44, Nanog, OCT4 and p-ERK were increased significantly (P<0.05 or P<0.01). CONCLUSIONS: Calpeptin can inhibit the transformation and the expression of stemness markers of human mammary epithelial cells MCF-10A, and the mechanism of it may be associated with inhibiting the activation of Calpain-ERK signaling pathway.
KEYWORDS? ?Calpeptin; Estradiol; Human mammary epithelial cells MCF-10A; Cell transformation; Stemness marker; Extracellular sigal-regulated kinase; Mechanism
雌二醇(E2)是誘導乳腺癌發生的主要風險因素[1],其可通過激活雌激素受體(ER)或代謝產生有毒代謝產物,從而誘導乳腺上皮細胞轉化以及癌變發生[2-3]。相關研究顯示,乳腺腫瘤干細胞(BCSCs)在乳腺癌的發生、維持、轉移、治療抵抗和復發中起著重要作用,而E2與BCSCs的產生密切相關[4]。人乳腺上皮細胞MCF-10A是一種非致瘤性乳腺上皮細胞,正常情況下其呈不規則多邊形貼壁生長,且增殖緩慢;但經E2長期誘導后,MCF-10A細胞將失去上皮細胞相關特性,胞體變大,呈長梭形貼壁生長,增殖能力增強,且具有一定的間質特征[5]。近期有研究發現,E2能誘導人乳腺上皮細胞MCF-10A的自我更新、多潛能分化等干性特征增強,促進該細胞向BCSCs轉化[6]。
鈣激活中性蛋白酶(Calcium-activated neutral protease,縮寫為“Calpain”)是一種Ca2+依賴型半胱氨酸蛋白酶,主要成員有Calpain-1和Calpain-2,可參與調控乳腺癌細胞的多種惡性生物學行為[7-8]。Calpeptin是一種具有細胞穿透性的Calpain抑制劑,據相關研究報道,Calpeptin可通過抑制ER陽性乳腺癌細胞MCF-7中Calpain的活性,從而抑制細胞的遷移和侵襲[9]。本課題組前期研究發現,在E2誘導人乳腺上皮細胞MCF-10A轉化的過程中,通常伴隨著Calpain活性的增強[10]。而Calpain活性增強在癌癥的發生發展中具有重要作用,其參與介導了上皮細胞轉化以及癌細胞的遷移、增殖[10-12]。但有關Calpain是否介導了E2誘導的乳腺上皮細胞MCF-10A干性特征增強,尚未見文獻報道。另有研究顯示,細胞外信號調節激酶(ERK)信號通路的激活與細胞的惡性轉化密切相關[13]。但Calpeptin是否能通過ERK通路干預乳腺上皮細胞MCF-10A轉化以及干性特征增強,也同樣尚未見文獻報道。鑒于此,本研究旨在通過探討Calpain抑制劑Calpeptin對E2誘導乳腺上皮細胞MCF-10A轉化及干性標志物(CD44、OCT4、Nanog)表達的影響,并通過探究Calpain-ERK信號通路在其中的介導作用,為闡明Calpeptin抑制E2誘導乳腺癌發生的作用機制提供參考。
1 材料
1.1 儀器
ND2000型超微量紫外分光光度計、2001HY-6003型CO2細胞培養箱(美國Thermo Fisher Scientific公司);HH-W21-Cr600型電熱恒溫水溫箱、DW-86L486型立式超低溫冰箱(青島海爾特種電器有限公司);SW-CJ-2D型超凈工作臺(蘇州凈化設備有限公司);FA2204N型電子天平(上海菁海儀器有限公司);ZHWY-103D型恒溫培養振蕩器(上海智城分析儀器制造有限公司);DYY-7C型電泳儀(北京市六一儀器廠);Epoch型全波長酶標儀(美國Bio-Tek公司);CKX41型倒置顯微鏡(日本Olympus公司);TI-U-DS-RI2型倒置熒光顯微鏡(日本Nikon公司);Centrifuge 5810R型高速冷凍離心機(德國Eppendorf公司);TS-8型轉移脫色搖床、VORTEX-5型渦旋振蕩儀(海門市其林貝爾儀器制造有限公司);Step One PlusTM型實時熒光定量-聚合酶鏈式反應(PCR)儀(美國Applied Biosystems公司)。
1.2 藥品與試劑
E2標準品(批號:WXBC5362V,純度:>98%)、Calpeptin(批號:C8999,純度:>98%)、氫化可的松標準品(批號:PHR1014,純度:100%)、霍亂毒素(批號:C8052,純度:95%)均購自美國Sigma公司;U0126(ERK抑制劑,美國Med Chem Express公司,批號:HY-12031,純度:>98%);馬血清、0.25%胰蛋白酶、B-27添加物(50×)(美國Gibco公司,批號分別為:1893656、2046777、2046964);表皮生長因子( EGF,美國PeproTech公司,批號:0515AFC05);成纖維細胞生長因子(FGFB,中國近岸蛋白質科技有限公司,批號:0331504);重組人胰島素(上海翊圣生物科技有限公司,批號:11820131,含量:95%~105%);磷酸鹽緩沖液(PBS)粉末、1%結晶紫染色液、5×蛋白質上樣緩沖液、十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(SDS-PAGE)制備試劑盒、高效RIPA組織/快速裂解液、膜再生液(北京索萊寶科技有限公司,批號分別為:1022Q021、20180627、20190328、20191104、20190711、20190715);青鏈霉素、DMEM/F12培養基(美國 Hyclone 公司,批號分別為:J150038、AE28870264);二喹啉甲酸(BCA)蛋白濃度試劑盒(美國Thermo Fisher Scientific公司,批號:UD277257);MTT試劑盒(北京博奧拓科技有限公司,批號:298-93-1);Trizol試劑(美國Ambion Life Technologies公司,批號:149002);反轉錄試劑盒PrimeScriptTM RT reagent Kit、PCR反應試劑SYBR? Premix Ex TaqTM Ⅱ(日本Takara公司,批號分別為:AK6301、AIG2363A);CD44小鼠單克隆抗體、ERK兔多克隆抗體(美國Cell Signaling Technolog公司,批號分別為:3570S、4695S);Nanog、OCT4兔單克隆抗體(美國Abcam公司,批號分別為:ab109250、ab109183);磷酸化ERK(p-ERK)小鼠多克隆抗體(美國Santa Cruz公司,批號:SC-7383);α-微管蛋白(α-tubulin)兔多克隆抗體、甘油醛-3-磷酸脫氫酶(GAPDH)鼠單克隆抗體、辣根過氧化物酶標記的山羊抗兔免疫球蛋白G(IgG)二抗、辣根過氧化物酶標記的山羊抗鼠 IgG二抗(美國 Bioworld 公司,批號分別為:BS1699、MB001、BS13278、BS12478);甲醇、二甲基亞砜(DMSO)、乙醇等均為分析純,水為雙蒸水。CD44、Nanog、OCT4、ERK和GAPDH引物均由生工生物工程(上海)股份有限公司合成。
1.3 細胞
人乳腺上皮細胞MCF-10A由陸軍軍醫大學生物化學教研室饋贈。
2 方法
2.1 細胞培養
將人乳腺上皮細胞MCF-10A培養于DMEM/F12全培養基中(含有10%馬血清、10 ng/mL霍亂毒素、50? ? ng/mL氫化可的松、10 μg/mL胰島素、20 ng/mL EGF以及1%青鏈霉素,下同),在37 ℃、5%CO2的培養箱(后文條件相同)中進行培養,每48 h更換1次培養液。
2.2 細胞轉化試驗
將乳腺上皮細胞MCF-10A隨機分為對照組、E2轉化組(DMSO終體積分數為0.1%,下同)和E2轉化+Calpeptin組(DMSO終體積分數為0.1%,下同)。3組細胞分別以0.1%DMSO、E2(50 nmol/L)、E2(50 nmol/L)+Calpeptin(1 μmol/L)連續處理15代,每次傳代時均加入相應藥物處理,然后按照“2.1”項下條件進行培養,觀察細胞形態變化并拍照。細胞轉化標志:細胞形態發生變化(細胞胞體變大,胞內出現黑色顆粒,排列紊亂,呈長梭形貼壁生長,具有一定的間質細胞樣特性),生長加速,克隆形成能力增強[5]。
2.3 MTT試驗檢測細胞的增殖能力
取“2.2”項下3組對數生長期細胞,分別用0.25%胰蛋白酶消化后,以1 000 r/min離心5 min,用DMEM/F12全培養基重懸并調整各組細胞密度至4×104個/mL,然后接種于96孔板中,每孔200 μL,每組設置5個復孔。另外設置不加細胞只加培養基的調零孔。將培養板置于培養箱中培養至細胞貼壁,吸棄培養液,每孔中加入200 μL不含血清的DMEM/F12培養基,繼續培養24、48 h后,每孔中均避光加入5%MTT試液20 μL,混勻,培養3 h后,終止培養;棄去培養基,加入150 μL DMSO溶液,低速振蕩10 min。使用酶標儀于490 nm波長下測定各孔吸光度(OD),計算細胞增殖率。細胞增殖率(%)=(給藥組OD值-調零孔OD值)/(對照組OD值-調零孔OD值)×100%。試驗重復3次。
2.4 平板克隆試驗檢測細胞的克隆形成能力
取“2.2”項下3組對數生長期細胞,分別按400個/孔接種于6孔板中,每組設置3個復孔。每孔中加入4 mL DMEM/F12全培養基,于培養箱中培養14 d;棄去培養液,以PBS洗滌3次,加入4%多聚甲醛溶液固定30 min;以0.1%結晶紫染色30 min后,洗去染色液,常溫晾干。用相機拍照并觀察其克隆集落形成情況,使用Image J 1.8.0軟件對克隆集落進行計數,并計算其克隆形成率。克隆形成率(%)=(克隆集落形成數/接種細胞總數)×100%。試驗重復3次。
2.5 懸浮成球試驗檢測細胞的自我更新能力
取“2.2”項下3組處于對數生長期細胞,分別按? ? ? ?5 000個/孔接種于24孔超低黏附板中,每組設置3個復孔。每孔中加入2 mL懸浮成球試驗培養基(含5 μg/mL胰島素、2%B-27添加物、20 ng/mL EGF、20 ng/mL FGFB、1 μg/mL氫化可的松和1%青鏈霉素的DMEM/F12培養基),在培養箱中培養10 d后,于顯微鏡下拍照并對每組的成球情況進行計數。試驗重復3次。
2.6 實時熒光定量-PCR試驗檢測細胞中CD44、Nanog、OCT4、ERK mRNA的表達情況
取“2.2”項下3組對數生長期細胞,分別按2×105個/孔接種于6孔板中,每組設置2個復孔。待細胞貼壁后,以DMEM/F12培養基(不含血清)于培養箱中培養48 h。按照Trizol說明書方法操作,分離提取細胞中的總RNA,用超微量分光光度計測定各組RNA濃度。使用PrimeScriptTM RT reagent Kit試劑盒并按說明書方法操作,將1 μg總RNA逆轉錄為cDNA,并以cDNA為模板進行PCR擴增。反應體系:cDNA模板2 μL,上、下游引物各0.8 μL,SYBR? Premix Ex TaqTM Ⅱ 10.4 μL、無酶水6 μL,總體系為20 μL。反應條件:95 ℃預變性30 s;95 ℃變性3 s,60 ℃退火30 s,72 ℃延伸30 s,共40個循環。以GAPDH為內參,采用2-ΔΔct法計算CD44、Nanog、OCT4和ERK mRNA的表達水平(其中ct表示每個反應管內的熒光信號達到設定閾值時所經歷的循環次數)。試驗重復3次。引物序列及擴增產物長度見表1。
2.7 Western bloting試驗檢測細胞中CD44、Nanog、OCT4、ERK和p-ERK蛋白的表達情況
取“2.2”項下3組對數生長期細胞,分別按“2.6”項下方法進行細胞接種、培養,然后以RIPA蛋白裂解液提取總蛋白,再以BCA法進行蛋白定量后進行制樣。蛋白樣品在80 V電壓下電泳30 min后,調節電壓至120 V繼續電泳1 h;然后以電流300 mA轉膜[聚偏氟乙烯(PVDF)膜]1.5 h,以5%脫脂奶粉室溫封閉1 h;分別加入稀釋比例均為1 ∶ 1 000的CD44、Nanog、OCT4、ERK、p-ERK一抗和稀釋比例為1 ∶ 10 000的GAPDH一抗,4 ℃下孵育過夜;以1×TBST溶液洗膜3次,每次10 min;加入相應二抗(稀釋比例均為1 ∶ 10 000),室溫下孵育1 h;以1×TBST溶液洗膜3次,每次10 min,再用ECL發光試劑盒顯色。以凝膠成像系統成像,并用Image J 1.8.0軟件分析,以目的蛋白條帶灰度值與內參GAPDH蛋白條帶灰度值的比值表示目的蛋白的表達水平。試驗重復3次。
2.8 U0126抑制ERK蛋白表達后對E2轉化細胞克隆形成能力、自我更新能力以及干性標志物表達的影響
取對數生長期的E2轉化細胞,隨機分為對照組(含0.1%DMSO)和U0126(ERK抑制劑)組(10 μmol/L)。分別按“2.4”項下方法檢測細胞的克隆形成能力,按“2.5”項下方法檢測細胞自我更新能力,按“2.7”項下方法檢測細胞中CD44、Nanog、OCT4和p-ERK蛋白的表達情況(以α-tubulin為內參,稀釋比例為1 ∶ 10 000)。試驗均重復3次。
2.9 統計學方法
采用SPSS 11.5軟件對數據進行統計處理和分析。數據以x±s表示。多組間比較采用單因素方差分析,兩獨立樣本組間比較采用t檢驗。P<0.05表示差異具有統計學意義。
3 結果
3.1 Calpeptin對E2轉化細胞形態學特征的影響
細胞形態學觀察發現,與對照組比較,E2轉化組細胞形態發生了明顯變化,細胞呈長梭形貼壁生長,細胞體積變大,具有一定的間質細胞樣特征;E2轉化+Calpeptin組細胞形態與對照組接近。各組細胞形態學特征顯微圖見圖1。
3.2 Calpeptin對E2轉化細胞增殖能力的影響
培養24、48 h后,與對照組比較,E2轉化組細胞的增殖率均顯著升高(P<0.01);與E2轉化組比較,E2轉化+Calpeptin組細胞的增殖率均顯著降低(P<0.01)。各組細胞增殖率測定結果見表2。
3.3 Calpeptin對E2轉化細胞克隆形成能力的影響
與對照組比較,E2轉化組細胞的克隆形成率顯著升高(P<0.01);與E2轉化組比較,E2轉化+Calpeptin組細胞的克隆形成率顯著降低(P<0.01)。各組細胞克隆形成情況平板圖見圖2,克隆形成率測定結果見表3。
3.4 Calpeptin對E2轉化細胞自我更新能力的影響
與對照組比較,E2轉化組細胞的成球數顯著增加(P<0.01);與E2轉化組比較,E2轉化+Calpeptin組細胞的成球數顯著減少(P<0.05)。各組細胞成球情況顯微圖見圖3,成球數測定結果表4。
3.5 Calpeptin對E2轉化細胞中CD44、Nanog、OCT4、ERK mRNA表達的影響
與對照組比較,E2轉化組細胞中CD44、Nanog、OCT4、ERK mRNA的表達水平均顯著升高(P<0.01);與E2轉化組比較,E2轉化+Calpeptin組細胞中CD44、Nanog、OCT4、ERK mRNA的表達水平均顯著降低(P<0.05或P<0.01)。各組細胞中4種標志物mRNA表達水平測定結果見表5。
3.6 Calpeptin對E2轉化細胞中CD44、Nanog、OCT4、ERK和p-ERK蛋白表達的影響
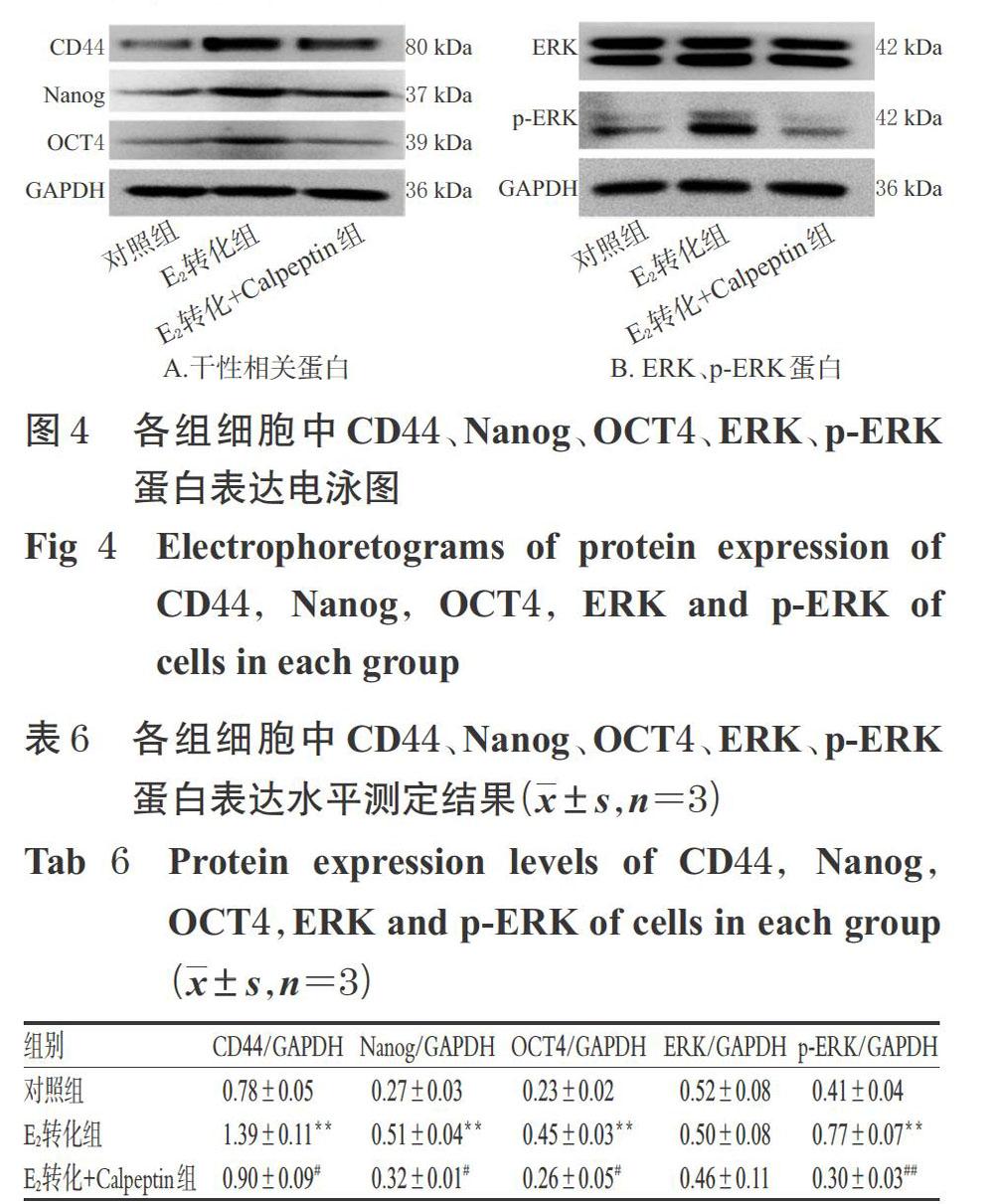
與對照組比較,E2轉化組細胞中CD44、Nanog、OCT4和p-ERK蛋白的表達水平均顯著升高(P<0.01);與E2轉化組比較,E2轉化+Calpeptin組細胞中CD44、Nanog、OCT4、p-ERK蛋白的表達水平均顯著降低(P<0.05或P<0.01);3組細胞中ERK蛋白表達水平間比較,差異均無統計學意義(P>0.05)。各組細胞中CD44、Nanog、OCT4、ERK、p-ERK蛋白表達電泳圖見圖4,蛋白表達水平測定結果見表6。
3.7 ERK表達被抑制后對E2轉化細胞的克隆形成能力、自我更新能力以及干性相關蛋白表達的影響
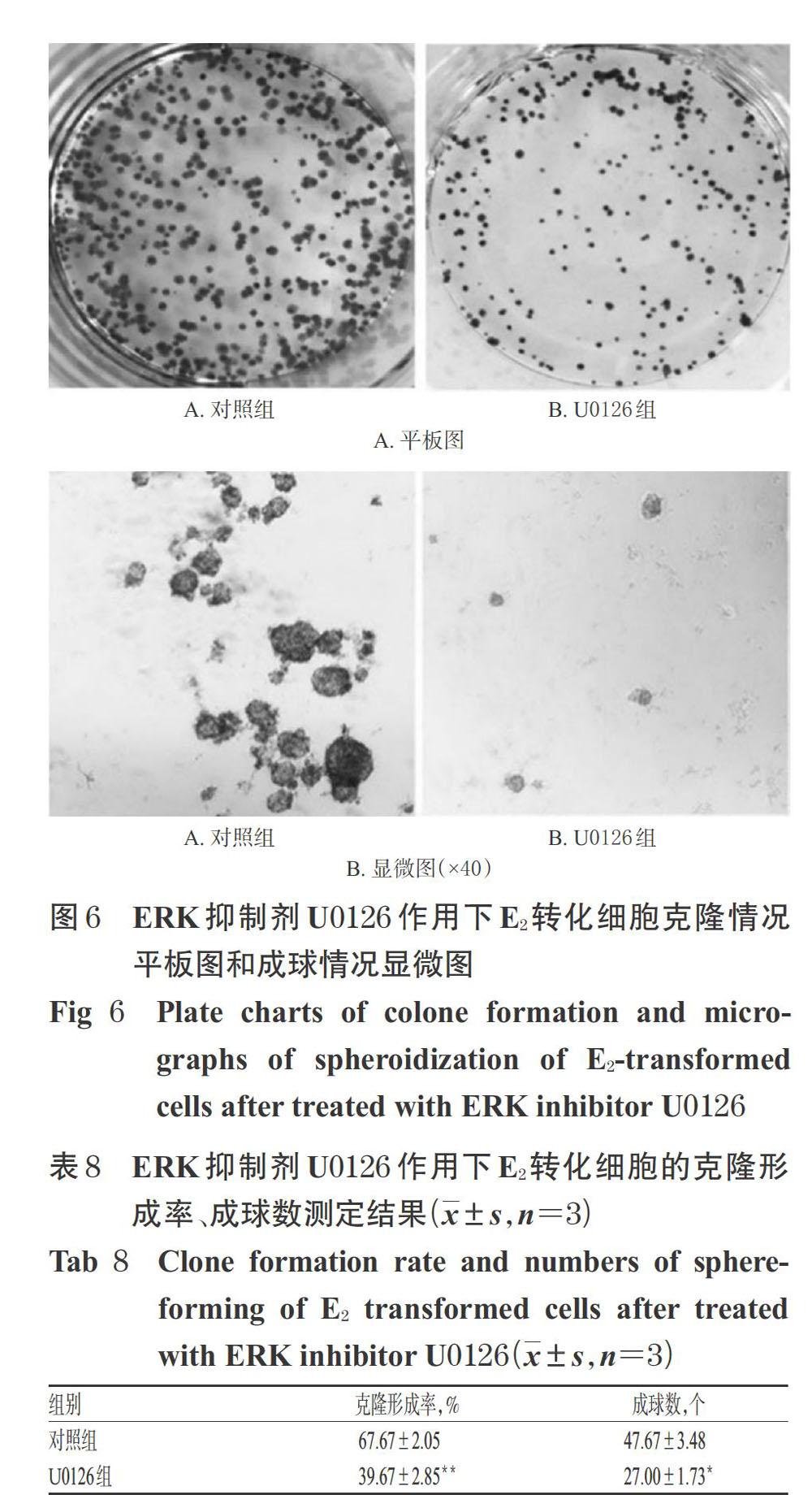
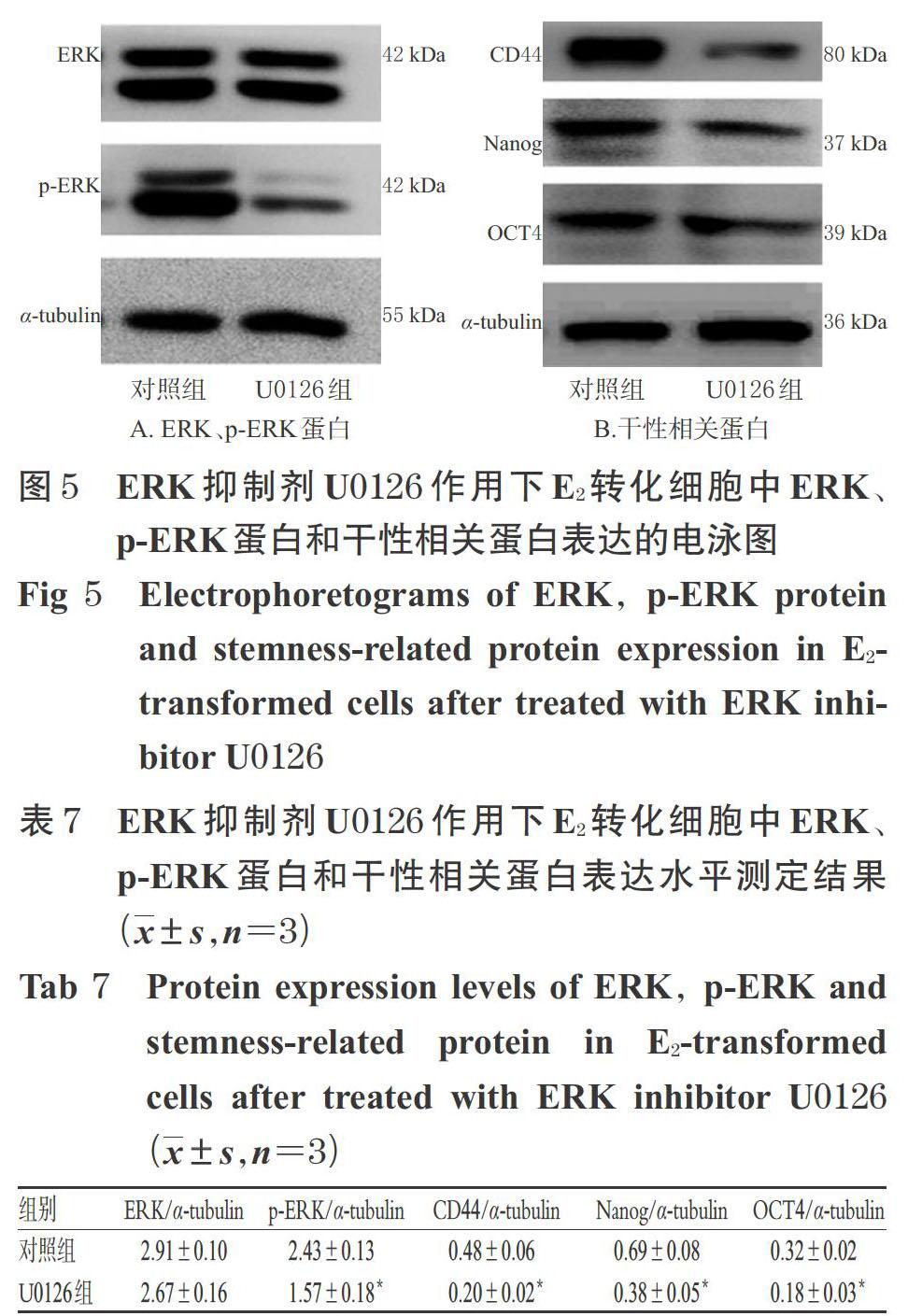
與對照組比較,U0126組中p-ERK蛋白表達水平顯著降低(P<0.05),表明ERK蛋白表達被抑制;細胞的克隆形成率顯著降低(P<0.01),成球數顯著減少(P<0.05),干性相關蛋白(CD44、Nanog、OCT4)的表達水平也顯著降低(P<0.05)。這提示抑制ERK表達后,E2轉化細胞的克隆形成能力、自我更新能力以及干性相關蛋白的表達均減弱。ERK抑制劑U0126作用下各組細胞中ERK、p-ERK蛋白和干性相關蛋白表達測定結果見圖5、表7,細胞克隆形成和細胞成球情況測定結果見圖6、表8。
4 討論
乳腺上皮細胞發生轉化是乳腺癌發生的必要過程。腫瘤干細胞是細胞內具有自我更新、多潛能分化和腫瘤特殊生物學行為的一類細胞亞群,與癌癥的發生發展密切相關[14]。近期有研究顯示,E2可以促進乳腺上皮細胞MCF-10A獲得干細胞特性[6]。CD44、Nanog和OCT4均是公認的癌癥干細胞標志物。據報道,CD44可通過與細胞外基質成分、生長因子和細胞因子相互作用來促進腫瘤的發生[15]。而Nanog和OCT4在多種癌癥干細胞中都呈異常高表達狀態,其高表達后能夠促進細胞的重新編程,從而調控腫瘤細胞增殖、自我更新和多能性分化等干細胞特征[16-17]。本研究采用E2連續培養乳腺上皮細胞MCF-10A 15代,發現E2處理后細胞出現了一定的間質細胞樣特征,細胞活力、克隆形成能力以及自我更新能力均顯著增強,這表明細胞在E2作用下發生了轉化。同時,E2轉化細胞中干性標志物CD44、Nanog、OCT4 mRNA及其蛋白的表達均顯著上調,這提示E2不僅可誘導細胞轉化,還可增強轉化細胞的干性特征。
Calpain的生物學活性與腫瘤的發生有關,其可通過修飾性剪切多種腫瘤抑制蛋白,促進上皮細胞的轉化[18-19]。Calpain抑制劑Calpeptin是一種具有細胞滲透性的特異性抑制劑。據相關文獻報道,Calpeptin在1~10 μmol/L濃度范圍內能顯著抑制E2誘導的人乳腺癌細胞MCF-7的增殖[20]。本課題組前期研究也發現,10? ? ? ? μmol/L Calpeptin能顯著抑制E2誘導的MCF-10A轉化細胞的增殖[21]。故在本次研究的預試驗中,筆者先是以1、5、10 μmol/L Calpeptin聯合E2連續處理細胞MCF-10A 15代。結果發現,在5、10 μmol/L Calpeptin的作用下細胞逐漸凋亡,只有在1 μmol/L濃度下細胞能夠正常生長,同時能顯著抑制E2誘導的細胞轉化。所以,在本次探討Calpeptin對E2誘導人乳腺上皮細胞MCF-10A轉化和干性特征的影響機制研究中,筆者選擇1 μmol/L為干預濃度。結果發現,該濃度下Calpeptin 可抑制E2誘導乳腺上皮細胞MCF-10A的轉化和干性特征的增強,這提示Calpain可能參與介導了E2誘導的細胞轉化和干性特征增強。
當ERK信號通路被激活時,非活性ERK被磷酸化為活化形式的p-ERK,并由細胞質轉移至細胞核內,轉錄激活核內的轉錄因子,進而促進細胞增殖、分化以及癌癥發生[22]。有研究顯示,ERK信號通路的激活與乳腺癌[23-24]、肺癌[25-26]、甲狀腺癌[27]等癌癥細胞的增殖、遷移以及干細胞特性增強相關。本研究結果顯示,E2轉化組細胞可高表達ERK mRNA和p-ERK蛋白,但E2轉化+Calpeptin組細胞ERK mRNA和p-ERK蛋白的表達明顯下調,這提示Calpeptin抑制E2誘導的細胞轉化以及干性標志物表達的作用可能與抑制ERK信號通路的激活有關。為了驗證以上結論,筆者進一步以ERK特異性抑制劑U0126處理E2轉化細胞。結果發現,經U0126處理后,細胞的增殖能力和自我更新能力均顯著減弱,干性相關蛋白的表達也顯著下調,這進一步說明ERK信號通路可能參與介導了E2誘導乳腺上皮細胞MCF-10A轉化及其干性增強。有文獻報道,E2可通過激活Calpain-ERK信號通路促進ER陽性乳腺癌細胞的增殖[28]。但本研究發現,Calpain抑制劑Calpeptin在抑制E2誘導細胞轉化的同時,能顯著下調E2誘導的p-ERK蛋白的表達。由此推測,細胞內可能存在Calpain-ERK的正反饋環路,后者在E2作用下被激活,促進Calpain活性增強,從而參與誘導細胞轉化及其干性增強;而當Calpain活性被抑制時,可能反饋性調節ERK的磷酸化作用,抑制了ERK的磷酸化,從而抑制細胞轉化以及干性增強。
綜上所述,Calpeptin能抑制E2誘導的人乳腺上皮細胞MCF-10A轉化及干性標志物的表達,其機制可能與抑制Calpain-ERK信號通路的激活有關,但其具體作用靶點和機制有待后續研究進一步確證。
參考文獻
[ 1 ] WEN C,WU L,FU L,et al. Unifying mechanism in the initiation of breast cancer by metabolism of estrogen:review[J]. Mol Med Rep,2017,16(2):1001-1006.
[ 2 ] CHEN JQ,RUSSO PA,COOKE C,et al. ERβ shifts from mitochondria to nucleus during estrogen-induced neoplastic transformation of human breast epithelial cells and is involved in estrogen-induced synthesis of mitochondrial respiratory chain proteins[J]. Biochim Biophys Acta,2007,1773(12):1732-1746.
[ 3 ] SAMAVAT H,KURZAR MS. Estrogen metabolism and breast cancer[J]. Cancer Lett,2015,356(200):231-243.
[ 4 ] VOUTSADAKIS IA. HER2 in stemness and epithelial- mesenchymal plasticity of breast cancer[J]. Clin Transl Oncol,2019,21(5):539-555.
[ 5 ] 楊莉,李陽,朱筑霞,等. FAK在雌激素誘導MCF-10A乳腺上皮細胞轉化中的表達及其意義[J].重慶醫學,2013,42(20):2376-2377.
[ 6 ] DAS JK,FELTY Q,POPPITI R,et al. Nuclear respiratory factor 1 acting as an oncoprotein drives estrogen-induced breast carcinogenesis[J]. Cells,2018,7(12):234-256.
[ 7 ] HOSKIN V,SZETO A,GHAFFARI A,et al. Ezrin regulates focal adhesion and invadopodia dynamics by altering calpain activity to promote breast cancer cell invasion[J]. Mol Biol Cell,2015,26(19):3464-3479.
[ 8 ] STORR SJ,THOMPSON N,PU X,et al. Calpain in breast cancer:role in disease progression and treatment respone[J]. Pathobiology,2015,82(3/4):133-141.
[ 9 ] LI CL,YANG D,CAO X,et al. Fibronectin induces epithelial-mesenchymal transition in human breast cancer MCF-7 cells via activation of calpain[J]. Oncol Lett,2017,13(5):3889-3895.
[10] 楊莉,朱筑霞,劉曉紅,等.鈣蛋白酶在乳腺上皮轉化細胞對雌激素刺激反應中的作用[J].基礎醫學與臨床,2013,33(7):819-823.
[11] CARRAGHER NO,FONSECA BD,FRAME MC. Calpain activity is generally elevated during transformation but has oncogene-specific biological function[J]. Neoplasia,2004,6(1):53-73.
[12] XU F,GU J,LU C,et al. Calpain-2 enhances non-small cell lung cancer progression and chemoresistance to paclitaxel via EGFR-pAKT pathway[J]. Int J Biol Sci,2019,15(1):127-137.
[13] MENG J,ZHOU X,YANG J,et al. Exposure to low dose ZnO nanoparticles induces hyperproliferation and malignant transformation through activating the CXCR2/NF- KappaB/STAT3/ERK and AKT pathways in colonic mucosal cells[J]. Environ Pollut,2020,263(PtB):114578- 114589.
[14] ASADZADEH Z,MANSOORI B,MOHAMMADI A,? ?et al. microRNAs in cancer stem cells:biology,pathways,and therapeutic opportunities[J]. J Cell Physiol,2019,234(7):10002-10017.
[15] MORATH I,HARTMAN TN,ORIAN-ROUSSEAU V. CD44:more than a mere stem cell marker[J]. Int J Biochem Cell Biol,2016,81(Pt A):166-173.
[16] ZHANG W,SUI Y,NI J,et al. Insights into the Nanog gene:a propeller for stemness in primitive stem cells [J]. Int J Biol Sci,2016,12(11):1372-1381.
[17] TSAI PH,CHIEN Y,WANG ML,et al. Ash21 interacts with Oct4-stemness circuity to promote super-enhancer- driver pluripotency network[J]. Nucleic Acids Res,2019,47(19):10115-10133.
[18] KIMURA Y,SAYA H,NAKAO M. Calpain-dependent proteolysis of NF2 protein:involvement in schwannomas and meningiomas[J]. Neuropathology,2000,20(3):153- 160.
[19] SALIMI R,BANDARU S,DEVARAKONDA S,et al.Blocking the cleavage of filamin A by Calpain inhibitor decreases tumor cell growth[J]. Anticancer Res,2018,38(4):2079-2085.
[20] 王旭東,丁姍姍,陳騰祥,等.鈣激活中性蛋白酶抑制劑對E2誘導的乳腺癌細胞增殖效應的影響及其意義[J].貴州醫藥,2009,33(4):302-304.
[21] 郭陽,金愛,楊莉,等.鈣蛋白酶2介導雌激素調控乳腺腫瘤細胞GREB1基因表達[J].貴州醫科大學學報,2018,43(6):630-635.
[22] RODRIGUEZ-AGUAYO C,BAYRAKTAR E,IVAN C,et al. PTGER3 induces ovary tumorigenesis and confers resistance to cisplatin therapy through up-regulation Ras- MAPK/Erk-ETS1-ELK1/CFTR1 axis[J]. EBioMedicine,2019. DOI:10.1016/j.ebiom.2018.11.045.
[23] TANG T,ZHU Q,LI X,et al. Protease NexinⅠis a feedback regulator of EGF/PKC/MAPK/EGFR1 signaling in breast cancer cells metastasis and stemness[J]. Cell Death Dis,2019,10(9):649-665.
[24] 田繼華,常思佳,郭海秀,等. ERK抑制劑U0126通過下調cyclin D1與survivin蛋白表達抑制乳腺癌細胞增殖[J].中國藥理學通報,2019,35(8):1061-1066.
[25] YANG YC,CHIOU PC,CHEN PC,et al. Melatonin reduced lung cancer stemness through inhibiting of PLC,ERK,P38,beta-catenin and Twist pathway[J]. Environ Toxicol,2019,34(2):203-209.
[26] 勞志云,吳東平,王志勇,等. Cathepsin B通過ERK信號通路促進肺癌細胞A549增殖和遷移[J].臨床腫瘤學雜志,2019,24(5):391-395.
[27] CHOI C,THI TT,VAN NGUT,et al. Promotion of tumor progression and cancer stemness by MUC15 in thyroid cancer via the GPCR/ERK and intergrin-FAK signaling pathways[J]. Oncogenesis,2018,7(11):85-97.
[28] WANG GS,HUANG YG,LI H,et al. ERK/CANP rapid signaling mediates 17 beta-estradiol-induced proliferation of human breast cancer cell line MCF-7 cells[J]. Int J Clin Exp Med,2014,7(1):156-162.
(收稿日期:2020-03-02 修回日期:2020-05-13)
(編輯:林 靜)

