參芪蛭龍湯聯合雷公藤多苷片對膜性腎病模型大鼠保護作用的實驗研究
薛丕良 李麗琦 劉欣欣 白茹 肖洪彬 牛雯穎


摘 要 目的:探討參芪蛭龍湯聯合雷公藤多苷片對膜性腎病(MN)模型大鼠的保護作用及可能機制。方法:采用皮下注射結合尾靜脈注射陽離子牛血清白蛋白+不完全費氏佐劑乳化液的方法復制MN大鼠模型,造模周期為6周。于造模第3周,根據24 h尿蛋白定量(UTP)和體質量將造模大鼠隨機分為模型對照組,參芪蛭龍湯低、高劑量組(4、8 g/kg,按生藥總量計),雷公藤多苷片組(9 mg/kg)以及參芪蛭龍湯低、高劑量+雷公藤多苷片組(劑量與各單藥組相同),每組10只;另取10只未造模的大鼠作為空白對照組。空白對照組大鼠灌胃等體積水,各給藥組大鼠灌胃相應藥物,每日1次,連續4周。于末次給藥前1天,檢測各組大鼠24 h UTP;于末次給藥后1 h,檢測各組大鼠血常規指標[白細胞(WBC)、紅細胞(RBC)、血小板(PLT)計數]、肝功能指標[總蛋白(TP)、白蛋白(ALB)、天冬氨酸轉氨酶(AST)、丙氨酸轉氨酶(ALT)]、血脂指標[膽固醇(TC)、三酰甘油(TG)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)]以及葡萄糖(GLU)、尿素氮(BUN)、血肌酐(Scr)含量;采用醋酸鈾-檸檬酸鉛染色法觀察大鼠腎臟超微結構;采用免疫組織化學法檢測大鼠腎組織中轉化生長因子β1(TGF-β1)、乙酰肝素酶1(HPA-1)蛋白的表達情況。結果:與空白對照組比較,模型對照組大鼠腎組織中腎小球足突廣泛融合或消失,可見微絨毛形成、基底膜重度增厚,上皮下可見大量電子致密物沉積,TGF-β1、HPA-1陽性細胞明顯增多;其24 h UTP,PLT計數,TC、TG、HDL-C含量以及TGF-β1、HPA-1陽性細胞百分比均顯著升高,RBC計數和TP、ALB含量均顯著降低(P<0.05或P<0.01)。與模型對照組比較,各給藥組上述超微結構變化均有不同程度的改善,TGF-β1、HPA-1陽性細胞均有所減少;其24 h UTP和TGF-β1陽性細胞百分比(參芪蛭龍湯低劑量組除外)、WBC計數(參芪蛭龍湯單用及聯用組除外)、PLT計數和TC含量(雷公藤多苷片組除外)、TG含量(參芪蛭龍湯低劑量單用以及與雷公藤多苷片聯用組除外)、HPA-1陽性細胞百分比均顯示降低,且參芪蛭龍湯高劑量+雷公藤多苷片組TGF-β1陽性細胞百分比以及參芪蛭龍湯低、高劑量+雷公藤多苷片組HPA-1陽性細胞百分比均顯著低于雷公藤多苷片組;RBC計數和GLU含量(參芪蛭龍湯低劑量組和雷公藤多苷片組除外)、TP和ALB含量(參芪蛭龍湯低劑量組除外)均顯著升高,且參芪蛭龍湯高劑量+雷公藤多苷片組GLU含量顯著高于雷公藤多苷片組(P<0.05或P<0.01)。結論:參芪蛭龍湯與雷公藤多苷片聯用可緩解雷公藤多苷片的骨髓抑制作用,減少MN模型大鼠蛋白尿,并改善其腎臟組織的病理損傷;上述作用可能與其下調腎臟組織中TGF-β1、HPA-1蛋白表達,降低血液中TC、TG含量有關。
關鍵詞 膜性腎病;參芪蛭龍湯;雷公藤多苷片;血常規指標;肝功能;血脂;轉化生長因子β1;乙酰肝素酶1;大鼠
ABSTRACT? ?OBJECTIVE: To investigate the protective effect and possible mechanism of Shenqi zhilong decoction (SZD) combined with Tripterygium polyglycoside tablets (TPT) on membranous nephropathy (MN) model rats. METHODS: MN rat model was established by subcutaneous and caudal vein injecting cationic bovine serum albumin+incomplete Freund adjuvant emulsion for 6 weeks. At the 3rd week of modeling, model rats were randomly divided into model control group, SZD low-dose and high-dose groups (4, 8 g/kg, by total crude drugs), TPT group (9 mg/kg), low-dose and high-dose of SZD+TPT groups (same dose as single group), with 10 rats in each group according to 24 h UTP and weight. Another 10 rats without modeling were taken as blank control group. Blank control group was given equal amount of water intragastrically, administration groups were given relevant medicine intragastrically, once a day, for consecutive 4 weeks. The? ?24 h UTP of rats were detected one day before the last administration; 1 h after the last administration, blood routine indexes (WBC, RBC, PLT), liver function indexes (TP, ALB, AST, ALT), blood lipid indexes (TC, TG, HDL-C, LDL-C), the contents of glucose (GLU), urea nitrogen (BUN) and serum creatinine (Scr) were detected in each group. Uranyl acetate-lead citrate staining was used to observe ultrastructural changes of renal tissue. Immunohistochemical method was used to detect the protein expression of TGF-β1 and HPA-1 in renal tissue. RESULTS: Compared with blank control group, in the model control group, the glomerular podocytes were widely fused or disappeared, microvilli were formed, basement membrane was heavily thickened, a large number of electron dense substance was deposited under the epithelium, TGF-β1 and HPA-1 positive cells were significantly increased; 24 h UTP, PLT, the contents of TC, TG and HDL-C, the percentage of TGF-β1 and HPA-1 positive cells were increased significantly, while RBC, the contents of TP and ALB were decreased significantly (P<0.05 or P<0.01). Compared with model control group, above ultrastructural changes of administration groups were improved to different extents, and TGF-β1 and HPA-1 positive cells were decreased. The 24 h UTP, the percentage of TGF-β1 positive cells (except for SZD low-dose group), WBC (except for SZD alone groups and combination groups), PLT and TC content (except for TPT group), TG content (except for SZD low-dose alone and its combination group), the percentage of HPA-1 positive cells were decreased significantly; the percentage of TGF-β1 positive cells in SZD high-dose+TPT group as well as the percentage of HPA-1 positive cells in SZD+TPT groups were significantly lower than TPT group. RBC and GLU content (except for SZD low-dose group and TPT group), TP and ALB content (except for SZD low-dose group) were increased significantly, while the content of GLU in SZD high-dose+TPT group was significantly higher than TPT tablets group (P<0.05 or P<0.01). CONCLUSIONS:SZD combined with TPT can relieve myelosuppression caused by TPT, reduce proteinuria of MN model rats and improve pathological damage of renal tissue in rats. Its mechanism is related to the down-regulation of protein expression of TGF-β1 and HPA-1, and the reduction of TC and TG content in the blood.
KEYWORDS? ?Membranous nephropathy; Shenqi zhilong decoction; Tripterygium polyglycoside tablets; Blood routine indexes; Liver function; Blood lipid; TGF-β1; HPA-1; Rat
膜性腎病(MN)是臨床上常見的腎小球疾病之一,多以腎病綜合征的形式起病,根據發病原因可分為原發性膜性腎病(IMN)和繼發性膜性腎病(SMN),其中IMN患者約占MN患者總數的75%[1]。研究表明,近年來MN的發生率逐年上升,可能與環境污染有關[2]。目前,MN的西醫治療以糖皮質激素聯合免疫抑制劑為主,上述療法雖有一定的療效,但伴有明顯的副作用(如股骨頭壞死、高血壓、糖尿病、嚴重感染、肝腎毒性等),且停藥后容易復發[2-3]。
參芪蛭龍湯是黑龍江省中醫藥科學院腎病科治療MN的特色醫院制劑,由黨參、黃芪、當歸、川芎等10味藥材組成,臨床使用十余年,療效較好,具有一定的新藥開發價值[3]。雷公藤(Tripterygium wilfordii Hook. f.)為衛矛科雷公藤屬木質藤本植物,具殺蟲、消炎、解毒之功效[4-5]。雷公藤多苷是從雷公藤根木質部中提取所得的化合物[6]。現代藥理研究表明,雷公藤多苷具有抑制免疫細胞活化、修復免疫復合物介導的足細胞損傷、減少蛋白尿的作用[7]。多項研究表明,以雷公藤多苷為主要成分的雷公藤多苷片具有較好的緩解蛋白尿的作用[8-10];但該藥具有骨髓抑制、肝功能損害、性腺抑制等副作用,使得其臨床應用受到了限制[5,11]。本課題組在臨床實踐中發現,參芪蛭龍湯在緩解MN患者水腫等癥狀方面的效果較好,但在降低尿蛋白方面卻起效較慢;雷公藤多苷片具有較好的降低尿蛋白作用,但存在明顯的骨髓抑制;而二藥聯合應用后,既能明顯降低MN患者尿蛋白水平,又能改善其水腫癥狀,同時雷公藤多苷片所致的骨髓抑制亦有所減輕。鑒于此,本研究通過建立MN大鼠模型,觀察參芪蛭龍湯聯合雷公藤多苷片對大鼠血常規、血糖、血脂、肝腎功能、尿蛋白、腎組織超微結構、乙酰肝素酶1(HPA-1)、轉化生長因子β1(TGF-β1)等指標的影響,探討參芪蛭龍湯對雷公藤多苷片的增效減毒作用及可能機制,旨在為臨床聯合用藥提供理論依據。
1 材料
1.1 儀器
XS-500i型全自動血液分析儀[希森美康醫用電子(上海)有限公司];7600-020型全自動生化分析儀、H-7650型透射電子顯微鏡(日本Hitachi公司);DM6B型熒光正置顯微鏡、RM2235型石蠟切片機(德國Leica公司);KQ-600DE型超聲儀(昆山市超聲儀器有限公司);H-2050R型超速冷凍離心機(湖南湘儀實驗室儀器開發有限公司)。
1.2 藥品與試劑
參芪蛭龍湯組方藥材黨參、黃芪、當歸、川芎、水蛭、地龍、僵蠶、虎杖、淫羊藿、鳳尾草的飲片均由黑龍江中醫藥大學附屬第一醫院提供,經黑龍江中醫藥大學基礎醫學院田明教授鑒定均為真品。
雷公藤多苷片(浙江得恩德制藥股份有限公司,批號:1901113B,規格:10 mg);陽離子牛血清白蛋白(C-BSA)凍干粉(美國Chondrex公司,批號:190538);不完全弗氏佐劑(美國Sigma公司,批號:SLBQ2284V);白蛋白(ALB)、總蛋白(TP)、血肌酐(Scr)、尿素氮(BUN)、葡萄糖(GLU)、膽固醇(TC)、三酰甘油(TG)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、丙氨酸轉氨酶(ALT)、天冬氨酸轉氨酶(AST)測定試劑盒(中生北控生物科技股份有限公司,批號分別為171419、171341、183531、183537、183642、182011、167651、170641、170541、182661、171351);微量總蛋白測定試劑盒[德賽診斷系統(上海)有限公司,批號:6012790];兔抗大鼠TGF-β1、HPA-1抗體(美國Affinity公司,批號分別為AF1027、AF6086);辣根過氧化物酶(HRP)標記的山羊抗兔免疫球蛋白G(IgG)二抗(美國Thermo Fisher Scientific公司,批號:31490);山羊血清、二氨基聯苯胺(DAB)顯色液、蘇木精染液、2.5%Gluta固定液(電鏡專用)(北京索萊寶科技有限公司,批號分別為20170203、20170508、20180612、20180202);檸檬酸鈉抗原修復液(北京碧云天科技有限公司,批號:20170815);磷酸鹽緩沖液(PBS,pH 7.2,美國GE Healthcare Life Sciences公司);檸檬酸鉛(海德創業北京生物科技有限公司);3%醋酸鈾(西安鼎天化工有限公司);過氧化氫、二甲苯、無水乙醇等試劑均為分析純,水為蒸餾水。
1.3 動物
清潔級Wistar大鼠,雌雄各半,體質量(228±19) g,由黑龍江中醫藥大學實驗動物中心提供,動物生產合格證號:SCXK(黑)2016-003。
2 方法
2.1 參芪蛭龍湯藥液制備
取黨參20 g、黃芪30 g、當歸15 g、川芎15 g、水蛭5 g(需研末)、地龍20 g、僵蠶15 g、虎杖15 g、淫羊藿30 g、鳳尾草15 g,加12倍量(約2 160 mL)水浸泡1 h,加熱至沸騰后,武火煎煮1 h,濾過;藥渣加10倍量水(約1 800 mL),再次武火煎煮1 h,濾過。合并兩次濾液,濃縮至0.8 g/mL(按生藥總量計),置于4 ℃冰箱中保存,備用。給藥時用水適量稀釋。
2.2 造模、分組與給藥
所有大鼠均適應性喂養3 d后,隨機分為空白對照組(10只)和造模組(60只)。參照Border法[12-13],取C-BSA凍干粉160 mg溶于PBS 30 mL中,與等體積的不完全弗氏佐劑混合后,超聲(功率:250 W,頻率:40 kHz)使其完全乳化。取上述乳化液適量,于造模組大鼠腋窩和腹股溝區域內的6個不同部位進行皮下注射,每處0.05 mL,每只注射總體積為0.3 mL。1周后,于造模組大鼠尾靜脈注射乳化液,每次16 mg/kg(以C-BSA質量計,下同),每周注射3次,隔天1次,在6周內將注射劑量逐漸增加至25 mg/kg。于造模第3周(以首次尾靜脈注射開始計算),測定大鼠24 h尿蛋白定量(UTP),若超過20 mg即為造模成功[14]。將造模成功的大鼠(共60只)按體質量和UTP隨機分為模型對照組,參芪蛭龍湯低、高劑量組(4、8 g/kg,按生藥總量計;給藥劑量參照成人臨床等效劑量的0.25、0.5倍按體表面積法換算而得),雷公藤多苷片組(9 mg/kg,給藥劑量參照成人臨床等效劑量按體表面積法換算而得)以及參芪蛭龍湯低、高劑量+雷公藤多苷片組(劑量與各單藥組相同),每組10只。空白對照組和模型對照組大鼠灌胃等體積水,各給藥組大鼠灌胃相應藥物10 mL/kg,每日1次,連續4周。
2.3 相關指標檢測
2.3.1 UTP 末次給藥前1天,留取各組大鼠的24 h尿液,采用鄰苯三酚紅比色法以全自動生化分析儀檢測大鼠24 h UTP。嚴格參照微量總蛋白測定試劑盒說明書操作。
2.3.2 血常規指標 末次給藥后1 h,各組大鼠腹腔注射5%水合氯醛溶液(0.7 mL/100 g)進行麻醉,于腹主動脈取血。血樣經乙二胺四乙酸二鉀(EDTA-K2)抗凝后,采用全自動血液分析儀檢測血漿中白細胞(WBC)、紅細胞(RBC)、血小板(PLT)計數。
2.3.3 血液生化指標 在各組大鼠麻醉后分別用枸櫞酸鈉抗凝采血管及不含抗凝劑的采血管于腹主動脈取血,血樣以3 000 r/min離心10 min,分離血漿及血清,分別采用溴甲酚綠微板法、雙縮脲比色法、直接法-選擇抑制法、甘油磷酸氧化酶-過氧化物法、直接法-表面活性劑清除法、雙抗體夾心法、丙氨酸底物法、天門冬氨酸底物法、固相夾心法、葡萄糖氧化酶法,以全自動生化分析儀測定大鼠血漿中的ALB、TP、HDL-C、TG、TC、LDL-C以及血清中BUN、ALT、AST、Scr、GLU的含量。嚴格按照相應試劑盒說明書操作。
2.3.4 大鼠腎組織超微結構改變觀察 取血后處死大鼠,取其腎皮質適量(大小約1 mm×1 mm×1 mm),于2.5% Gluta固定液中固定24 h,經乙醇梯度脫水、環氧樹脂包埋后,切片(厚度約60 nm)。將切片置于銅網上,用3%醋酸鈾-檸檬酸鉛溶液染色后,用透射電子顯微鏡觀察大鼠腎臟中腎小球足細胞等超微結構的變化情況。
2.3.5 大鼠腎組織中TGF-β1、HPA-1蛋白表達檢測 采用免疫組織化學法檢測。各組大鼠處死后取腎組織適量,經乙醇梯度脫水、二甲苯透明后,用石蠟包埋,切片(厚度約5 μm)。切片脫蠟后,用檸檬酸鈉抗原修復液修復抗原10 min,然后于室溫條件下,用3%過氧化氫溶液孵育15 min后,滴加山羊血清封閉15 min,加入相應一抗(稀釋度均為1 ∶ 200),于4 ℃孵育過夜;加入二抗(稀釋度為1 ∶ 500),于37 ℃孵育30 min;滴加DAB顯色液100 μL,顯色后以蘇木精復染,經乙醇脫水、二甲苯透明后,用中性樹膠封片。使用熒光正置顯微鏡觀察大鼠腎臟組織中TGF-β1、HPA-1蛋白的表達情況,應用Image J 1.8.0軟件分析上述蛋白陽性細胞(即胞漿呈深棕色者)占細胞總數的百分比(以下簡稱“陽性細胞百分比”)。
2.4 統計學方法
采用SPSS 16.0軟件對數據進行統計分析。計量資料均以x±s表示,多組間比較采用單因素方差分析,組間兩兩比較采用LSD-t檢驗。P<0.05為差異有統計學意義。
3 結果
3.1 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠24 h UTP的影響
與空白對照組比較,模型對照組大鼠24 h UTP顯著升高(P<0.01)。與模型對照組比較,雷公藤多苷片組、參芪蛭龍湯高劑量組、參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠24 h UTP均顯著降低(P<0.05或P<0.01)。參芪蛭龍湯低劑量組與模型對照組比較,參芪蛭龍湯低、高劑量+雷公藤多苷片組與雷公藤多苷片組比較,差異均無統計學意義(P>0.05),詳見表1。
3.2 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠血常規指標的影響
與空白對照組比較,模型對照組大鼠RBC計數顯著降低,PTL計數顯著升高(P<0.01)。與模型對照組比較,雷公藤多苷片組大鼠WBC計數和參芪蛭龍湯低、高劑量單用以及與雷公藤多苷片聯用組大鼠PLT計數均顯著降低,參芪蛭龍湯高劑量組和參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠RBC計數均顯著升高(P<0.05)。各給藥組大鼠其余指標與模型對照組比較,參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠血常規指標與雷公藤多苷片組比較,差異均無統計學意義(P>0.05),詳見表1。
3.3 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠肝功能指標的影響
與空白對照組比較,模型對照組大鼠TP、ALB含量均顯著降低(P<0.01)。與模型對照組比較,參芪蛭龍湯高劑量組、雷公藤多苷片組和參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠TP、ALB含量均顯著升高(P<0.05)。各組大鼠AST、ALT含量組間比較,參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠各肝功能指標與雷公藤多苷片組比較,差異均無統計學意義(P>0.05),詳見表2。
3.4 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠血脂指標的影響
與空白對照組比較,模型對照組大鼠TC、TG、HDL-C含量均顯著升高(P<0.05或P<0.01)。與模型對照組比較,參芪蛭龍湯低、高劑量單用以及與雷公藤多苷片聯用組大鼠TC含量,參芪蛭龍湯高劑量組、雷公藤多苷片組和參芪蛭龍湯高劑量+雷公藤多苷片組大鼠TG含量均顯著降低(P<0.05或P<0.01)。其余各給藥組TC、TG含量以及各給藥組HDL-C、LDL-C含量與模型對照組比較,參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠各血脂指標與雷公藤多苷片組比較,差異均無統計學意義(P>0.05),詳見表3。
3.5 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠GLU、BUN、Scr含量的影響
與空白對照組比較,模型對照組大鼠GLU、BUN、Scr含量均無顯著變化(P>0.05)。與模型對照組比較,參芪蛭龍湯高劑量組、參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠GLU含量均顯著升高,且參芪蛭龍湯高劑量+雷公藤多苷片組顯著高于雷公藤多苷片組(P<0.05或P<0.01)。各給藥組BUN、Scr含量與模型對照組比較,參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠BUN、Scr含量與雷公藤多苷片組比較,差異均無統計學意義(P>0.05),詳見表4。
3.6 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠腎臟超微結構的影響
空白組對照大鼠腎臟組織中腎小球足細胞結構清晰、足突無融合,基底膜均勻、無增厚、上皮下無電子致密物形成;模型對照組大鼠腎臟組織中腎小球足突廣泛融合或消失,并可見微絨毛形成、基底膜彌散性重度增厚,上皮下可見大量電子致密物沉積;參芪蛭龍湯低劑量組大鼠腎臟組織中腎小球足突廣泛融合,基底膜彌散性中度增厚,多數可見電子致密物沉積;參芪蛭龍湯高劑量組大鼠腎臟組織中腎小球足突彌散融合,基底膜部分增厚,電子致密物沉積明顯減少;雷公藤多苷片組大鼠腎臟組織中腎小球足突節段融合,基底膜彌散性輕度增厚,可見少量電子致密物沉積;參芪蛭龍湯低劑量+雷公藤多苷片組大鼠腎臟組織中腎小球足突節段融合、基底膜彌散性輕度增厚,偶見電子致密物沉積;參芪蛭龍湯高劑量+雷公藤多苷片組大鼠腎臟組織中腎小球足突少量融合,基底膜節段輕度增厚,未見電子致密物沉積,詳見圖1(圖中,細箭頭表示腎小球足細胞上的足突,粗箭頭表示上皮下沉積的電子致密物)。
3.7 參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠腎組織中TGF-β1、HPA-1蛋白表達影響
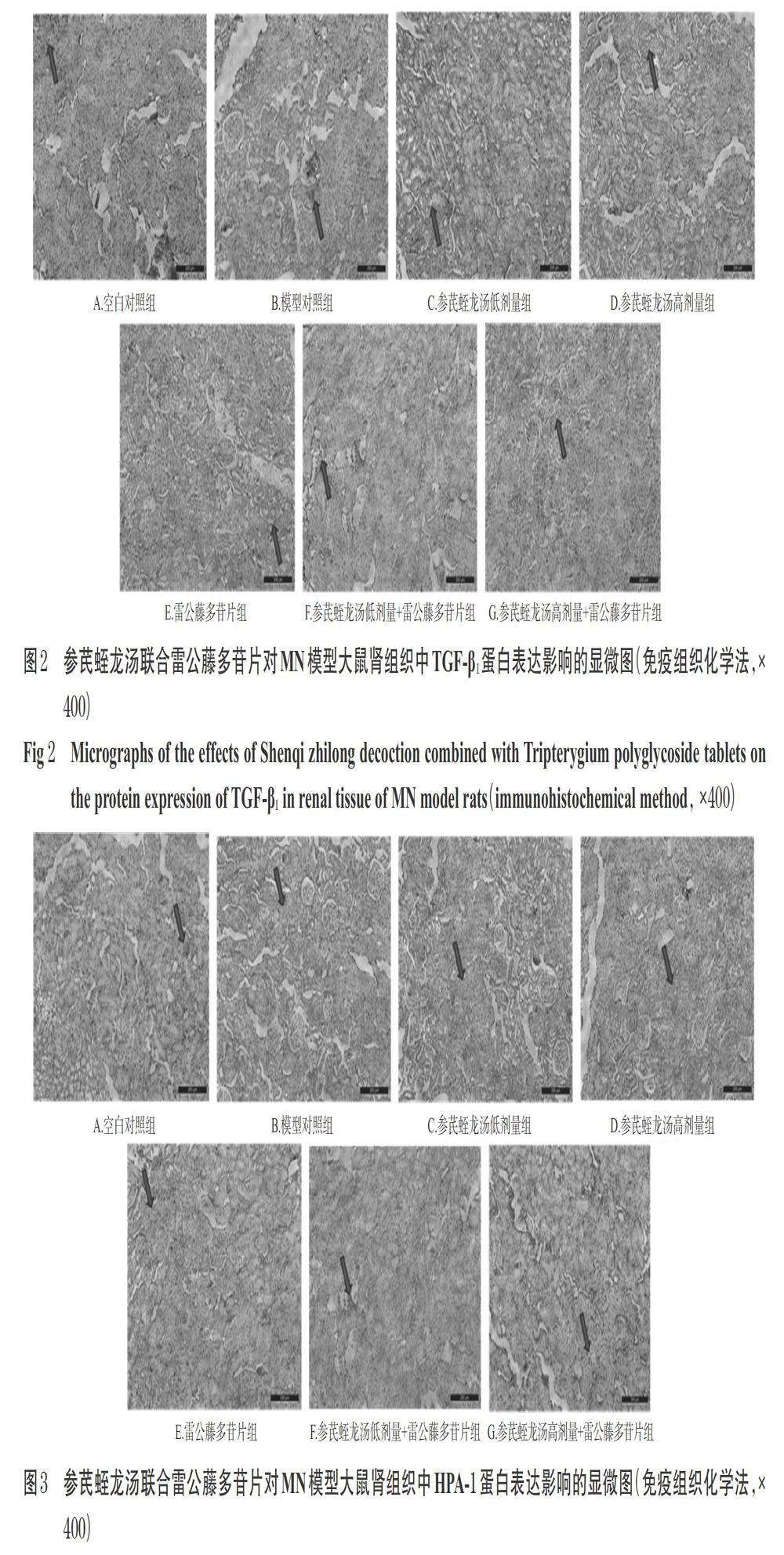
與空白對照組比較,模型對照組大鼠腎臟組織中TGF-β1、HPA-1陽性細胞明顯增多,其陽性細胞百分比均顯著升高(P<0.01)。與模型對照組比較,各給藥組大鼠腎臟組織TGF-β1、HPA-1陽性細胞均有所減少,其中參芪蛭龍湯高劑量組、雷公藤多苷片組、參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠TGF-β1陽性細胞百分比以及各給藥組大鼠HPA-1陽性細胞百分比均顯著降低,且參芪蛭龍湯高劑量+雷公藤多苷片組TGF-β1陽性細胞百分比以及參芪蛭龍湯低、高劑量+雷公藤多苷片組HPA-1陽性細胞百分比均顯著低于雷公藤多苷片組(P<0.01),詳見圖2、圖3(圖中,箭頭所指分別為TGF-β1、HPA-1陽性細胞)、表5。
4 討論
MN為現代醫學的病理診斷名稱,由于該病具有水腫、大量蛋白尿等臨床表現,故屬中醫“水腫”“尿濁”范疇。中醫認為,MN以脾腎虧虛為本、濕濁瘀血為標。參芪蛭龍湯是黑龍江省中醫藥科學院腎病科治療MN的特色醫院制劑,療效較好。方中黨參補中益氣,為脾胃氣虛之要藥,黃芪補氣升陽、利水消腫,淫羊藿補益腎陽、鼓舞腎氣,共為君藥;川芎、當歸活血化瘀,地龍、水蛭、僵蠶蟲類入絡、化瘀消癥,共為臣藥;鳳尾草、虎杖活血化瘀、利水消腫,為佐藥;諸藥合用,共奏補益脾腎、化瘀利濕之效[3]。在臨證中,由于MN病情復雜、臨床表現多樣,多在參芪蛭龍湯基礎上加減應用:如水腫明顯,加茯苓、澤瀉;如腹脹明顯,加大腹皮、厚樸、陳皮;如惡心嘔吐,加半夏、生姜、砂仁;如大便稀,加炒山藥、炒白術、炒薏苡仁;如倦怠乏力明顯,加炒白術,同時加大黃芪、黨參用量;如腰痛明顯,加桑寄生、狗脊、川牛膝等[3]。雷公藤多苷片在臨床上廣泛應用于類風濕性關節炎、紅斑狼瘡和慢性腎炎等自身免疫性疾病的治療[15]。余霄等[16]研究發現,雷公藤多苷片治療MN可明顯減少患者的蛋白尿并減輕其臨床癥狀,臨床療效與潑尼松聯合環磷酰胺相當;王潤秀等[10]在雷公藤多苷片和環磷酰胺治療MN的療效對比研究中發現,雷公藤多苷片組患者的總有效率為80%,顯著高于環磷酰胺組的50%,總體療效更好。然而,雷公藤多苷片在緩解MN患者蛋白尿方面雖具有較好的療效,但會引起骨髓抑制、肝功能和腎間質損傷等毒副作用,包括WBC減少、PLT下降,黃疸、轉氨酶升高,肝臟腫大,急性腎功能衰竭等[5,11]。本課題組在長期的臨床實踐中發現,參芪蛭龍湯在緩解臨床水腫等癥狀方面效果較好,但在降低尿蛋白方面卻起效較慢;雷公藤多苷片具有較好的降低尿蛋白作用,但存在明顯的骨髓抑制作用;而二者聯合應用則可取長補短。在本研究中,雷公藤多苷片選用成人等效劑量以考察其骨髓抑制作用;參芪蛭龍湯在臨床上可明顯緩解雷公藤多苷片引起的骨髓抑制作用,故選用成人等效劑量的0.25、0.5倍作為該方低、高劑量。
本研究結果顯示,模型對照組大鼠RBC計數較模型對照組顯著降低,PLT計數較空白對照組顯著升高;經藥物作用后,給藥組大鼠RBC計數(參芪蛭龍湯高劑量組和參芪蛭龍湯低、高劑量+雷公藤多苷片組)顯著升高,而PLT計數(參芪蛭龍湯低、高劑量單用以及與雷公藤多苷片聯用組)顯著下降,提示參芪蛭龍湯單用或與雷公藤多苷片聯用均可不同程度地上調RBC計數、下調PLT計數。此外,經藥物作用后,雷公藤多苷片組大鼠WBC計數顯著降低,提示大鼠出現骨髓抑制;而參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠均未見WBC計數顯著改變,提示聯用參芪蛭龍湯可一定程度緩解雷公藤多苷片引起的骨髓抑制。與空白對照組比較,模型對照組大鼠24 h UTP顯著升高;經藥物作用后,除參芪蛭龍湯低劑量組外,其余各給藥組大鼠24 h UTP均顯著降低。這提示低劑量的參芪蛭龍湯在調節蛋白尿方面的作用較弱,與本課題組的臨床實踐結果基本相符。同時,腎臟超微結構觀察結果顯示,雷公藤多苷片組大鼠腎小球足突節段融合、基底膜彌散性輕度增厚,并可見少量電子致密物沉積;參芪蛭龍湯高劑量+雷公藤多苷片組大鼠腎小球足突少量融合、基底膜節段輕度增厚,未見電子致密物沉積。這表明參芪蛭龍湯高劑量+雷公藤多苷片組大鼠的腎臟病理損傷較雷公藤多苷片組輕,聯合用藥有減輕雷公藤多苷片單用導致的大鼠腎臟病理損傷的效果。
MN患者會大量丟失血漿TP、ALB,可導致低蛋白血癥的發生;且低蛋白血癥在促使肝臟進一步代償性合成TP、ALB的同時也增加了肝臟脂蛋白的合成,從而導致TC、TG、LDL-C的合成增多,最終引發高脂血癥[17]。另外,當肝細胞發生損傷時,細胞內的AST、ALT會釋放入血,導致血清中上述酶的含量明顯升高[18]。一般情況下,MN患者血清中AST、ALT處于正常水平,但是部分患者在服用雷公藤多苷片治療蛋白尿的時候,可能出現肝功能損傷,即血清中AST、ALT含量升高[5,11]。本研究結果顯示,與空白對照組比較,模型組大鼠TP、ALB含量均顯著降低;經藥物作用后,除參芪蛭龍湯低劑量組外,其余各給藥組大鼠TP、ALB含量均顯著升高。這提示參芪蛭龍湯單用或與雷公藤多苷片聯用可不同程度地改善MN模型大鼠的低蛋白狀態。本研究并未發現雷公藤多苷片致大鼠肝功能損傷的副作用,筆者認為可能與本研究樣本量小且研究時間較短有關。
本研究結果顯示,模型對照組大鼠TC、TG、HDL-C含量均較空白對照組顯著升高;經藥物作用后,參芪蛭龍湯低、高劑量單用及與雷公藤多苷片聯用組大鼠TC含量以及參芪蛭龍湯高劑量組、雷公藤多苷片組和參芪蛭龍湯高劑量+雷公藤多苷片組大鼠TG含量均較模型對照組顯著降低。這表明參芪蛭龍湯聯合雷公藤多苷片可通過降低TC、TG水平來改善MN模型大鼠的高脂狀態。值得注意的是,本研究發現模型對照組大鼠HDL-C含量顯著升高,與臨床實踐略有出入。鑒于該指標與MN相關性的文獻報道較少,故有待后續研究予以論證。
本研究結果還顯示,模型對照組大鼠GLU、BUN、Scr含量均較空白對照組無顯著變化;但經藥物作用后,參芪蛭龍湯高劑量組和參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠GLU含量均顯著升高,且參芪蛭龍湯高劑量+雷公藤多苷片組顯著高于雷公藤多苷片組。這提示高劑量參芪蛭龍湯單用以及與雷公藤多苷片聯用均可提高MN大鼠體內的GLU含量,而雷公藤多苷片單用并不會影響GLU含量。此外有研究指出,雷公藤多苷片可導致腎間質損傷,并引起急性腎功能衰竭,從而導致機體BUN、Scr含量升高[5,11]。但本研究并未發現雷公藤多苷片對大鼠腎功能有顯著影響,有待后續研究繼續探討。
MN是血清特異性抗體與足細胞表達的自身抗原相結合所引發的自身免疫性疾病,上皮下免疫復合物沉積和補體激活均可導致腎小球濾過屏障功能障礙和蛋白尿形成,其病理特點以腎小球臟層上皮細胞下彌散性電子致密物沉積伴基底膜彌散性增厚為主[19]。本研究結果顯示,與空白對照組比較,模型對照組大鼠腎臟組織中腎小球足突廣泛融合或消失,基底膜彌散性重度增厚、上皮下有大量電子致密物沉積;經藥物作用后,參芪蛭龍湯低、高劑量組,雷公藤多苷片組,參芪蛭龍湯低、高劑量+雷公藤多苷片組大鼠腎組織中電子致密物沉積減少、基底膜增厚減輕、足突部分恢復。這表明參芪蛭龍湯聯合雷公藤多苷片可通過減少大鼠腎小球上皮下電子致密物的沉積、修復腎小球基底膜和足細胞的損傷來發揮對MN模型大鼠的保護作用。
腎小球基底膜、內皮細胞和足細胞及其裂孔膜共同構成腎小球濾過膜的機械和電荷屏障,在蛋白尿的形成中具有重要作用[20]。硫酸乙酰肝素蛋白聚糖(HSPG)由核心蛋白和硫酸乙酰肝素經側鏈共價連接而成,是構成腎小球基底膜及細胞外基質的生物大分子[20]。在腎小球基底膜上,HSPG帶有大量負電荷,對腎小球濾過膜電荷屏障的維持意義重大[21]。HPA-1是哺乳動物中唯一可剪切HSPG的內源性β-葡糖醛酸內切酶[22]。若機體內HPA-1表達升高,HSPG將被剪切,基底膜上HSPG的完整性將受到破壞,使電荷屏障被削弱,白蛋白更容易透過腎小球,從而導致蛋白尿的產生[23]。TGF-β1是多功能細胞因子,具有促炎、促纖維化的作用,同時還可誘導組織細胞損傷、抑制創面愈合[24]。張倩等[25]研究發現,MN模型大鼠腎臟組織中HPA-1、TGF-β1的表達均較正常組顯著增多,尿蛋白含量顯著升高;經藥物干預后,上述指標均明顯減少或下降,提示HPA-1、TGF-β1與MN模型大鼠蛋白尿的產生有關。本研究結果顯示,模型對照組大鼠在24 h UTP顯著升高的同時,其腎組織中TGF-β1、HPA-1蛋白陽性細胞百分比均較空白對照組顯著升高;經藥物作用后,各給藥組TGF-β1(除參芪蛭龍湯低劑量組外)、HPA-1陽性細胞百分比均顯著降低,且參芪蛭龍湯高劑量+雷公藤多苷片組TGF-β1陽性細胞百分比以及參芪蛭龍湯低、高劑量+雷公藤多苷片組HPA-1陽性細胞百分比均顯著低于雷公藤多苷片組。這提示參芪蛭龍湯聯合雷公藤多苷片對MN模型大鼠尿蛋白的降低作用可能與其下調TGF-β1、HPA-1蛋白的表達密切相關,且作用強于雷公藤多苷片單用。
綜上所述,參芪蛭龍湯與雷公藤多苷片聯用可緩解雷公藤多苷片的骨髓抑制作用,減少MN模型大鼠蛋白尿,并改善其腎臟組織的病理損傷;上述作用可能與其下調腎臟組織中TGF-β1、HPA-1蛋白表達,降低血液中TC、TG含量有關。本研究初步證實了兩藥聯用對MN模型大鼠的增效減毒作用及可能機制,可為臨床MN的治療提供參考。
參考文獻
[ 1 ] 趙凱,張曉鳳,劉建紅,等.特發性膜性腎病發病機制的研究進展[J].云南中醫中藥雜志,2017,38(11):77-80.
[ 2 ] BECK L,BOMBACK AS,CHOI MJ,et al. KDOQI US commentary on the 2012 KDIGO clinical practice guideline for glomerulonephritis[J]. Am J Kidney Dis,2013,62(3):403-441.
[ 3 ] 薛丕良,張玉昆,袁茵,等.參芪蛭龍湯對大鼠膜性腎病的實驗研究[J].中醫藥學報,2019,47(2):24-28.
[ 4 ] 蘇海萍,馬悅寧.雷公藤減毒增效方法研究進展[J].山西中醫,2018,34(9):55-56.
[ 5 ] 楊冬梅,劉俊.雷公藤多苷臨床應用及不良反應的研究進展[J].中國醫院藥學雜志,2018,38(20):2185-2190.
[ 6 ] 薛璟,賈曉斌,譚曉斌,等.雷公藤化學成分及其毒性研究進展[J].中華中醫藥雜志,2010,25(5):726-733.
[ 7 ] 高月,任桐,姜晨.雷公藤多苷治療特發性膜性腎病的Meta分析[J].河南中醫,2019,39(5):746-752.
[ 8 ] 左科,李世軍,吳燕,等.雷公藤多苷治療特發性膜性腎病的前瞻性隨機對照研究[J].腎臟病與透析腎移植雜志,2014,23(6):507-511、545.
[ 9 ] 劉志紅,李世軍,吳燕,等.雷公藤多苷聯合小劑量激素治療特發性膜性腎病前瞻性對照研究[J].腎臟病與透析腎移植雜志,2009,18(4):303-309.
[10] 王潤秀,曹春瑜,湯顯湖.雷公藤多苷和環磷酰胺治療膜性腎病的效果對比[J].實用醫學雜志,2016,32(10):1726-1727.
[11] 江峽.雷公藤多苷和小劑量激素聯合治療特發性膜性腎病的有效性及可行性分析[J].中國中西醫結合腎病雜志,2015,16(1):51-53.
[12] DING G,REDDY K,KAPASI AA,et al. Angiotensin Ⅱ induces apoptosis in rat glomerular epithelial cells[J]. Am J Physiol Renal Physiol,2002,283(1):F173-F180.
[13] 柴桂芳.車前子性味拆分組分治療膜性腎炎的藥理作用研究[D].哈爾濱:黑龍江中醫藥大學,2015.
[14] 陳文軍,陳素枝,靳曉華,等.降脂通絡軟膠囊對膜性腎病大鼠腎保護作用及對腎組織Bcl-2和Bad表達的影響[J].中草藥,2016,47(18):3263-3267.
[15] 劉為萍,劉素香,唐慧珠,等.雷公藤研究新進展[J].中草藥,2010,41(7):1215-1218.
[16] 余霄,歐陽曉琴,姜寶霞,等.雷公藤多苷對特發性膜性腎病患者抗磷脂酶A2受體抗體的影響[J].世界中醫藥,2018,13(5):1168-1171.
[17] 王吉耀.內科學[M].北京:人民衛生出版社,2005:575- 576.
[18] 陳文彬,潘祥林.診斷學[M]. 6版.北京:人民衛生出版社,2006:402-403.
[19] 謝璇.特發性膜性腎病證素探討及補氣健脾益腎法治療膜性腎病大鼠實驗研究[D].北京:北京中醫藥大學,2015.
[20] GARSEN M,ROPS AL,RABELINK TJ,et al. The role of heparanase and the endothelial glycocalyx in the development of proteinuria[J]. Nephrol Dial Transplant,2014,29(1):49-55.
[21] 呂喆,劉建華,秦曉松.乙酰肝素酶在膜性腎病中的研究進展[J].臨床檢驗雜志,2018,36(6):444-445.
[22] CASSINELLI G,ZAFFARONI N,LANZI C. The heparanase/heparan sulfate proteoglycan axis:a potential new therapeutic target in sarcomas[J]. Cancer Lett,2016,382 (2) :245-254.
[23] 趙琛.從氣血水論治特發性膜性腎病及乙酰肝素酶與IMN尿蛋白相關性的研究[D].北京:北京中醫藥大學,2012.
[24] 劉國菊,李叢叢,李睿坤,等.轉化生長因子β1在纖維化疾病發病中作用的研究進展[J].山東醫藥,2018,58(30):106-109.
[25] 張倩,范華平,張秀俠,等.益腎通絡方對膜性腎病大鼠腎組織中乙酰肝素酶、轉化生長因子β1表達的影響[J].中國中西醫結合腎病雜志,2015,16(3):228-229.
(收稿日期:2019-09-20 修回日期:2020-04-14)
(編輯:張元媛)

