麥麩阿拉伯木聚糖-牛血清蛋白質(zhì)酶促共聚物制備及表征
呂丁陽,殷麗君,陳復生*
1. 河南工業(yè)大學糧油食品學院(鄭州 450001);2. 中國農(nóng)業(yè)大學食品科學與營養(yǎng)工程學院(北京 100083)
多糖及蛋白質(zhì)作為生物活性大分子被廣泛利用在食品乳狀液體系中[1-2]。多糖富含羥基且分子量較大,可通過改善乳狀液流變學特性進而提升乳狀液穩(wěn)定性[3]。蛋白質(zhì)大多含有兩親性氨基酸,可通過提升油水界面張力進而提升乳狀液乳化活性[4]。然而,多糖往往缺少與親水性基團相對應的疏水性基團[5],蛋白質(zhì)易受環(huán)境條件影響[6],為了改善多糖與蛋白質(zhì)乳化特性,研究人員利用物理化學方法使多糖與蛋白質(zhì)交聯(lián)制備多糖-蛋白質(zhì)共聚物,共聚物能夠集合兩者優(yōu)良特性[7]。
多糖及蛋白質(zhì)結合方式主要分為自然交聯(lián)、靜電交聯(lián)及共價交聯(lián)[8]。自然交聯(lián)代表物質(zhì)為阿拉伯樹膠,阿拉伯樹膠由阿拉伯半乳聚糖、阿拉伯半乳聚糖-蛋白質(zhì)及糖蛋白三部分構成,但阿拉伯樹膠取材困難且價格昂貴[9]。靜電交聯(lián)對環(huán)境變化較為敏感,形成的多糖蛋白質(zhì)靜電共聚物容易發(fā)生解離[10]。共價交聯(lián)主要分為美拉德反應[11]及酶促交聯(lián)反應,其中酶促交聯(lián)反應因產(chǎn)物無毒性、反應條件溫和逐漸成為研究熱點[12]。多糖與蛋白質(zhì)的酶促交聯(lián)反應通常由過氧化物酶、轉(zhuǎn)谷氨酰胺酶、漆酶實現(xiàn),漆酶主要作用于多糖的酚酸及蛋白質(zhì)的酪氨酸,二者在漆酶的催化下發(fā)生交聯(lián)進而形成多糖-多糖、蛋白質(zhì)-蛋白質(zhì)及多糖-蛋白質(zhì)共聚物[13-15]。
我國是小麥生產(chǎn)大國,每年因小麥制粉產(chǎn)生約2 000萬 t麥麩,大部分麥麩用作飼料,造成極大的資源浪費[16]。近些年來,國內(nèi)外研究人員對麥麩中含有的膳食纖維、蛋白等進行深入研究,表明麥麩中含有的阿拉伯木聚糖在食品乳化劑行業(yè)具有應用前景[17]。試驗利用小麥麩皮為原料,從中提取麥麩阿拉伯木聚糖(WBAX)作為模型多糖。選取牛血清白蛋白(第五組分)(BSA)作為模型蛋白,BSA為一種球狀蛋白,其酪氨酸主要分布在球狀結構外側,較易與WBAX中含有的阿魏酸交聯(lián)[18]。選取漆酶作為多糖與蛋白質(zhì)之間的交聯(lián)酶[19]。利用漆酶交聯(lián)WBAX及BSA,并對酶促共聚物進行表征,以期為多糖-蛋白質(zhì)酶促共聚物的研究及應用提供參考。
1 材料與方法
1.1 材料與儀器
小麥麩皮(河南省農(nóng)業(yè)科學院);BSA(北京索萊寶科技有限公司);漆酶(200 U/mg,北京索萊寶科技有限公司));H2O2(體積分數(shù)30%,天津科密歐化學試劑有限公司);疊氮化鈉(天津化工試劑三廠);乙腈(色譜級,德國CNW Technologies GmbH公司);無水乙醇(色譜級,天津市津科精細化工);其他試劑均為分析級。
Waters 1525型高效液相色譜儀(美國Waters公司);Aligent 1200型高效液相色譜儀(安捷倫科技有限公司);UV-1901紫外分光光度計(北京普析通用儀器有限公司);DYY-6D電泳設備(北京市六一儀器廠);BS210S分析天平(德國Sartorius公司);LGL-25C冷凍干燥機(北京四環(huán)科學儀器廠);GL-20C高速離心機(上海安亭科學儀器有限公司);微孔濾膜(0.45 μm,美國Millipore 生物科技技術公司);MTN-2800D-24氮吹儀(天津奧特賽恩斯儀器有限公司)。
1.2 WBAX提取及成分分析
1.2.1 提取步驟
取200 g粉碎過40目篩的熱風干燥小麥麩皮,加入5倍質(zhì)量的蒸餾水浸泡并加熱30 min(沸水浴),待溫度降至70 ℃時,加入α-淀粉酶70 ℃水浴加熱,通過碘液變色測試麩皮中是否有淀粉殘留。待淀粉分解完全,過濾富集沉淀,沸騰蒸餾水沖洗4~5次,75 ℃烘箱干燥。向100 g去淀粉麥麩中加入1.5 L 0.15 mol/L NaOH及25 mL體積分數(shù)30%的H2O2,85 ℃恒溫水浴鍋中堿提3 h。反應后料液離心(4 000 r/min,20 min),取上清液加入4 mol/L HCl將混合液調(diào)至pH 4.3,離心(4 000 r/min,20 min)后取上清液,邊攪拌邊加入無水乙醇(乙醇與料液體積比13∶7),離心(4 000 r/min,20 min),所得沉淀冷凍干燥4 ℃條件下保存[20]。
1.2.2 水分、灰分、蛋白質(zhì)、阿拉伯木聚糖含量測定
分別根據(jù)AACC-Methods 44-19、08-01方法來測定1.2.1中提取的WBAX粗產(chǎn)物中的水分及灰分[21]。利用海能K1100全自動凱氏定氮儀測定樣品中蛋白質(zhì)。利用地衣酚-鹽酸法測定阿拉伯木聚糖含量[22]。
1.3 WBAX-BSA酶促共聚物制備
分別利用0.1 mol/L磷酸鹽緩沖溶液(pH 6.5)配置質(zhì)量分數(shù)1.0%的WBAX、0.4% BSA,100 U/mL漆酶溶液,濃度0.5 mol/L的H2O2。取50 μL漆酶溶液與50 μL H2O2與1 mL BSA混合,將4 mL WBAX分成體積相同的10份,每隔5 min以400 μL體積添加到上述混合溶液中,配置成WBAX 與BSA質(zhì)量比10∶1的溶液。對照組為單獨的WBAX、BSA溶液及不含漆酶的WBAX/BSA復合物及漆酶催化的WBAX(質(zhì)量分數(shù)1.0%)或BSA(質(zhì)量分數(shù)0.4%),分別記作WBAX、BSA、WBAX/BSA復合物、WBAX(漆酶)、BSA(漆酶)。試驗組及對照組放置于35 ℃恒溫振蕩水浴鍋中反應4 h,利用20 μL質(zhì)量分數(shù)1.0%的疊氮化鈉終止反應[23]。
1.4 WBAX-BSA酶促共聚物表征
1.4.1 UV-vis分析
當WBAX與BSA在漆酶作用下發(fā)生反應時,WBAX結構中含有的阿魏酸及BSA含有的酪氨酸含量會降低,據(jù)Oudgenoeg報道[24],阿魏酸、酪氨酸、二阿魏酸、二酪氨酸分別在325,280,348和318 nm處具有最大吸光度。可通過監(jiān)測各樣品在325,280,348和318 nm處吸光度的變化監(jiān)測酶促反應進程。取1.3制備的樣品利用0.1 mol/L pH 6.5的磷酸鹽緩沖溶液稀釋1倍,以磷酸鹽緩沖溶液為標定液,測定各樣品分別在325,280,348和318 nm處的吸光度[25]。
1.4.2 SDS-PAGE分析
分別將10 μL樣品溶液(WBAX、BSA、WBAX(漆酶)、BSA(漆酶)、WBAX/BSA酶促共聚物、WBAX/BSA復合物)與10 μL樣品緩沖液混合,樣品緩沖液由質(zhì)量分數(shù)25%甘油、60 mmol/L Tris-HCl(pH 6.8)、質(zhì)量分數(shù)2% SDS、14.4 mmol/L β-巰基乙醇、質(zhì)量分數(shù)0.1%溴酚藍和50 mmol/L EDTA組成。樣品緩沖液混合物煮沸3 min,取10 μL上樣,電泳凝膠由5%濃縮膠和12%分離膠組成,在恒流條件下進行,其中濃縮膠電流20 mA,分離膠電流40 mA。凝膠電泳結束后進行振蕩染色1 h,脫色處理1 h,蛋白質(zhì)染色液配方為1.0 g考馬斯亮藍R250、體積分數(shù)45%甲醇、45%蒸餾水、10%甲酸;脫色液配方為體積分數(shù)10%甲醇、80%蒸餾水、10%甲酸。將經(jīng)過蛋白染色的凝膠電泳進行糖染色處理,將凝膠先至于體積分數(shù)50%乙醇中固定30 min,經(jīng)過質(zhì)量分數(shù)1%高碘酸+3%乙酸溶液中氧化30 min,利用0.1%偏重亞硫酸鈉+10 mmol/L HCl中漂洗2次,在席夫堿試劑中避光染色1 h,用0.5%偏重亞硫酸鈉漂洗脫色。
1.4.3 FT-IR分析
采用傅里葉紅外掃描儀,分析WBAX-BSA酶促共聚物及WBAX/BSA復合物化學鍵變化,采用溴化鉀壓片法,將冷凍干燥的樣品與充分干燥的溴化鉀以1∶100混合,并用瑪瑙研缽研成均勻粉末,以溴化鉀為空白對照,掃描區(qū)間400~4 000 cm-1,掃描次數(shù)32次,分辨率4 cm-1。
1.4.4 乳化穩(wěn)定性分析
取30 mL制備好的樣品溶液于平底小燒杯中,加入10 mL大豆油,在10 000 r/min下均質(zhì)1 min,分別于0和10 min從燒杯底部0.5 cm處取50 μL勻漿液稀釋在5 mL 0.1% SDS溶液中,混勻后在500 nm波長處測定吸光度分別記作A0和A10。用0.1% SDS溶液作為空白對照。根據(jù)式(1)、(2)計算乳化活性指數(shù)(EAI)和乳化穩(wěn)定性指數(shù)(ESI)[26]。


式中:N為稀釋倍數(shù),100;θ為油相體積比,0.25;L為比色杯厚度,1 cm;C為蛋白質(zhì)濃度;A0、A10分別為0 min和10 min的吸光度;10為2次測定的間隔時間,min。
2 結果與分析
2.1 小麥麩皮阿拉伯木聚糖化學組成分析
WBAX化學組分如表1所示,WBAX中含有的少量蛋白質(zhì)是由于堿提過程中調(diào)至pH 4.3時,不能完全沉淀某些游離蛋白質(zhì)。WBAX中阿魏酸含量是由阿魏酸標準曲線得出,阿拉伯木聚糖含量是根據(jù)地衣酚-鹽酸法算得,此方法原理是地衣酚與酸解后WBAX釋放的戊糖反應,根據(jù)標準曲線得出WBAX中阿拉伯木聚糖含量為67%。

表1 WBAX組成成分分析 %
2.2 酶促共聚物表征
2.2.1 UV-vis分析
WBAX與BSA的酶促反應體系中,會形成WBAXBSA、WBAX-WBAX、BSA-BSA這3種產(chǎn)物。WBAXWBAX、BSA-BSA共聚物分別由阿魏酸的脫氫耦合及酪氨酸的脫氫反應制得,而目標產(chǎn)物WBAX-BSA共聚物是通過阿魏酸與酪氨酸結合制得。WBAX-BSA酶促共聚物的形成通常通過反應物阿魏酸、酪氨酸及副產(chǎn)物(二阿魏酸、二酪氨酸)吸光度變化表征[27]。WBAX與BSA在漆酶作用下形成WBAX-BSA共聚物時,阿魏酸及酪氨酸含量會減少,且減少的阿魏酸及酪氨酸分別可參與WBAX及BSA的分子內(nèi)交聯(lián),也可參與WBAX與BSA的分子間交聯(lián),所以需要通過二阿魏酸及二酪氨酸含量進行判斷。由表2可知,WBAX經(jīng)過漆酶處理后,自身含有的阿魏酸能夠交聯(lián)形成二阿魏酸,所以WBAX經(jīng)過酶處理后,325 nm處吸光度下降19.3%,348 nm處吸光度增加47.3%。而280 nm、318 nm處吸光度無明顯變化,說明WBAX自身含有的蛋白質(zhì)的酪氨酸與阿魏酸交聯(lián)程度較低或者無交聯(lián)作用。BSA經(jīng)漆酶處理過后,280 nm處吸光度降低8.5%,318 nm處吸光度上升10.1%,說明在漆酶作用下,酪氨酸能夠形成二酪氨酸進而使BSA發(fā)生分子內(nèi)交聯(lián)。WBAX與BSA利用漆酶處理時,與未經(jīng)漆酶處理得WBAX/BSA復合物對照組相比,阿魏酸、酪氨酸含量分別降低34.4%及9.7%,大于WBAX及BSA的分子內(nèi)交聯(lián)消耗的阿魏酸及酪氨酸量。二阿魏酸含量低于經(jīng)過漆酶處理得WBAX,說明WBAX與BSA處在酶反應體系中時,WBAX中的阿魏酸主要與BSA中酪氨酸反應,且WBAX-BSA酶促共聚物的二阿魏酸(318 nm)、二酪氨酸(348 nm)含量低于未經(jīng)漆酶處理的WBAX/BSA復合物組,說明BSA與漆酶反應體系中引入WBAX時,酪氨酸與阿魏酸的交聯(lián)會暫時阻礙阿魏酸和酪氨酸的分子內(nèi)交聯(lián)。

表2 各樣品紫外-可見光吸光度
2.2.2 SDS-PAGE分析
糖蛋白產(chǎn)物的鑒別可以通過SDS-PAGE分析,多糖與蛋白質(zhì)之間形成多糖-蛋白質(zhì)共聚物時,濃縮膠與分離膠的交界處會有染色條帶出現(xiàn)或者分離膠中會出現(xiàn)拖尾條帶[28]。在圖1(A)中蛋白染色的凝膠中,WBAX-BSA酶促共聚物(泳道1)在濃縮膠中有一條淺藍色的染色條帶,且進樣孔為藍色,說明有大分子量的蛋白質(zhì)或者糖蛋白未能進入凝膠。而未經(jīng)漆酶處理的對照組WBAX/BSA復合物(泳道2)進樣孔無藍色出現(xiàn),且濃縮膠中無藍色條帶出現(xiàn)。圖1(B)為糖染色凝膠電泳,可以看到WBAX-BSA酶促共聚物與WBAX/BSA復合物進樣孔均有糖色出現(xiàn),說明截留在進樣孔外的物質(zhì)為糖蛋白,為驗證是否由WBAX、BSA分子內(nèi)交聯(lián)產(chǎn)物產(chǎn)生,分別對WBAX及BSA的分子內(nèi)交聯(lián)產(chǎn)物的對照組進行驗證(圖1(C)),泳道1、2中無染色條帶出現(xiàn),說明WBAX中的蛋白質(zhì)分子量較小沒有進入泳道且WBAX分子內(nèi)交聯(lián)效果較弱或者交聯(lián)產(chǎn)物分子量較小不足以截留在泳道內(nèi)。BSA純度較高,且經(jīng)過漆酶處理的BSA無高分子量條帶出現(xiàn),說明WBAX-BSA共價復合物(圖1(A)泳道1)在濃縮膠中出現(xiàn)的淺藍色的染色條帶是由WBAX與BSA分子間交聯(lián)產(chǎn)生。
2.2.3 FT-IR分析
FT-IR用來鑒定WBAX與BSA的異質(zhì)結合,WBAX與BSA之間形成WBAX-BSA酶促共聚物時,WBAX中的阿魏酸與BSA中的酪氨酸會通過阿魏酸及酪氨酸的芳香環(huán)形成C—O—C鍵。與WBAX/BSA復合物相比,WBAX-BSA酶促共聚物在667 cm-1處出現(xiàn)新峰。芳環(huán)上氫鍵在650~900 cm-1范圍內(nèi)振動,結果表明WBAX可以通過阿魏酸或蛋白質(zhì)與BSA的酪氨酸分子間反應形成C—O—C鍵。

圖1 各樣品凝膠電泳圖

圖2 各樣品紅外光譜圖
2.2.4 乳化特性分析
由圖3可知,WBAX與BSA交聯(lián)影響產(chǎn)物EAI及ESI,WBAX與BSA在漆酶作用下生成WBAX-BSA酶促共聚物時,EAI及ESI值均增加,與WBAX(75.3 m2/g,17.5 min)、BSA(128.0 m2/g,15.7 min)、WBAX/BSA(144.8 m2/g,18.5 min)復合物的EAI及ESI相比,WBAX-BSA酶促共聚物(155.8 m2/g,23.7 min)上升明顯,這是因為WBA與BSA交聯(lián)時,形成的WBAX-BSA酶促共聚物運用在乳狀液中時會遷移到油水界面,其中酶促共聚物的WBAX部分提供大量親水羥基,BSA部分提供疏水性氨基酸,使得油水界面張力增加,界面膜增厚,因此EAI及ESI增加。
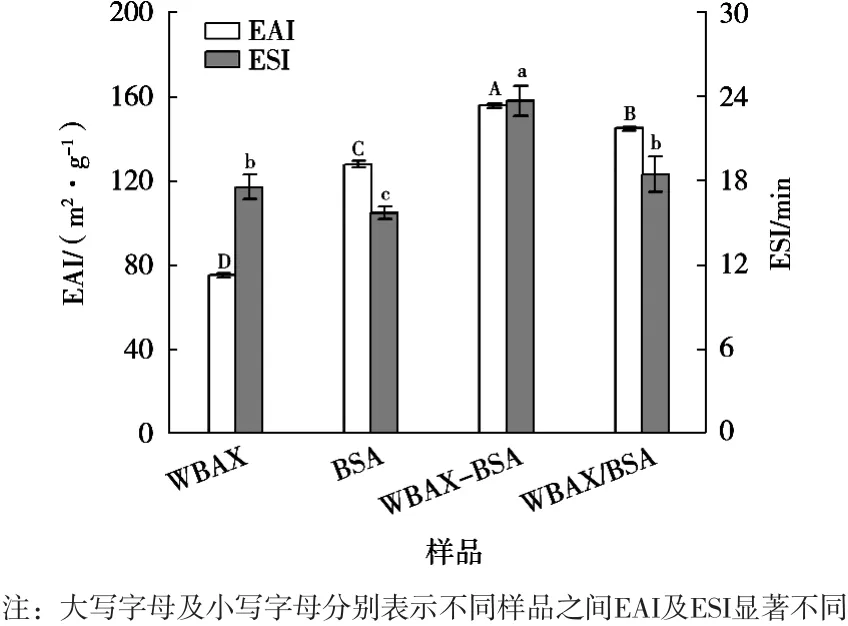
圖3 各樣品乳化特性分析
3 結論
在漆酶體系下交聯(lián)麥麩阿拉伯木聚糖與牛血清白蛋白,并利用紫外分光光度計,十二烷基硫酸鈉聚丙烯胺凝膠電泳,紅外光譜等技術表征了酶促產(chǎn)物形成,結果表面漆酶能夠催化麥麩阿拉伯木聚糖及牛血清白蛋白交聯(lián),且酶促共聚物能夠改善麥麩阿拉伯木聚糖及牛血清白蛋白單體的乳化特性。

