白葉枯病菌效應子XopN在擁有OsSWEET11同源基因的水稻品種上發揮毒性作用
李麗 莫旭艷 李甜甜 張麗媛, 董漢松, ,
(1山東農業大學 植物保護學院,山東 泰安 271018;2南京農業大學 植物保護學院,南京 210095;3作物生物學國家重點實驗室,山東 泰安 271018;*通信聯系人,E-mail: lyZhang@sdau.edu.cn)
水稻白葉枯病是水稻上最重要的細菌性病害,發生于熱帶和溫帶水稻產區[1]。最近半個世紀,水稻白葉枯病主要在中國、日本等東亞國家,菲律賓等東南亞國家或地區、美國等北美國家、澳大利亞等大洋洲國家以及非洲西部國家或地區造成持續危害[1],常年引起的農田水稻產量損失高達10%~50%[1-3]。水稻白葉枯病菌學名叫“水稻黃單胞菌水稻致病變種(Xanthomonas oryzae pv. oryzae,Xoo)”,屬于只有活動細胞而無休眠態芽孢的革蘭氏陰性細菌,是植物病理學研究使用的一種模式病原菌[4,5]。Xoo從水稻葉片上的氣孔或者傷口侵入水稻葉片,在葉片薄壁細胞間隙繁殖,擴展進入木質部,在繁殖與擴展過程中陸續發揮致病作用[5-7]。同包括黃單胞菌在內的其他革蘭氏陰性植物病原細菌一樣,Xoo的一個關鍵致病機制是通過Ⅲ型(typeⅢ, T3)分泌系統分泌效應子(effectors)[3-6,9-13]。T3效應子通過植物識別因子的介導,從細菌細胞轉運到植物細胞[10-12],在寄主植物感病品種(cultivars or varieties)上發揮毒性(virulence, vir)亦即致病作用(pathogenicity, pth),誘發病害[5,9-14],而在寄主植物抗病品種或非寄主植物上行使無毒功能(avirulence,avr),激發抗病性,經常伴隨過敏反應(hypersensitive response, HR)[11]。HR屬于抗病防衛反應,表現為植物器官在受侵染的部位快速發生細胞死亡,抑制病菌生長繁殖與擴展蔓延,保護植物免受進一步侵害[14]。
與植物病原黃單胞菌其他種類一樣,Xoo通過T3分泌系統分泌類似于轉錄激活子效應子(transcription-activator-like effectors, TALEs)和non-TALE蛋白質共近40種效應子[2,15]。TALEs包括冠名為Pth和Avr的蛋白質,non-TALEs主要是“黃單胞菌細胞外蛋白質(Xanthomonas outer proteins,Xops)”[2]。TALEs通過調控它們在植物體內的靶標基因SWEET的表達而發揮致病作用的機制已得到深入研究[5,16-19],其中了解最清楚的是PthXo1操縱水稻OsSWEET11 (異名Xa13)基因表達的分子機制與結構基礎以及OsSWEET蛋白質作為糖分運輸載體的生化機理[3,9-13,16-19],但關于Xops的功能機制卻了解較少。從不同種類黃單胞菌鑒定出的Xops現已多達30種以上[15],但病理功能得到研究的只有7種(XopD、XopN、XopQ、XopR、XopX、XopZ、XopAO1),而且來自不同種類而非同一種細菌,寄主植物也是多種而非一種[20-25]。例如,在侵染番茄的過程中,辣椒斑點病菌(X. campestrispv. vesicatoria,Xcv)分泌的XopD發揮毒性作用,抑制番茄水楊酸與茉莉酸介導的防衛反應基因表達[20]。同時,XopD通過擬泛素化作用來削弱乙烯介導的轉錄因子SIERF4編碼基因的表達,并抑制SIERF4蛋白質產生[21]。水楊酸和乙烯/茉莉酸信號傳導對植物抗病性的調控作用通常相反[26],Xcv侵染番茄而分泌的XopD同時抑制這三種激素信號傳導,機制尚不明確。木薯萎焉病菌(X. axonopodispv.manihotis)產生至少17種Xops,其中XopX、XopZ、XopAO1對病菌的完全毒性起決定作用,XopN與XopQ毒性功能冗余,XopR和XopAO1抑制木薯抗病免疫反應[23]。可見,對不同病菌產生的不同Xops進行全面研究闡釋,尚需時日。
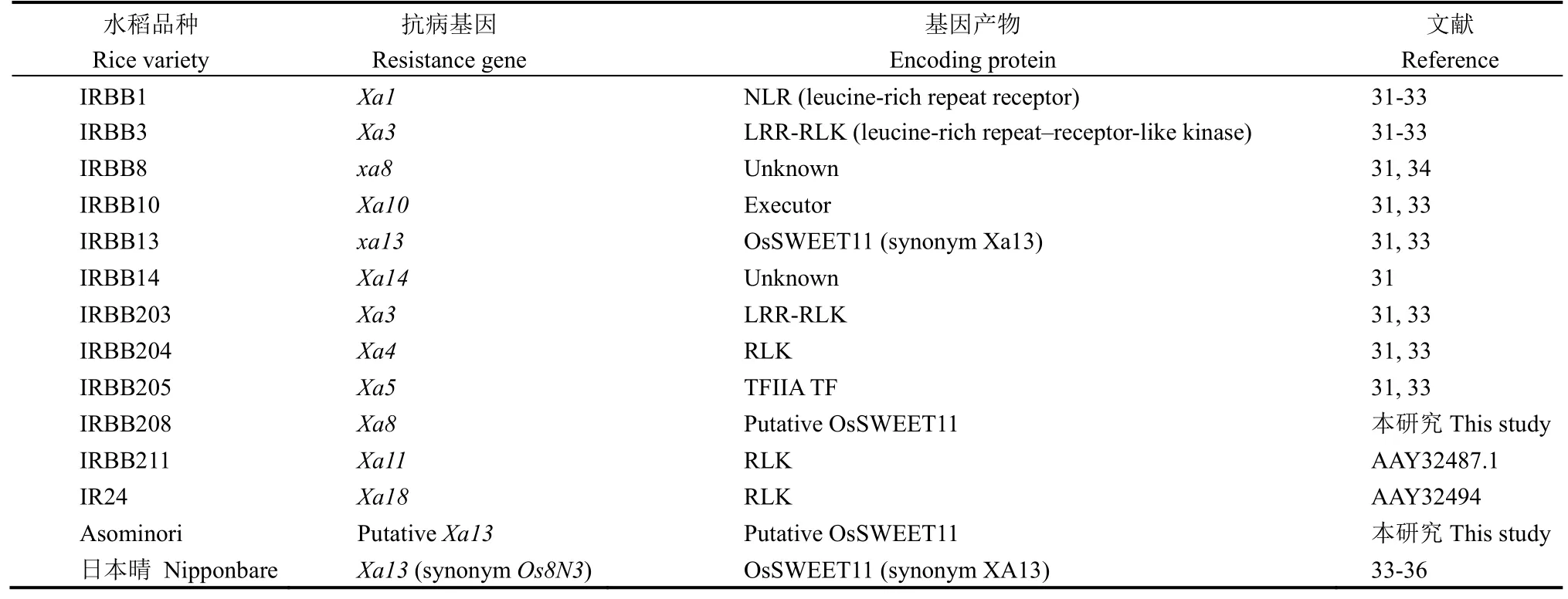
表1 供試水稻品種中白葉枯病的抗病基因及基因表達產物Table 1. Xoo-relevant resistance gene and encoding proteins in the tested rice varieties.
較之上述Xops,XopN病理功能得到較好的研究。XopN有分子接頭的結構特征,可能通過結合植物免疫反應因子而發揮毒性作用[27],互作的抗病免疫因子已知有14-3-3蛋白質家族成員[25]。在侵染過程中,Xcv產生的XopN與番茄14-3-3蛋白質TFT1結合,從而抑制TFT1對病原物模式分子觸發的免疫反應(pattern-triggered immunity, PTI)的調控能力[25]。此外,XopN對甘藍褐腐病菌(X. campestrispv.campestris)[28]、水稻條斑病菌(X. oryzaepv.orizicola)[29]和Xoo[30]毒性的貢獻也得到確認。XopN決定Xoo菌株KXO85對水稻感病品種Dongjin的毒性,與水稻抗病相關蛋白質VOZ2互作,調控病菌毒性[30]。這些研究提出了一個問題,即XopN的病理功能是否因水稻品種對病菌的抗感性(susceptibilities)而異?作者使用Xoo標準菌株PXO99A和水稻不同品種進行研究,試圖解答這個問題。目前對PXO99A產生的XopN的認知,僅限于它是一種Ⅲ型效應子,病理功能還有待揭示[3,15]。本研究主要測定了PXO99A對水稻14個品種的毒性,分析了XopN基因敲除和回補對病菌毒性的影響,以及病菌毒性與水稻OsSWEET11基因誘導表達的關系。結果表明,XopN是一個有限廣譜性(pluripotent)效應子。
1 材料與方法
1.1 試驗材料
1.1.1 供試植物
病菌毒性測定使用了14個水稻品種(表1),各含至少1個抗性基因[31],基因產物性質不同[32-35],植物HR測定使用本氏煙(Nicotiana benthamiana)。兩種植物均在裝有植物培養基質(PINOSTR substrate)的花盆內培育,煙草種子播種后10 d移栽,水稻采用催芽的方式培育。催芽和幼苗培育均使用26℃~28℃植物培育室(12 h光照/12 h黑暗)。
1.1.2 供試菌株與質粒
供試細菌菌株、質粒載體或重組載體有從專業公司購買的,也有參與本研究的師生先后在南京農業大學(南京)和山東農業大學(泰安)構建的(表2)。
1.2 實驗方法
1.2.1 病菌XopN基因敲除
構建基因敲除載體所用引物依據 NCBI(National Center Biotechnology Information)上PXO99A的全基因組序列,設計XopN上游序列(F1,996 bp)和下游序列(F2, 794 bp)的引物(表 3),由金斯瑞生物公司合成。以PXO99A基因組DNA為模板,用ExTaq酶擴增XopN基因的上游片段F1和下游片段F2。將擴增好的F1、F2片段用TA克隆連接到pMD19-Ts載體上,挑選陽性克隆送測序。用同種方法將擴增好的卡那霉素(Kan)基因連接到載體 pMD20-T上,挑選陽性克隆送測序。挑選測序正確的片段,利用對應的酶切位點將 F1、F2片段從載體pMD19-Ts上酶切下來,凝膠回收正確的F1、F2片段,連接到pMD20-T(帶有正確的Kan片段)載體上,構建XopN的敲除重組載體pMD20-T::F1::Kan::F2。制備PXO99A感受態細胞,將敲除重組載體電轉PXO99A感受態細胞。轉化的細菌接到NA培養基上,放入28℃培養箱進行培養。待長出單菌落,將單菌落分別對應,點在含有氨芐霉素和卡那霉素的NA培養基上,再放入28℃培養箱,培養2 d,對單菌落進行PCR擴增,為驗證目的基因敲除效果。另外,本實驗室此前使用上述類似方法對XopQ進行敲除,獲得突變菌株ΔXopQ[33]。
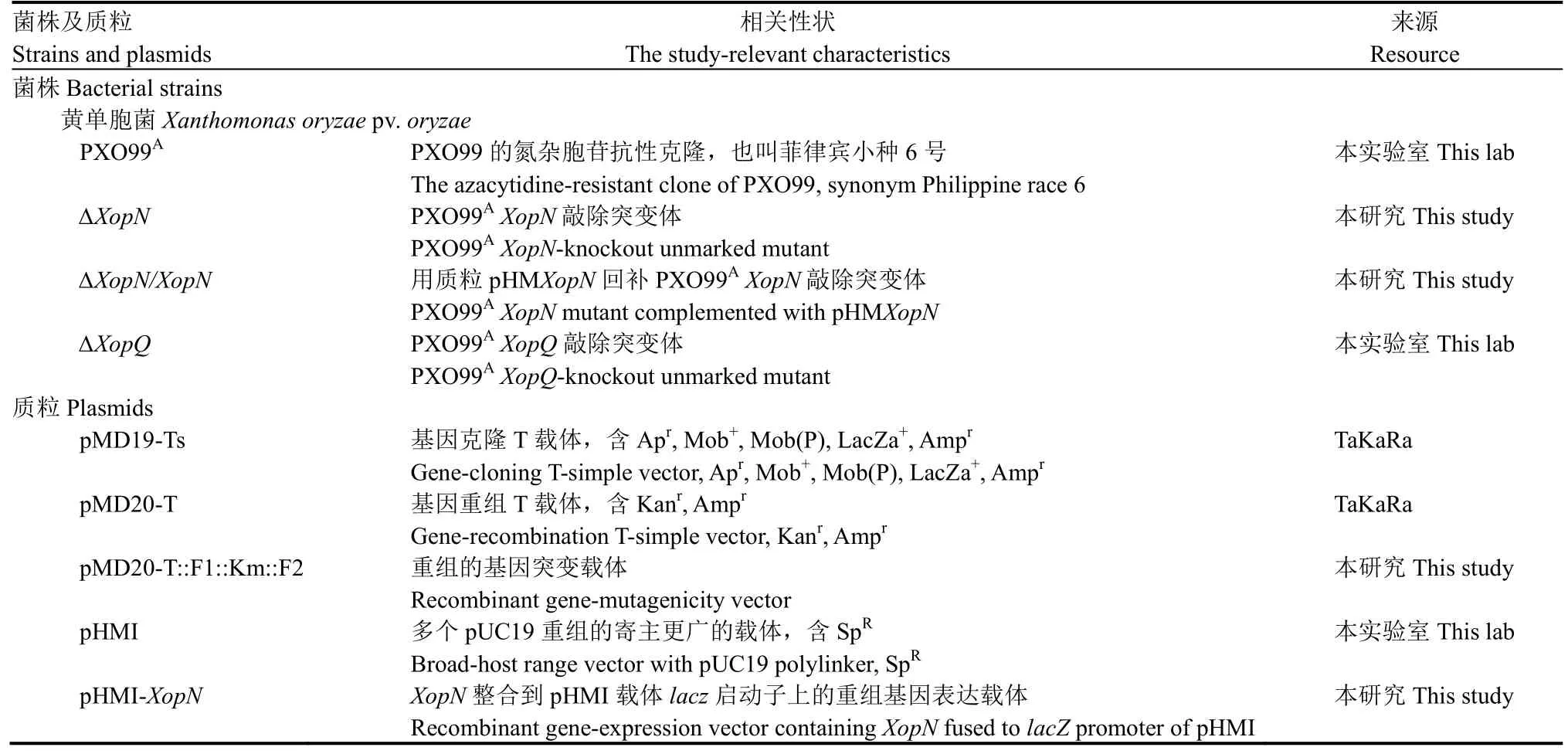
表2 供試菌株與質粒Table 2. Bacterial strains and plasmid vectors used and created in this study.

表3 用于病菌XopN基因敲除和回補的PCR引物相關信息Table 3. Information of primers used in PCR protocols for Xoo XopN knockout and complementation.
1.2.2ΔXopN突變體遺傳回補
根據諾唯贊公司的一步法克隆試劑盒(One Step Cloning Kit)使用說明書設計引物(表 3),以PXO99A的DNA為模板,通過PCR擴增XopN全長(表3)。用限制性內切酶HindⅢ分別將擴增好的XopN片段和 pHMI載體進行酶切,將酶切后的產物純化后進行重組反應。反應體系包括 5×CE Ⅱ緩沖液4 μL,線性化克隆載體50~200 μg,插入擴增片段產物20~200 ng,ExnaseTMⅡ 2 μL,加dd H2O至20 μL。反應后轉化至大腸桿菌DH5α感受態細胞中,涂板,待長出單菌落后挑選單菌落,進行菌落PCR鑒定,將菌落PCR鑒定為陽性克隆的單菌落再用 Hind Ⅲ酶進行酶切鑒定。將驗證成功的回補載體送測序鑒定。將測序正確的pHMI::XopN回補載體,電轉入ΔXopN感受態細胞中,菌液涂布于含有卡那霉素的NA培養基上,在28℃條件下培養3 d,將長出的單菌落搖菌提取基因組,用作模板,使用XopN基因的特異引物,通過PCR進行驗證,PCR結果為陽性的即為ΔXopN突變體回補菌株。
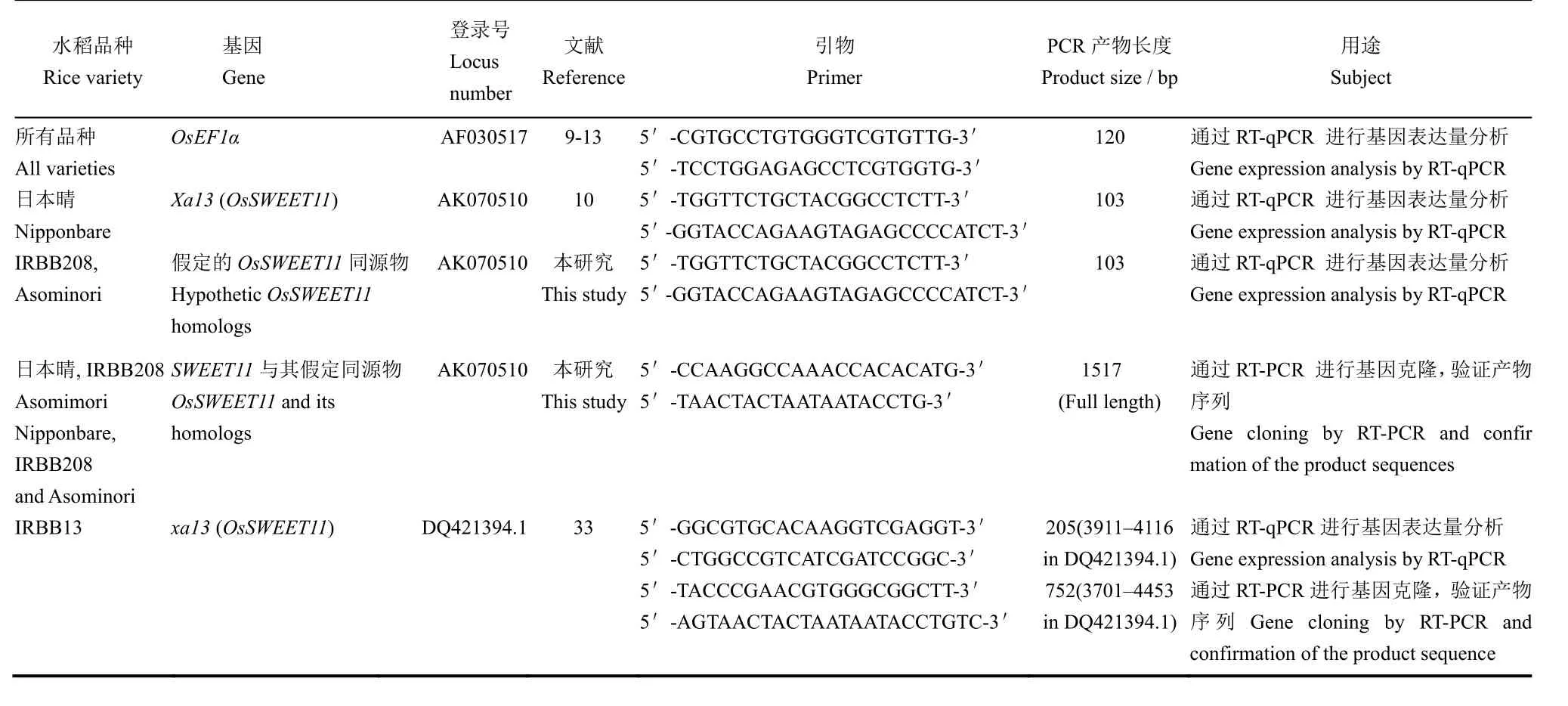
表4 水稻基因及其RT-PCR與RT-qPCR分析所用引物信息Table 4. Information on rice genes and their primers used for RT-PCR and RT-qPCR analyses.
1.2.3 細菌繁殖量測定
將 PXO99A、ΔXopN和ΔXopQ細菌儲備物移入營養肉湯(nutrient broth, NB)培養液,活化培養至OD600=1,各取20 μL菌液轉入新的NB培養液,28 ℃下振蕩培養,在10~24 h期間每隔2 h取樣,測定不同菌株 NB培養物的 OD600值,然后通過Excel制作細菌生長曲線。
1.2.4 接種實驗
接種采取兩種通用方法,即剪葉和注射[9-14]。使用剪葉接種法時,剪刀先用OD600為0.5的菌懸液蘸一下,立即剪切水稻葉片尖端約3 mm的部分。使用一個月齡的水稻苗,每個菌株接種6株幼苗,各選取心葉下方的2張完全展開葉片進行接種。接種3 d后,取樣測定細菌繁殖量,14 d后測量病斑長度。注射法接種使用 14日齡的水稻苗,每個菌株接種6株稻苗,各注射6張葉片,3 d后測定葉片含菌量。無論剪葉還是注射接種,葉片含菌量測定都是采用細菌回收的方法。每株稻苗取3張葉片,用酒精棉球表面消毒后,用經過滅菌的打孔器(0.5 cm×0.5 cm, 0.19625 cm2)取葉圓片,葉圓片再用滅菌的剪刀剪碎,葉片碎片置于3 mL滅菌水中,借助研棒用力研磨。含菌的葉片組織研磨物懸浮液經10倍系列稀釋后,各取10 μL,涂布在含相應抗生素的NB瓊脂(NB agar, NA)培養基平板上,28℃下培養3~5 d,計數菌落形成單位(colony formation unit,cfu)。
1.2.5 水稻基因克隆和表達分析
根據已知信息(表3),從水稻不同品種克隆抗病(感病)基因,包括 IRBB13的隱性抗病基因 xa13(OsSWEET11)[33]、日本晴顯性感病基因 Xa13(OsSWEET11)[35]、IRBB208和Asominori可能含有的OsSWEET11同源基因。水稻這4個品種30日齡幼苗所有葉片均剪葉接種,分別接種 PXO99A、ΔXopN和ΔXopN/XopN。一部分幼苗立即取樣,另一部分幼苗到24 h再取樣,均剪取全部葉片,立即提取RNA,兩次提取的RNA依次用于基因克隆和表達分析。采用RT-PCR克隆的方法,使用不同引物(表4),從水稻上述品種克隆相應的抗病(感病)基因。RT-PCR產物經過測序和BLAST比對,確認基因或同源物。通過實時定量RT-PCR (RT-qPCR)來測定基因表達水平[10]。
1.2.6 煙草HR測定
通過NA培養活化PXO99A、ΔXopN、ΔXopN/XopN細菌,挑選單菌落移入NB培養液,于28 ℃培養箱中振蕩培養 16~18 h。收集培養液,離心沉淀菌體,菌體用純水懸浮,重復離心1次,沉淀的菌體再用純水懸浮,稀釋菌懸液至 OD600=0.5。選取5~6葉期的本氏煙,用一次性注射器吸取細菌懸浮液,在葉片側脈之間約中心點注入葉肉細胞間隙。到12 h,用臺盼藍染色法[37]顯示葉片細胞過敏性死亡(microscopic HR, micro-HR)情況,并于12~36 h觀察HR。
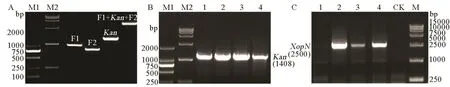
圖1 PXO99A的XopN基因敲除Fig. 1. XopN gene knockout from PXO99A.
1.3 數據分析
所有實驗至少重復3次,即包括至少3個生物學重復,結果一致時予以使用。對定量分析獲得的實驗數據,使用IBM SPSS19.0軟件中文指導書[38]和配套的軟件包進行三項統計分析。一、使用Levene方差齊性檢驗來檢驗方差整齊性。二、使用Kolmogorov-Smirnov檢驗和P-P圖,確認數據的正態分布。三、差異顯著性測定,又有兩種。1)成對數據比較,例如比較病菌野生型與突變菌株誘發的病斑長度,通過方差分析(analysis of variance,ANOVA)和F測驗(Fisher’s test),估計差異顯著性。2)多重比較,例如比較野生型、突變體、遺傳回補的菌株誘發的病斑長度,通過ANOVA和鄧肯新復極差測驗(Duncan’s multiple-range test),估計差異顯著性。統計分析的材料單元根據測定的項目而有不同,只有病斑長度以葉片為單位[39],水稻基因表達和細菌繁殖測定則以每個樣品為單位,計為生物學重復數。
2 結果與分析
2.1 XopN敲除成功
為了研究 XopN基因的病理功能,必須把它從PXO99A敲除,獲得ΔXopN突變體,對突變體進行遺傳回補,獲得回補菌株,然后比較野生型、突變體和回補菌株對水稻的毒性。因此,我們首先構建了 XopN的敲除載體 pMD20-T::F1::Kan::F2。PCR擴增與測序驗證表明構建驗證成功,重組載體所含XopN基因上游片段F1為996 bp,下游片段F2為794 bp,Kan基因為1408 bp(圖1-A)。用電擊轉化的方法,將構建好的ΔXopN敲除重組載體轉入PXO99A感受態細胞,轉化的細菌經過3 d培養,長出單菌落。然后,將單菌落分別對應點在含有氨芐青霉素和卡那霉素的NA培養基上。若該菌落在含氨芐青霉素的平板上不能生長但能夠在含卡那霉素的平板上生長,則該菌落可能是XopN敲除突變體。根據這一原理,初步篩選出了XopN敲除突變體菌株。對初選菌株做了進一步分子鑒定,挑取單菌落進行震蕩培養,從培養物提取基因組DNA用作模板進行PCR擴增,分別擴增Kan基因和XopN基因,挑選了4個轉化子,均具有Kan基因(圖1-B),其中轉化子1不含XopN基因(圖1-C),說明它是敲除了XopN的PXO99A突變體ΔXopN。
2.2 ΔXopN突變體回補成功
為了后續試驗能夠充分說明XopN基因的病理功能,構建了ΔXopN突變體的遺傳回補載體pHMI::XopN。用此載體轉化大腸工程菌株DH5α的感受態細胞,轉化后的細菌經過培養長出單菌落。這樣的單菌落用來進行菌落PCR和酶切驗證,結果表明回補載體pHMI::XopN構建成功(圖2-A)。將構建成功的pHMI::XopN質粒電轉入ΔXopN敲除突變體感受態,涂布在含有鏈霉素和壯觀霉素的NA培養基上進行培養,3 d后長出單菌落。從這種單菌落提取DNA,通過PCR擴增XopN基因進行驗證。結果見圖 2-B。其中,轉化子 1、2、3含有 XopN基因,基因擴增效果與陽性對照(control)相當。轉化子1、2、3就是ΔXopN突變體的回補菌株,記做ΔXopN/XopN。

圖2 突變體ΔXopN遺傳回補效果驗證Fig. 2. Genetic complementation of the ΔXopN mutant.
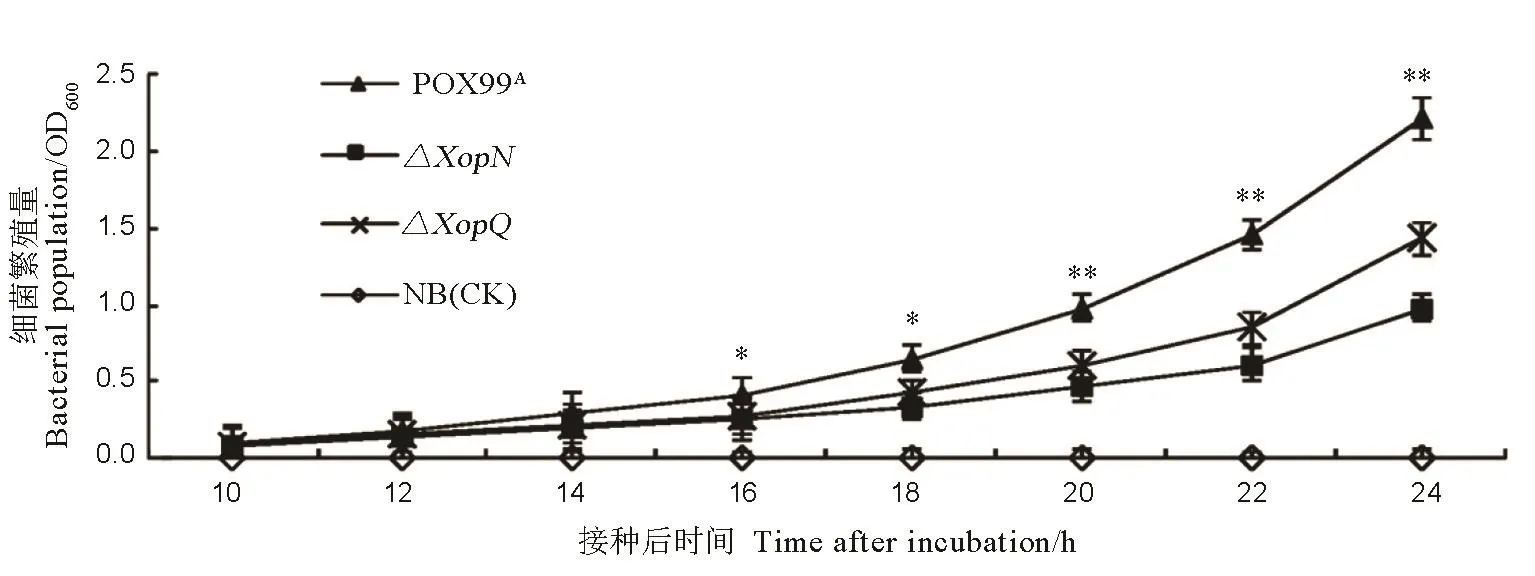
圖3 Xoo不同菌株在NB液體培養基中的生長曲線Fig. 3. Bacterial population of the indicated Xoo strains in NB medium.
2.3 XopN影響細菌繁殖
為了探討XopN敲除是否影響細菌在培養基上繁殖的能力,我們把 Xoo野生型菌株 PXO99A和XopN敲除突變體ΔXopN在NB液體培養上進行培養,于10~24 h內每隔2 h做一次細菌繁殖量測定。已知XopQ與XopN一樣,也是PXO99A的一個效應因子,較之 PXO99A,XopQ敲除突變體ΔXopQ的繁殖量大為降低[24,33]。因此,我們對ΔXopQ做了同步測定。以NB培養液為對照,不同菌株在NB培養液中細菌繁殖量的變化曲線見于圖 3。圖上顯示,從14 h起,突變體菌株ΔXopN、ΔXopQ的繁殖速度慢于野生型PXO99A,ΔXopN比ΔXopQ繁殖速度更慢,到24 h相差約10倍。這說明,XopN和XopQ對細菌繁殖速度都有影響,比較來看,XopN的影響更大一些。
2.4 對水稻14個品種的測試表明XopN決定病菌在其中4個品種上的毒性水平
根據本實驗室[9-13,31,36]和世界同行[32-35]的相關研究,我們選出14個水稻品種(表1),即IRBB1、IRBB3、IRBB8、IRBB10、IRBB13、IRBB14、IR24、IRBB203、IRBB204、IRBB205、IRBB208、IRBB211、Asominori、日本晴(Nipponbare),用來評估 XopN毒性功能的專化性程度。通過接種實驗,采取兩項通用的指標[9-14,20-25]測評Xoo不同菌株對水稻不同品種的毒性:一是水稻葉片白葉枯癥狀嚴重程度;二是細菌在水稻葉片內的繁殖量。
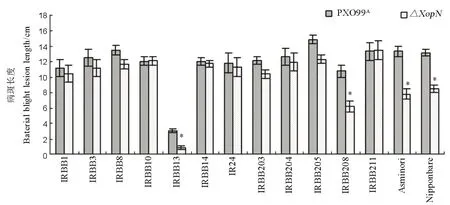
圖4 用XopN與PXO99A剪葉接種水稻不同品種引起的白葉枯病斑長度Fig. 4. Lesion Length of leaf blight caused by the Xoo strains in different rice varieties.
首先,我們用野生型菌株PXO99A和ΔXopN突變體的細菌懸浮液(OD600=0.5)分別對上述 14個水稻品種的30日齡幼苗進行剪葉接種,14 d后(兩周) 觀察白葉枯病癥狀,測量病斑長度,用以評價病情嚴重度。結果顯示,PXO99A對13個水稻品種均有很強的毒性,引起的白葉枯病斑長度平均都超過10 cm,僅對 IRBB13毒性微弱(圖 4),該品種葉片病斑長度平均只有3.1 cm。PXO99A和ΔXopN在水稻10個品種上毒性相近(圖 4),引起的葉片病斑長度無顯著差別(ANOVA和F測驗)。但是,在IRBB13、IRBB208、Asominori、日本晴這4個水稻品種上,PXO99A毒性明顯高于ΔXopN突變體(圖4)。亦即,較之PXO99A,ΔXopN毒性大為減弱,在這4個水稻品種葉片上引起的病斑長度顯著縮短(ANOVA和 F 測驗,P < 0.05)。
為了確認XopN的病理功能,我們選擇水稻品種IR24(XopN基因敲除對菌株在水稻葉片上的致病性不起作用)和 IRBB208(XopN發揮作用)進行重復接種,驗證了ΔXopN遺傳回補的效果。我們制備了PXO99A、ΔXopN突變體及其回補菌株ΔXopN/XopN的菌懸液,循例采用剪葉接種法,對這兩個水稻品種的30日齡幼苗分別予以接種,14 d后觀察并記錄病斑長度。結果顯示,回補菌株ΔXopN/XopN能恢復 PXO99A對水稻 IR24、IRBB208的致病力(圖5)。根據ANOVA和鄧肯新復極差測驗,PXO99A、ΔXopN、ΔXopN/XopN在IR24葉片上引起的病斑長度差異不顯著,但在IRBB208上,較之PXO99A或ΔXopN /XopN,ΔXopN 引起的病斑長度顯著(P <0.01)縮短(圖5)。顯而易見,用野生型XopN基因對ΔXopN進行遺傳回補,達到了應有的效果。
植物體內細菌數量測定表明,XopN影響 Xoo在水稻葉片組織內的繁殖能力和種群數量。采取注射接種法,用PXO99A、ΔXopN、ΔXopN/XopN菌懸液分別接種IR24、IRBB208的14日齡幼苗的葉片,3 d后剪取接種的葉片,從中回收病菌并進行定量比較,結果見表 6。與病斑長度結果一致,ΔXopN突變體降低了IRBB208水稻葉片組織內的含菌量,但對 IR24水稻葉片內的含菌量沒有顯著影響,再次說明XopN對不同水稻品種的毒性存在差異。
為了在所有供試水稻品種上獲得關于病菌毒性的完整資料,根據細菌毒性測評的上述第二個參數,我們又制備了PXO99A、ΔXopN、ΔXopN/XopN細菌懸浮液,分別用來注射接種上述 14個水稻品種14日齡幼苗的葉片,3 d后剪取接種的葉片,從中回收病菌并進行定量比較。結果顯示,病菌3個菌株在水稻 10個品種葉片內繁殖量非常接近,只有IRBB13、IRBB208、Asominori和日本晴這4個水稻品種葉片內,PXO99A和ΔXopN/XopN充分繁殖,但ΔXopN的繁殖能力明顯受抑,顯著降低了其種群數量(圖7)。無論與 PXO99A還是ΔXopN/XopN相比,ΔXopN在IRBB13、IRBB208、Asominori和日本晴幼苗葉片內的細菌數量都顯著降低(ANOVA和鄧肯新復極差測驗,P < 0.01)。
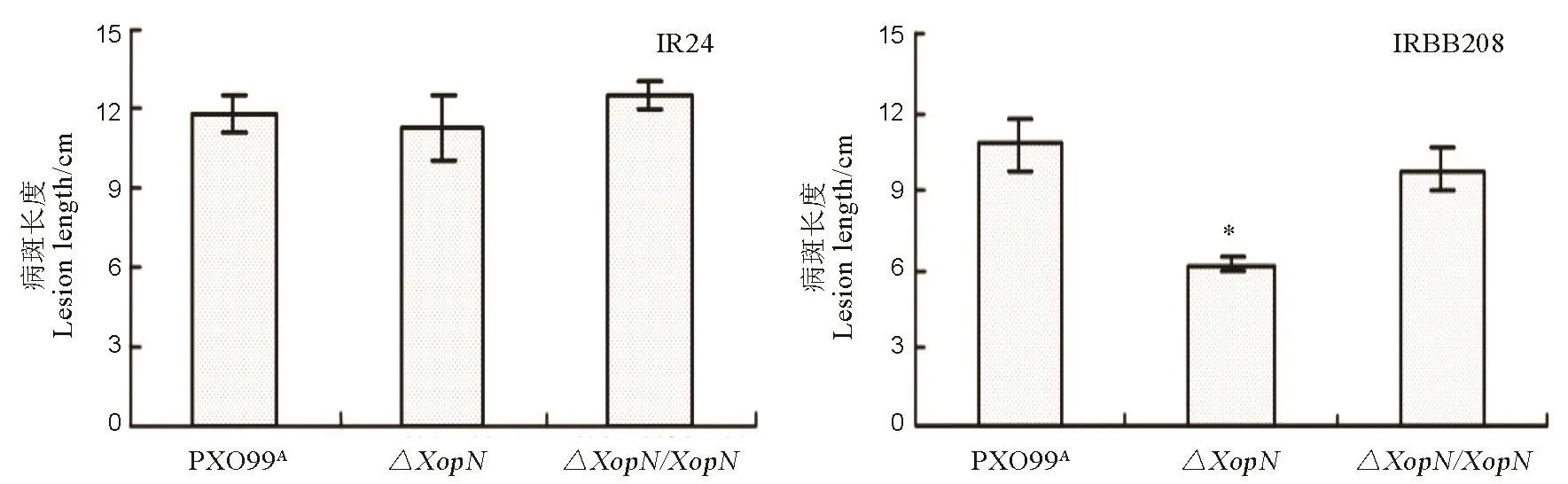
圖5 PXO99A、ΔXopN、ΔXopN/XopN在水稻品種IR24和IRBB208上的白葉枯病病斑長度Fig. 5. Lesion length of leaf blight caused by the three Xoo strains in the two rice varieties.
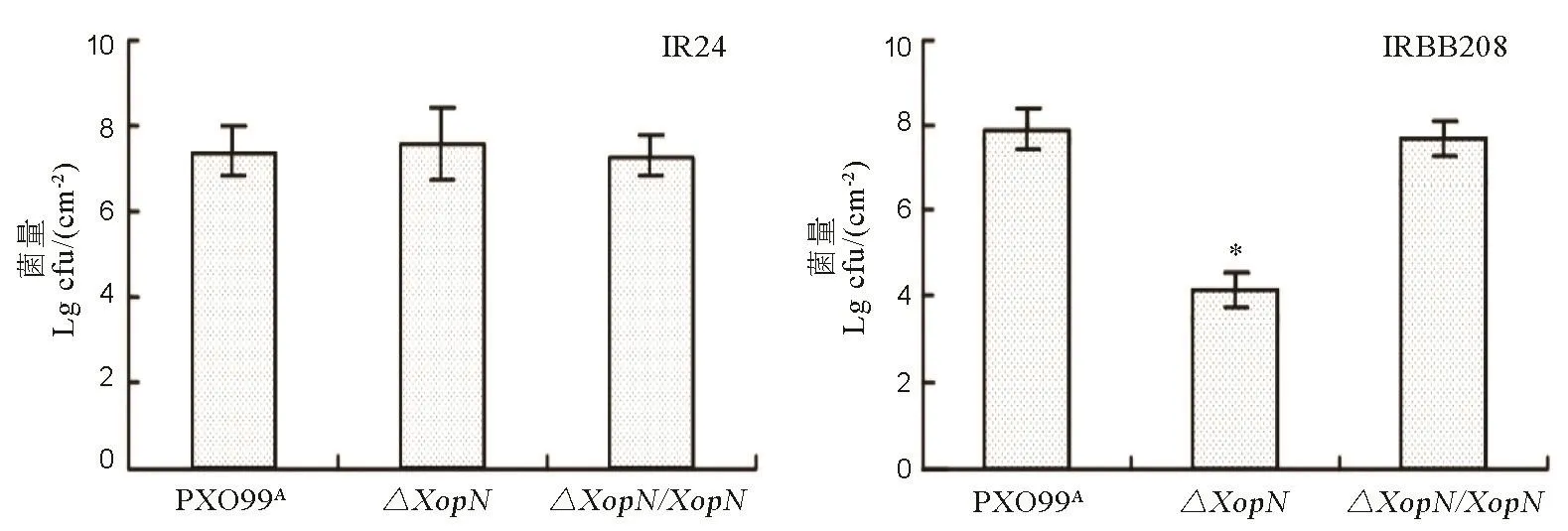
圖6 PXO99A、ΔXopN和ΔXopN/XopN在水稻品種IR24和IRBB208葉片內的繁殖量Fig. 6. Bacterial population of PXO99A, ΔXopN and ΔXopN/XopN in leaves of IR24 and IRBB208.
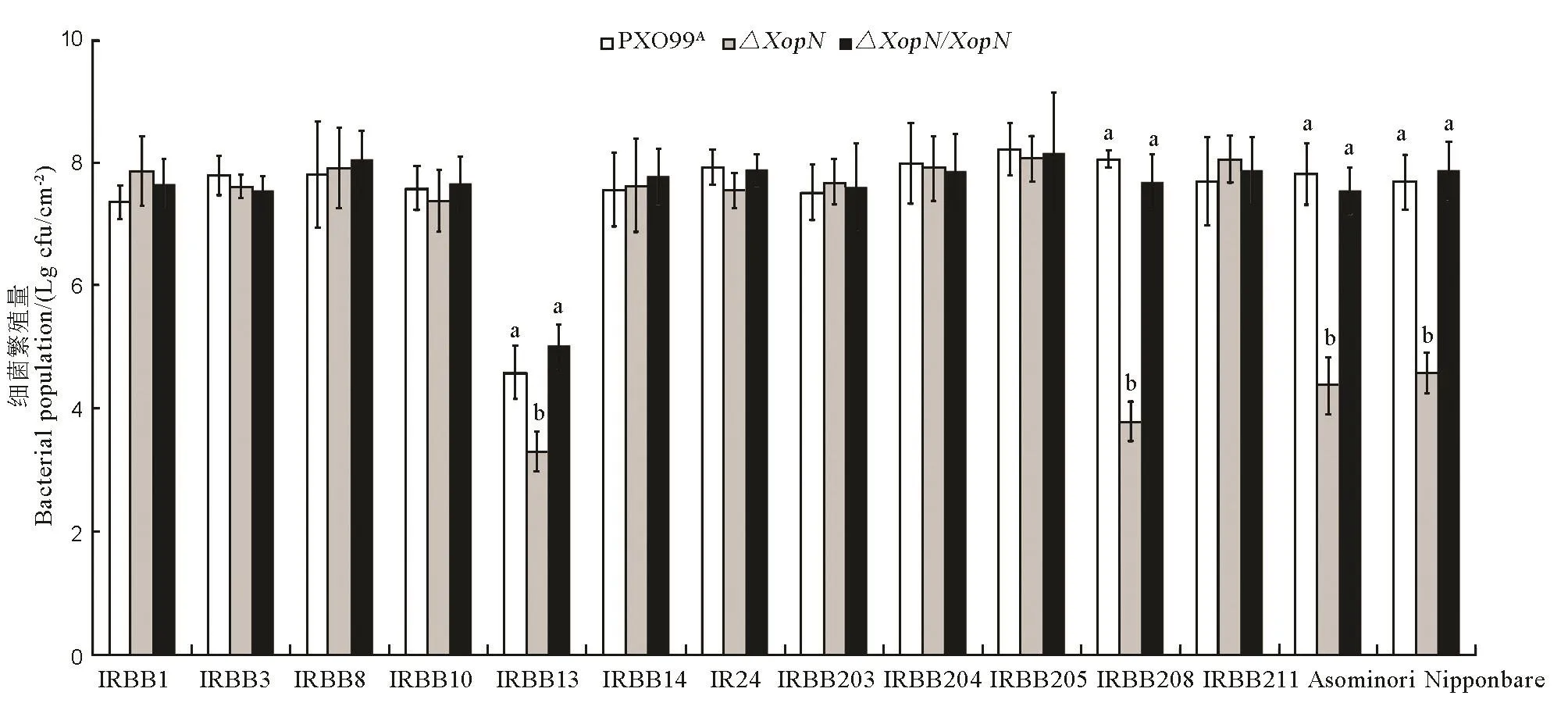
圖7 PXO99A、ΔXopN和ΔXAopN/XopN在14個水稻品種體內的繁殖量Fig. 7. Populations of PXO99, ΔXopN and ΔXopN/XopN bacteria multiplied in leaves of the 14 rice varieties.
綜合分析比較上述實驗結果,可以明確看出,從水稻不同品種葉片內的Xoo繁殖量和葉片白葉枯病癥狀差別這兩項評定病菌毒性的指標[9-14,20-25]來看,敲除XopN基因對Xoo毒性的影響因為水稻品種的不同而有很大差別。測定的 14個水稻品種僅有 4個(IRBB13、IRBB208、Asominori、日本晴)病理反應受病菌效應子XopN的影響,對Xoo的敏感性或對白葉枯病的感病性因為病菌XopN的敲除與否而有顯著差別(P < 0.05)。換言之,XopN決定Xoo菌株PXO99A對這4個水稻品種的毒性水平。根據病菌繁殖量和引發白葉枯病的嚴重程度,在IRBB13上,PXO99A毒性水平較低,但XopN對病菌毒性的貢獻很大,約占75%,而對其他3個水稻品種(IRBB208、Asominori、日本晴),PXO99A有很強的毒性,但XopN對病菌毒性的貢獻卻比較低(分別為43%、42%、31%)。顯而易見,XopN是一個有限廣譜性(pluripotent)[40]效應子。
2.5 XopN影響病菌誘導水稻OsSWEET11同源基因表達的能力
為了探討XopN毒性功能這種有限廣譜性的機制,我們考查了上述XopN發揮作用的4個水稻品種對白葉枯病抗感反應的遺傳基礎和分子機制(表1)。IRBB13對白葉枯病的抗性取決于隱性抗病基因xa13,該基因的編碼產物是OsSWEET11/Xa13蛋白質[31,33]。相反,日本晴擁有顯性的Xa13基因[35],即xa13的等位基因[32],Xa13編碼的OsSWEET11/XA13/Os8N3與xa13編碼的OsSWEET11/Xa13僅有三個氨基酸的差別[41],但決定日本晴對白葉枯病的感病性,即決定菌株PXO99A對日本晴的毒性[10,12,35]。我們通過接種實驗和RT-qPCR分析發現,PXO99A對OsSWEET11/xa13在IRBB13葉片內的表達有顯著(P<0.01)的抑制作用,卻能大幅度提高OsSWEET11/Xa13在日本晴葉片內的表達水平(圖8)。這種相反的影響在XopN基因敲除(ΔXopN)的情況下便不再發生,但在ΔXopN遺傳回補(ΔXopN/XopN)以后,又重新出現(圖8)。這說明XopN對病菌促進顯性基因OsSWEET11/Xa13表達,抑制隱性基因OsSWEET11 /xa13表達起重要作用。
如前所述,與IRBB13和日本晴一樣,IRBB208和Asominori對PXO99A的敏感性也受病菌 XopN控制(圖 4~7)。但是,IRBB208和 Asominori是否擁有顯性或隱性OsSWEET1基因,文獻和網絡數據庫均無記錄。由于PXO99A的毒性和XopN的影響在日本晴上與在IRBB208和Asominori上的效果相似(圖 4和圖 7),我們推測,IRBB208和 Asominori可能也含有顯性基因OsSWEET1/Xa13,這一設想隨即得到實驗支持。根據日本晴 OsSWEET1/Xa13基因 cDNA序列(登錄號 AK070510)設計可以擴增該基因 cDNA全長的一對引物(表 4)。這對引物用于RT-PCR,對IRBB208和Asominori在PXO99A接種前后分離的 RNA樣本進行擴增,均能得到約為1500bp的產物。該產物經過回收、測序,測到的序列與OsSWEET1/Xa13基因cDNA序列完全相同。又根據 IRBB13隱性抗病基因 OsSWEET1/xa13的DNA 序列(登錄號 DQ421394.1),選取最長的第 5個也是最后一個外顯子(3701-4453bp),設計可以覆蓋此區全長的一對引物(圖 4)。這對引物用于RT-PCR,擴增來自IRBB208和Asominori的RNA樣品,得到約為750 bp的產物。該產物經過回收、測序,測到的序列與OsSWEET1/xa13基因DNA序列第5個外顯子序列完全相同。顯而易見,IRBB208和 Asominori擁有 OsSWEET11同源基因。由于IRBB208和Asominori感病性同日本晴相近,但顯著高于 IRBB13(圖 4)。我們推測,IRBB208和Asominori的OsSWEET11同源基因屬于顯性感病基因。然后,我們發現,PXO99A接種 IRBB208和Asominori以后,大幅度提高了這兩個水稻品種的OsSWEET11同源基因在各自葉片內的表達水平(圖8)。這一作用在XopN基因敲除(ΔXopN)的情況下便不再發生,但在ΔXopN 遺傳回補(ΔXopN/XopN)以后,又重新出現(圖 8)。因此,對病菌促進OsSWEET11同源基因在IRBB208和Asominori葉片內表達的這一反應,XopN起重要作用。
2.6 XopN影響Xoo誘發煙草HR的能力
為了明確XopN是否影響Xoo誘發煙草HR的能力,我們將純水制備的 PXO99A、ΔXopN、ΔXopN/XopN 3個菌株的細菌懸浮液分別注射煙草葉片,純水注射葉片用作對照(control),在12~36 h期間觀察煙草HR反應情況。到12 h,煙草葉片所有注射部位均未出現HR反應。到24 h,對照區域無HR反應,注射了PXO99A或ΔXopN/XopN菌懸液的部位已經出現明顯的HR反應,而在注射接種ΔXopN菌懸液的區域,HR反應較微弱。36 h后,注射ΔXopN菌懸液的區域也出現了明顯的HR反應(圖9-A)。這說明XopN基因敲除延遲HR反應的發生。另外,煙草葉片用PXO99A菌懸液注射以后,在12 h之內出現了微敏反應,但用ΔXopN菌懸液注射的葉片,未見發生(圖9-B),說明XopN影響病菌誘發煙草HR發生的程度。
3 討論
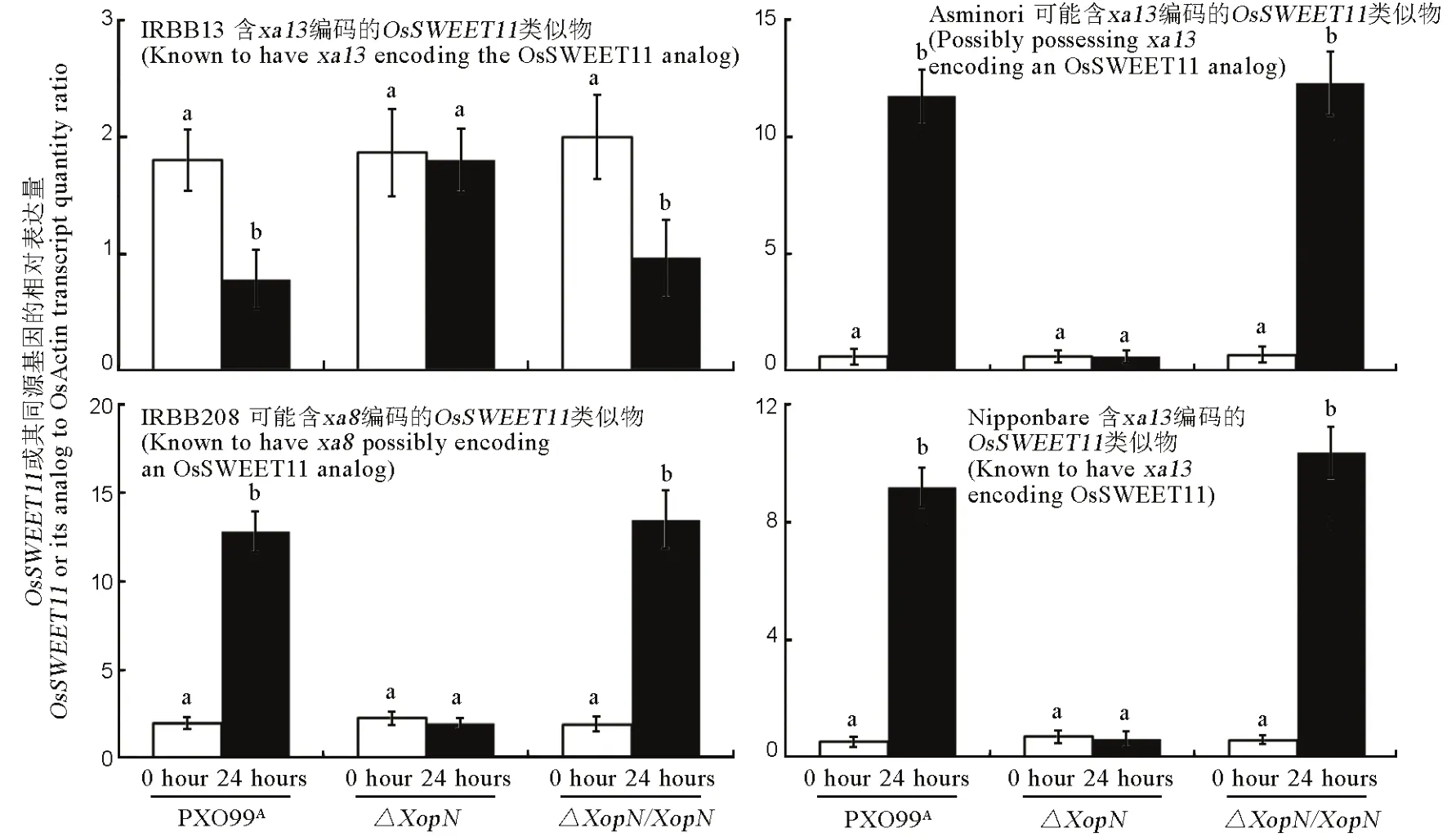
圖8 XopN對OsSWEET11或其同源基因在水稻4個品種葉片內表達水平的影響Fig. 8. Effects of XopN on expression levels of OsSWEET11 or its analogs in leaves of the 4 rice varieties.
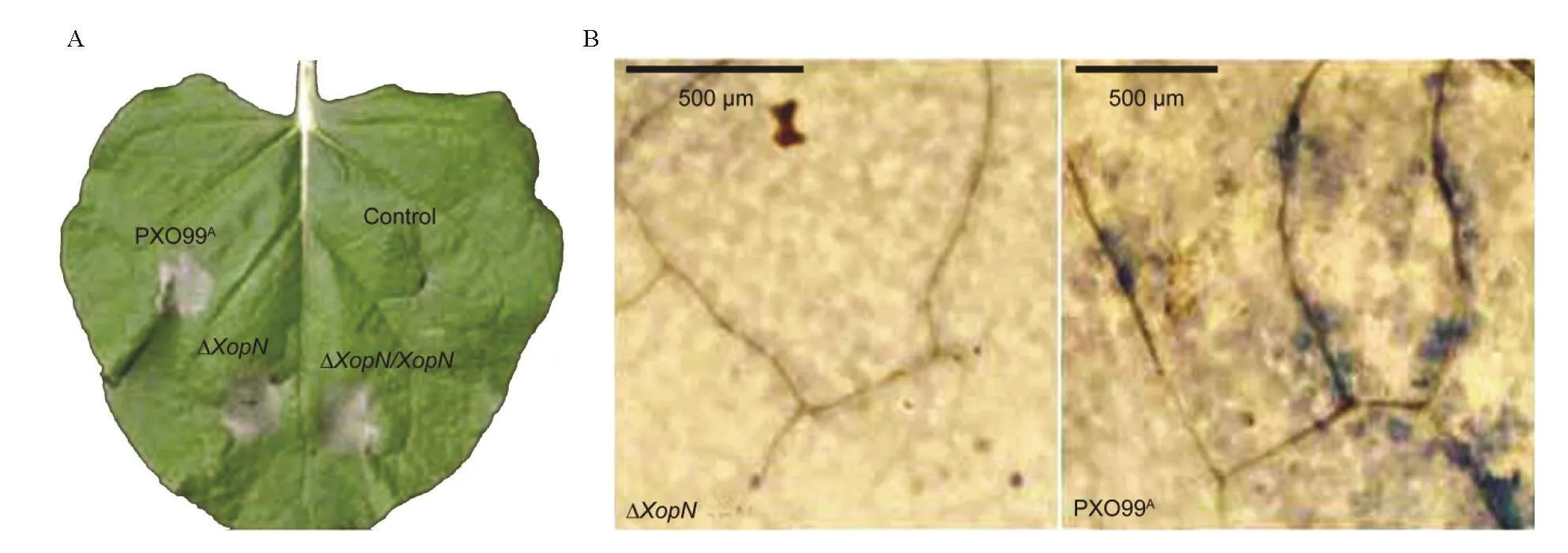
圖9 XopN對Xoo誘發煙草葉片過敏反應的影響Fig. 9. Effect of XopN on the ability of Xoo to induce hypersensitive response in tobacco leaves.
在本研究之前,中國植物病理學學者宋從鳳教授和美國同行學者楊兵教授通過合作,從Xoo菲律賓菌株PXO99A鑒定了18種Xop效應子[42],中國植物病理學學者馮家勛教授課題組又從水稻黃單胞菌水稻致病變種中國菌株13751鑒定出9種Xop[43],但是,病理功能得到研究的只有兩種。一是XopZ,它在水稻品種IR24上具有毒性作用,通過原核表達獲得的蛋白外施于本氏煙上以后,大幅度減少胼胝質在葉片表面的沉積量[42],說明XopZ能夠抑制植物基本防衛反應[44]。二是XopR,它部分決定中國菌株13751對水稻品種特優63的低毒性,但不影響IR24的感病性[43]。另外,還有來自Xoo非洲菌株MAFF311018的XopR,病理功能通過擬南芥轉基因的病理效應得到部分解析,在表達ZopR基因的擬南芥轉基因系上,PTI受到抑制[45]。根據這些研究,聯系上文引言部分援引關于不同病菌不同Xop在不同植物上病理功能的文獻[20-25],我們對Xop效應子的了解還相當貧乏,既缺少不同Xop功能機制的知識,又亟需探討不同水稻品種對特定Xop的病理反應,明確某一特定的Xop發揮毒性作用的專化性程度。
本研究解析了PXO99A對14個水稻品種的毒性和XopN所發揮的作用。根據病菌野生型菌株PXO99A、XopN敲除突變體ΔXopN和回補菌株ΔXopN/XopN在水稻葉片內的繁殖量和引起白葉枯癥狀的嚴重程度,XopN作為一個有限廣譜性(pluripotent)效應子發揮作用,在水稻4個品種而非供試的所有14個品種上行使毒性功能,它也是Xoo培養繁殖的必要因子,對病菌在非寄主植物上誘發抗病防衛反應(HR)[44]還有增效作用。無獨有偶,與病菌效應子功能對應的植物抗病或感病基因,例如OsSWEET1/Xa13,也表現出“有限多效(pluripotent)”的功能特征[9-13,40],既是水稻對白葉枯病感病性的決定因子[9-11,13,35],又參與花藥和種子發育調控[46]。附帶一筆,“多能性(multipotent)”、“亞全能性(pluripotent)”、“全能性(totipotent)”通常用來區分干細胞的發育潛能,從限于長成特定的而非全部的組織、器官,或限于某些生理過程,到產生所有胚胎細胞類型,再到產生所有胚胎和胚外細胞類型[47]。
推而廣之,這些界定用于病菌效應子和植物抗病或感病基因或蛋白質也相當有意義[44]。正如本研究所指,XopN的毒性功能指向部分而非全部供試水稻品種。1)攜帶隱性抗病基因OsSWEET11/xa13的IRBB13[31,36],在這個水稻品種上,PXO99A顯示弱毒性,但XopN對病菌毒性的貢獻卻高達70%以上。2)攜帶顯性感病基因OsSWEET11/Xa13的日本晴,是典型的白葉枯病感病品種,在此水稻品種上,PXO99A有高毒性[33-36],而XopN對病菌毒性的貢獻卻只有30%左右。3)攜帶OsSWEET11/Xa13同源基因的IRBB208和Asominori,同源基因尚未發現進行功能測定,缺乏遺傳和生理生化方面的實驗證據,所以指稱“同源基因”而非“顯性感病基因”。對IRBB208和Asominori,PXO99A也顯示高毒性,XopN對病菌毒性的貢獻率在40%左右。這些結果簡單而有趣,說明了XopN和OsSWEET11功能機制的復雜性。此處要義是,它們的功能機制有助于思考和解答POX99A的XopN為什么能在上述4個水稻品種上發揮毒性作用這一問題。
先看XopN,案例見于Xcv-番茄互作體系。在侵染番茄的過程中,Xcv分泌的XopN定位于番茄細胞膜與細胞質界面,與番茄非典型性受體型激酶TARK1互作[48]。在酵母細胞中,這個XopN還能同番茄14-3-3蛋白質的4個同源異構體(TFT1、TFT3、TFT5、TFT6)發生互作[48]。在番茄細胞內,TFT1是XopN的靶標,二者相結合,而TFT1又能結合TARK1,形成的TARK1/TFT1復合體可能為XopN發揮毒性功能提供合適的平臺結構[25]。在此之前,XopN經由病菌T3分泌途徑而運輸,到達細菌-植物細胞界面,但必須繼續前進,直到在植物細胞膜上定位。病原細菌效應子如果在植物細胞內發揮作用,例如PXO99A的TALE蛋白質PthXo1,它就必須從細菌細胞轉入植物細胞[9-12],這種轉運過程(translocation)需要病菌T3轉位子(translocon)的幫助[9-13,49]。T3轉位子由親水性和疏水性蛋白質組成,執行底物轉運功能對拓撲學結構的一個基本要求就是,轉位子蛋白質必須經由植物細胞膜上的蛋白質和脂類受體的識別作用,進而定位到植物細胞膜上或插入其中[11,49]。根據在動物病原細菌上的研究,T3轉位子蛋白質有三種,但對植物病原細菌,迄今還沒有在哪個種群(種/species、致病變種/pathovar、菌株/strain等)上鑒定出三種轉位子蛋白質[11,49]。最近,我們發表了從2003年開始研究Xoo效應子轉運調控機制的部分結果,證明Xoo的T3分泌系統輔助因子Hpa1蛋白質作為疏水性轉位子蛋白質起作用[12],幫助病菌效應子PthXo1從Xoo細胞轉入水稻細胞,PthXo1進而調控它的靶標基因OsSWEET11表達,誘發白葉枯病[9-10]。同其他植物病原細菌一樣,Xoo還沒有第二個轉位子蛋白質得到鑒定。但有研究表明,植物病原細菌某種T3蛋白質如果定位到植物細胞膜,它就有可能擔當T3轉位子組分和毒性/無毒性效應子這種雙重功能[49-50]。根據XopN定位于植物細胞膜[48]及其功能的“亞全能性(pluripotent)”,我們推測,除了毒性效應子的作用,XopN還可能擔當T3轉位子蛋白質的功能。對此假設,我們的研究現已接近收官,可望對XopN的“亞全能性”提供一種解釋。
再看OsSWEET11,研究集中在黃單胞菌致病性與水稻抗病性機制方面。顯性感病基因Xa13編碼的OsSWEET11/Xa13能與銅轉運載體蛋白質COPT1和COPT5合作,調節銅離子在植物細胞間的重新分布,把銅離子移出木質部,免除它對細菌的毒害,病菌得以繁殖、擴展、致病[53]。除了蛋白質功能調控,基因轉錄調控也有重要作用。顯性感病基因Xa13而非隱性抗病基因xa13的啟動子區內的“效應子結合元件(effector-binding elements,EBEs)”是PthXo1的靶標[41,51],PthXo1因此可以靶向OsSWEET11/Xa13基因,進而發揮毒性作用[35]。相反,OsSWEET11/xa13啟動子區內的EBEs存在突變,拒絕TALEs結合,導致植物抗病性,這可能是IRBB13對白葉枯病防衛反應的一種機制[32]。
根據上述XopN與OsSWEET11在轉錄調控和轉錄后調控水平上的作用機制,在PXO99A誘導隱性感病基因OsSWEET11/Xa13及其同源基因表達或抑制顯性感病基因OsSWEET11/xa13表達的過程中,XopN可能按三種模式參與調控。1)作為T3轉位子蛋白質,幫助PthXo1從細菌細胞向植物細胞轉運,PthXo1隨后按上述機制發揮毒性作用,尤其是激活顯性感病基因OsSWEET11/Xa13表達[41,51]。2)按此方式,EBEs存在突變、拒絕TALEs結合[32]的隱性抗病基因OsSWEET11/xa13的誘導表達自然受到抑制。3)XopN具有毒性效應子兼T3轉位子蛋白質的雙重功能,與其他轉位子組分(如Hpa1[12])合作,實現轉運,功能靶向PTI[25,48]。對這三種模式的設想,需要通過實驗加以驗證。

