血清CYP2R1含量對慢性乙肝患者病毒載量及抗病毒的療效研究*
李鳳中,陳衛國,劉劍榮,陳小林
(江西省萍鄉市人民醫院,1.檢驗科;2.肝病科,萍鄉 337055)
乙型肝炎病毒(HBV)感染呈世界性流行,有超過3.5億人是HBV的慢性攜帶者[1]。目前尚無可有效治療慢性乙型肝炎(CHB)的藥物。當前臨床可用的藥物包括具有抗病毒活性和抑制HBV DNA 的核苷(酸)類似物[2],如恩替卡韋[3],但大多數患者需要終身治療[4]。因此除了抗病毒藥物之外,尋找輔助性治療CHB的藥物尤為重要。25-羥維生素D3[25(OH)D3]由維生素D3前體在肝細胞內經25-羥化作用合成,這個過程由兩種羥化酶催化,其均是細胞色素 (Cytochrome P450 proteins,CYP)的同工酶[5],分別為肝細胞微粒體羥化酶CYP2R1和線粒體羥化酶CYP27A1,而正常情況下CYP2R1在合成25(OH)D3中發揮主導作用[6]。有研究表明,CHB患者血清25(OH)D3含量與HBV DNA水平呈負相關[7,8]。也有研究表明,對CHB患者補充維生素D可以提高患者的抗病毒治療效果,提示維生素D在CHB患者的抗病毒治療可能發揮重要作用[9]。目前有關維生素D3合成酶CYP 2R1與CHB患者體內HBVDNA水平的關系及其對抗病毒治療效果的影響尚少見報道。本研究旨在探討CHB患者血清CYP2R1含量與恩替卡韋治療后的抗病毒效果之間的關系。
1 資料與方法
1.1 研究對象 選擇2016年9月-2017年9月就診于我院的CHB患者100例,其中男55例,女45例,年齡 21-52歲,平均(40.6±2.6)歲。所選患者均符合中華醫學會肝病學分會和感染病學分會2015年制訂的 《乙型肝炎防治指南》中CHB的診斷標準。納入標準:⑴患者乙肝表面抗原 (HBsAg)陽性≥6個月;⑵年齡>18歲;⑶既往未接受過抗病毒藥物或者干擾素治療。排除標準:⑴失代償肝硬化(Child-Pugh)評分>6分;⑵肝癌或者甲胎蛋白(AFP)>50ng/ml;⑶患其他肝臟疾病或細菌感染;⑷惡性腫瘤或者嚴重的慢性疾病。
1.2 方法
1.2.1 治療方法 給予CHB患者恩替卡韋(恩替卡韋片,南京正大天晴)常規治療,每次0.5 mg,每天1次,治療12個月后停用,在治療前及治療期間的第6個月和第12個月時收集患者靜脈血5ml,分離血清后及時檢測HBV DNA含量及肝功能生化指標。
1.2.2 實驗室常規指標檢測 乙肝病毒學指標乙肝表面抗原(HBsAg)、乙肝表面抗體(HBsAb)、乙肝e抗原(HBeAg)、乙肝e抗體(HBeAb)、乙肝核心抗體(HBcAb)采用免疫發光法檢測,所用儀器及試劑盒均購自羅氏公司,儀器為羅氏CobasE411;試劑盒為HBsAg定性試劑盒 (批號:168216-04)、HBeAg定量試劑盒(批號:169476-01),按照試劑盒說明書進行操作。血清CYP2R1含量采用酶聯免疫吸附法(ELISA)檢測,試劑盒購自上海江萊生物科技有限公司(JL20581-96T),按照試劑盒說明書進行操作。肝功能指標血清谷草轉氨酶(AST,IFCC速率法)、谷丙轉氨酶(ALT,IFCC速率法)、總膽紅素(TBiL,重氮鹽法,STB070)等采用生化儀貝克曼庫爾特AU5800生化儀檢測,試劑盒購自北京利德曼生化股份有限公司。
1.2.3 血清HBVDNA檢測 采用實時熒光定量PCR法對患者血清中HBV DNA進行定量檢測。檢測試劑為中山大學達安基因 (PCR-熒光探針法)HBV DNA試劑盒(貨號DA0031)最低檢測限值為500 IU/ml,分離血清后將200μl血清樣本與450μl DNA提取液混合,置于100℃溫育器中預熱10min。反應總體積 20μl,SYBR Green Master 10μl,上下游引物各 2μl,血清 DNA 模板 2μl,RNase-free H2O補足至20μl,將定量所需試劑加入后,輕彈混勻后離心,按照如下反應體系進行:95℃預變性5min;95℃變性 15s,60℃退火 30s,72℃延伸 30s,共 35 個循環,最后維持4℃。引物序列達安基因試劑盒中提供。設置陰性對照、弱陽性與強陽性對照、陽性標準品對照。所有操作均嚴格按照說明書執行。
1.3 統計學方法 實驗數據采用SPSS17.0軟件進行統計分析。計量資料以均數±標準差(±s)表示,組間比較采用獨立樣本t檢驗,組內多時間點比較采用重復測量設計的方差分析。計數資料以例(%)表示,組間比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 不同血清CYP2R1含量患者的基線資料比較根據患者中位血清CYP2R1含量 (26.5 ng/L),把CYP2R1>26.5 ng/L分為CYP2R1高濃度組 (50例)和 CYP2R1<26.5 ng/L為低濃度組(50例)。CYP2R1高濃度組患者 25(OH)D3水平高于CYP2R1 低濃度組(P<0.05),兩組患者性別、年齡、身體質量指數(BMI)、Child-Pugh評分差異均無統計學意義(P>0.05),見表1。

表1 2組患者基線資料比較
2.2 不同濃度CYP2R1的CHB患者治療后肝功能的變化 2組患者治療前、治療6個月、治療12個月AST、ALT和TBiL水平依次降低,組間多重比較差異均有統計學意義(P<0.05);各時間點2組間差異均無統計學意義(P>0.05),見表2。
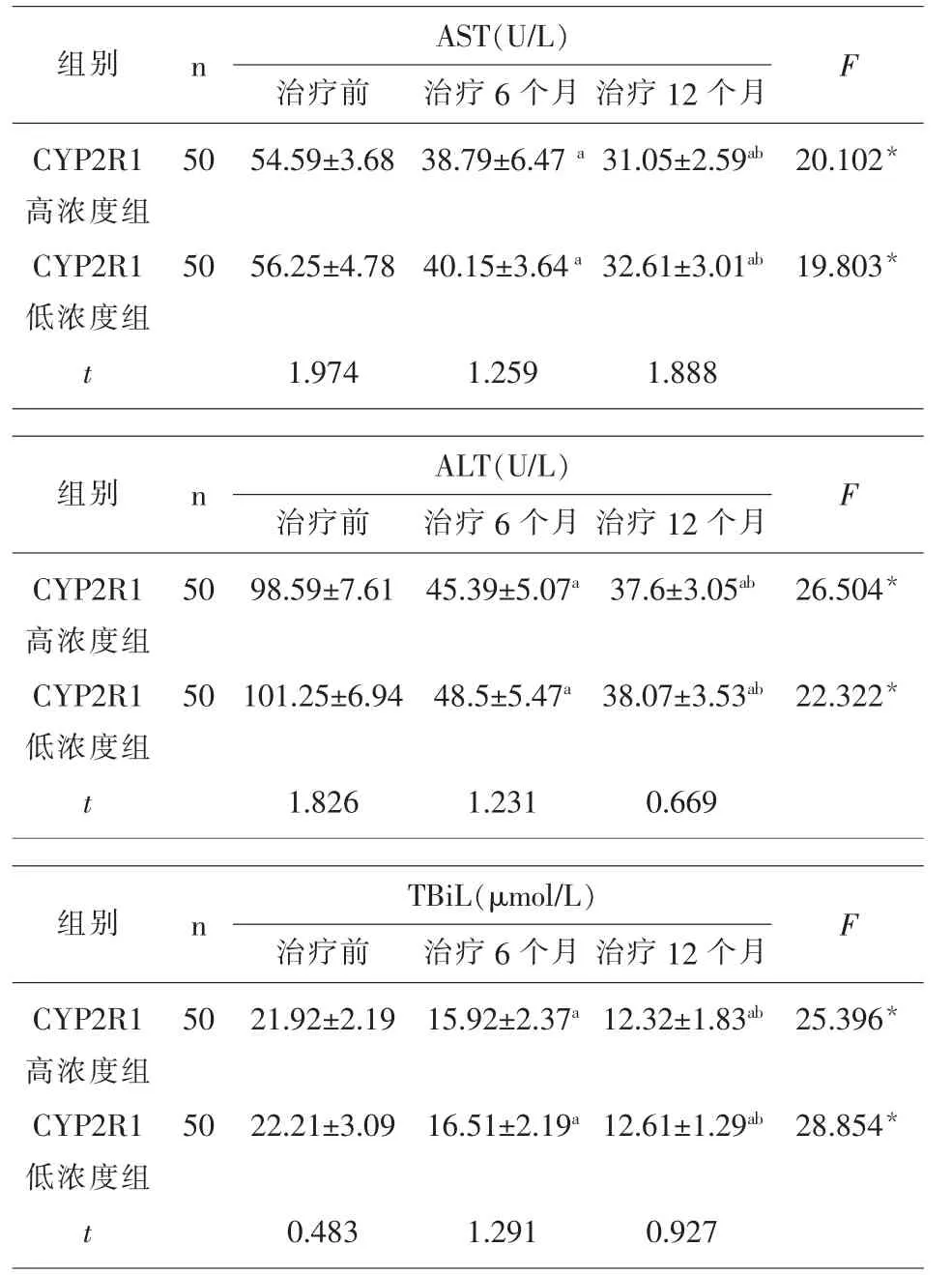
表2 恩替卡韋治療前后2組CHB患者肝功能指標比較
2.3 不同濃度CYP2R1的CHB患者抗病毒治療后HBV DNA含量改變 2組患者治療前、治療6個月、治療12個月病毒載量HBV DNA依次降低,組間多重比較差異均有統計學意義 (P<0.05);治療前,2組病毒載量HBV DNA差異無統計學意義,治療6個月和12個月時,CYP2R1高濃度組均低于 CYP2R1 低濃度組(P<0.05),見表3。

表3 2組患者治療后病毒載量HBV DNA的變化
3 討論
在HBV通過體液入侵機體后,造成肝臟組織慢性炎癥感染的過程中,病毒因素、環境因素及宿主本身因素均在此過程中起重要作用[10]。大量的臨床試驗和臨床薈萃分析均顯示,患者維生素D缺乏與CHB感染病情發生進展有關[11],維生素D合成障礙或維生素D缺乏均是促進CHB慢性病理炎癥發生的因素之一[12]。有研究報道,體內維生素D缺乏的CHB患者,通常都伴隨著高乙肝病毒載量(HBV DNA含量高),而且維生素D含量高的患者治療結局會優于水平較低者[13]。研究還發現補充維生素D與抗病毒治療手段聯合應用時,可顯著提高機體的免疫應答率,提示維生素D可用于抗病毒治療[14]。機體25(OH)D3的含量與其代謝酶的關系密切[15]。25(OH)D3由維生素D3前體在肝細胞內經25-羥化作用合成,主要由CYP2R1酶催化。CHB患者25(OH)D3降低不僅與維生素D3的合成原料不足[16],也與肝細胞合成維生素D相關代謝酶的活性下降、表達減少、線粒體損傷有關[17]。目前的報道都是僅針對患者血清維生素D3的含量與HBV在體內復制致病的相關性及其對抗病毒治療的作用。而對于機體本身維生素D的合成和代謝在CHB發生發展中的作用尚不明確。
本研究結果顯示,2組患者治療前、治療6個月、治療12個月病毒載量HBV DNA依次降低,且治療6個月和12個月時,CYP2R1高濃度組均低于CYP2R1低濃度組,提示CHB患者血清CYP2R1濃度可能與患者病毒DNA復制情況呈負相關,與Zhao等[18]研究結果一致。但是血清CYP2R1含量對CHB患者治療后肝功能指標AST、ALT和TBiL并沒有差異,提示血清CYP2R1含量是影響CHB患者HBV DNA的因素之一,其機制可能是通過影響維生素D的合成,進而影響患者體內的乙肝病毒復制,而不影響宿主的本身肝功能水平。和本研究的結果一致,有相關的研究表明乙肝患者的CYP2R1的水平與患者肝功能AST、ALT和 TBiL等指標沒有關聯,但是和患者的HBV DNA水平由呈負相關,具體的作用機制并不清楚[19]。
最近大規模的全基因組關聯研究結果顯示,血清CYP2R1含量與基線25(OH)D3水平相關[20]。本研究結果顯示,使用恩替卡韋抗病毒治療12個月后,CYP2R1高濃度組HBsAg、HBeAg陽性率均低于CYP2R1低濃度組,CYP2R1高濃度組患者能更好地獲得病毒學應答,提示血清CYP2R1水平可能與CHB的發病機制以及抗病毒治療的病毒學應答有關,而且是通過影響維生素D3合成而產生的作用。有研究顯示,在HBV感染初期,HBV攜帶者體內25(OH)D3的含量與健康人相比無明顯變化,但是其羥化酶CYP2R1含量已出現異常[21],在此基礎上,隨著肝病進展至失代償期肝硬化階段,25(OH)D3含量降至最低[11]。但是是否因HBV感染引起肝細胞功能受損,導致羥化酶CYP2R1降低,目前尚不明確,有待進一步研究驗證。

