基于治療前磁共振影像組學預測鼻咽癌誘導化療的療效
江海濤 王方正 邵國良 劉璐璐 阮磊 龐佩佩
鼻咽癌是一種特殊類型的頭頸部惡性腫瘤,主要發生在東南亞國家、北非、中歐[1],2018年全球新增病例約129,079,死亡72,987人,其中47.7%發生在中國[2]。放射治療是鼻咽癌的主要治療手段[3],對于局部晚期鼻咽癌最新的NCCN指南推薦的標準療法為同步放化療加誘導化療或輔助化療。誘導化療(induction chemotherapy,IC)能縮小原發病灶與頸部轉移淋巴結,為調強放療計劃制定時降低危及器官劑量,同時也能顯著降低局部晚期鼻咽癌的復發率[4]。本文探討基于磁共振影像組學特征參數與鼻咽癌誘導化療敏感性的相關性,揭示影像組學預測鼻咽癌誘導化療療效的可行性。
1 資料與方法
1.1 臨床資料 收集2016年1月至12月本院病理檢查證實為非角化性局部晚期鼻咽癌患者27例,男20例,女7例;年齡22~70歲。所有患者同步放化療前行>2周期誘導化療,采用TP方案:順鉑(75mg/m2)聯合多西紫杉醇(75mg/m2),每周期間隔21d。(1)納入標準:①經鼻咽鏡證實為非角化性癌;②接受>2個周期的TP方案誘導化療;③化療前1個月內曾行鼻咽部磁共振增強檢查,且圖像清晰無假牙偽影等影響;④治療前MR圖像鼻咽部原發占位病灶可測量(>10mm)。(2)排除標準:①患者既往曾接受抗腫瘤治療;②復發鼻咽癌;③有心內科的嚴重疾病。
1.2 方法 (1)分組:誘導化療2周期后3周內復查鼻咽MR和鼻咽鏡,對比基線鼻咽MR評價誘導化療的療效。根據RECIST 1.1標準評估療效[5],完全緩解(CR):靶病灶消失;部分緩解(PR):與治療前基線靶病灶直徑相比減少>30%;部分進展(PD):靶病變直徑相比基線時直徑總和增加>20%,穩定(SD):對比治療前基線靶病灶達不到PR也達不到PD標準。誘導化療后經MR評估為PR或CR者13例納入敏感組,評估為SD或PD14例納入不敏感組。(2)MR掃描方案:所有患者均使用3.0TMR掃描儀(Verio3.0T,Siemens Medical Solutions,Germany)頭頸部線圈進行鼻咽和頸部區域對比增強MR檢查。軸位T1WI快速自旋回波圖像[重復時間(TR)450ms;回波時間(TE)8.8ms,90°翻轉角;256×168矩陣,層厚4mm;層間距0.8mm],T2WI軸位自旋回波MR圖像(TR6000ms;TE95ms;90°翻轉角;256×168矩陣;層厚4mm;層間距0.8mm)和T2加權脂肪抑制的自旋回波序列(TR6360ms;TE95ms;90°翻轉角;256×168矩陣;層厚4mm;層間距0.8mm)。靜脈推注造影劑歐乃影(0.5mmol/ml)15ml,速率1.5ml/s,造影劑推注完成后,推注15ml生理鹽水,速率1.5ml/s,20s后行軸位T1WI快速自旋回波序列(具體參數同軸位T1WI參數)。(3)磁共振組學分析:①圖像分割:從本院PACS上搜索每個病例誘導化療前鼻咽部MR檢查并保存CE T1WI序列的DICOM格式圖像,使用ITK-SNAP軟件導入DICOM格式圖像,由2名放射科副主任醫師協商后選取鼻咽部原發腫瘤最大層面,手動沿不均質強化腫瘤邊緣勾畫出靶病灶ROI,盡量避開頸動脈等大血管、出血及壞死囊變區域,分割出單層腫瘤圖像(見圖1)。②特征參數的提取和預處理:使用AI-Kit 軟件對26例誘導化療前分割出的ROI圖像進行特征計算提取。特征參數計算方式包括5類,分別為一階統計特征、二階紋理特征、灰度共生矩陣(GLCM),灰度梯度共生矩陣(GLGCM),小波轉換(wavelet transform)共396個定量參數。為保證數據間的可比性,先將不同量級的數據轉為同一量級進行數據預處理,步驟為:奇異值nan使用中值代替;對每一個紋理特征進行Z-Score標準化,計算公式為(參數值-均值)/標準差,具體如下(μ均值,σ為標準差,N為病例數):

圖1 磁共振組學圖像分割圖
1.3 統計學方法 采用SPSS 20.0軟件。計量資料以()表示,采用獨立樣本t檢驗,計數資料用卡方檢驗。以P<0.05為差異有統計學意義。提取的參數分5大類396個,如果將所有這些參數一起評估會造成過擬合,且不相關和冗余的參數會混淆學習算法[6],因此采用R語言進行統計分析。通過ANOVA/KW檢驗、單因素邏輯回歸和去冗余(r>0.9)來篩選特征參數,對篩選出的參數按敏感性分組進行多元邏輯回歸建模,繪制受試者操作特性曲線(ROC),計算曲線下面積(AUC),繪制交互式點圖得到兩組間分界值,敏感性,特異性。
2 結果
2.1 一般資料比較 入組27例患者,均為局部晚期鼻咽非角化性癌,誘導化療敏感組13例,男10例,女3例;年齡39~68(56.23±10.21)歲。不敏感組14例,男10例,女4例,年齡22~70(53.57±14.51)歲。敏感組與不敏感組間治療前年齡、性別比較差異無統計學意義(P>0.05)。
2.2 影像組學特征參數分析 使用AI-kit軟件提取共396個定量MR影像組學特征,從中篩選出2個紋理特征參數,分別為135度集群陰影-步長4(clustershade_angle135_offset4)和全角度相關性方差-步長 1(correlation_alldirection_offshe1_SD),135度集群陰影-步長4的AUC為0.804(95%CI 0.602~0.932),全角度相關性方差-步長1的AUC為0.762(95%CI 0.556~0.905),聯合兩個紋理特征邏輯回歸后建模(combine)的 AUC 為 0.905(95%CI 0.724~0.984),分界值為0.4525時,敏感度85.7%,特異度為83.3%(見圖 2~5)。
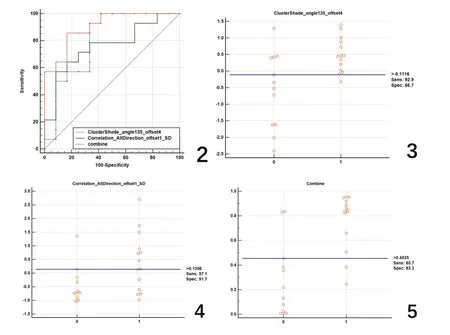
圖2 定量組學特征clustershade_angle135_offset4、correlation_alldirection_offset1_SD和兩個組學特征邏輯回歸后建模(combine)ROC曲線,AUC分別為0.804(95%CI 0.602~0.932)、0.762(95%CI 0.556~0.905)、0.905(95%CI 0.724~0.984);圖3 組學特征參數clustershade_angle135_offset4敏感組和不敏感組分界值為-0.01116,敏感度為92.9%,特異度66.7%;圖4 組學特征參數correlation_alldirection_offshe1_SD敏感組和不敏感組分界值為0.1356,敏感度為57.1%,特異度91.7%;圖5 combine(聯合兩個紋理特征邏輯回歸后建模)敏感組和不敏感組分界值為0.4535,敏感度為85.7%,特異度83.3%
3 討論
鼻咽癌誘導化療在鼻咽癌治療過程中起著重要的作用,然而,并不是所有鼻咽癌患者都對誘導化療有效,大約<50%的患者對IC敏感[7-8]。鼻咽癌誘導化療前預測患者的治療敏感性有較大的臨床價值,因為治療是否有效能夠作為鼻咽癌預后獨立預測因子。Liu等研究發現誘導化療后是否敏感可以作為晚期鼻咽癌患者的預測指標[9],Hao等報道腫瘤對IC的反應是4年無疾病生存期(DFS)、總生存率(OS)和局部無復發生存率(LRRFS)的獨立因素[8]。同時接受不敏感的誘導化療增加患者的經濟負擔,增大毒副作用,且延誤后期治療方案的實施。然而目前缺乏有效的生物標記預測鼻咽癌誘導化療的療效。
2012年Lambin等[10]首次提出影像組學的概念,旨在通過機器學習的方法,提取大量的定量參數,用以評價腫瘤的異質性。影像組學可通過高通量自動化數據分析發掘與量化影像特征,提取與腫瘤生物學行為相關的放射組學特征;可以支持腫瘤檢測、診斷、療效評價、腫瘤進展狀況的無損傷和可重復性檢查;在輔助鑒別腫瘤組織、判斷腫瘤療效、預后等方面的臨床應用前景良好,對腫瘤精準醫療的發展具有重要意義。已有的研究表明,影像組學能夠反映腫瘤的異質性,反映基因層面的信息,在肺癌等腫瘤基因突變、治療效果、預后等方面預測有大量的研究及廣泛應用,并顯示其生物標記的優勢[11],而鼻咽癌療效預測及早期評價的研究大多基于磁共振擴散加權成像[12],Yen等[13]在誘導化療后的早期行全身PET-CT再分期,通過再分期后的降期為I及II期患者對比未降期患者,無復發生存期和總生存期顯著延長,PET-CT再分期可以幫助預測誘導化療療效。但這些標記應用在鼻咽癌誘導化療的療效預測仍有爭議。最近,有研究將基于MR的影像組學應用于鼻咽癌同步放化療反應的預測和生存預后的關系[14]。MR具有較高的軟組織分辨率、多參數及多平面成像等優點,成為目前臨床上鼻咽癌的首選檢查方法,用于治療前分期,療效評估及治療后復查。
本結果顯示,鼻咽癌原發腫瘤的紋理特征及灰度共生矩陣這兩個特征參數在誘導化療后敏感組與不敏感組間的差異有統計學意義。clustershade_angle135_offset4為紋理特征,描述了腫瘤的表面情況,光滑或粗糙,correlation_alldirection_offset1_SD屬于灰度共生矩陣,具有方向性,反映圖像中不同灰度像素分布的相似性、對稱性以及各像素間的空間位置關系,從而反映腫瘤內部細節的差異程度是影響誘導化療療效的重要因素。影像組學特征參數是根據體素排列計算的數學測量值,可以表征腫瘤空間中體素排列的異質性[15],另一方面,腫瘤異質性可能是與區域腫瘤細胞的增殖,血管生成以及壞死相關,甚至在一定程度反映基因層面相關信息[16]。MR圖像上的組學特征可以通過腫瘤空間中體素的排列反映腫瘤的異質性,而異質性可能是與療效和預后相關的因素。
研究表明,三維分析能夠更完整的反映腫瘤組織的異質性[17],但三維分析更為復雜和耗時,且因為磁共振層厚為4mm,導致邊緣部分會受部分容積效應的影響,在手動勾畫病灶的頭尾側邊界時難以把握病灶的邊界。Lubner等研究顯示三維(VOI)和二維(ROI)影像組學分析結果間差異無統計學意義,表明基于單層二維ROI組學分析結果是可信的[18]。因此,作者采用單層二維ROI組學分析,但進一步探討三維組學分析在鼻咽癌患者誘導化療療效預測中的潛在價值仍舊具有重要意義。
本研究局限性:(1)納入分析的樣本量較少未能設置數據驗證,可能會使結果產生一定的偏倚;(2)本研究為單中心研究,使用單一的MR掃描儀器,未能區分不同中心不同MR掃描儀的預測效能。今后研究需要擴大樣本量,并設置驗證組,同時需要擴大樣本量及多中心前瞻性研究以建立可重復性及準確度更高的預測模型。
總之,本研究篩選出兩個影像組學特征并建立預測組學預測模型,證實這個模型能夠較好的預測鼻咽癌患者對誘導化療的敏感性。這個模型作為一種基于MR組學的影像生物標志物,可以為臨床提供一種新的方法來預測誘導化療的療效,指導鼻咽癌的個體化治療。

