基于網絡藥理學探討太子參、赤芍治療糖尿病合并冠心病的作用機制
灑曉亮,高之苑,張 蘭
糖尿病(diabetes mellitus,DM)是由于胰島素分泌缺陷或胰島素功能障礙而導致的一組以高血糖為特征的內分泌代謝性疾病[1]。隨著現代社會的發展,糖尿病病人數量呈逐年增加的趨勢。根據一項流行病學調查顯示,糖尿病病人的心血管病發病率均高于非糖尿病病人,且與其年齡、性別等無關[2]。糖尿病合并冠心病作為糖尿病常見的心血管病變之一,同時也是導致糖尿病病人死亡的重要原因。中醫認為飲食失調、七情內傷、年邁體虛等因素皆可以導致其發生發展,臨床上多采用益氣養陰、活血化痰去瘀之法對其進行治療。
太子參又名孩兒參、童參等,是石竹科植物孩兒參的干燥塊根,具有益氣健脾、生津潤肺之功效,可降糖、降脂,并且對心肌細胞有明顯的保護作用。赤芍為毛茛科植物芍藥或川赤芍的干燥根莖,可清熱涼血、散瘀止痛,具有抗動脈粥樣硬化、抗血栓、降糖等作用,臨床上常重用其治療冠心病。太子參與赤芍兩藥配伍,益氣活血,可從根本上治療糖尿病合并冠心病。
網絡藥理學(network pharmacology,NP)是一門基于系統生物學理論和多向藥理學理論,以整體性、系統性為研究特點,分析生物系統網絡并選取特定信號節點,進行多靶點藥物分子設計的新學科。網絡藥理學可用于預測或推斷小分子與基因、蛋白質、代謝物等靶點和網絡的相關性,進而構建“藥物-靶點-疾病”相互作用網絡,全面系統地闡明藥物對疾病的干預和影響,為中藥現代化的研究提供了新的思路與方向[3]。本研究應用網絡藥理學的方法,探討太子參、赤芍兩味中藥治療糖尿病合并冠心病的作用機制,旨在為其臨床和基礎研究提供新的科學依據。
1 資料與方法
1.1 中藥化學成分及靶點信息的獲取 通過中藥系統藥理學數據庫與分析平臺TCMSP(http://lsp.nwsuaf.edu.cn/tcmsp)收集太子參、赤芍兩味中藥的全部化學成分,選取同時滿足口服吸收率(OB)≥30%、類藥性(DL)≥0.18、半衰期(HL)≥4 h的化學成分作為其潛在的活性成分。并通過有機小分子生物活性數據庫PubChem(https:// pubchem.ncbi.nlm.nih.gov/)以及查閱文獻獲得這些成分的化學結構,將其保存為Smiles格式。將篩選出的潛在活性分子Smiles結構導入Swiss Target Prediction數據庫(http://www.swisstarget-prediction.ch/),限定研究對象為人類(homo sapiens),由此獲得與活性成分最相關的靶點信息。采用Uniprot 數據庫(http://www.uniprot.org/)對靶點蛋白的名稱進行標準化,挖掘太子參、赤芍兩味中藥的活性成分所對應的作用靶點。
1.2 疾病靶點的篩選 在TTD(http://www.genecards.org/)數據庫、DisGeNET數據庫(http://www.disgenet.org/web/ DisGeNET/menu)和OMIM數據庫(http://www.omim.org/)中,分別搜索疾病關鍵詞為糖尿病、冠心病,合并3個數據庫結果,去除重復和假陽性靶點,篩選出糖尿病、冠心病相關的疾病靶點。
1.3 中藥-疾病靶點網絡構建及核心靶點的篩選 為明確糖尿病合并冠心病的疾病相關靶點與太子參、赤芍兩味中藥的潛在靶點之間的相互作用關系,將疾病相關靶點與中藥相關靶點進行交集,應用Venny軟件(http://bioinfogp.cnb.csic.es/tools/venny/index.html)對糖尿病靶點、冠心病靶點與太子參、赤芍兩味中藥的作用靶點繪制韋恩圖,篩選出中藥活性成分-疾病共同作用靶點。將篩選得到的共同作用靶點在STRING平臺(https://string-db.org/)構建蛋白-蛋白相互作用(protein-protein interaction,PPI)網絡模型,其中蛋白種類設置為“Homo sapiens”,“highest confidence”設定為 >0.9,其他參數保持默認設置不變,獲得中藥-疾病共同作用靶點的PPI網絡,導出文件。并將該文件中node1、node2和Combined score信息導入Cytoscape軟件得到網絡分析結果,同時利用“Network Analyzer”模塊分析PPI網絡的拓撲屬性參數,計算整體網絡的“節點度值分布(node degree distribution)和介數中心性(betweenness centrality)”。度值(degree)和介數(betweenness)是判斷網絡節點重要性的兩個主要拓撲參數,度值和介數越大,節點在該網絡就越重要。本研究選取度值和介數同時在中位數以上的靶點為“核心靶點”,研究核心靶點可能的作用機制。
1.4 靶點生物功能注釋及通路分析 為進一步闡明上述篩選出的核心靶點基因的生物學功能以及在信號通路中的作用,通過Cytoscape軟件的ClueGO插件對核心靶點進行GO-BP生物功能富集分析,探索太子參、赤芍治療糖尿病合并冠心病核心靶點的生物學過程。并利用DAVID平臺(https://david. ncifcrf.gov/),輸入核心靶點基因,選擇Pathway分析中KEGG Pathway,設定顯著性為P<0.05,進一步尋找中藥-疾病核心靶點的KEGG(KEGG pathway analysis)代謝通路。應用Cytoscape軟件繪制核心靶點-信號通路-生物功能互作網絡。
2 結 果
2.1 太子參、赤芍主要活性化合物及靶點的篩選 通過TCMSP數據庫檢索,以及對其ADME中 OB≥30%、DL≥0.18和HL≥4 h進一步篩選,共收集6個太子參活性化合物,25個赤芍活性化合物。化合物詳細信息見表1。將活性化合物的Smiles格式上傳到Swiss Target Prediction,篩選出418個太子參作用靶點、1 124個赤芍作用靶點,充分體現了太子參、赤芍多成分、多靶點的作用機制。通過對太子參、赤芍的作用靶點進行匯總,去除重復靶點,發現太子參和赤芍共有靶點451個。
2.2 太子參、赤芍與糖尿病合并冠心病共同作用靶點的選擇 通過對 TTD、DisGeNET 和 OMIM 數據庫進行檢索,共獲得糖尿病的相關疾病靶點1 802個、冠心病的相關疾病靶點1 188個。將451個太子參和赤芍共有作用靶點與1 802個糖尿病相關疾病靶點和1 188個冠心病相關疾病靶點輸入Venny軟件繪制韋恩圖,三者取交集后獲得太子參、赤芍與糖尿病合并冠心病共同作用靶點173個。詳見圖1。
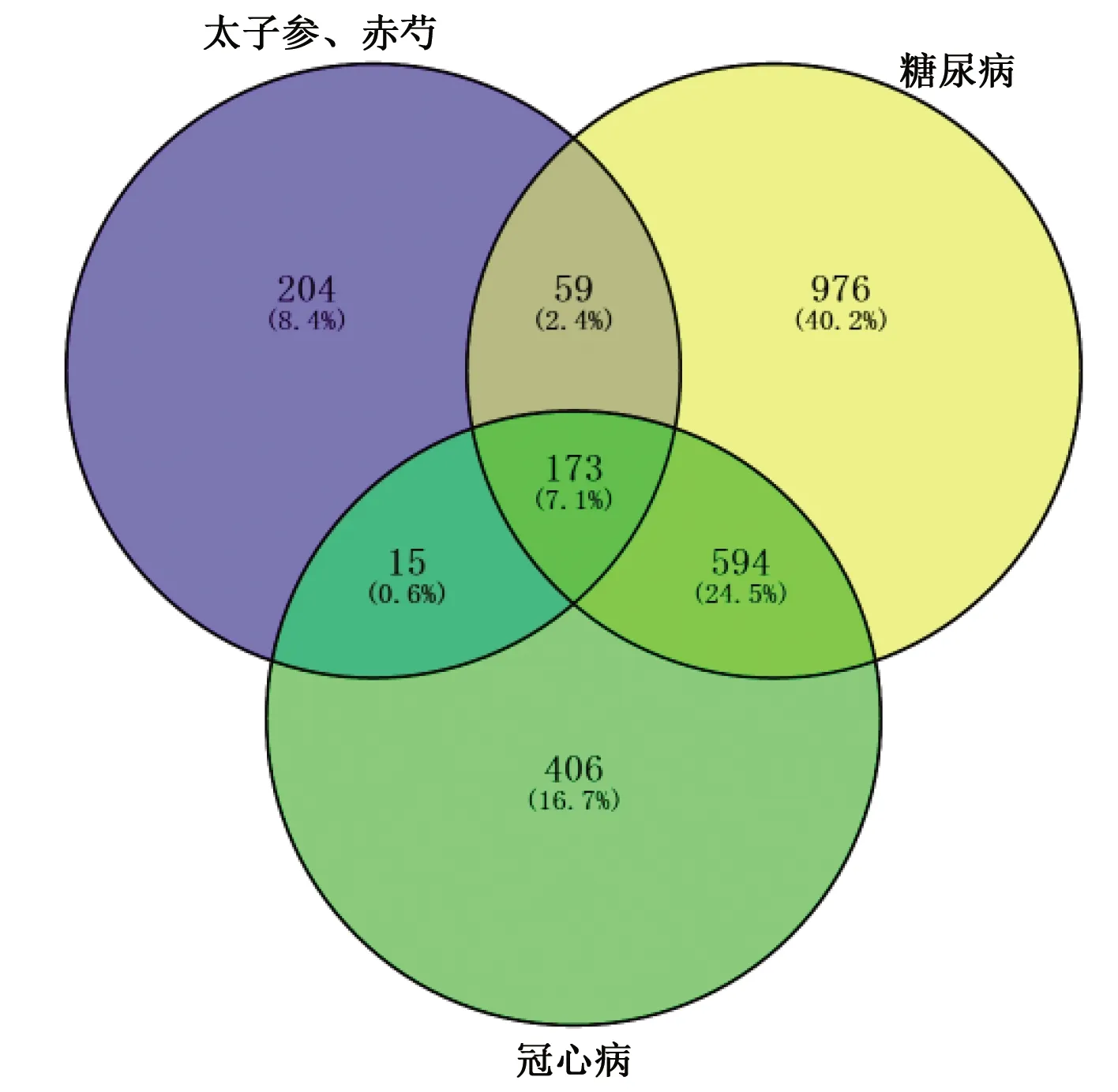
圖1 太子參、赤芍與疾病共同作用靶點韋恩圖
2.3 PPI網絡與核心靶點分析 將上述共同作用靶點導入String數據庫得到PPI互作網絡圖,詳見圖2。圖中共有173個相互作用節點、694條邊。利用Cytoscape軟件對網絡中所有點的拓撲參數(度和介度中心度)進行分析,拓撲參數值大于中位數,即度≥6、介數中心度≥1.83×10-2,作為篩選核心關鍵靶點的條件,共篩選出49個核心靶點。包括血管內皮生長因子A(VEGFA)、轉錄激活因子-3 (STAT3)、過氧化物酶體增殖激活受體-γ(PPARG)、絲氨酸/蘇氨酸激酶1(AKT1)、類固醇受體輔激活因子(SRC)、維甲酸類受體α(RXRA)、1-磷酸鞘氨醇受體1(S1PR1)等。
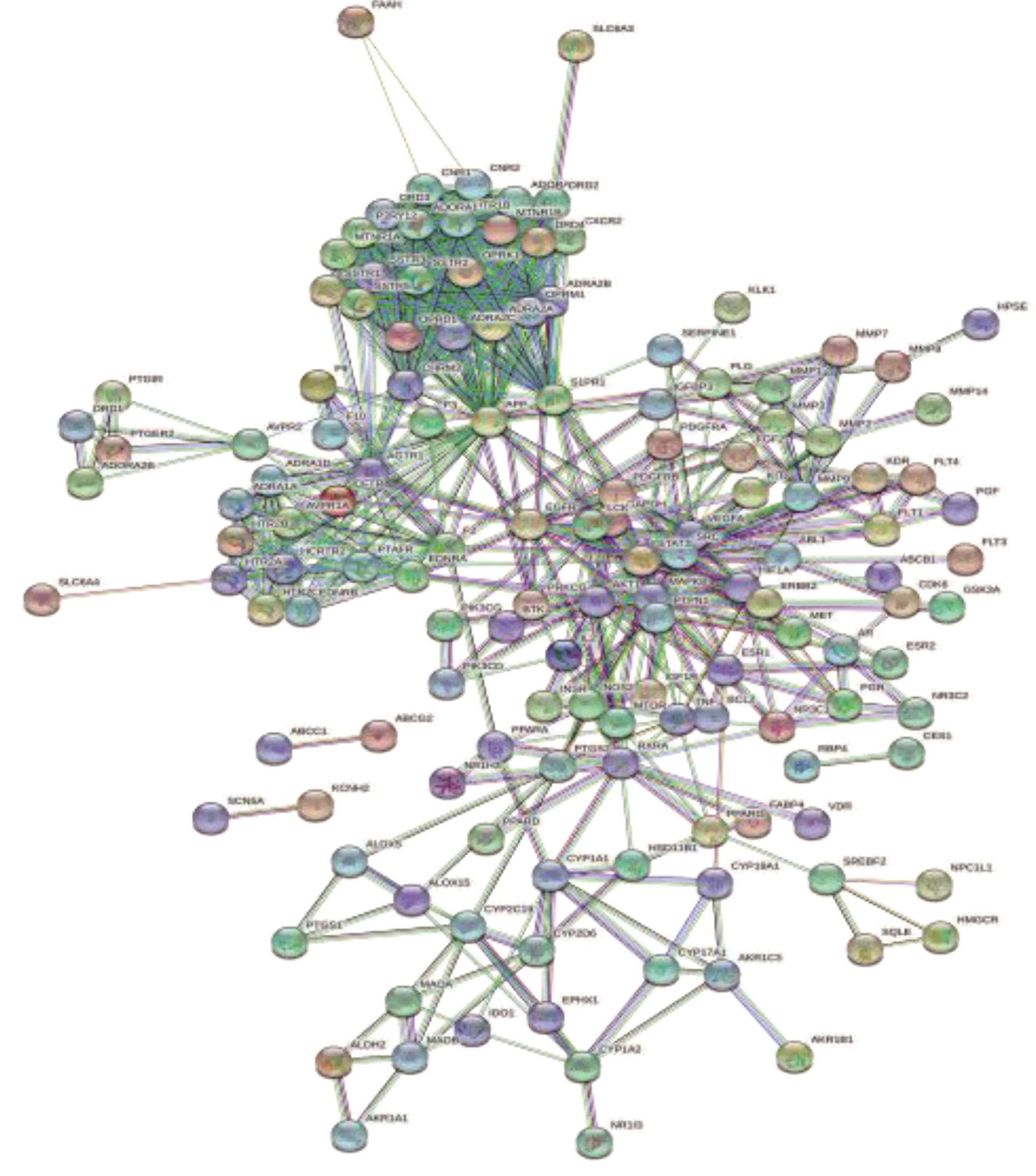
圖2 共同作用靶點的PPI網絡
2.4 核心靶點生物功能富集分析與KEGG通路分析 利用Cytoscape軟件的ClueGO插件對篩選出的49個核心靶點進行GO-BP生物學功能富集分析,可見多個生物學功能與糖尿病合并冠心病的發生發展關系密切,其主要富集于對脂多糖的反應(response to lipopolysaccharide)、活性氧物質代謝過程(reactive oxygen species metabolic process)、循環系統中的血管過程(vascular process in circulatory system)、肌肉細胞增殖(muscle cell proliferation)、血液循環調節(regulation of blood circulation)、ERK1和ERK2級聯調節(regulation of ERK1 and ERK2 cascade)、血管收縮(vasoconstriction)、蛋白偶聯受體信號通路、偶聯環核苷酸第二信使(G-protein coupled receptor signaling pathway,coupled to cyclic nucleotide second messengerg)、平滑肌細胞增殖的調節(regulation of smooth muscle cell proliferation)以及血壓調節(regulation of blood pressure)。詳見圖3。
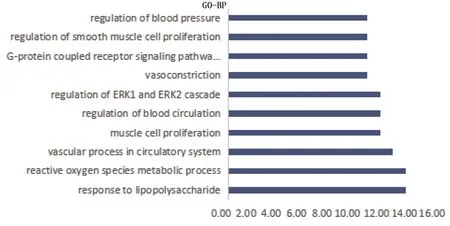
圖3 核心靶點GO-BP功能信息
利用DAVID平臺對篩選出的49個核心靶點進行KEGG通路分析,獲得與核心靶點相關代謝通路38條,篩選出與糖尿病合并冠心病有關通路,結果表明太子參、赤芍可能主要通過脂肪細胞因子信號通路(adipocytokine signaling pathway)、ErbB 信號通路(ErbB signaling pathway)、間隙連接通路(gap junction)、焦點黏附通路(focal adhesion)、過氧化物酶體增殖物激活受體(PPAR)信號通路(PPAR signaling pathway)、血管內皮生長因子(VEGF)信號通路(VEGF signaling pathway)、促黃體生成素釋放激素(GnRH)信號通路(GnRH signaling pathway)等發揮治療作用,詳見圖4。并利用Cytoscape軟件構建太子參與赤芍核心靶點-生物功能-信號通路網絡,詳見圖5。
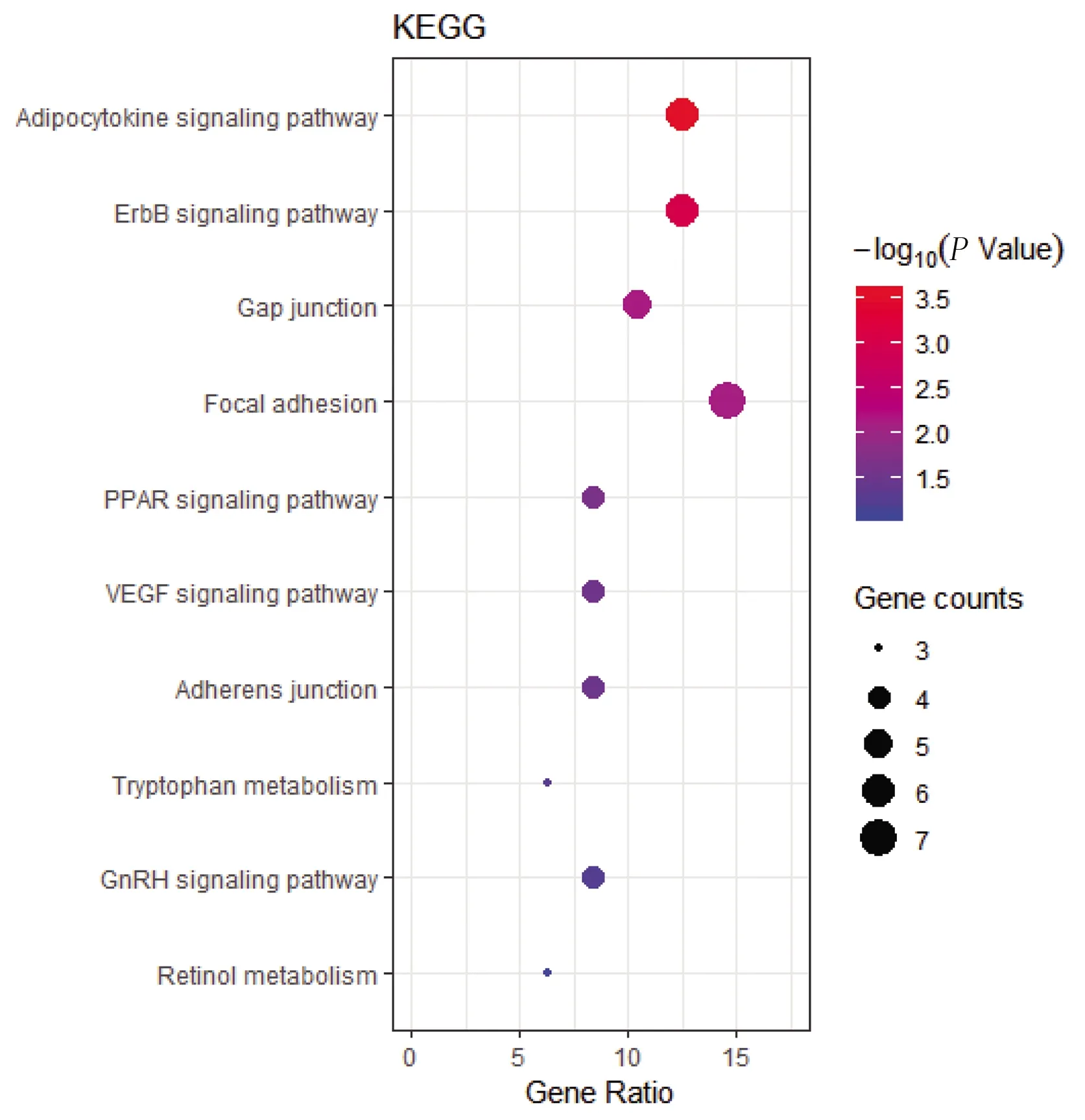
圖4 核心靶點KEGG通路分析

圖5 太子參與赤芍核心靶點-生物功能-信號通路網絡(紫色節點為核心靶點;綠色節點為KEGG信號通路;粉色節點為主要生物功能)
3 討 論
中醫學根據糖尿病病人多飲、多食、多尿、消瘦的臨床表現,將其歸屬于“消渴”“消癉”“三消”等范疇,其首見于《素問·奇病論》:“此人必數食甘美而多肥也,肥者令人內熱,甘者令人中滿,其氣上溢,轉為消渴”[4]。根據冠心病病人胸部悶痛,甚則胸痛徹背,背痛徹心,喘息不得臥等臨床表現,將其歸屬于“胸痹”“心痛”等范疇。《靈樞·五邪》中 “邪在心,則病心痛”[4]是對其最早的記載。現代醫家基于古籍中“消渴”“胸痹”的記載,提出了“消心病”“糖心病”等病名[5]。《靈樞·本臟》中云:“心脆則善病消癉熱中”[4]。漢代張仲景在《傷寒論》中曾提出“消渴,氣上撞心,心中疼熱”。宋代巢元方在《諸病源候論》中論述其為:“消渴重,心中痛”[6]。以上皆說明消渴常累及于心,心中痛為消渴之重癥,糖尿病與冠心病二者之間關系密切,常合而為病。對于其病因病機,歷代醫家認為是因為氣陰兩虛日久引起痰濁血瘀痹阻心脈所致。臨床上糖尿病病人多以氣陰兩虛為主,血為氣之母,氣為血之帥,氣虛則無力推動血液運行,血不行則成瘀;陰虛則燥熱,日久灼津煉液生痰,津液枯竭,進而形成血瘀,瘀血痹阻心脈,導致冠心病的發生。同時痰濁、血瘀也會反過來加重氣血、津液的虛損,使糖尿病合并冠心病病情加重,纏綿難愈。因此,在治療上多應用益氣養陰、活血化痰去瘀之法對其進行治療。太子參味甘、微苦,性平,歸脾、肺經,可益氣健脾、養陰生津,常用于治療脾虛食欲不振、困倦乏力或病后虛弱、氣陰不足、津傷口渴等癥。赤芍味苦,性微寒,歸肝經,具有清熱涼血、散瘀止痛等功效,可用于治療冠心病、心絞痛、急慢性肝炎等疾病。
本研究基于網絡藥理學技術,挖掘太子參、赤芍治療糖尿病合并冠心病的核心靶點,分別構建了太子參-赤芍的主要活性成分-靶點網絡以及太子參-赤芍主要活性成分-核心靶點-生物功能-信號通路的共表達網絡,從多個角度探索了太子參、赤芍兩味中藥治療糖尿病合并冠心病的作用機制。通過對太子參、赤芍主要活性成分及篩選作用靶點,共得到太子參6個、赤芍25個活性成分和451個作用靶點。通過對疾病靶點的篩選,共獲得糖尿病靶點1 802個、冠心病靶點1 188個。三者取交集后得到共有靶點173個,充分體現了中藥多成分、多靶點的治療特點。通過構建PPI蛋白互作網絡以及核心靶點的篩選,得到49個核心靶點,其中相關活性最高的靶點基因有VEGFA、STAT3、PPARG、AKT1、SRC等。VEGFA是VEGF信號通路的重要調節因子,可啟動內皮細胞增殖、分裂和遷移,從而誘導血管生成,有利于病變血管內膜的修復,維持內膜完整性,在血管內皮損傷機制中發揮著重要的作用[7-8]。STAT3是JAK/STAT3信號通路的重要組成部分[9],JAK/STAT3信號通路是細胞因子信號轉導的調節劑,可用于多種應激反應,包括缺血、缺氧和氧化應激,在介導胰島素抵抗(IR)損傷心肌保護中發揮著重要作用。PPARG主要參與脂肪組織中脂質攝取和脂肪形成相關基因的轉錄激活,其基因突變可引起IR[10]。AKT1可以調控胰島素PI3K-AKT信號通路[11],SRC與胰高血糖素的調節有關[12]。
現代研究表明,糖尿病病人引起冠心病并發癥皆是由于糖與脂的代謝紊亂、血管內皮功能障礙、高血壓等導致[13]。GO-BP生物功能富集分析發現,太子參、赤芍的核心靶點中有14個靶點參與了脂多糖的調節,14個參與了活性氧物質的代謝過程,12個參與了血液循環的調節,11個參與血管收縮的調節,從而共同發揮治療糖尿病合并冠心病的作用。KEGG通路富集分析發現太子參、赤芍可通過脂肪細胞因子信號通路、ErbB 信號通路、間隙連接通路、焦點黏附通路、PPAR信號通路、VEGF信號通路、GnRH信號通路等發揮治療作用。糖尿病病人的血清中脂肪因子表達水平較高,其對糖脂代謝、胰島素分泌和心血管功能均有一定的調控作用[14-15]。ErbB 信號通路在維持心功能中發揮著重要作用,在心臟組織中神經調節蛋白-1(NRG-1)可結合ErbB4受體,與ErbB2受體形成異源二聚體,將受體C-末端上特定的酪氨酸殘基磷酸化,從而激活PI3K/Akt信號通路[16-17]。既往研究發現PPARG配體有胰島素致敏作用且與氨基酸代謝有關[18]。2010年10月20日美國食品藥品監督管理局(FDA)發出公告稱GnRH激動劑類藥物可導致心血管病和糖尿病的發生率升高[19],說明GnRH信號通路與糖尿病合并冠心病的發生有著重要聯系。太子參中含有多糖類、皂苷類、脂肪酸類、甾醇類等化學成分[20],王琪等[21]研究發現太子參中太子參多糖成分可通過改善胰島素信號通路,減輕氧化應激反應,從而抑制胰島素抵抗和炎癥信號的轉導,起到改善糖代謝紊亂的作用。赤芍中含有單萜類、多糖、有機酸等化學成分,現代藥理學研究表明其具有抗血小板聚集、抗血栓形成、抗動脈粥樣硬化、降低血糖的作用[22]。
綜上所述,本研究運用網絡藥理學的技術和方法,從多角度挖掘太子參、赤芍治療糖尿病合并冠心病的作用機制,體現了中藥多靶點、多通路的治療特色,符合中醫藥現代化的發展要求,為后續的臨床與基礎研究提供了新的思路。

