子宮動脈栓塞術治療有異常供血的剖宮產瘢痕妊娠臨床研究
張 偉, 王莉杰, 王 覓
剖宮產瘢痕妊娠(cesarean scar pregnancy,CSP)屬一類特殊且高風險異位妊娠,其自然發展會使孕婦面臨危及生命的出血、子宮破裂和子宮切除風險,盡管最終會有57%活產率,但其中63%產婦需要切除子宮[1]。因此一旦診斷為CSP應給出終止妊娠醫學建議,并盡早清除妊娠物[2]。目前子宮動脈栓塞術(uterine artery embolization,UAE)輔助下各式妊娠物清除術,已逐漸成為早期CSP治療的主流方案和常規策略[3-5]。為妊娠囊供血的靶動脈完全栓塞是UAE治療成功與否的關鍵因素[6]。CSP主要供血血管為子宮動脈,目前對于其異常供血的報道并不多。本研究對有異常供血的CSP患者UAE治療效果進行探討,旨在提高臨床療效和認識,確保產婦安全。
1 材料與方法
1.1 一般資料
收集鄭州市第一人民醫院2012年6月至2019年6月間92例接受UAE術CSP患者臨床和DSA影像資料。患者年齡20~42歲,中位年齡31歲;停經時間 34~118 d,平均(57.39±20.55) d;入院時 21例有下腹部疼痛,28例有陰道出血,48例無任何不適;經歷1次剖宮產42例,2次47例,3次3例;2例既往有CSP病史,分別于3年、5年前接受UAE和清宮術;首次剖宮產至此次確診CSP時間為10個月至18年,中位時間7年。患者入院時血清β-人絨毛膜促性腺激素(β-HCG)值為 465.20~134 583.41 mU/mL,均高于正常范圍。患者CSP均由經腹和經陰道超聲檢查確診,妊娠囊最大徑為6~82 mm,中位值為32 mm;妊娠囊與膀胱間子宮肌層厚度為1~9 mm,48例≤3.0 mm;均無“子宮肌瘤”、“子宮腺肌病”診斷。所有患者入院1~3 d后接受UAE。
1.2 手術方法
經右股動脈引入5 F豬尾導管(美國Cook公司)至腹主動脈腎動脈水平,DSA造影了解髂內動脈開口部位置和卵巢動脈顯影情況;5 F Cobra導管(美國Cook公司)送入左髂內動脈,造影顯示子宮動脈開口部位置和走行;5 F Cobra導管或以同軸導管技術引入2.7 F微導管(日本Terumo公司)并送入子宮動脈,造影顯示妊娠囊血供,經導管灌注甲氨蝶呤(MTX)35 mg,遂以 560~710μm 粒徑明膠海綿顆粒(杭州艾力康醫藥科技公司)栓塞子宮動脈,直至動脈分支完全栓塞,主干內對比劑流動緩慢;復查左髂內動脈造影,明確有無其他血管參與妊娠囊供血,如有異常供血則超選擇插管并栓塞;導管成襻后送入右髂內動脈,以上述方法行血管造影、藥物灌注和栓塞。
1.3 分析方法
根據92例患者DSA影像分析,其中15例妊娠囊有除子宮動脈以外的異常供血(A組)(表1),77例無異常供血(B組)。比較兩組UAE術后24 h血清β-HCG下降程度、術中大出血、輸血率、UAE后住院時間、血清β-HCG轉陰時間、UAE操作時間和月經恢復時間。根據UAE術后24 h血清β-HCG下降程度(與術前相比),分為下降幅度<20%組和≥20%組。參照Wang等[7]研究報道,術中大出血定義為清除妊娠囊術中有活動性出血,且出血量≥200 mL。
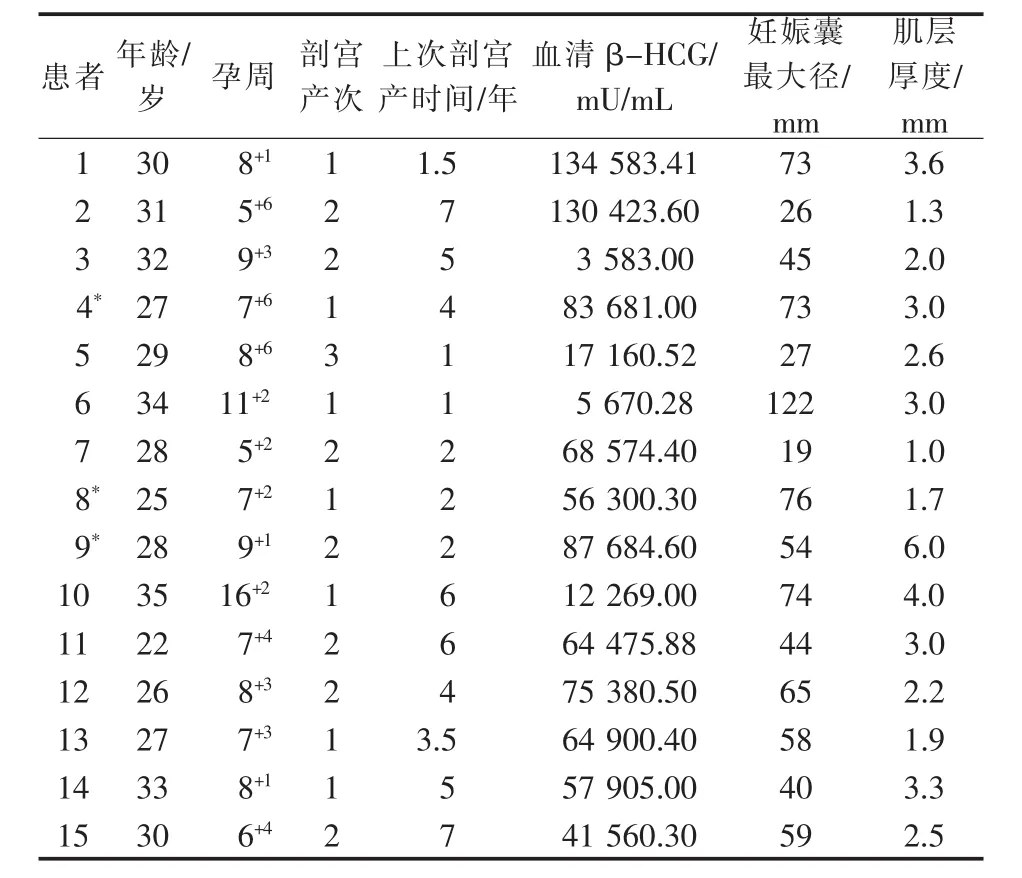
表1 15例妊娠囊有異常供血CSP患者一般資料
1.4 統計學方法
采用SPSS 19.0軟件作統計學分析。正態性檢驗用Explore法,正態分布的計量資料以均數±標準差(x±s)表示,計數資料以例表示,A、B 兩組間 UAE后住院時間、血清β-HCG轉陰時間、UAE操作時間和月經恢復時間對比用獨立樣本t檢驗,術后24 h血清β-HCG下降程度、術中大出血、輸血率對比用精確Fisher檢驗,P<0.05為差異有統計學意義。
2 結果
A、B組UAE術技術成功率均為100%。A組妊娠囊異常供血血管分布于左側4例,右側6例,雙側5例;20支異常供血血管中18支為膀胱動脈,1支為陰部內動脈,1支未能明確來源,其中16支成功完成超選擇性插管并栓塞(圖1),4支超選擇性插管失敗后改行髂內動脈前干栓塞。A、B組均未見卵巢動脈參與妊娠囊供血。89例于UAE術后1~13 d接受清除妊娠囊手術(表2),術中出血5~1 400 mL,無子宮切除事件發生,3例(B組)拒絕接受術后治療,經門診超聲復查隨訪,均于3周內妊娠囊娩出,無陰道大出血等嚴重不良事件發生。A、B組間術中大出血、輸血率、UAE操作時間差異有統計學意義(P<0.05),UAE 后 24 h血清 β-HCG 下降程度、UAE后住院時間、血清β-HCG轉陰時間和月經恢復時間差異無統計學意義(P>0.05),見表3。
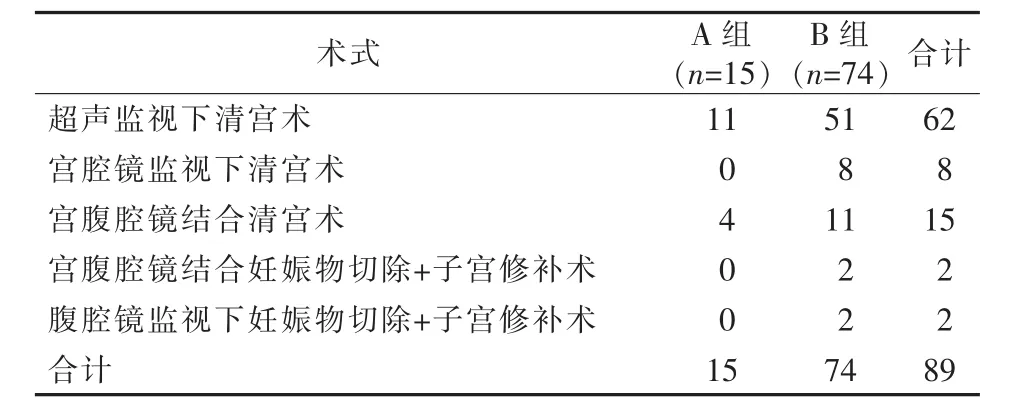
表2 UAE術后清除妊娠囊術式
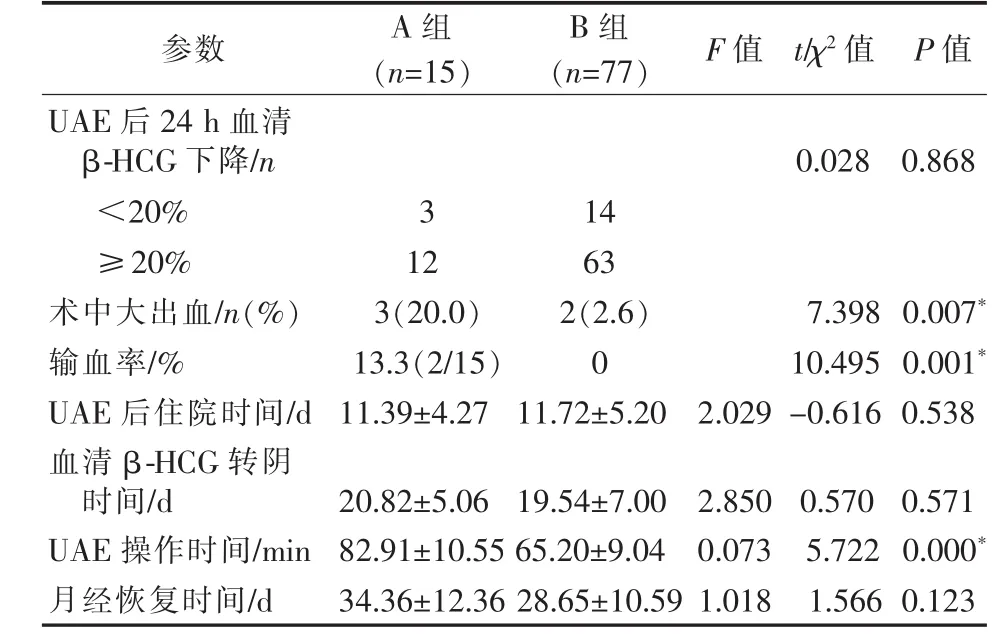
表3 A、B組臨床資料對比
3 討論
Larsen和Solomon 1978年首次報道CSP以來,這種與剖宮產密切相關的宮內異位妊娠危害性越來越受到關注。世界各地剖宮產率上升導致CSP增加[8],我國高剖宮產率雖得到一定程度控制[9],但人口基數大、二孩政策放開及高齡孕產婦增加所面臨CSP危害,日益顯現。
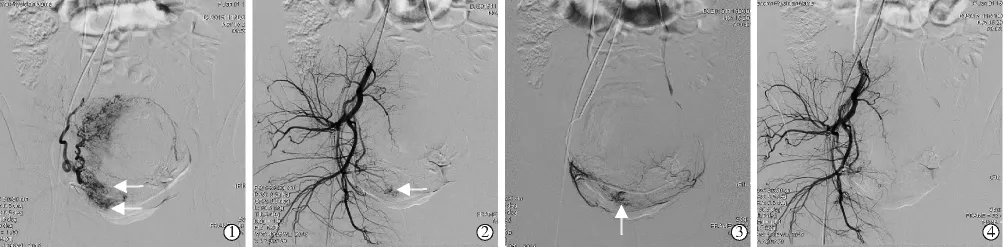
圖1 1例28歲CSP產婦成功完成超選擇性插管和栓塞影像
3.1 UAE治療CSP
CSP供血通常較普通肌層豐富,動脈在妊娠囊周圍環狀包繞病灶,妊娠囊周圍血流信號及其分級是 CSP 產婦出血的風險因素[1,10-11],血流分級越高,妊娠囊血供越豐富,出血風險越高。一些研究為指導CSP治療建立出血風險評分系統,均將妊娠囊血供豐富程度列為重要指標[7,12]。 CSP 終止妊娠、清除妊娠囊過程中最大風險是嚴重陰道出血,因此能否有效降低出血風險是CSP治療關鍵和前提。
UAE治療中超選擇性子宮動脈灌注MTX可極大地提高局部血藥濃度,有利于殺死胚胎并加速滋養葉細胞活性喪失,而明膠海綿顆粒栓塞子宮動脈可迅速阻斷妊娠囊血流,為后續清除妊娠囊手術降低嚴重出血風險創造有利條件。魯景元等[13]將492例CSP產婦分為高危組、低危組,根據是否UAE治療分別分為UAE組和非UAE組,多因素logistic回歸分析顯示,治療方法是CSP再發風險的獨立預測因素,采用包含UAE在內的綜合治療方法可降低CSP再發風險。
由于子宮動脈上行支存在卵巢供血及栓塞、X線輻射可引起子宮內膜缺血缺氧和放射性損傷,UAE術對產婦生育功能的影響存在一定爭議。但多數學者認為UAE術對卵巢功能影響很小,尤其是40歲以下產婦卵巢功能幾乎不受影響[14]。魏麗坤等[15]研究報道138例CSP,根據治療方式分為UAE+清宮術治療組、清宮術治療組、腹腔鏡治療組,其中50例有再生育要求,37例在隨訪時間內獲自然妊娠42次;認為CSP治療后自然妊娠率較滿意,且個體化治療方式對自然妊娠率無顯著影響。
3.2 CSP妊娠囊異常供血與UAE治療
有關CSP UAE術后清宮術中出血相關因素分析,可歸結為妊娠囊直徑>5 cm[16-17]、Ⅱ型 CSP[16]、孕齡[18]、妊娠囊與膀胱間子宮肌層厚度[18]、介入治療與清宮術時間間隔延長等因素[19]。異常供血血管未得到栓塞是原發性肝癌肝動脈化療栓塞治療失敗的重要原因,雖然目前并無大型研究證實CSP妊娠囊異常供血與陰道大出血間是否存在關聯,但對異常供血加以注意、提高認識很有必要。
An 等[6]研究報道 4 例(4/23)患者 UAE 術后 3周妊娠囊仍持續生長,遂行子宮切除術。這雖無直接依據,但作者提示卵巢動脈可能參與了妊娠囊供血。徐玉靜等[20]應用數字化三維模型分析5例CSP血供,發現2例由雙側子宮動脈和卵巢動脈共同供血,3例僅由子宮動脈供血。葉斌等[21]報道CSP側支動脈發生率為23.6%(34/144),其中76.5%(26/34)側支動脈起自髂內動脈;認為前置胎盤、盆腔炎癥、人流手術史及子宮肌瘤或腺肌癥,是CSP側支動脈形成的危險因素。本研究中CSP異常供血發生率為16.3%(15/92),異常供血來源多為膀胱動脈(90%,18/20),A、B 組間術中大出血、輸血率、UAE 操作時間差異有統計學意義,A組上述3項指標均高于B組。由于本研究樣本量小,難以對此進行相關因素研究,但對研究結果進行分析有以下提示:①有異常供血的CSP患者往往妊娠囊血供豐富、直徑較大(A組15例中12例直徑>30 mm,術中大出血3例均>50 mm),栓塞后易于出現側支循環建立,因此術中妊娠囊供血血管盡管已栓塞,仍需警惕清除妊娠囊術中大出血,術前需做好應對預案;②A、B組中5例清除妊娠囊術中大出血患者清宮時間均為UAE術后5~10 d,為避免止血效果降低,建議UAE后72 h內完成清除妊娠囊手術操作;③有異常供血的CSP患者UAE操作過程會顯著延長,因此出于對產婦卵巢功能的保護及術者放射線防護,有必要通過適當縮小透視光圈、低劑量透視和造影、應用路圖功能等方式減少放射線劑量和照射時間;④一側UAE結束后再行髂內動脈造影旨在評估子宮動脈栓塞程度,同時需關注有無異常供血血管,尤其是膀胱動脈和陰部內動脈,并注意多角度造影觀察,以避免因正位像血管重疊導致遺漏需栓塞的靶血管。
成功的UAE術不僅要栓塞子宮動脈,還要栓塞包括妊娠囊異常供血支在內的血管,以降低出血風險。UAE術在有異常供血的CSP治療中取得了滿意效果,但需要注意的是,UAE術后續清除妊娠囊手術過程中仍有大出血可能,需要加以重視,也需要對此開展進一步研究。

