煉鋼精煉渣氣固碳酸化反應吸附CO2
李志雄,李玲玲,陳 韌,史原鑫,王耀國,鄒宗樹
(1. 遼寧科技學院 冶金工程學院遼寧省本溪低品位非伴生鐵礦優化應用重點實驗室,遼寧 本溪 117004;2. 東北大學 冶金學院,遼寧 沈陽 110819)
伴隨著化石能源的消耗,CO2氣體不斷被排放到大氣中,導致溫室效應日益嚴重。2018年全球CO2平均質量濃度達到733.87 mg/m3,是1750年工業化前水平的147%。CO2濃度的持續增加可能導致極端天氣事件,且對人體健康產生危害[1-3]。CO2的捕集和儲存被認為是緩解全球性氣候變暖問題的有效途徑之一。
鋼渣是煉鋼生產中排出的大宗固體廢棄物。在日本和歐洲一些地區,約60%的鋼渣被用于道路工程[4]。我國對于冶金鋼渣資源綜合利用技術的研究起步較晚,目前鋼渣利用率僅為25%左右,如何提高鋼渣的資源綜合利用率是亟待解決的科學問題之一。鋼渣的主要化學成分包括CaO,SiO2,Al2O3,FeO,Fe2O3,MgO,MnO,P2O5[5-9],其中鈣鎂組分可以通過碳酸化反應固定CO2氣體,因此鋼渣可用于捕集CO2。
據報道,顆粒尺寸和反應溫度是影響鋼渣固定CO2反應過程中碳酸化反應速率的主要因素,減小顆粒粒徑有利于鋼渣中堿性氧化物與CO2充分接觸,提高CO2固定量,而反應溫度對CO2固定反應的影響機制因反應體系不同而有所區別[10-15]。目前,關于鋼渣對CO2固定反應的影響的研究報道較多,但對于工業煙氣中CO2固定方面的研究有限。在鋼鐵冶煉環節中,排放的工業廢氣如高爐煤氣中不僅含有CO2氣體,還含有可再利用的CO氣體。將CO2從高爐煤氣中分離并固定,可以提高煤氣熱值,提高能源的二次利用價值。因此,鋼渣在冶金燃燒煙氣中CO2捕集方面的應用有必要進一步研究。
本工作以煉鋼精煉渣為吸附劑,分別以純CO2和模擬鋼鐵冶煉環節排放的高爐煤氣為吸附質氣體,對比研究精煉渣對純CO2和模擬高爐煤氣中CO2的吸附性能,考察吸附溫度對精煉渣吸附CO2性能的影響。
1 實驗部分
1.1 材料、試劑和儀器
精煉渣:煉鋼精煉工序的鋼渣,由北營鋼鐵(集團)有限公司提供;純CO2氣體:純度大于等于99.99%,由本溪市新特氣體有限公司提供;模擬高爐煤氣:CO219.89%(φ),CO 25.00%(φ),N2(含少量其他氣體)55.11%(φ),由本溪市新特氣體有限公司提供。
CaCO3,CaO,MgCO3:均為分析純。
PCA-2200型化學吸附分析儀:中國北京彼奧德電子技術有限公司。Axios PW4400型X射線熒光光譜(XRF)儀:荷蘭帕納科公司(PANalytical B.V.);D8 Advance 型X射線衍射(XRD)儀:德國布魯克(北京)科技有限公司;Evo 18型掃描電鏡(SEM)及能譜儀(EDS):德國卡爾·蔡司股份公司。
1.2 實驗方法
首先將精煉渣磨碎到粒徑74 μm以下,取破碎后的精煉渣約0.5 g放入化學吸附分析儀樣品管內,通入氦氣吹掃0.5 h。升溫至300 ℃脫水1 h。接著,在不同反應溫度下通入吸附質氣體進行吸附反應,反應時間為2 h。精煉渣在反應溫度下與CO2發生氣固碳酸化反應生成碳酸鹽產物。最后,吸附后的精煉渣經過程序升溫至990 ℃,碳酸鹽產物分解脫除CO2,檢測脫附CO2的特征峰。
1.3 分析方法
利用X射線熒光光譜檢測精煉渣主要成分;利用X射線衍射光譜分析精煉渣的礦物相成分;利用SEM照片及EDS譜圖分析精煉渣的形貌特征和物相組成。
在氣固碳酸化吸附CO2反應中,通過化學吸附分析儀檢測到的氣體脫附特征峰,逆向定量分析CO2氣體吸附情況。以純CaCO3分解脫除CO2的峰面積為標準,標定精煉渣對CO2的吸附量,按式(1)計算。
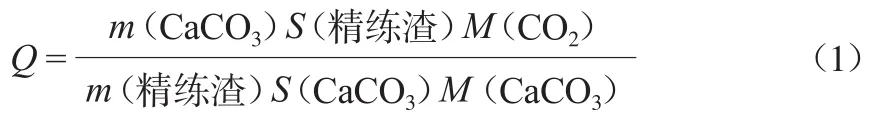
式中:Q為精煉渣對CO2的吸附量,mg/g;m(CaCO3)為純CaCO3的質量,mg;m(精練渣)為精煉渣的初始質量,g;S(精練渣)為吸附后精煉渣程序升溫脫除CO2的峰面積;S(CaCO3)為純CaCO3程序升溫脫除CO2的峰面積;M(CO2)為CO2的相對分子質量,44;M(CaCO3)為CaCO3的相對分子質量,100。
2 結果與討論
2.1 精練渣組成分析
經XRF測定,精煉渣的主要成分見表1。由表1可見,精煉渣中含量最大的是CaO,其次是SiO2,Al2O3,MgO,Fe2O3等。吸附質CO2氣體在氧化物上的化學吸附強度依次為:堿性氧化物(CaO和MgO)>兩性氧化物(鐵氧化物和Al2O3)>酸性氧化物(SiO2),可以看出CO2優先與精煉渣中的CaO和MgO堿性氧化物進行吸附反應[16]。

表1 精煉渣的主要成分
精煉渣的礦物組成非常復雜,經XRD檢測分析的礦物相成分如圖1所示。由圖1可見,精煉渣主要為Si-Ca相,包括鈣鎂橄欖石(Ca14Mg2(SiO4)8)、硅酸二鈣(Ca2SiO4)、少量Ca(OH)2以及硅鋁酸鈣(CaAl2SiO6),還有少量的鐵氧化物和CaF2。前人在精煉渣組成研究中也檢測到了硅鋁酸鈣物質[17]。精練渣中的游離CaO大部分被Si-Ca相礦物包裹著[12-13]。精煉渣在運輸或儲存過程中CaO吸收空氣中的水可以生成Ca(OH)2。除此之外,課題組前期熱力學計算研究證明,鋼渣中Si-Ca相物種也可以與水反應,生成Ca(OH)2[18]。因此,檢測到了Ca(OH)2物種。MgO的存在形式有兩種,即化合態(鈣鎂橄欖石)和游離態。
精煉渣5個區域的SEM照片見圖2,EDS分析結果見表2。由圖2可見,精煉渣結構致密,孔隙較少。根據表2中A~E區域中各元素比例可知:圖2a所示精煉渣基體A區域的主要成分為硅酸二鈣,溶有少量的氧化物;圖2b所示B區域為檢測到的少量硅酸三鈣(Ca3SiO5),含有微量的鐵,C區域為硅鋁酸鈣;檢測到極少量的游離CaO,如圖2c所示D區域;圖2d所示的E區域為MgO物種,形狀有棱角,不圓潤。
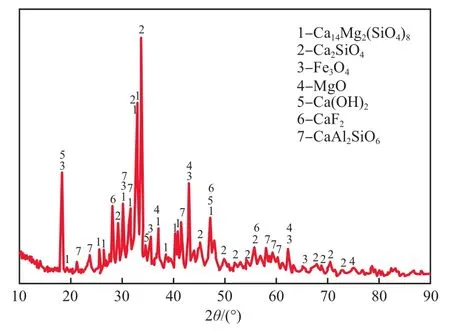
圖1 精煉渣的XRD譜圖
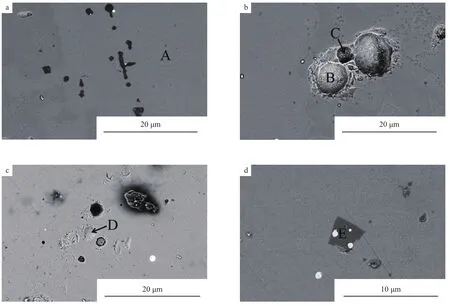
圖2 精煉渣5個區域的SEM照片
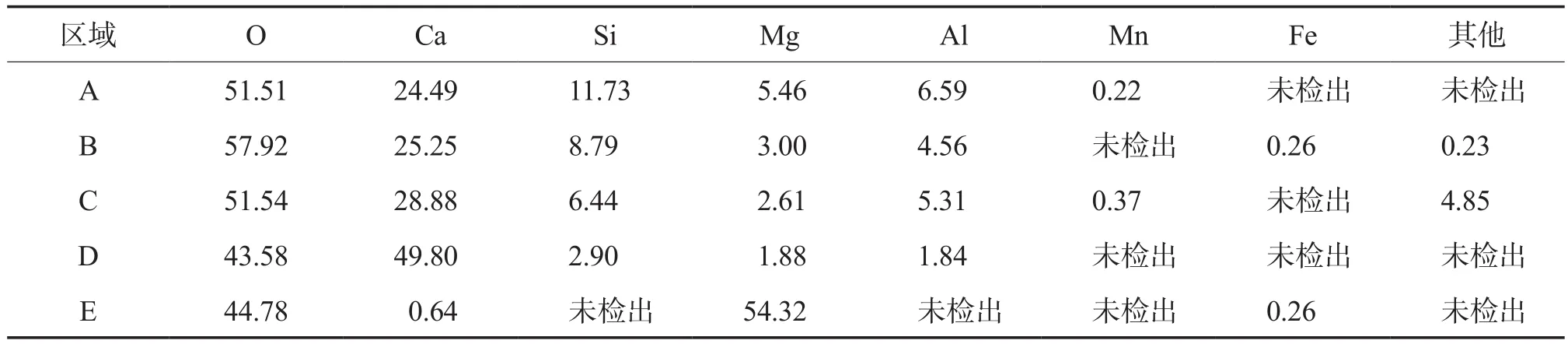
表2 精煉渣各物相的EDS分析結果 x,%
2.2 CO2的程序升溫脫附
精煉渣中的CaO[19-22]、MgO[23-24]和Ca(OH)2[25]可以吸附CO2生成CaCO3和MgCO3產物。為了更好的分析精煉渣吸附CO2后生成的碳酸鹽產物的分解溫度,分別考察了CaCO3、MgCO3及CaO吸附CO2產物的程序升溫脫附過程,獲得的程序升溫脫附曲線見圖3。由圖3可見:CaCO3分解溫度約為700~920 ℃,在885 ℃左右出現明顯脫附峰;CaO吸附CO2生成的CaCO3產物的分解溫度為650~850 ℃,在818 ℃左右出現明顯脫附峰,CaO體系吸附CO2生成的碳酸鹽產物的分解溫度比CaCO3的分解溫度向左偏移,分解溫度降低,說明碳酸鹽物質所在體系影響其分解;MgCO3的分解溫度約為440 ℃。
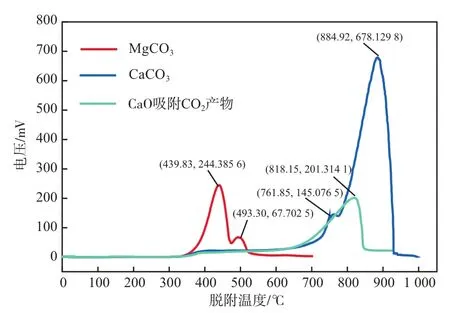
圖3 CaCO3、MgCO3及CaO吸附CO2產物的程序升溫脫附曲線
2.3 精煉渣對純CO2的吸附
精煉渣在不同溫度下吸附純CO2后的程序升溫脫附曲線見圖4。
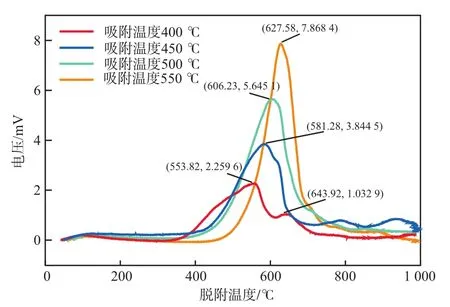
圖4 精煉渣在不同溫度下吸附純CO2后的程序升溫脫附曲線
由圖4可見:當吸附溫度為400 ℃時,精煉渣在脫附溫度400~500 ℃范圍的脫附對應MgCO3產物的分解,脫附溫度554 ℃和644 ℃處的脫附峰對應CaCO3產物的分解;當吸附溫度為450 ℃時,精煉渣在脫附溫度581 ℃處出現CaCO3分解生成CO2的脫附峰;當吸附溫度為500 ℃時,精煉渣在脫附溫度606 ℃處出現1個脫附峰,對應為CaCO3分解;當吸附溫度為550 ℃時,精煉渣在脫附溫度628 ℃處出現1個脫附峰,對應為CaCO3分解。比較各曲線可以看出,隨著吸附溫度的升高,精煉渣中CaCO3產物的分解溫度右移,分解溫度升高。此外,當吸附溫度在450 ℃及以上時,已經超出MgCO3分解溫度,基本上無MgCO3分解生成CO2的脫附峰,說明無MgCO3產物生成。因此,本文主要對比研究在本實驗吸附溫度范圍內精煉渣中鈣基物質對CO2的吸附固定。
不同吸附溫度下精煉渣對純CO2氣體的吸附量見表3。由表3可見,隨著吸附溫度的升高,精煉渣對CO2的吸附能力逐漸增強。

表3 不同吸附溫度下精煉渣對純CO2的吸附量
2.4 精煉渣對模擬高爐煤氣中CO2的吸附
精煉渣在不同溫度下吸附模擬高爐煤氣中CO2后的程序升溫脫附曲線見圖5。由圖5可見:當吸附溫度為400 ℃時,精煉渣在脫附溫度400~500 ℃范圍的脫附對應MgCO3分解,在脫附溫度500~800 ℃范圍的脫附峰對應CaCO3產物分解;當吸附溫度為450 ℃和500 ℃時,精煉渣在脫附溫度400~800 ℃范圍內均出現1個CaCO3分解生成的CO2氣體的脫附峰;當吸附溫度為550 ℃時,精煉渣在脫附溫度500~800 ℃范圍內出現1個脫附峰,對應CaCO3分解。比較各程序升溫脫附曲線可以看出:當吸附溫度超過450 ℃后,精煉渣吸附CO2反應無MgCO3產物生成。
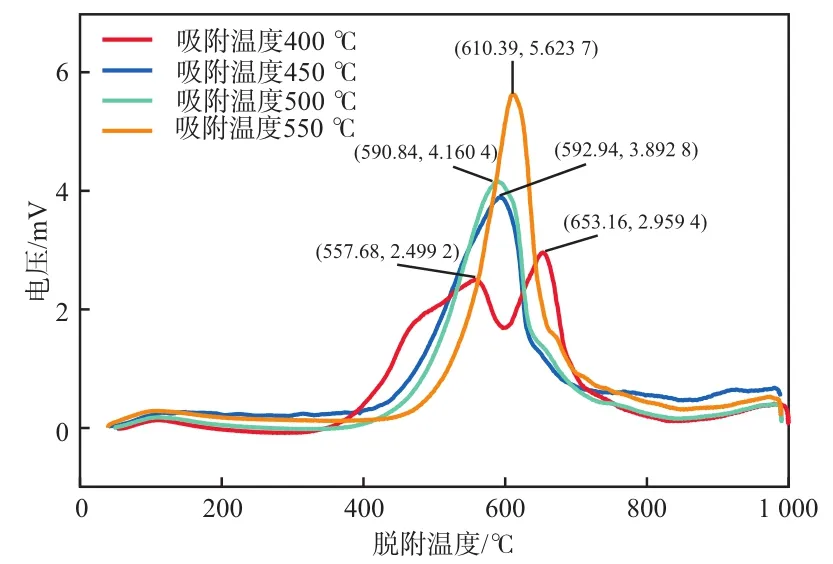
圖5 精煉渣在不同溫度下吸附模擬高爐煤氣中CO2后的程序升溫脫附曲線
不同反應溫度下精煉渣對高爐煤氣中CO2的吸附量見表4。由表4可見:當吸附溫度在400~500℃溫度范圍內時,精煉渣對高爐煤氣中CO2的吸附量相差不大。吸附溫度升高到550 ℃時,精煉渣對高爐煤氣中CO2氣體的吸附能力增強。與本課題組前期研究的轉爐渣對CO2的吸附性能相比,精煉渣在吸附溫度550 ℃下對高爐煤氣中CO2的吸附量(12.9 mg/g)高于轉爐渣(7.1 mg/g)[26]。
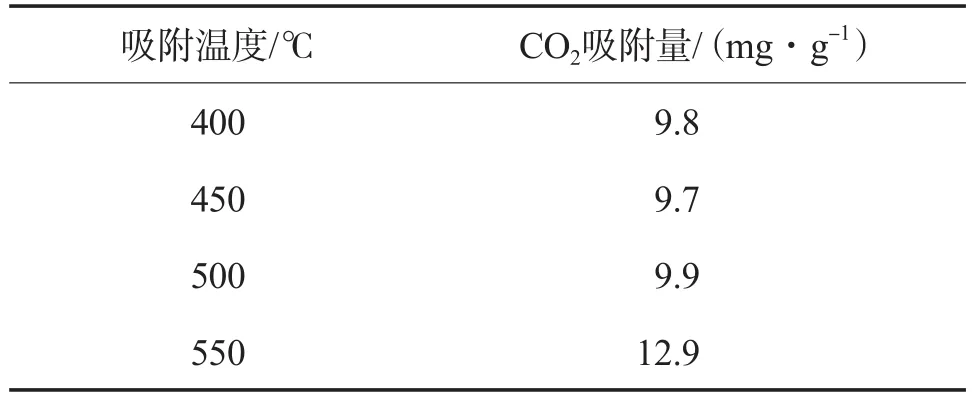
表4 不同吸附溫度條件下精煉渣對模擬高爐煤氣中CO2的吸附量
比較精煉渣對純CO2和高爐煤氣中CO2的吸附量發現:當吸附溫度為400 ℃時,前者比后者低5.1 mg/g;當吸附溫度為450 ℃時,前者比后者低2.4 mg/g;當吸附溫度為500 ℃時,精煉渣對兩種吸附氣體的CO2吸附能力發生了變化,前者比后者高0.7 mg/g;當吸附溫度為550 ℃時,前者比后者高1.8 mg/g。由以上實驗現象可以看出,雖然隨著吸附溫度升高,精煉渣對CO2的吸附能力都增強,但是增強的程度有所不同。在400 ℃和450 ℃時,精煉渣對高爐煤氣中CO2的吸附比對純CO2吸附更有優勢,當吸附溫度升高到500 ℃以上時,精煉渣對純CO2的吸附比對高爐煤氣中CO2的吸附更有優勢。這說明升高溫度,精煉渣對純CO2吸附能力升高得更快。FANG等[27]研究了β-2CaO·SiO2的碳酸化反應,β-2CaO·SiO2對模擬工業廢氣中CO2(φ=20.0%)的吸附量僅為純CO2(φ=99.9%)的46%。對于精煉渣吸附CO2反應來說,在550 ℃、碳酸化時間相同的情況下,精煉渣對高爐煤氣中CO2的吸附量僅比吸附純CO2(φ=99.99%)時降低了12%,證明精煉渣對于高爐煤氣中CO2的吸附有較好的反應性能。
3 結論
a)在400~550 ℃范圍內,升高吸附溫度,無論以純CO2還是模擬高爐煤氣中的CO2作為吸附質,精煉渣吸附CO2氣體的能力均逐漸增強。550 ℃時,精煉渣對純CO2和模擬高爐煤氣中CO2的吸附量均達到最高,分別為14.7 mg/g和12.9 mg/g。
b)當吸附溫度為400 ℃和450 ℃時,精煉渣吸附模擬高爐煤氣中CO2的能力強于吸附純CO2的能力;而當吸附溫度為500 ℃和550 ℃時,精煉渣對純CO2的吸附能力強于對模擬高爐煤氣中CO2的吸附能力。證明隨吸附溫度升高,精煉渣對純CO2吸附能力升高得更快。

