miR-142-3p對子宮內膜癌細胞增殖、遷移及侵襲的影響
孫沙沙,李玉華
子宮內膜癌是女性生殖系統常見的惡性腫瘤之一,其發病率逐年上升,嚴重影響患者的身心健康,甚至危及生命[1,2]。目前,子宮內膜癌的治療雖然取得了較大進展,但其預后較差且5年生存率<40%[3]。因此,尋找有效的治療靶點對子宮內膜癌的治療具有重要意義。微小RNA(miRNA)是一種內源性單鏈非編碼小分子RNA,可調控腫瘤細胞增殖、凋亡、遷移和侵襲等生物學功能[4-6],與癌癥進展密切相關。研究發現 miR-142-3p在乳腺癌、胰腺癌、結直腸癌、肺癌等多種癌癥中表達降低,可參與抑制癌細胞增殖、侵襲及遷移等過程[7-10]。有研究發現miR-142-3p在子宮內膜癌組織中的表達顯著降低[11],提示miR-142-3p可能是診斷治療子宮內膜癌的一個重要靶點。筆者通過上調子宮內膜癌細胞miR-142-3p的表達,探究miR-142-3p對子宮內膜癌細胞增殖,遷移及侵襲的影響。
1 材料與方法
1.1材料及主要試劑人子宮內膜癌細胞系(Ishikawa和HEC-1A)和正常子宮內膜細胞系(HEC-251)(中國科學院上海生物化學與細胞生物學研究所)。Lipofectamine 3000和Trizol試劑盒(美國Invitrogen公司),MTT試劑盒 (北京 solaibio公司),Tranwell小室(美國 Corning公司),逆轉錄試劑盒和實時熒光定量聚合酶鏈反應技術檢測試劑盒(日本TaKaRa公司),MMP-2和MMP-9一抗(美國Cell Signal公司),miR-142-3p mimics及相關引物由上海生工生物工程公司合成。
1.2方法
1.2.1 細胞培養 用含10%胎牛血清和1%青霉素/鏈霉素的 RPMI-1640培養基在37℃、5%CO2的培養箱中培養Ishikawa,HEC-1A和HEC-251細胞。取對數期生長的細胞進行實驗。
1.2.2 細胞轉染 分別將miR-142-3p mimics及其陰性對照(miR-NC)利用 Lipofectamine 3000試劑盒法瞬時共轉染HEC-1A,分為3組:空白對照組(Control)、陰性對照組(miR-NC)、miR-142-3p過表達組(miR-142-3p mimics)。
1.2.3 MTT法 將轉染后的HEC-1A細胞制成單細胞懸液,接種于96孔板中,每孔接種4×103個細胞。于 37℃,5%CO2培養箱培養 0h、24h、48h、72h、96 h 后,每孔加 20 μL MTT 液(5 mg/ml)呈色。 繼續培養箱孵育4 h,棄去培養液。隨后,每孔加入DMSO(150 μl),避光孵育 10 min。 酶標儀測定各組HEC-1A細胞在490 nm處的OD值。
1.2.4 Transwell實驗 將轉染的HEC-1A細胞置于以Matrigel基底膠包被或不包被的Transwell小室上室、下室中加入500 μl含10%胎牛血清的培養基,在37℃,5%CO2培養箱中培養48 h后,用棉簽擦去上室面上的細胞,4%多聚甲醛固定15 min,結晶紫染色15 min,隨機取6個視野顯微鏡下拍照,計數遷移和侵襲細胞數。
1.2.5 熒光定量PCR檢測 采用Trizol試劑抽提總RNA。經微量核酸定量儀測定RNA濃度和純度后,將RNA反轉錄合成cDNA。用ABI7500定量PCR儀進行熒光定量PCR實驗,反應條件為95℃預變性 10 min,95℃變性10 s,60℃退火 20 s,72℃延伸 34 s,40 個循環。以 U6 為內參,采用 2-ΔΔCt法計算細胞中miR-142-3p的相對表達量。引物設計如下:miR-142-3p F:5’-GGGTGTAGTGTTTCCTACT-3’,R:5’-CAGTGCGTGTCGTGGAGT-3’;U6 F:5’-TGCGGGTGCTCCGCTTCGGCAGC-3’,R:5’-CAG TGCAGGGTCCGAGGT-3’。
1.2.6 Western blot檢測 蛋白樣品按照 50 μg/孔上樣,經10%SDS-PAGE電泳分離后、電轉移到PVDF膜上,經5%脫脂奶粉PBST溶液封閉后,加入一抗(MMP-2,1∶1000;MMP-9,1∶1000;β-actin,1∶1000)4℃孵育過夜。加入HRP標記的二抗,室溫孵育1 h,ECL顯色。
1.3統計學分析實驗數據的結果以(±s)表示,使用GraphPad Prism 8.0進行數據統計學分析。兩組之間的比較采用t檢驗,多組之間的比較采用單因素方差分析。P<0.05為差異具有統計學意義。
2 結果
2.1 miR-142-3p在子宮內膜癌細胞中低表達qRT-PCR結果表明,與HEC-251細胞比較,miR-142-3p在Ishikawa細胞尤其是HEC-1A細胞中的表達明顯下調(P<0.05)(圖 1)。因此,選 HEC-1A 細胞進行后續實驗。
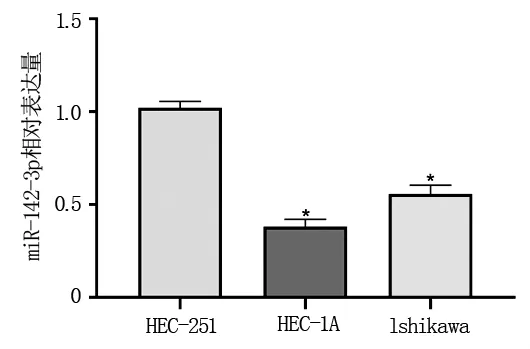
圖 1qRT-PCR 檢測 miR-142-3p在HEC-251、Ishikawa和HEC-1A細胞中的表達與HEC-251比較(*P<0.05)
2.2 miR-142-3p mimics增加HEC-1A細胞中miR-142-3p的表達qRT-PCR檢測發現,miR-142-3p轉染后HEC-1A細胞中miR-142-3p的表達水平明顯高于Control組和miR-NC組 (P<0.05)(圖2)。證明miR-142-3p被成功轉入HEC-1A細胞中。
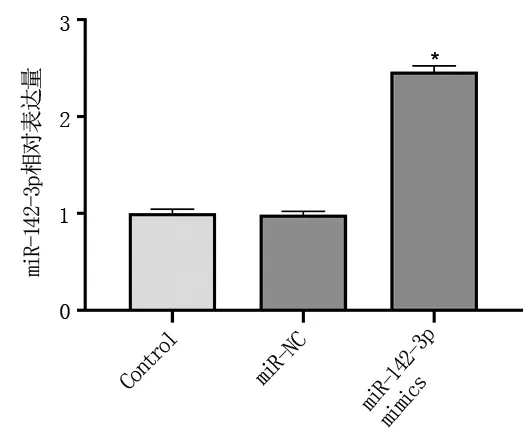
圖2qRT-PCR檢測miR-142-3p在各組HEC-1A細胞中的表達與Control組和miR-NC組比較(*P<0.05)
2.3 miR-142-3p過表達抑制HEC-1A細胞增殖MTT實驗表明,與Control組和miR-NC組比較,轉染 24 h、48 h、72 h 及 96 h 后,miR-142-3p 組HEC-1A細胞的吸光度值顯著降低 (P<0.05)(圖3),表明miR-142-3p過表達能夠抑制子宮內膜癌細胞HEC-1A的增殖。
圖3見封三。
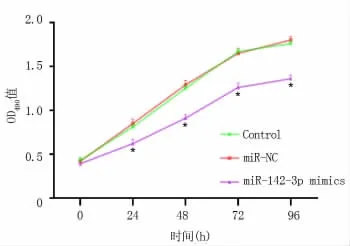
圖3 MTT檢測miR-142-3p對HEC-1A細胞增殖的影響與Control組和miR-NC組比較(*P<0.05)
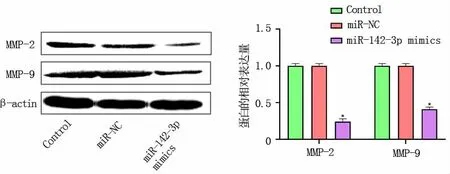
圖6 Western blot檢測miR-142-3p對HEC-1A細胞中MMP-2和MMP-9蛋白水平的影響與Control組和miR-NC組比較(*P<0.05)
2.4 miR-142-3p過表達抑制HEC-1A細胞的遷移和侵襲Transwell實驗結果表明,與Control組和miR-NC組比較,miR-142-3p組HEC-1A細胞的遷移率和侵襲率均顯著降低 (P<0.05)(圖4和5),表明miR-142-3p過表達能夠抑制子宮內膜癌細胞HEC-1A的遷移和侵襲。
2.5 miR-142-3p過表達抑制HEC-1A細胞中MMP-2和MMP-9的表達Western blot實驗結果表明,miR-142-3p轉染后 HEC-1A細胞中MMP-2和MMP-9的表達水平明顯低于Control組和 miR-NC 組(P<0.05)(圖 6),進一步證實 miR-142-3p過表達能夠抑制子宮內膜癌細胞HEC-1A的遷移和侵襲能力。
圖6見封三。
3 討論
研究表明,miR-142-3p能夠通過調控細胞生物學功能在癌癥中發揮重要作用。朱翔宇等[12]發現miR-142-3p在結直腸癌組織及癌細胞中表達水平明顯低于正常組織和細胞,且發現miR-142-3p高表達能夠抑制結直腸癌細胞增殖。國外學者Behzad Mansoori等[13]證實 miR-142-3p 作為一種抑癌miRNA通過靶向Bach-1抑制乳腺癌細胞的侵襲和遷移能力。此外,高建連等[14]研究發現miR-142-3p在卵巢癌組織及癌細胞中低表達。該研究同時也表明miR-142-3p能夠通過靶向調控sirtuin 1抑制卵巢癌細胞增殖。有研究發現miR-142-3p在子宮內膜癌中低表達[11],但其對子宮內膜癌生物學行為的影響尚無報道。
該研究發現與正常子宮內膜細胞相比,miR-142-3p在子宮內膜癌細胞中低表達,與Muralidharan Jayaraman 等[11]研究一致,揭示 miR-142-3p可能是診斷治療子宮內膜癌的一個重要靶點。MTT和Transwell實驗結果表明miR-142-3p過表達顯著抑制子宮內膜癌細胞HEC-1A的增殖,遷移和侵襲。惡性腫瘤的重要特征是生長不受限制,這不僅是由腫瘤細胞增殖和分化失控導致的,也與腫瘤細胞的侵襲性密切相關。研究發現活化的MMP-2和MMP-9可以參與細胞外基質元素的降解,減少細胞黏附,進而促進腫瘤細胞遠處遷移[15]。發現miR-142-3p過表達能夠顯著抑制MMP-2和MMP-9的表達水平,進一步證實miR-142-3p能夠抑制子宮內膜癌細胞的遷移和侵襲。
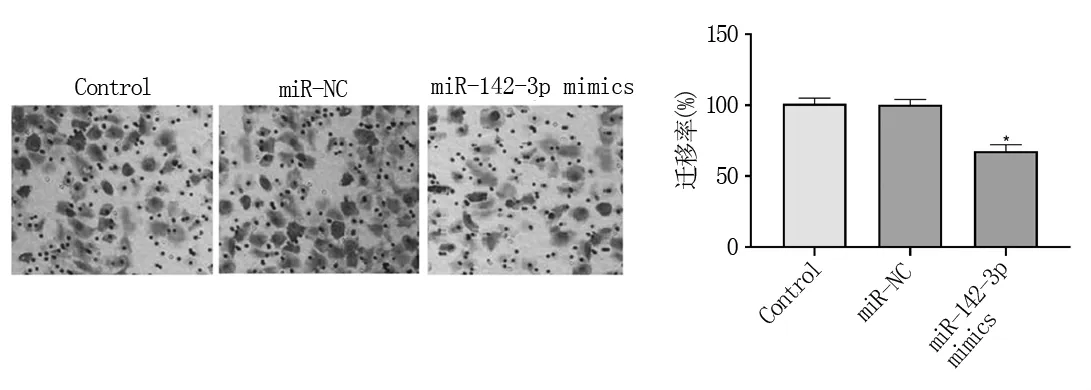
圖4 Transwell檢測miR-142-3p對HEC-1A細胞遷移的影響與Control組和miR-NC組比較(*P<0.05)
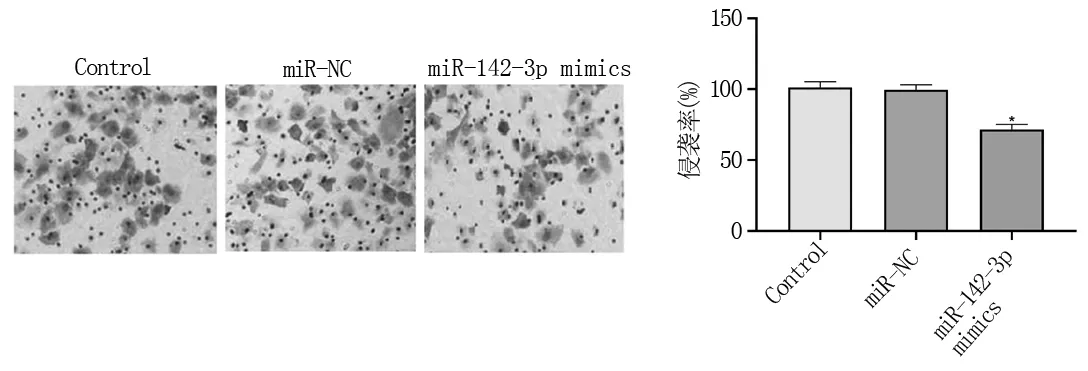
圖5 Transwell檢測miR-142-3p對HEC-1A細胞侵襲的影響與Control組和miR-NC組比較(*P<0.05)
綜上所述,miR-142-3p在子宮內膜癌細胞中低表達,通過提高miR-142-3p的表達可以抑制子宮內膜癌細胞增殖、遷移和侵襲,抑制子宮內膜癌的發展。結果提示miR-142-3p參與子宮內膜癌的發生和發展,有望成為子宮內膜癌治療的新靶點。

