化學性交感神經切除對肌筋膜激痛點炎癥和肌衛星細胞成肌分化的影響
袁仕國 顏麗滿 武凱 徐明奎 李義凱 鄒宇聰
1南方醫科大學第三附屬醫院,廣東省骨科研究院(廣州510630);2海南省中醫院骨傷科(海口570203);3廣州中醫藥大學第四臨床醫學院(廣州510006)
肌筋膜疼痛綜合征(myofascial pain syndrome,MPS)在疼痛中心占比可高達95%[1],但也是臨床最常被忽視的疾病之一[2]。MPS 的關鍵特征是肌筋膜激痛點(myofascial trigger points,MTrPs),按壓可產生局部顫搐反應、牽涉痛和自主神經癥狀[3]。部分臨床癥狀,如局部膚溫高、出汗異常、顫搐反應等,指向與自主神經過度活躍有關[4]。研究[5]顯示MTrPs 可能受交感神經影響,MTrPs 內的交感-感覺相互作用可能會導致局部疼痛和牽涉痛以及出現交感神經癥狀,因此臨床治療有必要重新評估針對交感神經的治療。心肌損傷后會導致心交感神經芽生重構并高支配[6-7],骨骼肌和心肌同屬于橫紋肌,骨骼肌損傷后是否也會發生交感神經重構和高支配,目前還沒有定論。研究[8-10]發現白細胞介素-6(IL-6)、腫瘤壞死因子-α(TNF-α)等炎癥因子對機體損傷及修復起著復雜的作用。研究[8-10]也發現MTrPs 局部存在炎癥因子的高表達。因此,MTrPs 局部交感神經存在怎樣的變化,靶向交感神經的治療是否能促進MTrPs 修復,對骨骼肌損傷修復的關鍵干細胞-肌衛星細胞(muscle satellite cells,MuSC)及炎癥因子等有何影響都成為本研究關注點。本研究擬在大鼠上探索MTrPs 造模后交感神經的支配情況,并予以化學性交感神經切除(chemical sympathectomy,CS),觀測相關的炎癥因子變化,評估肌衛星細胞激活、成肌分化和骨骼肌修復的情況,探索和拓展MPS的病理機制和新的治療靶點可能。
1 材料與方法
1.1 實驗動物8 周的健康雄性SD 大鼠18 只,體質量為220~250 g,購自南方醫科大學動物實驗中心,動物許可證號:SCXK(粵)20160041。常規飼養,動物房維持(65 ± 5)%的濕度和(25 ± 3)℃的溫度,自由飲水、飲食。所有實驗均在南方醫科大學實驗動物倫理委員會的批準下進行,符合動物管理與使用倫理準則。
1.2 實驗儀器與試劑根據文獻[12-13]自制木質打擊器1 臺(打擊面直徑1 cm,總質量為1 200 g,打擊高度為20 cm,動能為2.352 J)。動物試驗跑臺(上海欣軟信息科技有限公司,XR-PT-10A),全波長多功能讀數酶標儀(美國Thermo 賽默飛,Varioskan LUX),實時熒光定量PCR 儀(美國Thermo 賽默飛,ABI Stpone plus),光學顯微鏡(日本OLYMPUS,BX-53)。6-羥基多巴胺氫溴酸鹽(6-hydroxydopamine hydrobromide,6-OHDA)(中國阿拉丁,H4381),Rat TNF-α ELISA-Kit(中國Multi Sciences,EK382/3-48),Rat Noradrenaline-(NE)ELISA-Kit(中國Cloud-Clone Corp,CEA907Ge),Rat Interleukin 6,IL-6 ELISA KIT(中國CSB,CSBE04640r),Anti-TH Rabbit pAb抗體(中國ZEN BIO,511027),PAX7 抗體(美國Affinity,AF7584),RTPCR 引物由上海生工提供。
1.3 大鼠分組及干預
1.3.1 大鼠分組將18 只大鼠按照隨機表法分配到3 組中,每組6 只:A 組為空白對照組,B 組為MTrPs 造模組,C 組為MTrPs 造模+CS 組。
1.3.2 MTrPs 造模B、C 組大鼠采用打擊結合離心運動的造模方法進行MTrPs 造模[12-13]。第1 天進行右側股內側肌打擊損傷,第2 天進行力竭運動。每周進行打擊和跑臺運動1 次,連續4 周,然后再恢復4 周。
1.3.3 化學性交感神經切除C 組大鼠在第8 周MTrPs 造模完成后開始,每3 天腹腔注射6-ODHA 1 次,用量為100 mg/kg,連續腹腔注射2 次以完全阻斷交感神經[14]。A組和B組注射等量生理鹽水。
1.3.4 取材化學性交感神經切除10 d,過量麻醉處死大鼠取材。按文獻方法取材,具體方法:暴露右股四頭肌,輕輕按壓探尋股內側肌打擊部位及周圍的肌緊張帶,可觸及明顯的緊張帶和/或膨大的結節,并予以針灸針刺入此處,引出顫搐反應者即為MTrPs。A 組取右股內側肌相應部位。標本取材約1 cm3。
1.4 組織切片處理
1.4.1 固定與切片標本取材后于40 g/L 多聚甲醛4 ℃固定24 h,30%蔗糖脫水約24 h 至標本沉底,OCT 包埋,10 μm 厚冰凍切片。
1.4.2 蘇木素-伊紅(Hamematoxylin-eosin,HE)染色常規HE 染色:蘇木素染色2.5 min,伊紅染色2 min。光鏡下觀察,每個標本隨機取5 個切片,每個切片采集5 個200 倍視野圖片,使用Image J 軟件分析肌細胞所占面積,計數攣縮結節數量,最終取其均數,下同。
1.4.3 免疫熒光切片于山羊血清常溫封閉1 h,Pax7 和TH 一抗濃度為1∶150,4 ℃孵育16 h,避光加入濃度為1∶400 的二抗,4 ℃孵育2 h,4′,6-二脒基-2-苯基吲哚封片,熒光顯微鏡拍照。
1.5 ELISA 測定NE 和炎癥因子IL-6、TNF-α表達在4 ℃下MTrPs組織勻漿加入去離子水(1∶9),勻漿液10 000 r/min 離心30 min,上清液12 000 r/min 離心60 min。各樣品嚴格按照ELISA 試劑盒說明書操作,并采用Curve Expert 2.20 軟件進行標準曲線擬合,計算樣本各指標濃度值進行統計分析。所有樣品均一式兩份進行檢測。
1.6 RT-PCR 測定MyoG、MyoD 基因表達按100 mg組織加入1 mL TRIzol,勻漿,加入1/5體積氯仿,其余按常規步驟提取RNA。依次加入抑制劑和逆轉錄酶進行反轉錄。取0.2 mL 無酶管,分別加入如下反應體系:12.5 μL 2 × qPCR Mix,2.0 μL 7.5 μmol/L 基因引物,2.5 μL 反轉錄產物和8.0 μL ddH2O,每個反轉錄產物配制3 管復孔,進行實時定量擴增(表1)。結果通過2-ΔΔCt方法計算的MyoD和MyoG 基因表達的倍數變化。

表1 MyoG 和MyoD 引物序列Tab.1 MyoG and MyoD primer sequences
1.7 統計學方法應用SPSS 19.0 軟件進行統計分析,所采集數據用()表示。Levene 法進行方差齊性檢驗。方差齊時,多組間均數比較采用單因素方差分析(one-way ANOVA),組間兩兩比較采用SNK-q法比較;方差不齊時用Welch 法進行近似方差分析,組間兩兩比較采用Dunnett′s T3 法比較;以P<0.05 為差異有統計學意義。
2 結果
2.1 一般資料大鼠造模后無骨折、皮膚破潰、感染等。C 組在注射第2 次后死亡1 只。
2.2 各組肌細胞病理形態的變化A 組肌細胞呈規則排列的多邊形或長條形,間隙均勻,無斷裂,無明顯炎癥細胞浸潤(圖1A、B)。B 組的肌細胞形成攣縮結節、間隙明顯增寬,同時肌細胞萎縮、斷裂,可見炎癥細胞浸潤;橫截面上呈現出類圓形和不規則形,縱截面上呈扭曲長條形(圖1C、D)。C組肌細胞明顯較B 組再生;可見少量攣縮結節,較B 組減少;肌細胞橫截面上呈大小不等的多邊形或類圓形,炎癥細胞浸潤基本消失(圖1E、F)。
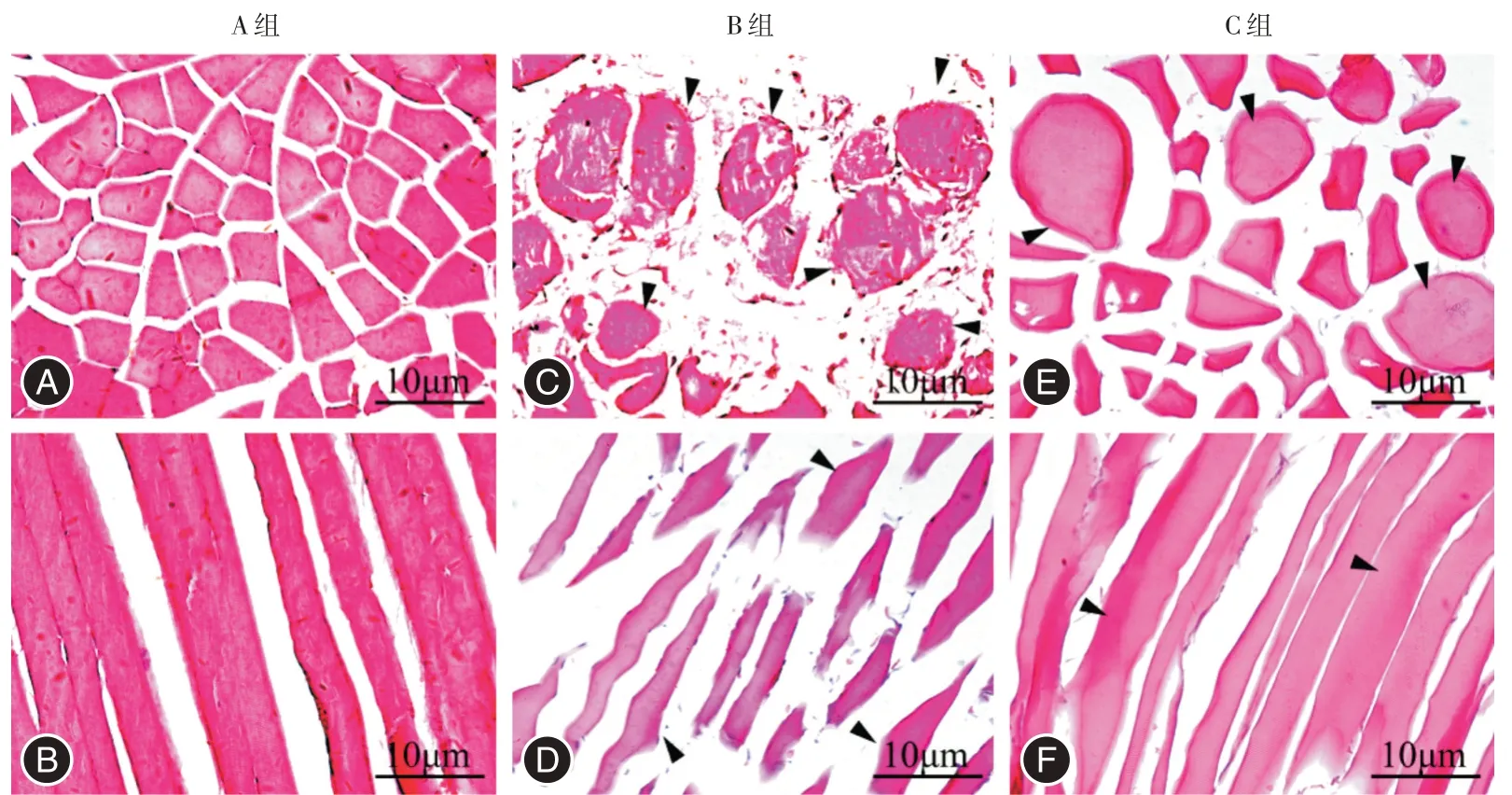
圖1 各組骨骼肌HE 染色(箭頭所示為攣縮結節)Fig.1 HE staining of skeletal muscle in each group(arrows show contracture knots)
2.3 各組肌細胞面積比例和攣縮結節數量3組中橫截面和縱截面的肌細胞面積比例均為A >C >B,差異有統計學意義(F=22.31、34.59,P<0.01,圖2A、B,表2)。說明交感神經阻斷可促進肌細胞面積恢復。攣縮結節數量均為B >C >A,差異有統計學意義(F= 32.83、326.15,P<0.01,圖2C、D,表2)。結果說明CS 可減少攣縮結節。
2.4 IL-6、TNF-α和NE 的表達A、B、C 3 組中MTrPs 局部的IL-6 分別為(6.87 ± 2.73)、(87.99 ±20.09)、(47.66 ± 15.91)pg/g,TNF-α分別為(32.39±31.72)、(665.82±124.62)、(230.29 ± 96.15)pg/g,均為B >C >A,差異有統計學意義(F=45.07、73.33,P<0.01,圖3A、B)。而NE 分別為(293.55±60.37)pg/g、(722.67 ± 185.61)pg/g、(60.70 ± 10.87)ng/g,B >A >C,差異有統計學意義(F= 46.15,P<0.01,圖3C)。說明CS 處理后NE 明顯降低,且可降低IL-6 和TNF-α炎癥因子的表達。
2.5 MyoD 和MyoG 基因的表達A、B、C 3 組中MTrPs 局 部MyoD 分 別 為(0.84 ± 0.14)、(1.95 ±0.36)、(1.20 ±0.16),B >C >A,差異有統計學意義(F= 31.95,P<0.01,圖4A)。MyoG 分別為(0.42±0.19)、(0.53 ± 0.22)、(0.93 ± 0.17),3 組差異有統計學意義(F= 10.33,P<0.01,圖4B),C 組最高,組間比較顯示雖然B 組數值較A 組高,但差異無統計學意義(P= 0.77)。即造模后成肌分化因子MyoD 基因激活表達,但成肌分化的終末因子MyoG 在B 組上升不明顯,而C 組較B 組相對降低MyoD 和提升MyoG 基因的表達,且仍較正常對照的A 組高。
表2 各組肌細胞面積比例和攣縮結節數量Tab.2 Proportion of muscle cell area and number of contracture knots in each group ±s
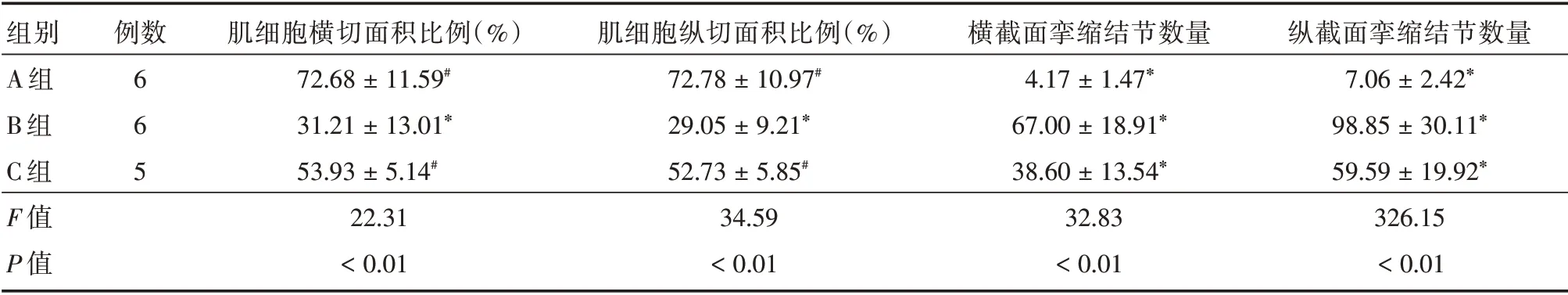
表2 各組肌細胞面積比例和攣縮結節數量Tab.2 Proportion of muscle cell area and number of contracture knots in each group ±s
注:組間兩兩比較,**P <0.05,*P <0.01,#P >0.05
組別A 組B 組C 組F 值P 值例數6 6 5肌細胞橫切面積比例(%)72.68±11.59#31.21±13.01*53.93±5.14#22.31<0.01肌細胞縱切面積比例(%)72.78±10.97#29.05±9.21*52.73±5.85#34.59<0.01橫截面攣縮結節數量4.17±1.47*67.00±18.91*38.60±13.54*32.83<0.01縱截面攣縮結節數量7.06±2.42*98.85±30.11*59.59±19.92*326.15<0.01
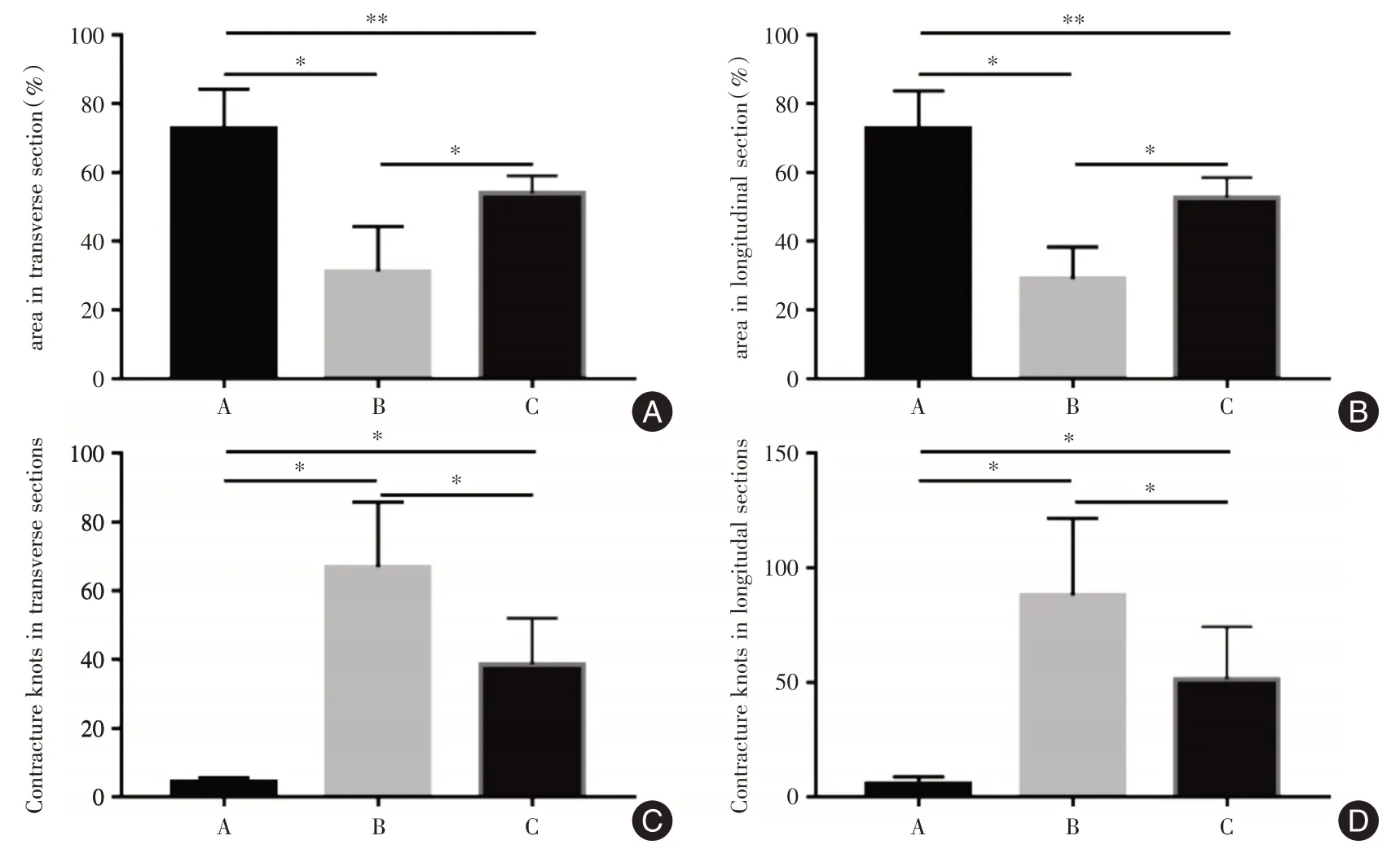
圖2 各組肌細胞面積比例和攣縮結節數量Fig.2 Proportion of muscle cell area and number of contracture knots in each group

圖3 各組IL-6、TNF-α和NE 的表達Fig.3 Expression of IL-6,TNF-α and NE in each group
2.6 TH的免疫熒光檢測A、B、C 3組TH的熒光強度值橫截面上分別為(2.51 ± 0.39)、(3.74 ± 0.42)、(1.04±0.19)μm2/(mm2·103),縱截面上分別為(1.70±0.41)、(4.66±0.72)、(1.03±0.24)μm2/(mm2·103),B >A >C,差異有統計學意義(F= 75.97、81.73,P<0.01)。即MTrPs 造模后TH 高表達,交感神經存在重構和高支配現象。CS 可明顯下調TH 的表達,即CS 可明顯抑制交感神經活性。見圖5、圖6A、B。
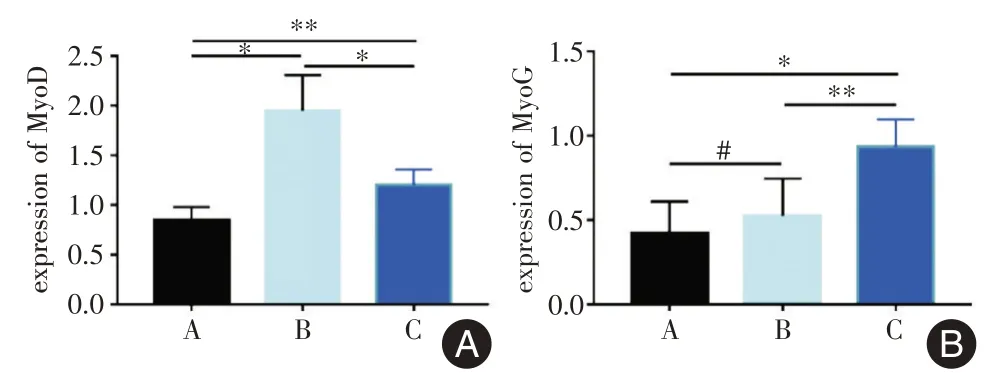
圖4 各組MyoD 和MyoG 基因的表達Fig.4 MyoD and MyoG gene expression in each group
2.7 Pax7 的免疫熒光檢測A、B、C 3 組Pax7 的熒光強度值橫截面上分別為(4.29 ± 1.29)、(1.09± 0.26)、(2.80 ± 0.48)μm2/(mm2·103),縱截面上分別為(4.53 ±1.25)、(1.03±0.41)、(2.58±0.60)μm2/(mm2·103),差異有統計學意義,A >C >B(F=30.73、25.94,P<0.01,圖6C、D 和7)。即MTrPs 造模后Pax7 低表達,MuSC 大量激活并分化,并有耗竭趨勢。MTrPs 造模后,給予CS 可明顯上調Pax7 的表達,即CS 可抑制MuSC 的過度激活分化,對維持MuSC 的數量具有重要的意義。
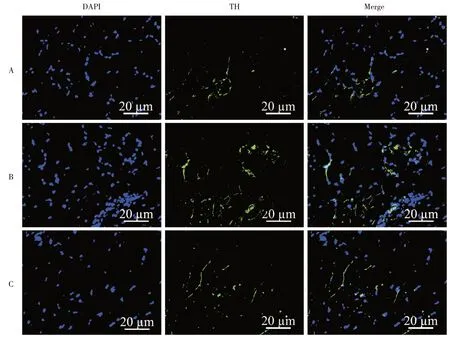
圖5 TH 的免疫熒光的表達(200×)Fig.5 Expression of TH immunofluorescence(200×)
3 討論
MPS 是由MTrPs 引起的感覺、運動和自主神經癥狀的綜合征,常由急慢性肌肉損傷導致的,適度的炎癥細胞如單核細胞浸潤可促進肌肉的修復。炎癥細胞的過度浸潤則導致纖維化[15],肌肉組織失去原有的功能,對功能恢復是不利的。炎癥因子可激活并促MuSC 分化,但過度的炎癥刺激導致其成肌分化受抑制,并可能導致MuSC 的耗竭[16]。需要調節炎癥細胞和炎癥因子合適的表達以促進MTrPs 成肌修復、快速修復,達到良好的功能和形態的修復。
本實驗中發現MTrPs 造模后,MTrPs 骨骼肌萎縮,并且造模組同時肌細胞還形成攣縮結節,且數量眾多。這些組織病理學發現與先前的研究一致[17]。MTrPs 造模后IL-6 和TNF-α均顯著升高,炎癥細胞明顯浸潤[9]。IL-6 和TNF-α是眾多炎癥因子的代表,IL-6 既可促進又可抑制炎癥[18]。而炎癥因子可激活MuSC,MuSC 激活后其干性的標志之一Pax7 消失[19]。MuSC 激活后進行增殖,重新歸于靜止并恢復MuSC 的數量并保持其干性,或分化為成肌或成纖維細胞等。本實驗中發現MTrPs 造模后MyoD 明顯高表達,而Pax7 顯著降低,即MuSC大量激活,但成肌生長因子MyoG 則升高不明顯,提示MuSC 激活后可能因局部微環境的變化向非成肌方向分化。同時Pax7 顯著降低,提示MTrPs中可能微環境的變化會導致MuSC 的數量減少甚至耗竭,從而導致肌肉持續萎縮、無法成肌修復。
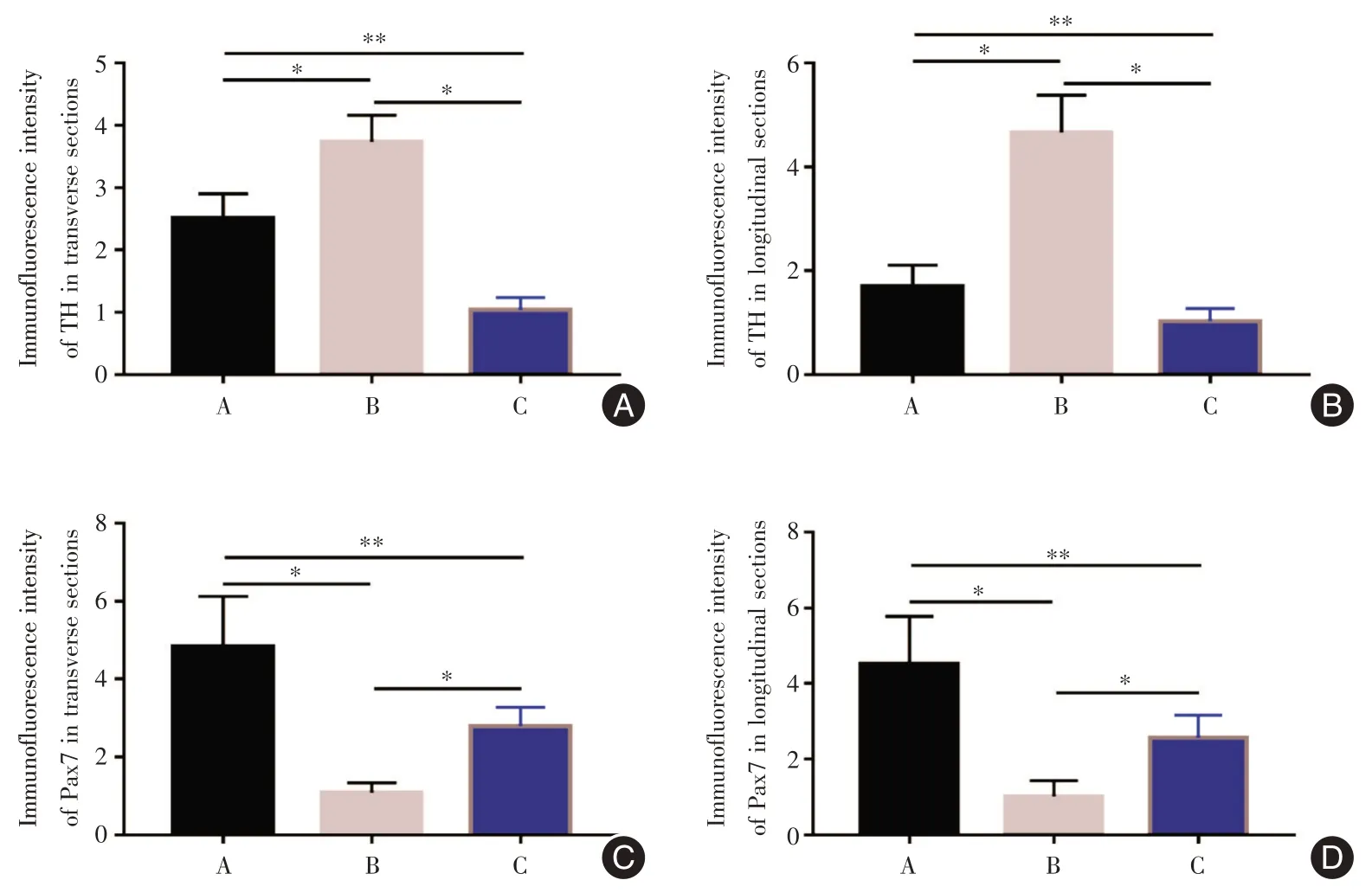
圖6 各組TH 熒光強度值Fig.6 Fluorescence intensity of TH in each group
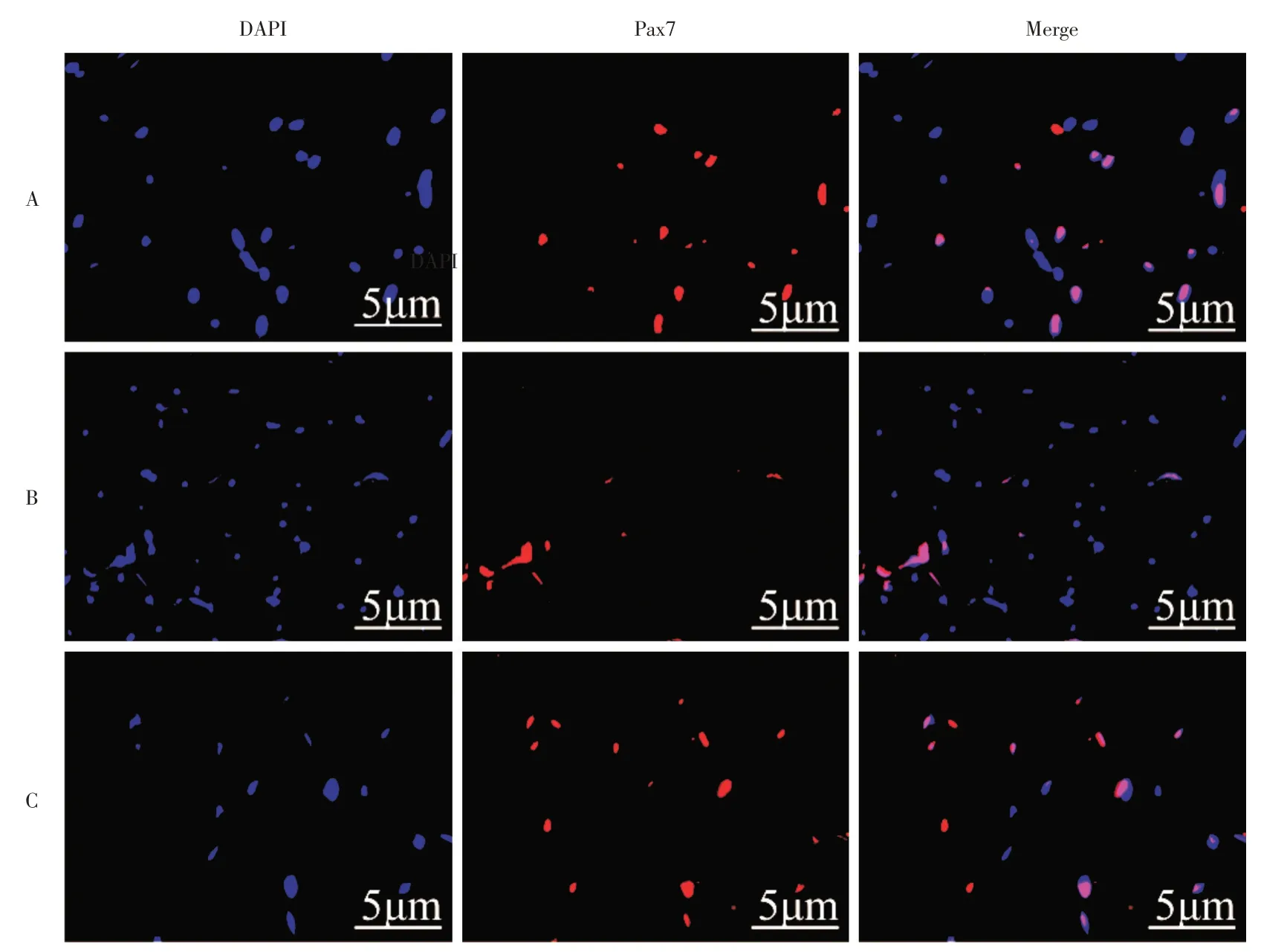
圖7 各組骨骼肌MTrPs 局部Pax7 表達(400×)Fig.7 Local MTrPs Pax7 expression of skeletal muscle in each group(400×)
MPS 患者局部顫搐反應、出汗異常、膚溫異常以及交感神經皮膚反應等癥狀指向MTrPs 局部可能存在交感神經重構和異常支配[20]。目前普遍認可的觀點認為神經遞質釋放異常是MTrPs 的中心環節[21]。文獻報道患者上部斜方肌的MTrPs 的NE 濃度較高,而較高濃度的神經遞質誘發形成MTrPs[22-23]。本實驗發現MTrPs 局部NE 濃度明顯較空白對照組高,而CS 處理后NE 的表達明顯降低,與此同時MTrPs 的肌細胞面積明顯增加,炎癥細胞浸潤基本消失,炎癥因子IL-6 和TNF-α均顯著降低。表明CS 可以促進MTrPs 成肌修復。然而矛盾的是,CS 處理后MTrPs 局部的MyoD 和MyoG基因表達反而較單純造模組降低,但Pax7 反而較單純造模組高,表明抑制交感神經的高支配有利于維持MuSC 的干性。這種抑制MuSC 的過度激活并維持其干性的作用機制,可能是CS 促進成肌修復的重要原因。
綜上所述,本實驗在動物模型中成功構建了MTrPs,證明了MTrPs 發生了交感神經的重構,導致其高支配,這可能對MTrPs 的病理認識以及MPS 的診治有益。抑制交感神經高支配,有利于維持MuSC 的干性,抑制MuSC 的過度激活,并促進成肌的終末分化,從而促進成肌修復。但是,本實驗為初步的在體動物實驗,由于缺乏時間梯度的研究,缺乏詳盡的作用機制研究,仍需要全面系統的實驗證明之。

