重癥超聲在膿毒癥機械通氣患者撤機中的評估價值*
楊曉英,顧華杰,戴曉勇,葉宥文
同濟大學附屬楊浦醫院急診科(上海200090)
膿毒癥是由于嚴重感染誘發機體反應失調而導致的多器官功能障礙,一直是ICU的主要死亡原因之一,發病率以每年1%~5%的速度增長,且病死率高達40%[1-2]。膿毒癥患者多需接受機械通氣(Mechanical ventilation,MV)治療,但長時間MV易伴發呼吸機相關肺損傷、膈肌功能障礙等多種并發癥。因此,能否在MV后適當時機成功撤機直接影響膿毒癥患者的預后,也是該領域研究的熱點。以往通常采用最大吸氣壓、淺快呼吸指數(Rapid shallow breathing index,RSBI)等呼吸力學指標預測撤機,但敏感性、特異度不理想,且參考閾值不統一[3]。近年來重癥超聲以其簡便快速、無創可重復、動態監測等優勢,已廣泛應用于撤機前心肺、膈肌功能的評估[4-5],但對其預測膿毒癥患者撤機成敗的研究仍較為少見。本研究通過分析心肺、膈肌指標與撤機結局的相關性,探討重癥超聲在膿毒癥MV患者撤機中的價值。
對象與方法
1 研究對象 回顧性分析2017年6月至2019年6月我院急診科收治的60例膿毒癥患者臨床資料。其中男33例,女27例;年齡19~75歲,平均(47.9±4.6)歲;膿毒癥48例,膿毒性休克12例;急性生理與慢性健康評分(Acute Physiology and Chronic Health EvaluationⅡ,APACHE Ⅱ)15~26分,平均(23.1±2.5)分;MV時間3.4~8.2 d,平均(5.4±1.6)d。根據撤機是否成功(成功拔除氣管插管或脫開呼吸機且自主呼吸>48 h視為撤機成功),分為撤機成功組(41例)和撤機失敗組(19例)。病例納入標準:①均符合《國際嚴重膿毒癥和膿毒癥休克指南(2016年)》的診斷標準[6],存在明確感染灶;②年齡18~75歲,MV時間>48 h;③原發病明顯好轉且無新發疾病,經自主呼吸試驗(Spontaneous breathing test,SBT)判定符合撤機標準[7]。排除標準:晚期惡性腫瘤、家屬放棄治療、無法接受超聲檢查或合并膈肌功能障礙、嚴重心肝腎功能障礙者。本研究通過倫理委員會審批,患者親屬知情同意并全程配合。
2 研究方法
2.1 一般資料收集:通過病例系統查閱患者基本資料,包括性別、年齡、APACHE Ⅱ評分、序貫器官衰竭(Sequential Organ Failure Assessment,SOFA)評分、MV時間、原發疾病、SBT前心率(Heart rate,HR)、收縮壓(Systolic blood pressure,SBP)、舒張壓(Diastolic blood pressure,DBP)、平均動脈壓(Mean arterial pressure,MAP)、呼吸頻率(Respiratory rate,RR)、潮氣量(Tidal volume,VT)、氧合指數(PaO2/FiO2)等,并計算RSBI,計算公式為RSBI=RR/VT。
2.2 心功能評估:采用西門子Acuson X300彩色超聲診斷儀進行心功能評估,包括左室舒張末內徑(Left ventricular end-diastolic diameter,LVED)和左房內徑(Left atrial diameter,LAD),并根據公式計算左心室射血分數(Left ventricular ejection fraction,LVEF)。
2.3 肺超聲(Lung Utrasonography Score,LUS)評分評估:以腋前線、腋后線為界,將一側胸壁分為前、側、后3個區,每個區分上、下部,左、右胸壁各6個區域,合計12個區域。SBT前對各個區域進行肺部超聲檢查并按照下列標準評分[8]:①0分(正常通氣區):存在肺滑動,A線和(或)不超過兩條B線;②1分(中度通肺通氣減少區):存在多條、分隔B線;③2分(重度通肺通氣減少區):存在多條、融合B線;④3分(肺實變區):呈支氣管充氣征。LUS評分為12個區域評分之和,分值范圍0~36分,得分越高提示肺通氣功能越差。
2.4 膈肌功能監測:采用西門子Acuson X300超聲儀在SBT開始后30 min監測膈肌功能。患者取仰臥位,選用2.5~5.0 MHz超聲探頭,從雙側腋前線移至肋弓下緣,以肝、脾為膈肌透聲窗。切換為M模式,監測膈肌運動,取樣線與膈肌垂直,測量膈肌運動范圍,即膈肌移動度(Diaphragm mobility, DE)=吸氣末膈肌幅度-呼氣末膈肌幅度。同時,于腋中線與肋間腋前線處測量吸氣末膈肌厚度(Diaphragm thickness at the end of inhalation,DTei)和呼氣末膈肌厚度(Diaphragmatic thickness at the end of expiration,DTee)。膈肌增厚率(Diaphragm thickening rate,DTF)=(DTei-DTee)/DTee×100%。所有測量均在一個呼吸周期內,取3次測量平均值,由取得重癥超聲資質的高年資醫師完成。
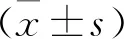
結 果
1 兩組患者一般資料比較 與撤機失敗組相比,撤機成功組年齡較小,MV時間較短,膿毒癥病情較輕,APEACHE Ⅱ評分、SOFA評分、LUS評分、RR、LAD、RSBI較低,LVEF、PaO2/FiO2、DE、DTF較高,差異均有統計學意義(P<0.05)。兩組性別、基礎疾病、HR、SBP、DBP、MAP、LVED比較,均無統計學差異(P>0.05)。見表1。
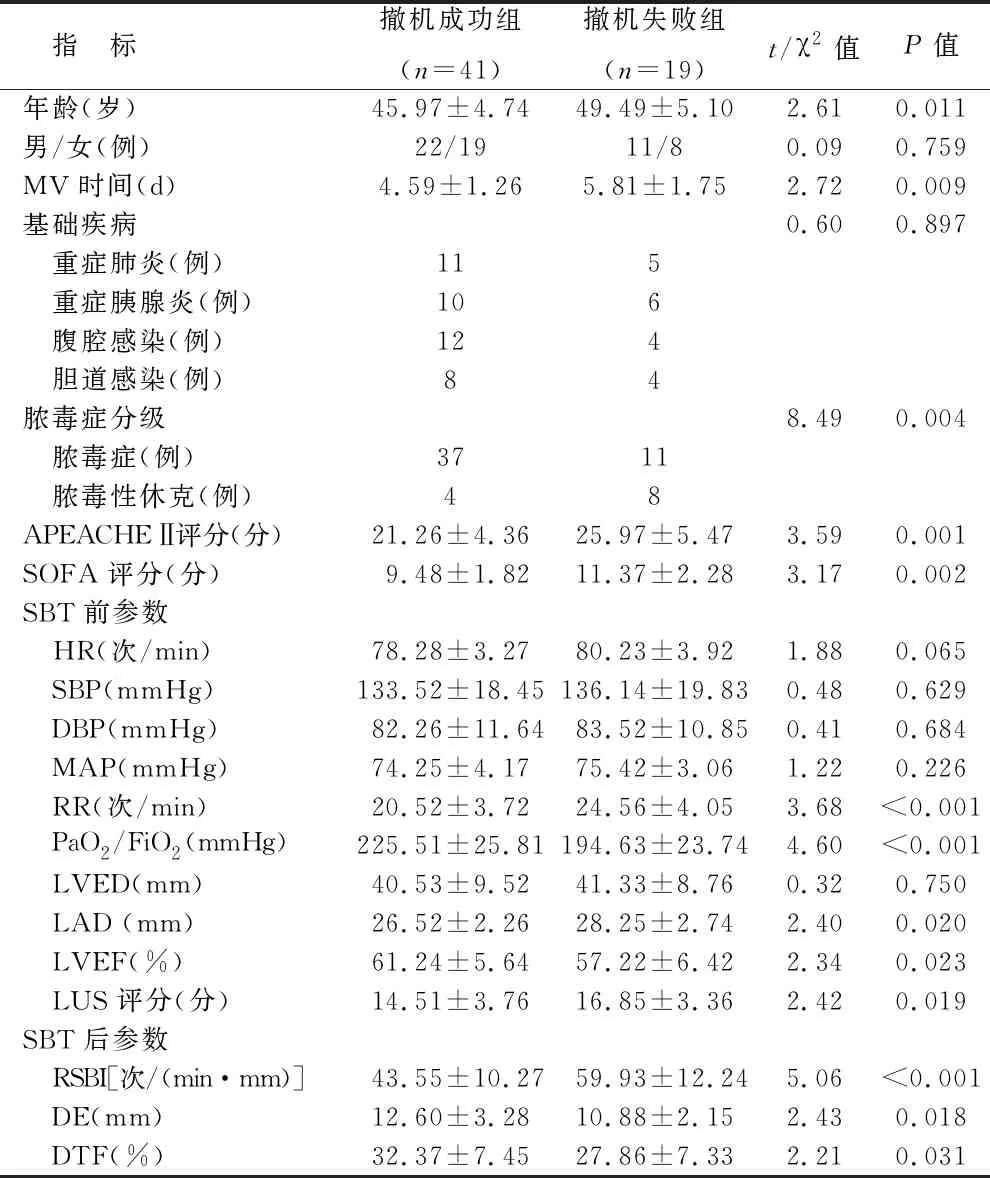
表1 兩組患者一般資料比較
2 膿毒癥MV患者撤機失敗的多因素回歸分析 將單因素分析有統計學意義的因素納入逐步非條件Logistic回歸分析,結果顯示RSBI、LAD、LUS評分是膿毒癥MV患者撤機失敗的獨立危險因素,而DTF則是保護性因素(P<0.05)。見表2。
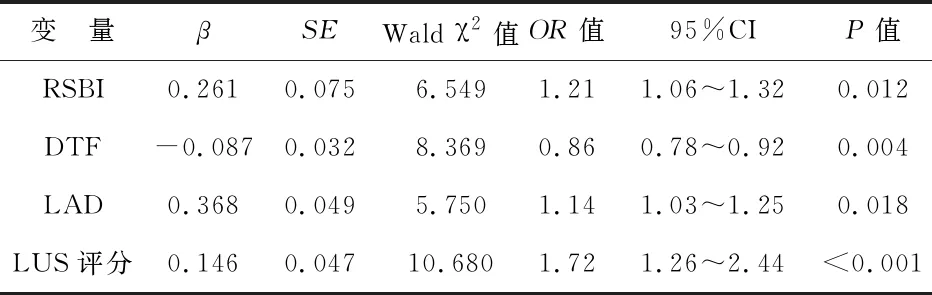
表2 膿毒癥MV患者撤機失敗的
3 各指標對膿毒癥MV患者撤機結局的預測價值 對RSBI、LAD、DTF、LUS評分進行ROC曲線分析,結果顯示RSBI、LAD、DTF、LUS評分聯合預測膿毒癥MV患者撤機失敗的AUC為0.956(95% CI:0.920~0.998),靈敏度為94.7%,特異度為97.6%,均顯著高于4個指標的單獨預測結果(P<0.05)。見表3(圖1)。

圖1 各指標預測膿毒癥MV患者撤機失敗的ROC曲線
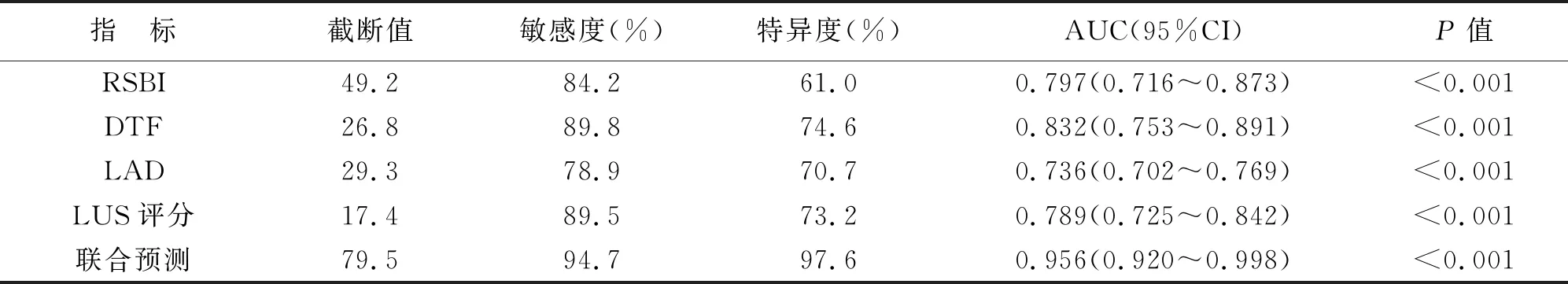
表3 各指標對膿毒癥MV患者撤機結局的預測價值
討 論
MV撤機與最小化機械通氣時程一直是急重癥領域研究的熱點與難點。眾所周知,當接受MV的原發疾病改善,自主呼吸能力可滿足通氣需求時,應及時撤除MV對呼吸的支持,恢復完全自主通氣,但超過20%的危重癥患者可能出現撤機失敗,從而導致再插管率與病死率升高,膿毒癥患者因普遍存在肺功能損傷,撤機問題更為突出[9-10]。Dehghani等[11]研究認為,MV撤機的成敗是多因素共同作用的結果,除原發疾病控制不佳外,主要包括呼吸道及肺功能障礙、腦功能障礙、心功能障礙、膈肌功能障礙、內分泌和代謝功能障礙。因此,及時準確地評估相關危險因素并積極干預是提高膿毒癥患者撤機成功率的關鍵。
RSBI既往被視為預測撤機結局的首選指標。Spadaro等[12]研究表明,RSBI>105次/(min·mm)時,對撤機結局預測的靈敏度高達95%,而當RSBI<105次/(min·mm)時,特異度僅為67%,且不同研究報道中RSBI預測撤機的閾值差異較大。本研究結果顯示,RSBI是膿毒癥MV患者撤機失敗的獨立危險因素,以RSBI<49.2次/(min·mm)為標準預測撤機成功,靈敏度可達84.2%,但特異度僅為61.0%。由此可見,單純依靠RSBI無法準確預測撤機結局,假陰性較高。近年來,隨著重癥超聲技術的快速發展,其作為一種重要床旁工具廣泛應用于心肺衰竭的重癥患者撤機評估,且在膈肌監測方面獨具優勢[13]。呼吸機相關膈肌功能障礙與MV時程的相關性愈發引起關注,MV 18~24 h即可導致膈肌功能障礙[14]。本研究發現,撤機成功組 DE、DTF較撤機失敗組高,尤其是DTF對預測撤機結局的靈敏度和特異度可達89.8%、74.6%,說明DTF作為膈肌厚度動態指標,可更真實地反映膈肌功能,避免SBT期間肋間內肌、外肌等輔助呼吸肌的干擾[15],有效識別并預測撤機失敗的高危患者。
由于微循環障礙、組織低灌注,膿毒癥患者多合并多器官局部缺血,可導致心臟收縮、舒張功能障礙,其中左心室舒張功能障礙可導致膿毒癥患者死亡風險增加[16]。撤機時,患者胸膜腔內壓逐漸下降,回心血量、心室跨壁壓增加,誘發心臟前、后負荷升高。同時,交感神經興奮,兒茶酚胺分泌增加,導致心肌氧耗增加,老年膿毒癥患者對心功能變化更為敏感。Landesberg等[17]研究認為,心功能不全可影響患者的撤機結局,導致撤機延遲或失敗,約占所有撤機失敗的87%,同時撤機可能進一步加重心肺功能下降,故膿毒癥患者撤機前尤其需要關注心肺功能。本研究中,SBT前LAD、LUS評分與撤機結果密切相關,與姜明明等[18]研究結果一致。LAD是反映左室舒張功能較敏感的指標,而LUS評分是肺通氣減少程度的量化評價工具,能夠有效反映肺部通氣丟失、肺泡塌陷情況。Soummer等[19]發現,當SBT末LUS評分>17分時,拔管后呼吸窘迫風險為85%,而當LUS評分<13分時撤機成功率高。進一步分析發現,上述各指標聯合評價對撤機成功率具有更高的敏感性和特異性,從而更加全面地評估撤機條件,以便于及時調整治療策略,最大限度地改善預后。
綜上所述,除RSBI等傳統指標外,結合重癥超聲監測DTF、LAD、LUS評分等指標有助于提高膿毒癥MV患者撤機結局預測準確性,從而指導臨床治療。

