LI-RADS超聲分類診斷肝臟占位性病變準確性分析*
羅利紅,胡 潔,周 啟
肝臟占位性病變包括多種良性或惡性病變,而惡性腫瘤發展迅速,死亡率高[1]。很多腫瘤患者是在病情進展到中晚期才出現臨床癥狀,因而早期診斷和鑒別出良惡性病變意義重大,對改善患者生活質量和提高生存率起著極為關鍵的作用[2,3]。超聲造影(contrast enhanced ultrasound,CEUS)可實時動態反映不同肝臟占位性病變在動脈期、門脈期和延遲期等不同時相下的特征變化,具有良好的分辨率,有助于正確判斷病灶的良惡性,且操作簡便,無腎毒性,無輻射危險,被廣泛應用于肝臟影像學報告和數據系統對于肝臟占位性病變的診斷[4,5]。2011年美國放射學會(ACR)發布的肝臟影像學報告和數據系統(liver imaging report and data system,LI-RADS)被世界各國學者廣泛采用[6,7]。本研究探討了應用LI-RADS超聲分類系統診斷肝臟占位性病變的準確性,以期為臨床早期診斷肝臟占位性病變提供依據,現報道如下。
1 資料與方法
1.1 一般資料 2018年1月~2019年9月在我院經穿刺細胞學或手術組織病理學檢查診斷為肝臟占位性病變患者60例,男38例,女22例;年齡為39~76歲,平均年齡為(56.83±8.12)歲。單發結節39例,2個或以上結節21例。排除對超聲造影劑過敏者,本研究經我院醫學倫理委員會審核批準,患者簽署知情同意書。
1.2 超聲造影 使用Philips IU22超聲造影診斷儀和Sono Vue超聲造影劑。檢查前一天,清淡飲食,檢查當天空腹。在造影前,先用生理鹽水5 ml與造影劑凍干粉末混合,搖晃至混勻的混懸液,抽取2.4 ml,經肘靜脈團注,繼之再注入生理鹽水5 ml。先使用常規超聲對全肝進行掃查,記錄病灶大小、數目、邊界和回聲等,并使用彩色多普勒超聲全面評估病灶。隨后,進入超聲造影模式,選擇最佳觀察面,調節聚焦點至圖像最低處,在注射造影劑的同時開始計時并持續觀察,直至掃查切面中的微氣泡消失時停止,儲存圖像。CEUS過程分為3個時相:即動脈期、門脈期和延遲期。
1.3 超聲造影LI-RADS分類標準[8]肝臟良性病變的主要超聲征象包括:(1)典型含液體性病變或囊腫;(2)后方回聲增強;(3)CDFI彩色多普勒超聲檢測病變無血流;(4)壓縮性好;(5)無明顯占位效應;(6)病變周邊血管無擠壓或繞行,或直接穿過其內。肝臟惡性病變的主要超聲征象包括:(1)形態不規則;(2)塊中塊、結中結;(3)邊界不清。模糊、微小分葉、成角或毛刺征;(4)占位效應:駱峰征、邊緣角變形征;(5)低回聲暈;(6)邊緣血管征:中斷、繞行,或者病變內可探及動脈血流頻譜;(7)與周圍器官或病變周圍的肝臟組織比,壓縮性差;(8)肝硬化背景:肝結節≥1.0 cm;(9)靜脈、膽道栓或其他器官轉移現象;(10)三個月隨訪,發現腫瘤增大≥3 mm。LR-1類為明確的良性病變,即根據超聲表現高度提示為良性病變;LR-2類為可能為良性病變,即根據超聲表現高度提示為良性病變;LR-3類為可疑惡性病變,即病灶既無主要的良性超聲征象,亦無主要的惡性超聲征象,或者有不典型良性主要超聲征象或不典型惡性主要超聲征象,似是而非無法確定,其患惡性腫瘤的風險<5%;LR-4類可能為惡性病變,即病灶超聲影像出現主要的惡性征象,或者既有良性主要征象又有惡性主要征象,尤其是惡性主要征象多于良性主要征象。有1個主要超聲惡性征象為LR-4a,有2個為LR-4b,有3個為LR-4c;LR-5類幾乎肯定為惡性病變或已經明確為惡性病變。根據超聲征象,醫師有把握確定病灶為惡性病灶時,其患惡性腫瘤的風險在95%以上。有4個或以上的惡性病變主要征象為LR5。本研究按照兩種方法定義良性與惡性腫塊,方法1:以LR-3為截斷點,將LR-1、LR-2和LR-3設定為良性腫塊,記為LR-1~3組,將LR-4和LR-5設定為惡性腫塊,記為LR-4a~5組;方法2:以LR-4a為截斷點,將LR-1~LR-4a設定為良性腫塊,記為LR-1~4a組,將LR-4b~LR-5設為惡性腫塊,記為LR-4b~5組。
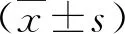
2 結果
2.1 LI-RADS分類診斷情況 見表1和圖1。

表1 LI-RADS分類診斷肝臟占位性病變【n(%)】情況

圖1 肝臟占位性病變患者超聲造影表現 A:肝內一直徑約4.2 cm低回聲占位,邊界不清。CEUS顯示動脈期呈高增強,邊界不清;B:與A為同一患者,CEUS顯示門脈期病灶可見廓清,呈低增強。術后病理學檢查證實為肝細胞癌;C:肝內數個低回聲占位,直徑約2.5 cm,邊界清。CEUS顯示動脈期環狀強化,邊界清;D:與C為同一患者,CEUS顯示門脈期病灶呈高增強,診斷為血管瘤
2.2 兩種LI-RADS分類方法與病理學檢查結果比較 在60例患者中,經病理學檢查診斷惡性14例,良性病變46例。兩種超聲分類方法診斷效能見表2和表3。

表2 兩種方法診斷60例患者情況
3 討論
肝內組織的異常增生、異常代謝等因素引起肝臟局部組織病理性改變,是肝臟較常見的占位性病變。如何對肝臟惡性占位性疾病進行快速、準確和無創的診斷成為當前的研究熱點[9,10]。超聲造影技術能夠清楚地顯示肝臟和腫瘤的血流狀況及組織灌注情況,更能突出腫瘤的實質病變,增加了肝占位性病變與正常組織的影像學表現的差異[11,12]。造影劑可被排泄,安全性較高[13,14]。LI-RADS超聲造影分類標準是一個規范的報告系統,其基于肝內病灶的大小、增強開始時間和方式、廓清開始時間和程度等進行分類[15,16]。LI-RADS分類多用于CT和MRI診斷肝細胞癌。研究表明LI-RADS的MRI分類對肝細胞癌的診斷有很好的臨床應用效果,有利于提高診斷的準確性[17]。近年來,也有應用超聲造影的LI-RADS報道。超聲造影LI-RADS分類可用于診斷混合型肝癌,其超聲模式主要是高增強和周邊環狀強化[18],但仍需大規模數據的驗證。本組肝細胞癌患者聲像學表現特點為動脈期顯示高回聲,門靜脈期和延遲期為低回聲,對比劑在占位處表現呈典型的“快進快出”。由于新生血管多,血流較為豐富。超聲造影檢查肝臟血管瘤為動脈期病灶周邊呈環狀高回聲增強,門靜脈期對比劑呈向心性填充進行性增強,延遲期仍見有顯著的對比劑攝取,呈典型的“慢進慢出”表現19]。
將超聲造影LI-RADS分類標準應用于肝細胞癌的診斷,一般分為兩種:一種將LR-1和LR-2類歸為陰性,將LR-3、LR-4和LR-5類確定為診斷;第2種將LR-1、LR-2和LR-3歸為陰性,將LR-4和LR-5類確定為診斷。應用第2種方法診斷的陽性預測值和特異性較高[20]。也有另2種分類,第一種同前,即將LR-3~LR-5類確定為診斷,第2種排除了LR-3類病灶,將LR-1~2歸為陰性,將LR-4和LR-5類確定為診斷。第二種方法診斷的正確率和特異性較第一種高。本研究應用兩種方法診斷,也發現第二種方法診斷的特異性和正確率更高,提示LI-RADS超聲分類診斷肝臟占位性病變具有很大的臨床價值。占位性病變聲像圖具有多樣性和復雜性,良惡性占位病變征象往往存在一些交叉。LI-RADS分類能夠將病變進行分級,提高了二維超聲診斷肝臟占位性病變的效能。在LI-RADS分類中,LR-3類表現為既不出現明顯的良性性征象也不出現明顯的惡性征象,而LR-4a出現1個惡性征象,因而以LR-4a為截斷點,將LR-4b~LR-5作為惡性腫塊,其診斷的陽性預測值稍高于方法1。
超聲造影用于診斷肝臟占位性病變較超聲和CT有一定的優勢,診斷的正確率高,且無輻射。有研究表明超聲造影檢查肝臟占位性病變,其診斷的敏感性、特異性和準確性分別為95.6%、98.6%和96.8%。超聲造影能使1.0 cm以下的肝癌檢出率從54%提高到96%,且經濟便捷,無X線損傷。LI-RADS分類可以增強影像學報告的診斷信息量,提升診斷的準確性,方便臨床醫師應用。本研究在鑒別肝臟占位性病變方面,應用該方法具有一定的應用價值。有時,對于一些超聲表現不典型的病灶很難對其進行有效的分類,因而仍存在假陽性和假陰性的可能。所以,結合CT或者MRI、病史、穿刺活檢和積極的隨訪仍屬必要。本研究還存在一些不足之處,本研究為回顧性研究,可能存在選擇偏倚,在后續研究中將聯合其他醫院擴大樣本量進行研究。超聲造影結果的評判依賴于操作者的主觀能力,其評估結果受醫生對疾病認知等多方面的影響。加強對超聲醫師LI-RADS和肝臟占位性病變診斷特征的系統培訓,以提高分類診斷的準確性。
綜上所述,超聲LI-RADS分類診斷肝臟占位性病變具有一定的臨床應用價值,將LR-1-4a以下設定為良性腫塊,將LR-4b-5設定為惡性腫塊的方法2診斷效能更佳。

