替格瑞洛改善心肌缺血再灌注損傷的機制
陳佩兒 陳燦 何原 莫少門 葉文桃 鐘劍鋒
廣東醫科大學附屬醫院(廣東湛江524001)
急性心肌梗死(acute myocardial infarction,AMI)是冠狀動脈急性、持續性缺血缺氧所引起的心肌壞死,嚴重威脅著人類的健康[1]。隨著冠狀動脈介入手術(percutaneous coronary intervention,PCI)的開展與藥物溶栓的應用,雖大大降低了急性心梗患者的短期病死率,但卻無法明顯改善患者的遠期預后,其主要原因在于閉塞的冠狀動脈再次開通后引起了缺血再灌注損傷(ischemiareperfusion injury,IRI)[2-3]。
再灌注后引發的氧化應激和炎癥反應是導致心肌損害的重要因素[4-6]。NF-κB 通路在調控氧化應激和炎癥損傷中起重要作用,在炎癥及腫瘤發展中發揮關鍵性的調控[7-8]。NADPH 氧化酶(NOX)是人血管系統中活性氧(reactive oxygen species,ROS)的主要來源[9]。近年來研究[10]發現,血管內皮細胞產生的ROS 主要來源于NOX4。再灌注后炎癥反應能夠上調心肌細胞中NOX4的表達,引起ROS 升高并直接損傷細胞,而ROS 亦可促使炎癥相關因子的表達提高間接地損傷細胞。
替格瑞洛(Ticagrelor)是新型P2Y12受體拮抗劑,可以在心腦血管系統中快速地發揮抗血小板作用[11-12]。替格瑞洛除了作用于P2Y12受體外,還有文獻報道替格瑞洛具有減輕缺血再灌注損傷的作用,降低心肌細胞需氧量、提高心肌組織中SOD 活性、抑制中性粒細胞黏附和減少自由基,改善了缺血再灌注后的心肌損害[13],而目前其機制尚未明確。筆者預實驗結果顯示替格瑞洛不僅可以降低炎癥因子的釋放、減輕ROS的生成,還可能抑制NF-κB信號通路的活化。本實驗旨在探討替格瑞洛是否通過NOX4/ROS/NF-κB信號通路軸下調炎癥因子表達及減輕氧化應激反應,從而改善缺血再灌注相關的心肌損傷,證實替格瑞洛治療AMI較氯吡格雷的有效性。
1 材料與方法
1.1 一般材料8~10周齡250~300 g 雄性SD大鼠,由廣東醫科大學實驗動物中心提供。細胞裂解液、BCA 蛋白濃度測定試劑盒、總抗氧化能力檢測試劑盒(碧云天,中國),ELISA 試劑盒(達科為,中國),兔抗鼠NOX4 抗體、P-p65 抗體、IκB 抗體、P-IKK抗體(Abcam,美國),替格瑞洛(Sigma,美國)。
1.2 動物分組與處理利用完全隨機數字法將60只250~300 g的雄性SD大鼠分為,Control(N):對照組;Sham(S):缺血再灌注損傷+生理鹽水組;Clopidogrel(C):缺血再灌注損傷+氯吡格雷組;Ticagrelor(T):缺血再灌注損傷+替格瑞洛組,每組15只。其中S、C、T組大鼠通過制備心肌缺血再灌注損傷模型,C、T組大鼠在手術前灌胃強飼抗血小板藥物,分別給予300 mg/kg(根據預實驗藥物濃度的篩選及文獻報道[16])Clopidogrel、Ticagrelor預處理,連續7 d,同時Control組和Sham組大鼠給予同等量的生理鹽水。
1.3 SD大鼠缺血再灌注損傷模型的建立選取約250 g的雄性SD大鼠,用5%水合氯醛麻醉,同時將自制的專用面罩套住大鼠外呼吸器官,固定好面罩后連接呼吸機,待呼吸平穩后接著在老鼠的胸部上進行刮毛備皮,用刀片小心切開大鼠胸前3-4 肋間皮膚,充分暴露大鼠心臟,視野清晰后在左側肺動脈圓錐和左心耳交界下緣2 mm的區域進針,用U型管以壓管的方式活結結扎LAD,一般可以看到心肌壞死后變色,大概30~45 min后可以解開活結開通血管,心臟缺血再灌注損傷的模型即完成。
1.4 SD大鼠內眥靜脈血液采取將大鼠放置于木板平面上,用左手的大拇指和食指從上而下輕輕按住大鼠的頭頸部,逐漸將大鼠的眼球突出,右手用鑷子夾起酒精棉球輕輕擦拭大鼠的眼球周圍,再用右手拇指和食指捏住一根已經用肝素進行過抗凝的毛細玻璃管,緩慢插入大鼠的眼睛前下方內眥處,可看到血液流入管內,然后取抗凝管在毛細管通道下接血,最后取出毛細玻璃管。
1.5 ELISA在預包被的酶標板中加入樣品和標準品,37℃反應90 min,不洗;加生物素標記抗體,37℃反應60 min,0.01 mol/L TBS洗滌3次;加ABC,37℃反應30 min,0.01 mol/L TBS洗滌3次;加TMB,37℃反應25 min,0.01 mol/L TBS洗滌3次;加入TMB 終止液,波長A450 測定,根據標準曲線計算出樣品中各指標的濃度。
1.6 總抗氧化能力檢測試劑盒(FRAP法)在96孔板的每個檢測孔中加入180 μL FRAP 工作液;空白對照孔中加入5 μL PBS;標準曲線檢測孔內加入5 μL 各種濃度的FeSO4標準溶液;樣品檢測孔內加入5 μL 各種樣品作為陽性對照,輕輕混勻;37℃孵育3~5 min后測定波長A593測定。
1.7 Western blot檢測NOX4/ROS/NF-κB信號通路軸表達。提取心臟組織的蛋白質,采用BCA 試劑盒(碧云天,中國)測量蛋白濃度,計算上樣量。蛋白電泳后轉膜、脫脂奶粉封閉、小鼠一抗4℃孵育過夜,次日復溫1 h后孵育二抗2 h后進行曝光,用α-tubulin 作為內參(稀釋比例1∶1 000,武漢博士德)。采用Image J分析灰度值,以目的條帶灰度值/內參條帶灰度值進行統計分析。
1.8 統計學方法采用GraphPad Prism 7 對結果進行統計學分析,數據以均數±標準差表示,多組之間總體均數比較使用單因素方差分析,兩組采用t檢驗進行數據比較。以P<0.05為差異有統計學意義。
2 結果
2.1 用ELISA法檢測靜脈血相關炎癥指標筆者發現大鼠在心肌缺血再灌注損傷模型術前、后連續7 d 服用替格瑞洛,靜脈血中的炎癥因子水平(IL-1β、IL-6、TNF-α)對比各組顯著減低,差異有統計學意義(圖1)。
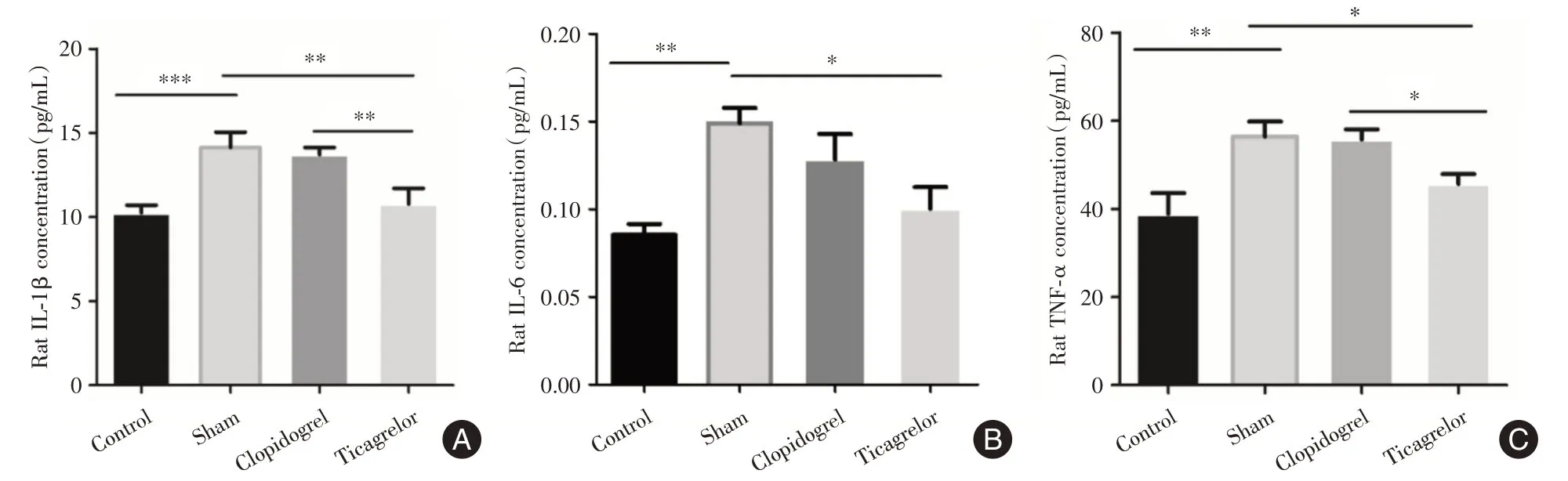
圖1 替格瑞洛可降低缺血再灌注損傷后炎性因子的積累Fig.1 Ticagrelor can reduce the accumulation of inflammatory factors after ischemia-reperfusion injury
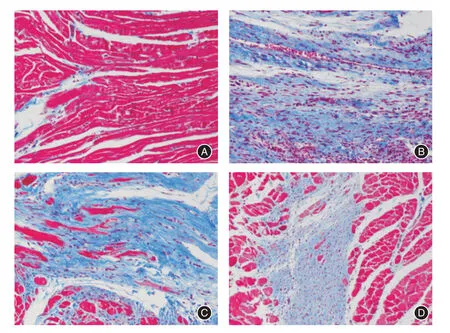
圖2 替格瑞洛干預處理組纖維面積明顯減少(×200)Fig.2 Ticagrelor can significantly reduce cardiac fibrosis after ischemia-reperfusion injury(×200)
2.2 在心肌缺血再灌注損傷模型后,光鏡下觀察不同處理組心肌組織馬松染色筆者通過光鏡下觀察心臟Masson 染色發現(圖2),與正常組(N組)心臟組織相比,生理鹽水組(S組)的心肌纖維化更嚴重,心肌壞死范圍和面積更大,而氯吡格雷組(C組)的心肌纖維化稍減輕,心肌纖維化面積稍減少,而令人振奮的是,替格瑞洛組(T組)的心肌細胞纖維化程度更低。
2.3 在心肌缺血再灌注損傷模型后,不同處理組NOX4的表達水平見圖3,相對于正常組(N組),生理鹽水組(S組)的NOX4表達顯著升高(P<0.001),提示缺血再灌注后心肌細胞的氧化應激反應被明顯激活,缺血再灌注損傷的替格瑞洛組(T組)和氯吡格雷組(C組)都可以相應地減少氧化應激相關因子NOX4的表達,但是替格瑞洛組相對于氯吡格雷組的氧化應激相關因子NOX4的表達相對更低(P<0.05)。
2.4 在心肌缺血再灌注損傷模型后,不同處理組FRAP值的水平用FRAP法測定血漿中總抗氧化能力,在心肌缺血再灌注模型中,術前連續7 d服用替格瑞洛組(T組),血漿中總抗氧化能力顯著高于氯吡格雷組(C組),差異具有統計學意義(圖4)。
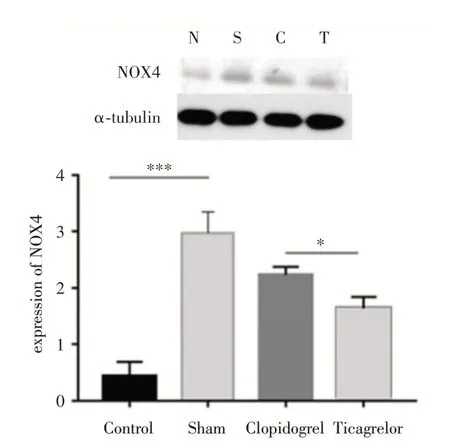
圖3 不同處理組NOX4的表達水平,替格瑞洛組NOX4 明顯較低Fig.3 Ticagrelor can significantly reduce the expression of NOX4
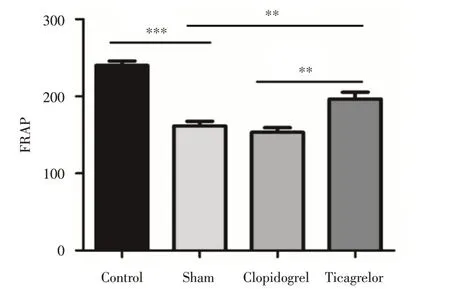
圖4 不同處理組FRAP值的水平,替格瑞洛組總抗氧化水平較高Fig.4 Among the different treatment groups,Ticagrelor had the highest FRAP level
2.5 在心肌缺血再灌注損傷模型后,不同處理組NF-κB信號通路相關激活因子表達情況為了探究替格瑞洛是否通過NOX4/ROS/NF-κB信號通路下調炎癥因子表達及減輕氧化應激反應,我們用Western Blot 法檢測NF-κB信號通路的相關因子。P-p65 主要存在于活化的NF-κB 二聚體中,與正常組對比,生理鹽水組(S組)和氯吡格雷組(C組)的P-p65表達水平顯著升高(P<0.05),而替格瑞洛組與正常組差異無統計學意義,說明替格瑞洛可以抑制NF-κB信號通路的活化(圖5A);如圖5B所示,替格瑞洛處理組(T組)相對于生理鹽水(S組)、氯吡格雷組(C組)的P-IKK表達均有明顯降低(P<0.01),說明替格瑞洛可以減少IKK的激活;同時IκBα是NF-κB信號通路的抑制因子,當缺血再灌注時IκBα被迅速降解,其表達可明顯降低(P<0.001),而替格瑞洛處理組相對于氯吡格雷組的IκBα表達相對降解減少(P<0.01),提示替格瑞洛可以減輕NF-κB信號通路的激活,減輕炎癥反應(圖5C)。
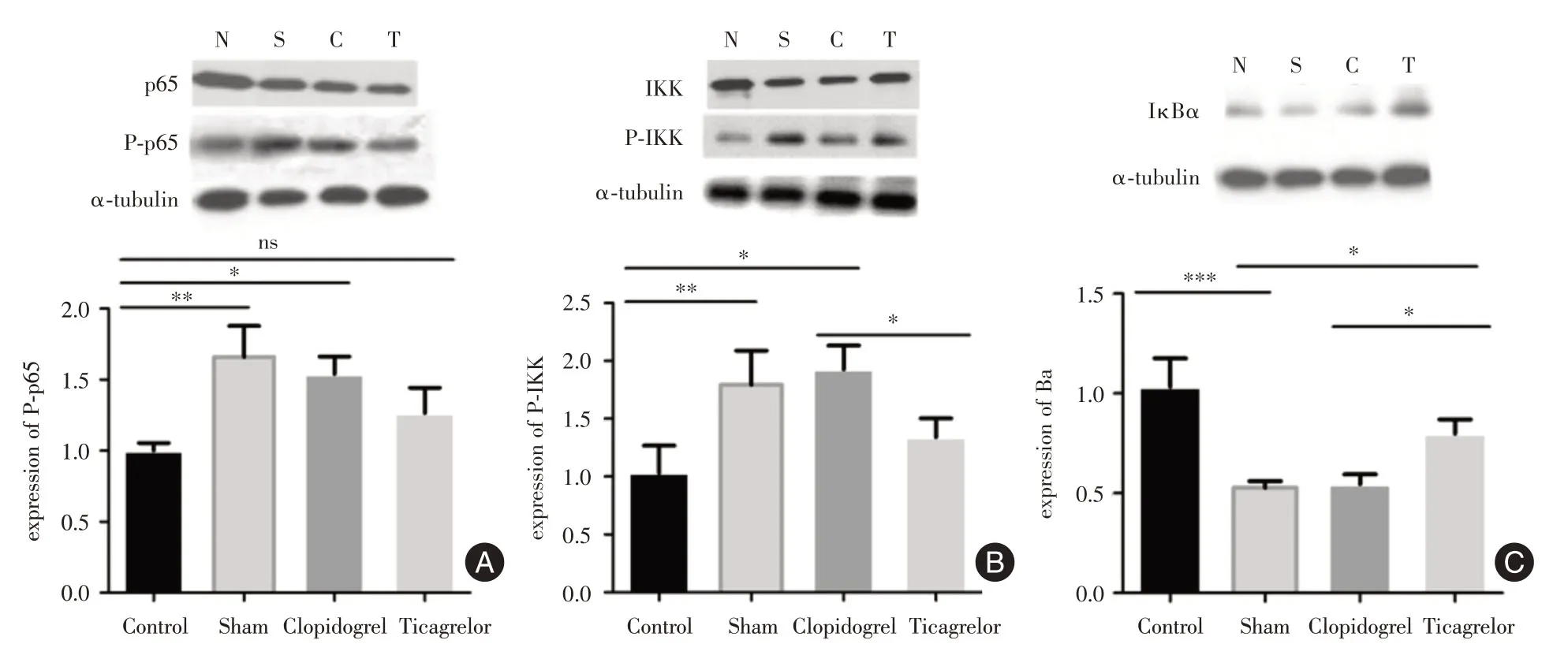
圖5 Western blot 中不同組別P-p65、P-IKK、IκBα的蛋白表達水平Fig.5 The protein expression levels of P-P65、P-IKK、IκBα in different groups
3 討論
目前的研究結果表明,心肌缺血再灌損傷的相關機制主要包括鈣超載[14]、pH 快速變化[15]、線粒體功能障礙[16-17]、氧化應激反應[18]、炎癥損傷[19]及細胞凋亡[20]等,并且各個機制并不是孤立發生的,而是可以相互之間調節的,其中鈣超載以及ROS 產生是缺血再灌注損傷的基石。
NADPH氧化酶在各個組織中主要存在7種NOX的同功酶[9],主要包括NOX1~NOX5,DOU X1~X2,而NOX4是存在于缺血再灌注心肌細胞中的NADPH 氧化酶亞基的主要類型。當NOX4 活性顯著增強時,胞內ROS水平顯著升高,導致心肌受損壞死,心臟纖維化面積增大,從而提示NOX4 源性的ROS可通過誘導氧化應激和炎癥反應參與心肌缺血再灌注損傷的過程[9-10]。同時,NF-κB 通路在調控氧化應激和炎癥損傷中也起重要作用。NF-κB家族有5個主要成員,分別為P50、P52、P65、c-Rel和RelB。這些轉錄因子在非激活狀態時主要位于細胞質,與其抑制蛋白IκBs(IκBα、IκBβ、IκBε)結合形成無活性的三聚體存在細胞中;當受到內外因素刺激時,可激活IκB 激酶(IKK),促使IκB 磷酸化,并被迅速降解,使NF-κB 通路被激活,并進入細胞核與靶基因中相應的DNA 結合位點結合,隨后啟動靶基因轉錄[19,21]。特別需要注意的是,NOX4/ROS/NF-κB信號通路不僅僅是單向進行的。在NOX4/ROS/NF-κB信號通路中,心肌缺血再灌注時,各種炎癥刺激NOX4的表達并產生大量胞內ROS,同時促使IKK 激活,促進IκB 磷酸化降解而活化NF-κB,而NF-κB的活化將會上調表達大量炎癥因子,進而又會反過來繼續刺激NOX4的表達及誘發產生更多的ROS 加劇氧化應激損傷,形成NOX4/ROS/NF-κB 正反饋信號環,對心肌造成持續性、不可逆性的損害。
目前抗血小板藥物主要由TXA2 抑制劑、P2Y12受體拮抗劑以及GPII b/Ⅲa 受體抑制劑、PDEs 抑制劑等組成。噻吩吡啶類如氯吡格雷等藥物主要在血小板壽命期間不可逆地與P2Y12受體結合,與氯吡格雷不同,替格瑞洛可逆地與受體結合并表現出快速起效[11]。除了抗血小板作用外,目前的文獻報道替格瑞洛能改善缺血再灌注后心肌的損傷[13],主要是通過調節血中的腺苷的水平而發揮作用[22-23]。張鳳等[24]研究納入125例計劃接受急診PCI的STEMI患者,隨機給予替格瑞洛或氯吡格雷治療。在PCI術前、術后等不同時間點測定Angptl 2(血清血管生成素樣蛋白2)水平。分析結果提示,替格瑞洛較氯吡格雷有更強降低炎性因子Angptl 2 水平,提高動脈粥樣硬化斑塊的穩定性。
本研究利用大鼠構建心肌缺血再灌注損傷模型,深入探討替格瑞洛的保護作用及相關分子機制。通過術前藥物灌胃處理,術后采集內眥血和心臟標本進行檢測,發現替格瑞洛更能降低IL-1β、IL-6、TNF-α炎癥水平(P<0.05)以及氧化應激相關因子NOX4的表達水平(P<0.05);同時總抗氧化能力提高和心肌纖維化程度減輕,說明替格瑞洛對缺血再灌注損傷有抗氧化應激、抗炎的作用。另外,使用替格瑞洛能降低的NF-κB信號通路相關激活因子Phospho-IKK、NF-κB p65 等的表達水平(P<0.05),相反NF-κB信號通路相關抑制因子IκB的降解減少(P<0.01),由此看出缺血再灌注損傷后的氧化應激和炎癥反應可以誘導NF-κB信號通路的活化,同時替格瑞洛可以通過降低NOX4的過表達,進而減少ROS 生成,抑制IKK的激活,減少IκB的降解,最終將抑制NF-κB信號通路的活化,減輕炎癥反應。
受到各種因素的影響,本實驗仍存在許多不足的地方。由于大鼠的動物模型機體內環境復雜,實驗結果可能收到多種混雜因子和不同的刺激因素交織影響,今后需在體外實驗進一步驗證替格瑞洛在缺血再灌注損傷的保護機制,同時需進行大樣本的臨床研究,在人體中證實其抗氧化應激、抗炎、減輕缺血再灌注損傷的作用。
冠脈介入手術聯合替格瑞洛能夠有效抗氧化應激、抗炎、減輕缺血再灌注損傷,減少術后不良事件,這使得STEMI患者大大獲益。

