微波等離子體原子發射光譜法測定食用堅果油中的金屬元素
張萍,劉宏偉
(湖南工學院 材料與化學工程學院,湖南 衡陽, 421002)
堅果作為植物的精華部分,富含不飽和脂肪酸、纖維、維生素、礦物質和許多其他生物活性物質[1],是地中海飲食的重要組成,增加堅果的攝入量可以降低患慢性病的風險[2]。堅果油是采用壓榨、超臨界以及亞臨界萃取工藝處理堅果獲得的食用植物油,是人們膳食結構中所需油脂的主要來源[3]。堅果油的總體質量等級和指標主要取決于其含有機成分[4-6],但其所含無機成分會直接影響堅果油的口味、保質期以及食用安全性[7]。堅果對生長環境中無機元素的吸收和富集,以及堅果在收獲、運輸或加工過程中與其他外來物接觸受到污染,構成了堅果油中無機元素的重要來源,準確檢測堅果油中無機元素的含量具有十分重要的意義。
食用植物油中無機元素的測定常采用原子吸收分光光度(atomic absorption spectrometry,AAS)法[8-10]、原子熒光光譜(atomic fluorescence spectrometry,AFS)法[11-13]、電感耦合等離子體原子發射光譜(inductively coupled plasma atomic emission spectrometry,ICP-AES)法和電感耦合等離子體質譜(inductively coupled plasma mass spectrometry,ICP-MS)法[14-16]。其中,AAS法不能同時進行多元素分析,且無法測定共振譜線處于真空紫外區的元素,AFS法可測元素很少,熒光信號強度弱且易受到雜散光的干擾,這些限制了AAS和AFS的推廣應用。采用以電感耦合等離子體(inductively coupled plasma,ICP)為離子源的ICP-AES和ICP-MS法具有線性范圍寬、檢出限(limit of detection,LOD)低、靈敏度高以及分析速度快等特點,尤其是ICP-MS比ICP-AES具有更高的靈敏度和更低的檢出限,但ICP高純氬氣為工作氣,導致ICP-AES和ICP-MS的分析運行成本高。采用氮等離子體源的微波等離子體原子發射光譜(microwave plasma atomic emission spectroscopy,MP-AES)是基于微波導波技術,將磁場與電場的能量通過激發和能量耦合并高效聚集于等離子體激發環境中,使用空氣和氮氣為等離子氣,運行成本較低,且具有穩定性好、性價比高、使用壽命長以及安全環保等特點[17-19]。本文采用微波消解對堅果油樣品進行預處理,利用MP-AES測定其中的金屬元素Na、Mg、K、Cu、Fe、Zn、Mn、Ba,旨在為堅果油中多種金屬元素的快速準確測定提供低成本分析方法。
1 材料與方法
1.1 材料和試劑
1 000 mg/L的Na、Mg、K、Cu、Fe、Zn、Mn、Ba單元素標準溶液,國藥集團化學試劑有限公司;1 000 mg/L的Y、La、Lu內標元素標準溶液,國藥集團化學試劑有限公司;質量分數為65%的超純HNO3,德國Merck公司,使用前亞沸蒸餾純化;質量分數為30%的超純H2O2,德國Merck公司;實驗用水為Milli-Q超純水處理系統制備的超純水。
堅果油樣品分別為花生油(產地山東)、榛子油(產地江西)、山核桃油(產地江西)、葵花籽油(產地江蘇)、山茶油(湖南),購于京東超市。實驗器皿使用前經體積分數為20%的HNO3浸泡24 h,超純水沖洗3次后備用。
1.2 儀器及設備
Agilent 4200型微波等離子體發射光譜儀,配置OneNeb霧化器和玻璃旋流霧化室,美國Agilent公司;MARs 5微波消解儀,美國CEM公司;Milli-Q超純水處理系統,美國Millipore公司;ELAN 6000型電感耦合等離子體質譜儀,美國PE-SCIEX 公司。
1.3 實驗方法
1.3.1 儀器參數
MP-AES參數:RF功率1 000 W;等離子體氣流速15 L/min;霧化氣流速0.75 L/min;泵速15 r/min;讀數時間3 s;樣品提升延遲時間30 s;沖洗時間40 s;穩定時間20 s;背景校正,自動;氣源Agilent 4107氮氣發生器。
微波消解參數:功率1 600 W,溫控100 ℃,爬升3 min,保持3 min;功率1 600 W,溫控150 ℃,爬升7 min,保持3 min;功率1 600 W,溫控170 ℃,爬升5 min,保持3 min;功率1 600 W,溫控190 ℃,爬升5 min,保持10 min。
1.3.2 樣品預處理
準確稱取0.5 g(精準至0.000 1g)堅果油于微波消解罐中,分別加入5 mL質量分數為65%的HNO3和1 mL質量分數為30%的H2O2,敞開罐蓋靜置20 min,置于微波消解儀中按所設參數消解,消解結束后用超純水將消解液轉移至50 mL容量瓶中定容制得樣品溶液,同時制得空白溶液,待測。
1.3.3 MP-AES分析
采用體積分數為5%的HNO3介質分別配制0.00、0.05、2.00、10.0、50.0 mg/L的Na、Mg、K和0.0、0.5、20、100、500 μg/L的Cu、Fe、Zn、Mn、Ba系列標準溶液,采用MP-AES進行測定,建立校準曲線,在相同分析條件下對樣品和空白溶液進行測定,根據校準曲線計算樣品溶液中各待測元素的含量。所有上機測定溶液均在線加入1 mg/L的Y、La、Lu內標溶液。
2 結果與分析
2.1 干擾及消除
2.1.1 光譜干擾及消除
本實驗存在的光譜干擾包括譜線重疊干擾和背景干擾,利用MP-AES的MP Expert分析軟件譜線庫選擇各待測元素的分析譜線消除譜線重疊干擾,通過對各待測元素的多條譜線進行掃描,將各待測元素的標準溶液圖譜與空白溶液圖譜進行對比,優選譜線強度高、信背比大、無干擾或干擾少的譜線為分析譜線。背景干擾與基體組成及來自微波等離子體本身所發射強烈雜散光的影響有關[20],實驗利用MP-AES自帶分析軟件自動扣除背景干擾。
2.1.2 電離干擾及消除
堅果油中的Mg、Na、K為主量金屬元素,為消除易電離元素Na和K所產生的電離干擾,通常加入改性劑或電離抑制劑[21],但同時也會帶入較大的空白值。本實驗為考察Mg、Na、K對元素Cu、Fe、Zn、Mn、Ba的電離干擾,分別配制20 μg/L的Cu、Fe、Zn、Mn、Ba單元素標準溶液,向各單元素標準溶液中分別加入低(0.2 mg/L)、中(2.0 mg/L)、高(20.0 mg/L)濃度的Mg、Na、K混合標準溶液,采用MP-AES進行測定。由圖1可以看出,高濃度的Mg、Na、K對分析元素的影響表現為Fe和Mn測定值偏高,Zn的測定值偏低,對Cu和Ba的測定無影響;低濃度和中濃度的Mg、Na、K不影響分析元素的測定。本實驗在樣品溶液的制備中Na、K的濃度均小于2.0 mg/L,從而消除了元素Na和K所產生的電離干擾。
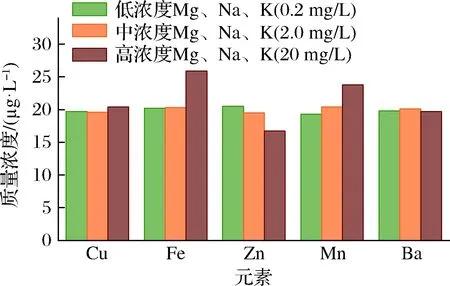
圖1 不同濃度的Mg、Na、K對微量元素的光譜干擾Fig.1 Spectral interference for trace elements by different concentrations of Mg, Na, and K
2.1.3 物理干擾及消除
樣品溶液、標準溶液以及空白溶液的基體組成差異產生物理干擾,本實驗利用內標元素進行消除。在體積分數為5%的HNO3介質中加入1 mg/L的Y、La、Lu內標元素標準溶液,使用帶有“Y”型三通接口的橙色/綠色泵管在線加入,使混合內標溶液在霧化之前與測試溶液匯合,分別選擇Y 371.029 nm、La 394.910 nm、Lu 261.542 nm為分析譜線消除了物理干擾。
2.2 分析穩定性
為檢驗MP-AES的分析穩定性,在3 h內連續測定市售堅果油樣品,每10 min分析1次,總共測定18次,考察分析元素的歸一化信號變化情況,結果見圖2。可以看出,所有分析元素3 h內測定的歸一化信號為1±0.1,表明分析方法為堅果油中8種金屬元素Na、Mg、K、Cu、Fe、Zn、Mn、Ba的測定提供了良好的穩定性。
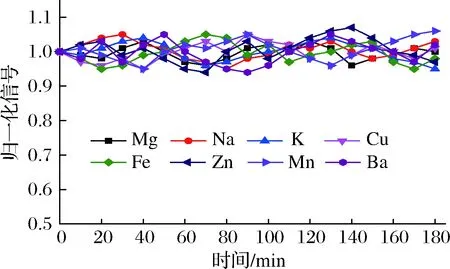
圖2 樣品溶液中分析元素3 h的穩定性Fig.2 Three-hour stability plot for analytes in sample solution
2.3 校準曲線與檢出限
根據8種元素配制的系列梯度混合標準溶液按實驗方法在選定的MP-AES工作條件下進行測試,利用MP-AES自帶MP Expert軟件建立校準曲線。取空白溶液重復測定10次,計算各元素的標準偏差,以3倍標準偏差所對應的濃度為儀器的檢出限,根據稱取的樣品質量和配制樣品溶液的稀釋倍數,將LOD換算為方法檢出限(method detection limit,MDL),結果見表1。由表1可以看出,所有元素的線性相關系數≥0.999 2,線性關系良好。各元素的MDL為0.02~0.12 μg/g。
2.4 方法的準確性驗證
為考察方法的準確性,選取堅果油樣品進行加標實驗。在樣品中分別加入標準溶液經微波消解處理后,采用MP-AES法平行測定6次,計算各元素的回收率和相對標準偏差(relative standard deviation,RSD),并采用ICP-MS進行對比分析,結果見表2。由表2可以看出,各元素的加標回收率為90%~110%,RSD≤5.9%,t檢驗法的統計分析顯示,在95%的置信度水平,方法的加標測定值與采用ICP-MS的測定值無顯著性差異(P>0.05),驗證了方法的準確性好,精密度高。
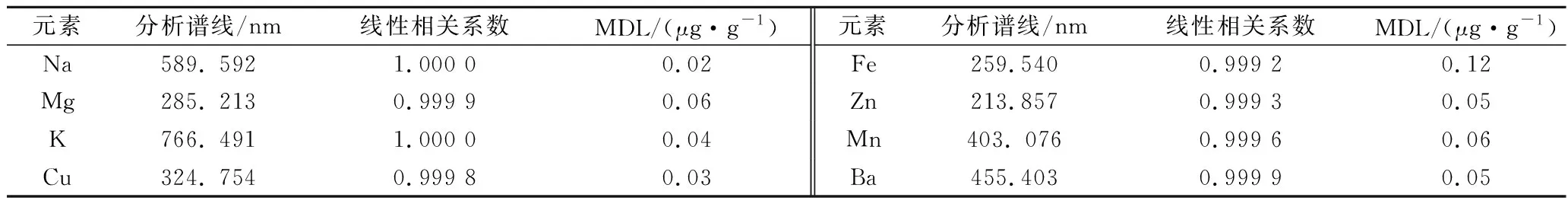
表1 元素的線性度與方法檢出限Table 1 Linearity and method detection limits for analytes

表2 方法的準確性與精密度(n=6)Table 2 Accuracy and precision of the method(n=6)
2.5 堅果油樣品分析
選取產地分別來自山東、江西、江蘇、湖南的5種食用堅果油樣品,采用微波消解處理樣品后,在選定的工作條件下對其中的8種金屬元素進行測定,每個樣品重復測定6次,結果見表3。5種食用堅果油中,花生油中的Na含量最高,榛子油中的Mg、K、Fe、Zn含量最高,山核桃中的Ba含量最高,葵花籽油中的Mn含量最高,山茶油中的Cu含量最高;5種食用堅果油中Cu、Fe、Zn的含量均<1 μg/g,處于較低水平。

表3 食用堅果油樣品的分析結果 單位:μg/g
3 結論
微波等離子體原子發射光譜法在分析過程中無需使用高純稀有氣體氬氣和危險性可燃氣體,是一種低運行成本的無機元素分析方法,可用于堅果油中金屬元素Na、Mg、K、Cu、Fe、Zn、Mn、Ba含量的測定。堅果油樣品經微波消解處理后進行測定,通過選擇合適的分析譜線和內標元素消除了干擾,采用加標回收實驗并與電感耦合等離子體質譜法進行對比分析驗證了方法準確可靠。各元素的方法檢出限為0.02~0.12 μg/g,加標回收率90%~110%,相對標準偏差≤5.9%。實際樣品的分析結果表明,方法滿足堅果油中多種金屬元素含量檢測和質量控制要求。

