早產兒及足月兒新生兒敗血癥臨床特征比較
張武棟
作為感染性疾病,新生兒敗血癥是患兒血液循環在新生兒時期受到真菌或細菌的感染,并不斷產生、繁殖毒素所致。由于新生兒敗血癥早期表現無特異性,會增加漏診及誤診率,錯過患兒的最佳治療時間,影響預后效果,更甚者會導致患兒的死亡[1]。相關研究發現[2],足月兒和早產兒的敗血癥臨床特征存在差異,若治療方案出現錯誤,不僅會延長患兒治療時間,還會帶給患兒較大痛苦,給患兒家屬帶來沉重的經濟負擔和心理負擔。在新生兒敗血癥治療中,以出生時是否足月作為依據確定治療方案,可提高治療方案的針對性和個性化,避免盲目治療的弊端,利于實現更好的臨床療效[3]。故本研究回顧性分析2019年2月—2020年2月本院78例新生兒敗血癥患兒的臨床資料,旨在比較分析早產兒及足月兒新生兒敗血癥臨床特征。
1 資料與方法
1.1 一般資料
回顧性分析2019年2月—2020年2月本院78例新生兒敗血癥患兒的臨床資料,依據出生時是否足月分組,早產組:共有患兒39例,男21例,女18例,年齡2~15 d,平均(6.78±2.41)d。足月組:共有患兒39例,男22例,女17例,年齡1~16 d,平均(7.03±2.28)d。兩組患兒一般資料比較差異無統計學意義(P>0.05),具有可比性。
納入標準:被確診為新生兒敗血癥的患兒;胎齡在28周以上的患兒;年齡在17 d以內的患兒;家屬簽署了知情同意書的患兒;本研究獲得倫理委員會批準。
排除標準:存在先天性疾病的患兒;入院前行抗生素治療的患兒;臨床資料不完整的患兒;哭鬧不止、依從性較差的患兒。
1.2 方法
回顧性分析本院78例新生兒敗血癥患兒的臨床資料,并依據出生時是否足月分組,觀察新生兒敗血癥的臨床特征。
1.3 觀察指標
觀察兩組高危因素及致病菌分布情況。高危因素:有創操作、羊水污染、胎膜早破、母體感染等。致病菌:真菌、革蘭陰性菌、革蘭陽性菌等。
1.4 統計學處理
數據以SPSS 20.0統計學軟件進行統計分析,其中計數資料以率(%)表示,使用χ2檢驗,計量資料以(±s)表示,使用t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 兩組高危因素比較
早產組有創操作、羊水污染、胎膜早破、母體感染等高危因素占比均高于足月組,差異均有統計學意義(P<0.05),見表1。
2.2 兩組致病菌分布情況比較
足月組革蘭陰性菌感染率低于早產組,革蘭陽性菌感染率高于早產組,比較差異均有統計學意義(P<0.05);兩組真菌感染率比較差異無統計學意義(P>0.05),見表2。
3 討論
新生兒敗血癥作為新生兒期危重癥,早期無明顯特征,發現時多已錯過最佳治療時間,會影響患兒預后情況,若治療不及時,會增加患兒死亡率,給患兒家庭帶來沉重負擔[4]。有學者指出[5],對早產兒和新生兒的病原菌分布特點和致病因素進行深入分析,能有效降低患兒院內感染率及死亡率,利于挽回患兒生命。本研究結果顯示,早產組有創操作、羊水污染、胎膜早破、母體感染占比分別為43.59%、30.77%、43.59%、23.08%,高于對照組的7.69%、2.56%、12.82%、5.13%,差異均有統計學意義(P<0.05)。可見有創操作、羊水污染等因素均會增加新生兒敗血癥的發病率,這就需要家屬在分娩前行定期檢查,遵醫囑行分娩前運動,嚴格規范運動、飲食,防止各高危因素的發生,以達到降低發病率的效果,讓患兒能夠正常的生活。
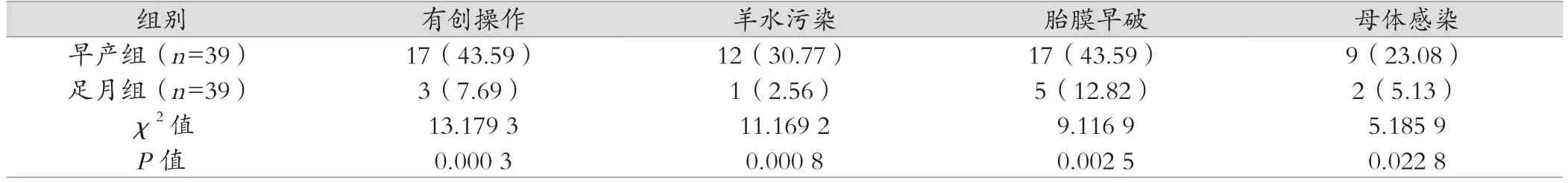
表1 兩組高危因素比較[例(%)]
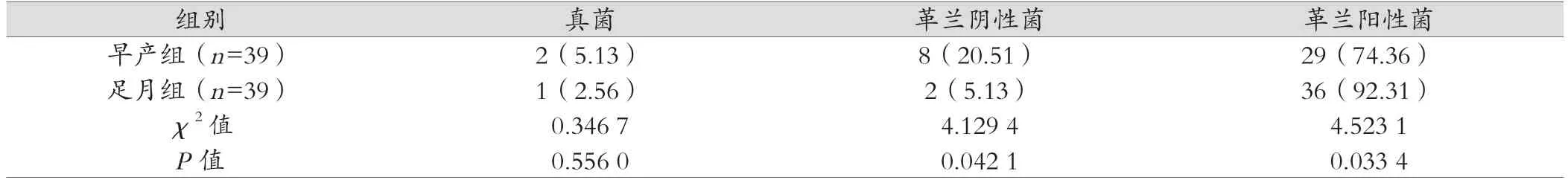
表2 兩組致病菌分布情況比較[例(%)]
本研究中,足月組革蘭陰性菌感染率為5.13%,低于早產組的20.51%,革蘭陽性菌感染率為92.31%,高于早產組的74.36%,差異均有統計學意義(P<0.05)。兩組真菌感染率差異無統計學意義(P>0.05)。可見足月兒與早產兒在新生兒敗血癥的病菌感染分布中存在顯著差異,以此為依據,可提高治療方案的針對性與專業性,讓治療方案更具有效性,從而更好的改善患兒預后。由于早產兒的適應能力、機體免疫力及藥物耐受性較差,在治療時需嚴格挑選抗生素藥物,避免過敏等情況的出現。而足月兒不僅能通過常規抗生素進行治療,還可選擇氨基糖苷類藥物及頭孢類藥物等,依據患兒具體情況,選擇合適的抗生素藥物,可達到更好的預后效果[6]。
在新生兒出生時期,若其存在有創操作、母體感染、胎膜早破等高危影響因素,應增加日常檢查,避免漏診或誤診的發生[7]。若患兒在早期已確診為新生兒敗血癥,可對癥選擇抗生素藥物;若患兒尚未確診,應進行細菌培養,并結合局部感染情況,對抗生素進行合理使用[8-10]。在新生兒敗血癥患兒的治療中,需要高度重視革蘭氏病菌及真菌感染情況,以致病菌感染分布情況作為依據,為患兒提供更好的治療,可避免病情加重,達到挽回患兒生命的效果[11-12]。
綜上所述,早產兒與足月兒新生兒敗血癥的高危致病因素存在較大差別,且致病菌分布有所不同,以此為依據進行治療方案的制定,可提高治療有效性,改善患兒預后恢復效果。

