急性缺血性卒中患者發生院內消化道出血的危險因素分析
劉佳,吳建維
急性缺血性卒中(acute ischemic stroke,AIS)是一種常見的腦血管疾病,消化道出血是其常見且嚴重的一種并發癥。研究表明消化道出血顯著增加AIS患者1年死亡和預后不良風險[1],給社會和患者家庭帶來沉重的經濟負擔。但既往關于卒中后消化道出血的研究多數來自于歐美人群,國內相關研究較少,且多為小樣本回顧性分析。本研究利用首都醫科大學附屬北京天壇醫院急性卒中院內并發癥(inhospital medical complication after acute stroke,iMCAS)前瞻性登記數據庫[2],分析AIS患者住院期間消化道出血的發生率、發生時間和相關危險因素,為臨床診療提供依據。
1 研究對象和方法
1.1 研究對象 本研究人群來自于2014-2016年首都醫科大學附屬北京天壇醫院的iMCAS研究[2],iMCAS是一項急性卒中前瞻性登記隊列研究。入組標準:①年齡≥18歲;②根據世界衛生組織標準[3],診斷為AIS的住院患者,并經頭顱CT/MRI證實;③發病到住院時間≤7 d;④患者或家屬簽署知情同意書。iMCAS研究通過北京天壇醫院倫理委員會批準。
1.2 診斷標準 院內消化道出血的診斷標準:住院期間發生鮮血或咖啡樣嘔吐、黑便、便血等癥狀,所有消化道出血病例,使用內窺鏡檢查出血的原因和來源[4-5]。根據患者住院期間是否發生消化道出血,分為兩組。
1.3 數據收集 本研究從iMCAS研究數據庫收集入組患者的臨床資料,包括:①人口學信息:年齡和性別。②卒中危險因素:高血壓、糖尿病、高脂血癥、心房顫動、冠心病、卒中史、吸煙及飲酒史。吸煙指一生中連續或累積吸煙6個月以上者,每天吸煙至少1支。飲酒分為不飲酒、適量飲酒、中-重度飲酒,其中適量飲酒指<2個標準飲酒量/日;中-重度飲酒指≥2個標準飲酒量/日。1個標準飲酒量相當于120 mL(2.5兩)葡萄酒、360 mL(1聽)啤酒或45 mL(1兩左右)白酒。③既往合并疾病:心力衰竭、心臟瓣膜病、慢性阻塞性肺疾病、周圍動脈病、肝硬化、消化道潰瘍、腎功能衰竭、關節炎和腫瘤。④藥物治療史:既往抗血小板藥物和抗凝藥物治療史。⑤入院NIHSS評分、入院收縮壓、入院舒張壓和BMI。⑥入院實驗室檢查:白細胞計數、紅細胞計數、血紅蛋白、血小板計數、TG、TC、LDL-C、HDL-C、血糖和血肌酐。⑦患者發病至入院天數和住院天數。
1.4 統計學方法 采用SAS 9.4和SPSS 17.0統計軟件進行統計分析。連續變量符合正態分布用表示,不符合正態分布用中位數(四分位數間距)表示;分類變量用例數和百分比表示。單因素分析中,連續變量組間比較采用獨立樣本t檢驗或Mann-WhitneyU檢驗,分類變量采用χ2檢驗或Fisher精確檢驗。按照性別、年齡和入院時NIHSS評分分層計算消化道出血的發生率,采用χ2檢驗比較不同性別的消化道出血發生率,采用Cochran-Armitage趨勢性檢驗,分析消化道出血發生率是否隨著年齡、入院時NIHSS評分的增加而增加。多因素分析中,納入單因素分析中P<0.2的變量作為自變量,采用多因素Logistic回歸模型分析AIS患者發生消化道出血的危險因素,采用后退法進行變量篩選,效應值采用OR和95%CI表示。P<0.05為差異具有統計學意義。
2 結果
2.1 臨床特征 共納入1129例AIS患者,年齡范圍18~89歲,平均年齡為58.7±12.5歲,男性899例(79.6%),女性230例(20.4%),其中發生消化道出血47例(4.2%)。消化道出血患者平均年齡為60.6±11.36歲,女性10例(21.3%);無消化道出血患者平均年齡為58.57±12.49歲,女性220例(20.3%)。消化道出血組心房顫動及合并肝硬化的患者比例、入院NIHSS評分、白細胞計數、血紅蛋白、LDL-C及血糖水平、住院時間等均高于無消化道出血組,發病至入院時間少于無消化道出血組,差異均有統計學意義;其余變量在兩組間差異無統計學意義(表1)。
2.2 消化道出血發生時間和發生率 AIS患者發生卒中至消化道出血確診時間為5(3~13)d,入院至消化道出血確診時間平均為4(1~7)d等。
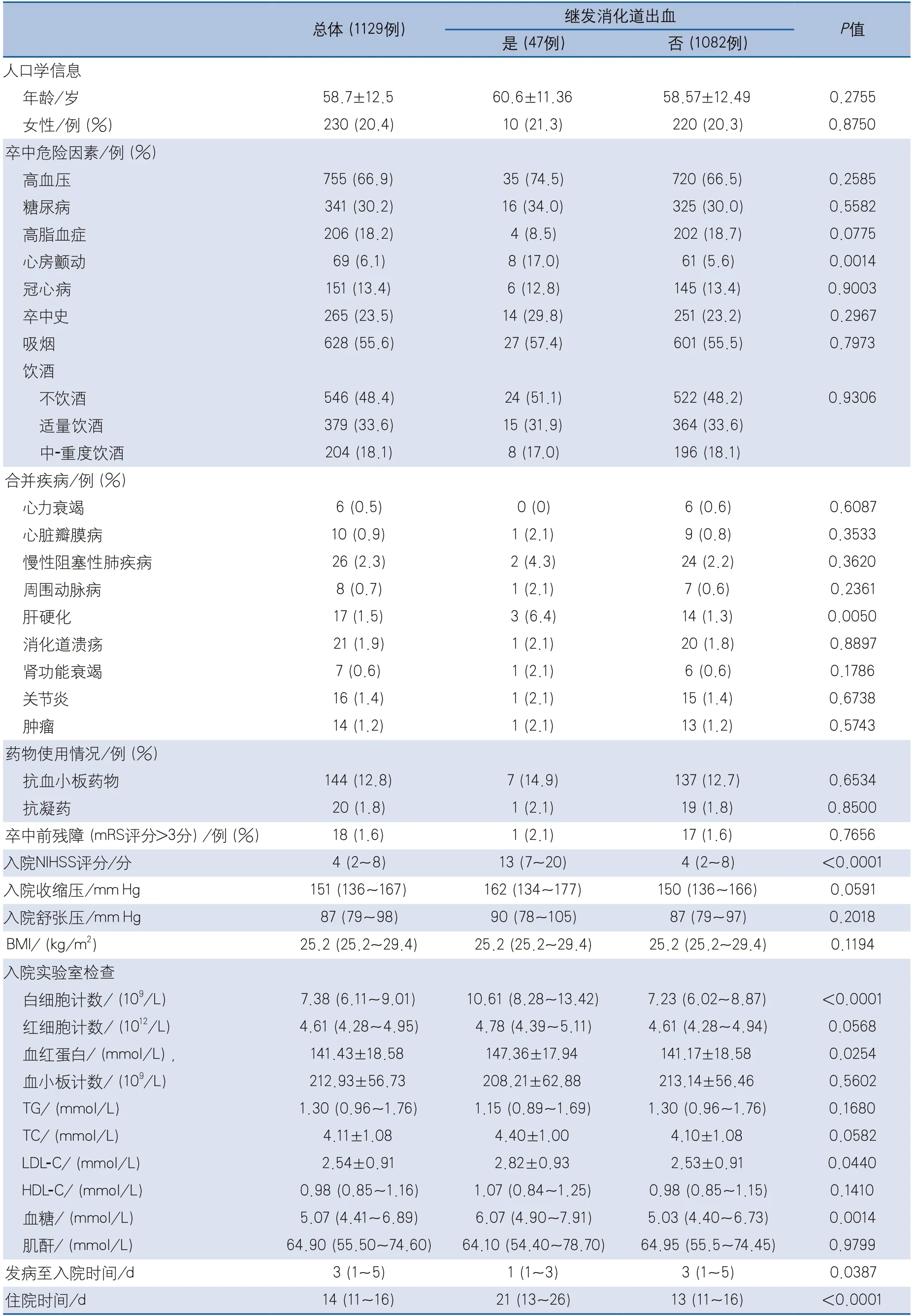
表1 急性缺血性卒中患者是否繼發消化道出血的兩組臨床資料比較
AIS繼發消化道出血發生率男性為4.12%,女性為4.35%,差異無統計學意義(P=0.88);40~49歲年齡段發生率為5.48%,50~59歲年齡段發生率為4.05%,60~69歲年齡段發生率為3.72%,70歲以上患者發生率為5.63%,各年齡組間消化道出血發生率差異無統計學意義(P=0.22);入院NIHSS評分0~2分患者消化道出血發生率為0.77%,NIHSS評分3~4分發生率為1.19%,NIHSS評分5~8分發生率為4.05%,NIHSS評分>8分發生率為11.99%,組間差異具有統計學意義(P<0.001)(表2)。
2.3 急性缺血性卒中繼發消化道出血的危險因素分析 多因素Logistic回歸模型分析結果顯示,合并肝硬化、入院NIHSS評分及白細胞計數高、住院時間長是AIS患者消化道出血發生的獨立危險因素(表3)。
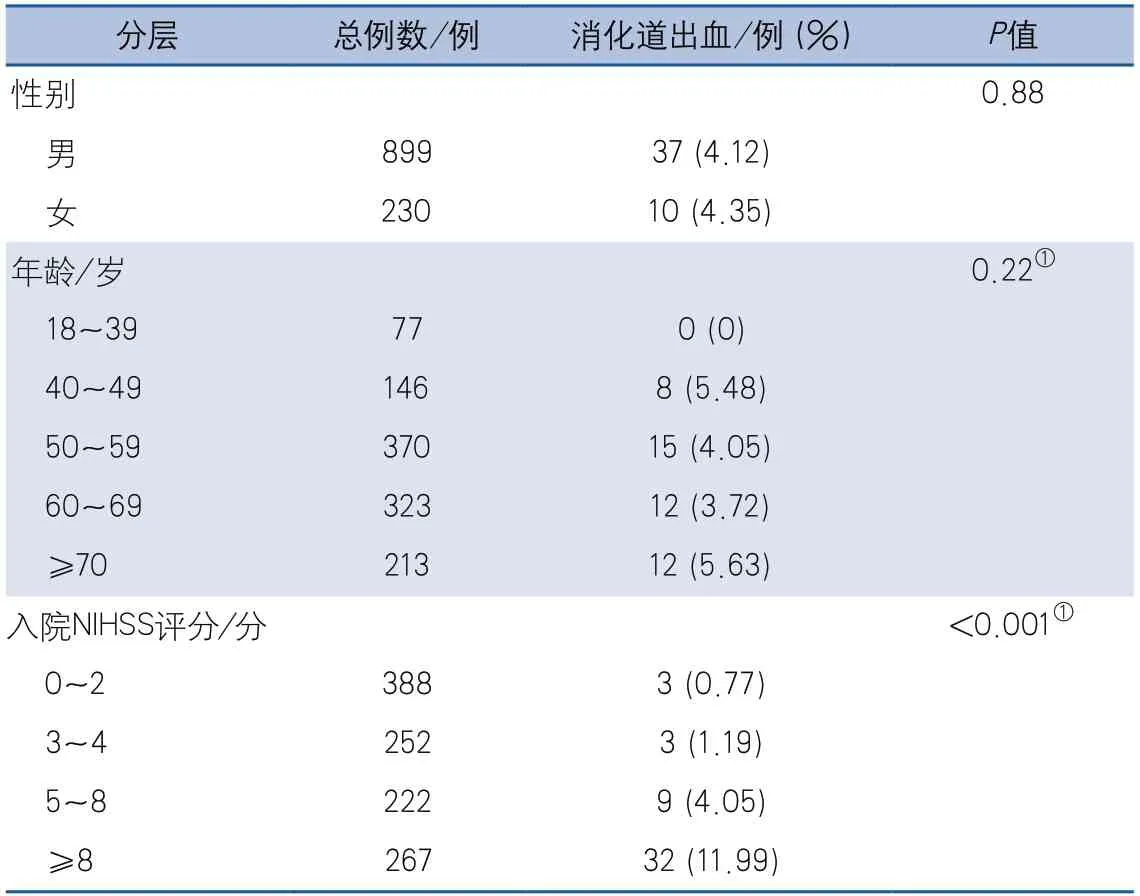
表2 急性缺血性卒中繼發消化道出血的發生率(按性別、年齡和NIHSS評分分層)
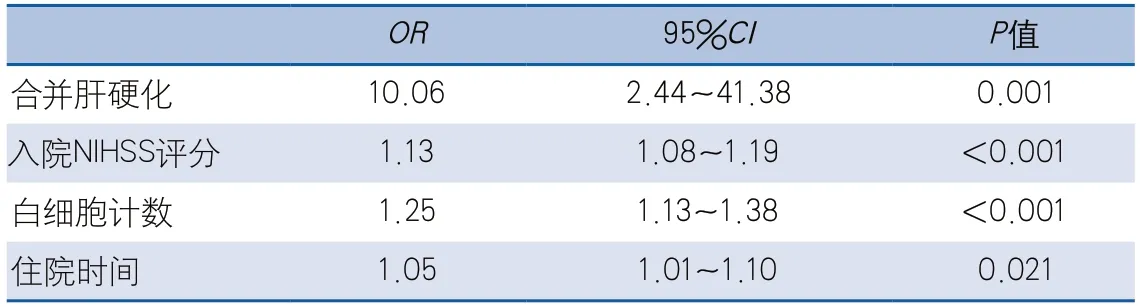
表3 急性缺血性卒中繼發消化道出血危險因素分析
3 討論
缺血性卒中患者常繼發消化道出血,有研究結果表明首次缺血性卒中患者急性期發生消化道出血可增加二次卒中、肺栓塞、深靜脈血栓等并發癥風險,并顯著增加患者死亡率[6-7]。因此,缺血性卒中后消化道出血與臨床預后不良有較強的相關性,是預后不良的一個預測因素。王擁軍等[8]在超過14 000例卒中患者登記研究中還發現缺血性卒中并發消化道出血會顯著增加肺部感染的發生率。
美國一項針對AIS患者的大樣本量研究顯示,消化道出血發生率為1.24%[9];加拿大的一項包含6853例AIS患者的回顧性研究顯示,1.5%的患者在住院期間發生消化道出血[7];中國臺灣地區的一項研究顯示,AIS患者中消化道出血發生率接近8%[10]。本研究中,AIS患者消化道出血發生率為4.2%。上述針對不同種族人群的數據提示,亞洲AIS患者中消化道出血的發生率高于歐美人群,推測可能與亞洲人幽門螺旋桿菌感染率較高和人種間遺傳因素差異有關。
AIS后繼發消化道出血的發病機制尚未完全闡明,AIS后消化道出血的可能影響因素在不同的研究中也有不同的結論。本研究的單因素分析顯示,消化道出血組心房顫動及合并肝硬化的患者比例、入院NIHSS評分、白細胞計數、血紅蛋白、LDL-C及血糖水平、住院時間等均高于無消化道出血組,發病至入院時間短于無消化道出血組;多因素分析顯示只有合并肝硬化、入院NIHSS評分高及白細胞計數高、住院時間長是AIS患者消化道出血發生的獨立危險因素。
NIHSS評分是應用最廣泛的評估AIS發病嚴重程度的量表之一,有研究顯示,NIHSS評分越高,AIS患者消化道出血發生率也越高,44%的重癥患者會繼發消化系統潰瘍[11],還有研究顯示NIHSS評分較高的AIS患者發生出血轉化的風險增高[7]。本研究顯示入院時NIHSS評分增高是消化道出血的獨立危險因素,與上述研究結果相似。因此,在臨床工作中,針對入院時NIHSS評分較高的AIS患者,應警惕消化道出血的發生,宜早期采取預防措施。
本研究還顯示白細胞計數增高及合并肝硬化與消化道出血獨立相關,而既往有研究顯示白細胞增多常見于上消化道出血的患者,并與出血的嚴重程度有關[13]。肝硬化可能導致門脈高壓、食管胃底靜脈曲張,并可能導致與肝功能相關的凝血異常,上述機制可能參與了合并肝硬化AIS患者消化道出血的病理生理過程,并導致此類患者消化道出血風險增加。
中國臺灣地區的研究顯示,消化道出血的發生時間平均為卒中后8.83 d[5],本研究中AIS發生至消化道出血確診時間平均為5(3~13)d,入院后至消化道出血確診時間平均為4(1~7)d,與上述研究結果基本一致,均提示AIS發病1周左右為發生消化道出血的高峰,提示臨床工作中在這段時間內要加強消化道出血的專項護理,嚴密觀察病情變化。
本研究存在一定局限性。首先,本研究來自單中心,樣本可能具有偏倚性。其次,本研究由于事件數(發生消化道出血)相對較少,可能未能發現實際有預測價值的因素。今后需要更大樣本量的前瞻性研究來驗證。

