賁門腺癌中DDX11-AS1的異常表達及其作用
郭艷麗,王會恩,尹 情,韓俊淑,郭 煒,沈素朋,梁 佳,董稚明
長鏈非編碼RNA(long noncoding RNA, lncRNA)在多種人類腫瘤中異常表達,失調的lncRNA可通過多種機制參與腫瘤的發生和發展[1-2]。研究發現,lncRNA DDX11-AS1在肝細胞癌[3]、結腸癌[4]、骨肉瘤[5]中均異常表達,但其在賁門腺癌(gastric cardia adenocarcinoma, GCA)中的表達及作用仍未完全闡明。本文著重探討DDX11-AS1在GCA中的表達及其與臨床病理特征、預后的關系,并進一步探討DDX11-AS1對胃癌細胞增殖及侵襲能力的影響,旨在闡明DDX11-AS1在GCA中可能發揮的作用,為GCA患者分子靶向治療提供候選分子靶點及預后評估提供有價值的指標。
1 材料與方法
1.1 材料選取河北醫科大學第四醫院2012~2014年收治的GCA患者136例,所有患者術前均未經放、化療。患者臨床病理資料見表1。其中臨床分期依據美國癌癥聯合會(AJCC)及國際抗癌聯盟(UICC)標準進行分類;腫瘤病理分級依據WHO標準進行分類。每例患者均取癌組織原發灶及距癌組織2~5 cm處的癌旁組織,手術切除標本一部分保存于-80 ℃低溫冰箱用于提取RNA,另一部分進行石蠟包埋,常規HE染色,經病理醫師診斷證實均為GCA,癌旁組織均為正常黏膜組織。對136例GCA患者進行隨訪,其中11例失訪。本實驗經醫院倫理委員會審查通過,入選患者均簽署知情同意書。
MGC803、BGC823、SGC7901、HGC27胃癌細胞株由河北醫科大學第四醫院腫瘤研究所病理研究室留存并傳代。Trizol購自美國Invitrogen公司;逆轉錄試劑盒(Reverse Transcription System A3500)、Lipofectamine 2000轉染試劑、MTS試劑均購自美國Promega公司;RPMI 1640細胞培養基購自美國Gibco公司,Transwell小室購自美國Corning公司,Matrigel膠購自美國BD Biosciences公司,siRNA由中國GenePharma公司合成,所用引物均由上海生工公司合成。
1.2 方法
1.2.1細胞培養及轉染 常規培養MGC803、BGC823、SGC7901、HGC27胃癌細胞株。待細胞處于指數分裂期時,胰酶消化BGC823,接種細胞于6孔板中,待板中細胞匯合度至70%時,按Lipofectanine 2000轉染試劑盒說明書進行siRNA轉染實驗。siRNA引物序列如下:siRNA1,5′-CTGTGTAGC TCTAGAGAAA-3′;siRNA2,5′-GGCCTTAAGTTTAGA GCAA-3′。轉染24 h后收集細胞,提取RNA,進行后續檢測。
1.2.2qRT-PCR法檢測DDX11-AS1表達 按Trizol試劑說明書提取組織及細胞株中總RNA,分別參照Promega逆轉錄試劑盒說明將RNA逆轉錄成cDNA,用于檢測目的基因的表達情況,并以GAPDH作為內參照。引物序列如下:DDX11-AS1上游引物5′-CAGCAACCTTTCTGGGAAGC-3′,下游引物5′-ACAAGAGCTGAGCTTGTCTTT-3′;GAPDH上游引物5′-AGGTGAAGGTCGGAGTCAACG-3′,下游引物5′-AGGGGTCATTGATGGCAACA-3′。結果采用相對定量法,目的基因的相對表達量用2-ΔΔCt表示,其中ΔCt=Ct目的基因-Ct內參基因,ΔΔCt=ΔCt-ΔCt對照。
1.2.3MTS實驗檢測DDX11-AS1對胃癌細胞BGC823增殖能力的影響 常規培養BGC823細胞,待細胞處于指數分裂期時,胰酶消化,將3×103個細胞接種于96孔板中,每組設置6個復孔。分別于細胞貼壁后0、24、48、72、96 h在每孔加入20 μL(500 μg/mL)MTS試劑,在37 ℃含5%CO2的加濕培養箱中培養2 h。用酶標儀在490 nm波長處檢測每個孔的吸光度值,實驗重復3次。
1.2.4Transwell侵襲實驗檢測DDX11-AS1對胃癌細胞BGC823侵襲能力的影響 Transwell小室上腔加入20 μL Matrigel膠,并在37 ℃下孵育2 h。下腔加入含10%FBS的600 μL RPMI 1640。常規消化并懸浮BGC823細胞于無血清培養基中,調整細胞密度接種于小室上腔(1×105個/孔)。培養24 h后,用4%多聚甲醛固定細胞,并用0.1%結晶紫染色。最后,在顯微鏡下對5個隨機視野的細胞進行計數。實驗重復3次。
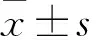
2 結果
2.1 GCA中DDX11-AS1表達與臨床病理特征的關系首先應用基因表達譜交互分析(gene expression profiling interactive analysis, GEPIA)(http://gepia.cancer-pku.cn/)和GENEBANK(https://www.ncbi. nlm.nih.gov/gene/100506119)在線數據分析網站分析DDX11-AS1在各腫瘤組織及正常黏膜組織中的表達,結果顯示DDX11-AS1在多個腫瘤組織中的表達均明顯高于正常黏膜組織,尤其在胃腺癌中差異高達數倍;而在多數正常黏膜組織中則表達較低(圖1)。進一步應用qRT-PCR檢測GCA及癌旁正常黏膜組織中DDX11-AS1的表達,發現癌組織中DDX11-AS1表達(8.813±6.243)明顯高于正常黏膜組織(2.671±1.970)(t=-10.942,P<0.001,圖2A)。與正常組織相比,136例GCA組織中,有123例表達上調,其中92例表達上調達2倍以上,15例表達上調高達10倍以上(圖2B)。癌組織中DDX11-AS1表達與GCA淋巴結轉移、浸潤深度及TNM分期有關(P<0.01),與患者年齡、性別、病理分級無關(P>0.05,表1)。

圖1 GEPIA及NCBI網站預測各個腫瘤組織及正常黏膜組織中DDX11-AS1的表達:A.GEPIA網站預測DDX11-AS1在各腫瘤及相應正常黏膜中的表達;B.GENEBANK數據庫(HPA RNA-seq)顯示DDX11-AS1在多個正常組織中的表達

圖2 qRT-PCR檢測GCA及癌旁正常黏膜組織中DDX11-AS1的表達:A.賁門正常組織及腫瘤組織中DDX11-AS1的相對表達;B.每一例GCA患者癌組織與正常組織中DDX11-AS1表達的比值

表1 GCA組織中DDX11-AS1表達與臨床病理特征的關系
2.2 DDX11-AS1對GCA患者生存期的影響根據DDX11-AS1在GCA組織中表達的均值將患者分為DDX11-AS1高表達組和低表達組,其中高表達組52例,低表達組84例。DDX11-AS1高表達組患者的5年存活率為7.69%(中位生存時間23個月),低表達組患者的5年存活率為33.2%(中位生存時間49個月),經Log-rank檢驗分析顯示,DDX11-AS1高表達可明顯縮短GCA患者的生存期(χ2=19.146,P<0.001,圖3);為排除混雜因素對實驗結果的影響,Cox多因素回歸分析發現,DDX11-AS1表達是GCA患者獨立的預后因素(表2)。

圖3 DDX11-AS1表達與GCA患者生存曲線分析

表2 GCA患者生存期的多因素分析
2.3 DDX11-AS1在胃癌細胞株中的表達及對BGC823細胞增殖及侵襲能力的影響隨機選取10例賁門正常黏膜組織的cDNA,按等比例混合后作為細胞表達的對照組。qRT-PCR結果顯示胃癌細胞株中DDX11-AS1表達均明顯高于對照組,尤其在BGC823細胞中的表達量最高(圖4A)。在BGC823細胞中分別轉染siRNA-DDX11-AS1(siRNA1、siRNA2),siRNA1沉默效果較好(圖4B)。分別應用MTS及Transwell小室侵襲實驗檢測DDX11-AS1對BGC823細胞增殖及侵襲的影響。結果顯示,與轉染空質粒的對照組相比,敲低DDX11-AS1表達(siRNA1組)可明顯降低胃癌細胞BGC823的增殖及侵襲能力(圖4C、D)。

圖4 DDX11-AS1對BGC823細胞增殖及侵襲能力的影響:A.DDX11-AS1在胃癌細胞株中的表達;B.qRT-PCR法檢測BGC823細胞中siRNAs的沉默效果;C.MTS檢測DDX11-AS1對BGC823細胞增殖能力的影響;D.Transwell侵襲實驗檢測DDX11-AS1對BGC823細胞侵襲能力的影響;pools.按等比例隨機混合10例賁門正常黏膜組織的cDNA;NC.轉染空質粒的對照組;*P<0.05,**P<0.01
3 討論
GCA位于食管和胃之間的轉化區,是胃癌最具侵襲性的亞型,具有較高的轉移率[6-7]。早期轉移是GCA患者預后差、生存率低的主要原因[8-9]。臨床資料顯示GCA患者術后復發率高達50%[8]。河北省太行山地區是我國上消化道腫瘤高發區[10],流行病學調查研究顯示,盡管非賁門胃腺癌的發病率和病死率呈下降趨勢,但賁門癌的發病率卻穩步上升[11-12]。不健康的生活方式、幽門螺桿菌感染、胃食管反流病、環境危險因素以及多種遺傳、表觀遺傳因素與GCA風險增加有關[13-15]。目前,GCA發生、發展的確切分子機制仍不清楚。
lncRNA長度在200 nt到100 kb,參與了許多重要生物學過程[16]。全基因組轉錄分析顯示,在多種人類腫瘤中lncRNA表達高度異常[1,16]。越來越多的證據表明,lncRNA在許多與腫瘤進展相關的基因調控中發揮著極其重要的作用,可以作為癌基因或抑癌基因驅動腫瘤的表型及進程[17]。有文獻[3-5]報道DDX11-AS1在多種腫瘤中異常表達,并可通過調節細胞增殖、侵襲、凋亡等惡性生物學行為參與腫瘤的發生、發展。如Li等[3]研究發現,肝細胞癌中DDX11-AS1表達異常增高,其過表達明顯促進肝癌細胞的增殖和侵襲,并可通過抑制LATS2表達在肝癌發生過程中發揮癌基因的作用,為肝癌治療提供了潛在的治療靶點。Tian等[4]研究也發現DDX11-AS1通過調控miR-873/CLDN7軸促進了結腸癌的發生和發展。同時,對骨肉瘤的研究提示DDX11-AS1可通過海綿吸附miR-873-5p上調DDX11的表達,并通過與IGF2BP2結合增強了DDX11 mRNA的穩定性,從而促進了骨肉瘤細胞的增殖、轉移和上皮-間質轉化過程[5]。本實驗發現在GCA組織和胃癌細胞系中DDX11-AS1表達均明顯上調。DDX11-AS1在腫瘤組織中的高表達與GCA的侵襲性臨床病理特征(包括淋巴結轉移、浸潤深度和臨床分期等)有關聯,提示DDX11-AS1可能在GCA侵襲轉移等惡性進程中扮演著重要角色。為明確DDX11-AS1表達對GCA患者生存期的影響,應用Kaplan-Meier生存曲線繪制DDX11-AS1表達與GCA患者累積生存率的關系,并用Log-rank檢驗進行分析。結果顯示,DDX11-AS1高表達明顯縮短了GCA患者的生存期,與不良預后密切相關。同時,利用Cox回歸模型進行多因素分析,校正潛在的混雜變量,發現DDX11-AS1高表達可作為GCA患者的獨立預后因素。同時,功能實驗結果進一步顯示敲低DDX11-AS1明顯抑制胃癌細胞的增殖和侵襲能力。因此,本實驗認為DDX11-AS1可能在GCA的惡性進展中扮演著重要作用,并可能是GCA患者預后不良的潛在預測因子。
綜上所述,本實驗結果揭示DDX11-AS1在GCA中可能扮演著癌基因的作用,其高表達促進了GCA的發生與發展,并有望成為GCA患者預后評估的候選分子標志物。

