miRNA-330-3p/Ap2m1軸在過表達GATA-4骨髓間充質干細胞外泌體抗心肌細胞凋亡中的作用
賀繼剛 王梓豪 李敏 謝巧麗 毛富剛
云南省第一人民醫院,昆明理工大學附屬醫院1心臟大血管外科,2心血管內科(昆明650032)
冠狀動脈硬化性心臟病(coronary arteriosclerotic heart disease,CAD)引起的心肌梗死(myocardial infarction,MI)已成為世界疾病譜中的頭號“殺手”。目前對此危險因素的研究雖有一定進展,但仍無法對其進行有效的治療[1-3]。至今,對冠心病引起的心梗治療的中心為對心梗區域心肌細胞的保護,而目前生物治療走在了前方。其中骨髓間充質干細胞(Bone marrow mesenchymal stem cells,BMSC)是生物治療的主要手段[4-6]。GATA-4是調控心臟基因表達的重要轉錄因子,并可以抗心肌細胞凋亡[7-10]。外泌體(exosome)是由細胞分泌的脂質雙層囊泡狀物質,其內含有的miRNA 是其主要生物學功能分子,其可隨exosome 遠距離運輸,并釋放入“受體”細胞,而改變受體細胞生物學功能[11-15]。結合以上研究背景,課題組進一步發現過表達GATA-4 的BMSC 分泌的exosome(BMSCGATA-4-exosome)能夠通過減少心肌細胞凋亡壞死,進而改善心梗后心功能。并證明在BMSCGATA-4-exosome 中miRNA-330-3p 表達明顯增高,提示其是BMSCGATA-4-exosome抑制心肌細胞凋亡,改善心梗后心功能的關鍵分子[16]。前期在BMSC體系內過表達miRNA-330-3p并提取分泌的外泌體(BMSCmiRNA-330-3p-mimic-exosome)與心肌細胞在低氧無血清下共培養,其可以明顯降低心肌細胞凋亡率。且miRNA-330-3p 在心肌細胞內高表達。進一步根據miRNA 靶基因數據庫預測miRNA-330-3p 對應靶基因為Ap2m1、Cnot4,通過Western blot 證實Ap2m1 蛋白表達呈規律性降低,且與對照組比較差異有統計學意義(P<0.05)。本實驗力圖進一步通過建立小鼠心梗模型,采用尾靜脈注射各組exosome,對miRNA-330-3p/Ap2m1軸在BMSCGATA-4-exosome 抗心肌細胞凋亡中的作用進行體內解析驗證。exosome 取代干細胞促進心肌修復,不僅能實現無細胞修復,且降低了干細胞注入后對全身造成的影響,為exosome 成為心肌梗死治療藥物提供依據。
1 材料與方法
1.1 材料
1.1.1 實驗動物37 只雄性C57BL/6 小鼠,購自成都達碩(SCXK(川)2015—030)。所有動物實驗均已獲得云南省第一人民醫院動物實驗倫理委員會批準(YS2018872)。
1.1.2 主要試劑和儀器miRNA-330-3p inhibitor試劑(廣州銳博生物科技有限公司),miRNA-330-3p mimic 試劑(廣州銳博生物科技有限公司),DMEM/F12 細胞培養基(Gibco 公司),提取exosome 試劑盒(廣州銳博科技公司),Bulge-Loop miRNA qRTPCR Starter Kit(廣州銳博科技公司),cel-miR-39 引物、miRNA-330-3p 引物(廣州銳博科技公司),Ap2m1 一抗(上海市玉博科技公司),Cnot4 一抗(上海市玉博科技公司)。
1.2 實驗方法
1.2.1 小鼠BMSC 分離、培養及鑒定小鼠脛骨全骨髓法提取骨髓間充質干細胞,采用酶消化法進行細胞傳代培養,至干細胞到達第3 代(P3)時收集細胞采用CD11b 磁珠負選,去除造雜細胞。繼續干細胞培養傳至第7 代(P7)。待細胞匯合達90%時。完成骨髓間充質干細胞三系分化檢測(三系分化按Cyagen Biosciences 公司分化試劑盒說明書操作)。
1.2.2 BMSCGATA-4通過采用基因開啟技術及病毒載體進行構建在慢病毒質粒GV308中導入GATA-4 mRNA,構建重組慢病毒包裝質粒。并轉染入小鼠骨髓間充質干細胞中需要時加入基因開啟劑強力霉素(Doxycycline,DOX)使GATA-4 基因表達。
1.2.3 細胞的分組及處理準備BMSC-exosome(5 μg/mL),BMSC空載體-exosome(5 μg/mL),BMSCGATA-4-exosome(5 μg/mL),BMSCmiRNA-330-3p-mimic-exosome(5 μg/mL),BMSCmiRNA-330-3p-inhibitor-exosome(5 μg/mL)經尾靜脈注射入心梗小鼠體內,并將心梗未處理組、正常小鼠作為對照組(每組5 只)。
1.2.4 小鼠心肌梗死模型的建立采用水合氯醛(4%,0.1 mL/10 g)麻醉小鼠。直視下氣管插管并連接呼吸機,左側三肋間入胸,以9/0 縫線于左心耳根部下方。可見左心室前壁及心尖周圍心肌組織運動減弱,關閉肋間隙。模型制作完成后,觀察模型小鼠48 h,確保模型小鼠可以存活,用于后續實驗[16]。本實驗共應用小鼠37 只,存活36 只,由于心衰死亡1 只(死于模型制作48 h 以內)。小鼠心梗模型制作的成功率為95%。
1.2.5 心臟彩超將BMSC-exosome(5 μg/mL),BMSC空載體-exosome(5 μg/mL),BMSCGATA-4-exosome(5 μg/mL),BMSCmiRNA-330-3p-mimic-exosome(5 μg/mL),BMSCmiRNA-330-3p-inhibitor-exosome(5 μg/mL)在小鼠心梗模型建模后48 h時經尾靜脈注射入體內,注射exosome的量為5 μg/mL,300 μL exosome,并將心梗未處理組、正常小鼠作為對照組(每組5 只)。于注射后48 h(前期已經證明在給予BMSCGATA-4-exosome后48 h 心梗心功能的改善開始出現[16])采用心臟彩超(PHILIPS EPIQ 7C)評估心功能改變。
1.2.6 RT-PCR取相同部位相同重量心肌組織,采用RT-PCR 方法檢測下述各組BMSC-exosome組,BMSC空載體-exosome 組,BMSCGATA-4-exosome 組,BMSCmiRNA-330-3p-mimic-exosome 組、BMSCmiRNA-330-3p-inhibitor-exosome 組及心梗未處理組、正常小鼠,心肌細胞內miRNA-330-3p 表達的量。
提取各組總RNA,將miRNA-330-3p逆轉錄合成cDNA第一條鏈。在對目的基因進行擴增(95 ℃,10 min;95 ℃,2 s ;60 ℃,20 s;70 ℃,10 s),進行分析。
1.2.7 利用TUNEL技術評估心梗部位心肌細胞的凋亡數量小鼠心梗模型建立48 h后給予注射BMSCexosome組,BMSC空載體-exosome組,BMSCGATA-4-exosome組,BMSCmiRNA-330-3p-mimic-exosome 組、BMSCmiRNA-330-3p-inhibitorexosome 組的exosome,并將心梗未處理組及正常小鼠組作為對照組,評估心梗部位心肌細胞凋亡數量(每組五只小鼠,取相同部位心臟組織,× 40倍,計數心肌細胞凋亡數量)。
1.2.8 靶基因預測對miRNA-330-3p 利用十二個小分子RNA 靶基因預測Database 進行預測(條件:相同靶基因存在于≥10 個數據庫同時靶基因和小分子RNA 匹配度≥8),提示Ap2m1、Cnot4 為miRNA-330-3p 靶基因。
1.2.9 Western blot用蛋白免疫印跡(Western blot)技術檢測各組心肌細胞內Ap2m1、Cnot4 蛋白的表達。提取體內各組心梗部位心肌細胞的蛋白質,評估其細胞內Ap2m1、Cnot4 表達。
1.3 統計學方法采用SPSS 15.0 統計分析。數據采用單因素方差分析比較,統計假設檢驗為雙側,P<0.05 為差異具有統計學意義。
2 結果
2.1 小鼠BMSC 3 系分化結果見圖1。
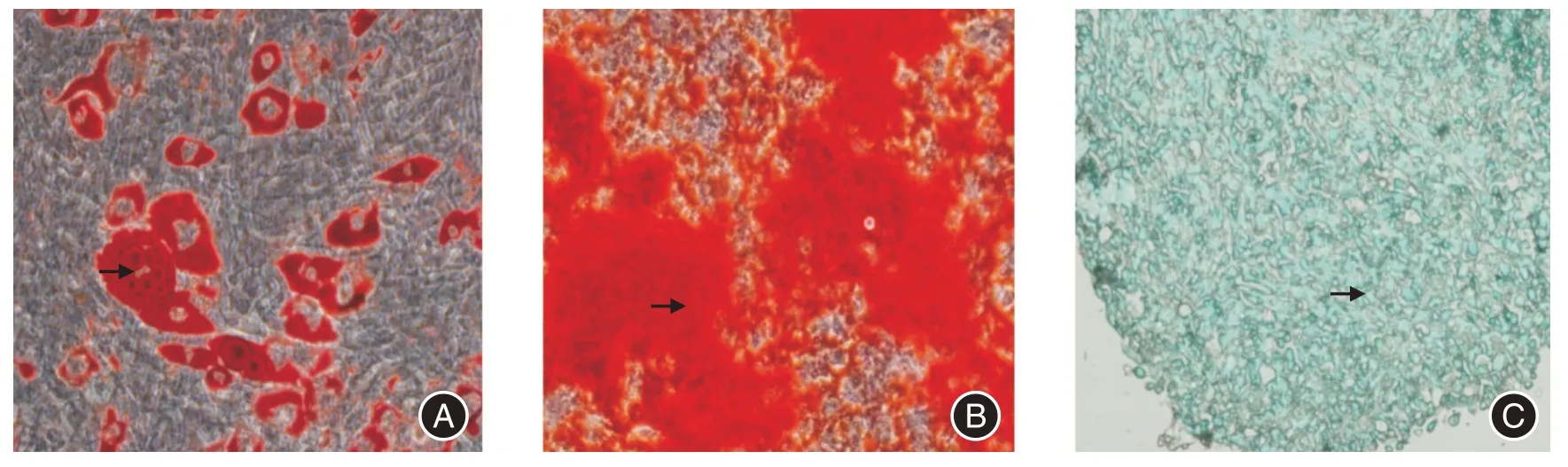
圖1 骨髓間充質干細胞3 系分化圖Fig.1 Mouse BMSC three-line differentiation
2.2 構建BMSCGATA-4 24 h 后采用RT-PCR 檢測GATA-4的表達BMSCGATA-4組較對照組其GATA-4基因表達增加97.27 倍,較對照組明顯增高(P<0.05)。見圖2。
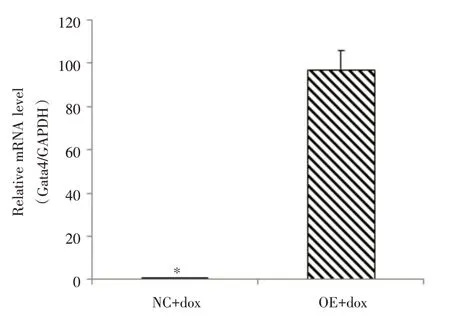
圖2 慢病毒轉染BMSC 后24 h GATA-4 的RT-PCRFig.2 RT-PCR of GATA-4 24 h after lentivirus transfection of BMSC
2.3 心功能改變采用心臟彩超(PHILIPS EPIQ 7C)評估心功能改變,每組共5 只小鼠,共3 次,見圖3。
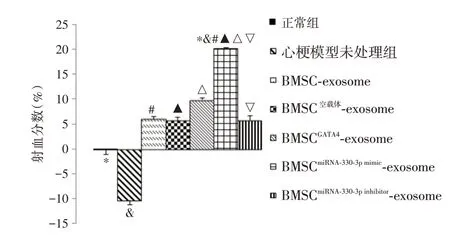
圖3 心梗模型建立48 h 后給予exosome 48 h 處理后射血分數評價Fig.3 Ejection fraction was evaluated after 48 hours of exosome treatment after myocardial infarction model was established
2.4 miRNA-330-3p 的表達采用RT-PCR 定量評估各組心肌細胞中miRNA-330-3p 的表達,見圖4。
2.5 利用TUNEL 技術評估心梗部位心肌細胞的凋亡數量小鼠心梗模型建立48 h 后給予注射BMSC-exosome 組、BMSC空載體-exosome 組,BMSCGATA-4-exosome 組、BMSCmiRNA-330-3p-mimic-exosome 組、BMSCmiRNA-330-3p-inhibitor-exosome 組的exosome,并將心梗未處理組及正常小鼠組作為對照組,每組5 只小鼠,取相同部位心臟組織,× 40 倍,計數心肌凋亡細胞,評估心梗部位心肌細胞凋亡數量(以一批為例展示),見圖5。每組5 只小鼠,取相同部位心梗組織,高倍鏡下觀察各實驗組及對照組心臟梗死區凋亡細胞量,見圖6。
2.6 心梗心肌細胞Ap2m1、Cnot4 表達水平BMSCmiRNA-330-3p-mimic-exosome 組中心梗心肌細胞內Ap2m1的表達規律性降低,且與對照組差異有統計學意義(P<0.05)。但Cnot4 表達未見規律性。見圖6、7。

圖4 心梗模型建立48 h 給予干預措施48 h 后心梗組織中miR-330-3p 表達Fig.4 miRNA-330-3p expression in myocardial infarction tissues 48 hours after myocardial infarction model was established and intervention was administered

圖5 各組心肌細胞凋亡數量(×40)Fig.5 Cardiomyocyte apoptosis each group(×40)
3 討論
結合目前國內外研究結果,前期課題組發現BMSCGATA-4-exosome 能減少心肌細胞凋亡壞死,進而提高心梗后心功能[16]。同時可見在exosome 中miRNA-330-3p 表達增高,提示其可能是BMSCGATA-4-exosome 改善心梗后心功能的關鍵分子。
microRNAs(miRNAs)為小分子非編碼RNA。成熟的miRNA 主要通過與靶基因的3′非翻譯區(3′-UTR)結合而降解或抑制mRNA 的轉錄或翻譯,從而調控細胞很多方面的功能,包括調控細胞周期、增殖、凋亡、分化和細胞應激[17]。在人類中,編碼miRNAs 的基因只占基因的3%左右,但它們對大約30%的蛋白質的表達都具有調節作用[18]。許多研究表明miRNA 可以在多種腫瘤中異常表達,這些異常表達的miRNAs 可能通過調節多種抑癌基因或致癌基因調控腫瘤的發展[19]。而miR-330-3p 是在文獻中經常被描述的一類miRNA[20-21]。
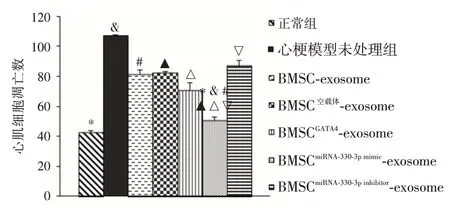
圖6 心梗模型建立48 h 后給予干預措施處理后心梗局部細胞凋亡數量Fig.6 Myocardial infarction model is established after 48 hours and after the intervention measures to deal with the local number of apoptosis
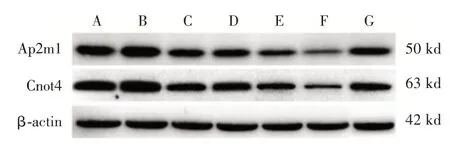
圖7 心梗心肌細胞在48 h Ap2m1 及Cnot4 表達水平Fig.7 The expression levels of Ap2m1 and Cnot4 in myocardial cells of myocardial infarction at 48 h

圖8 心梗模型建立48 h 給予干預措施48 h 后心梗組織中Ap2m1、Cnot4 表達Fig.8 Ap2m1 and Cnot4 expression were observed in myocardial infarction 48 h after intervention
miR-330-3p 是WEBER 首次發現的,Has-miR-330位于人類染色體19q13.32[22]。miR-330-3p 是一種新發現的miRNA,其在乳腺癌[23]、食道癌[24]中表達上調。通過研究表明miR-330-3p 在以上腫瘤中可以抑制腫瘤細胞的凋亡,促進腫瘤細胞的增殖。在乳癌中如用miR-330-3p 轉染乳腺癌細胞可減少G1 群體并促進了細胞存活[25]。在食管癌中,FACS研究表明,具有高miR-330-3p水平的食管上皮癌細胞具有較低比例的G0/G1 細胞。過表達和敲除實驗顯示,miR-330-3p水平與CDK 6和cyclinA水平呈正相關,與p21Waf1/Cip 1和p27Kip1水平呈負相關。CDK 6 和cyclinA 在DNA 合成前出現在G1 期,是S期進入和通過G2/M 期所必需的[26]。本實驗通過建立小鼠心梗模型,發現BMSCmiRNA-330-3p-mimicexosome組心肌細胞凋亡明顯減少,符合上述實驗結果。進一步采用miRNA 靶基因預測數據庫對miRNA-330-3p 的靶基因進行檢測,提示Ap2m1、Cnot4 為miRNA-330-3p靶基因。筆者進一步研究發現Ap2m1表達具有明顯的規律性,而Cnot4 規律性不明顯。HELBIG 等[27]報道,AP2m1 變異是發育性和癲癇性腦病基礎,Ap2m1 編碼銜接蛋白復合物2(AP-2)的μ亞基參與網格蛋白介導的內吞作用(CME)和突觸小泡回收。Ap2m1蛋白的變異缺失,導致了神經細胞的凋亡減少,異常增殖增加。此外據LE DUFF等[28]報道,細胞在誘導凋亡中AP2m1 的表達是上調的,與本研究結果一致。近幾年國內外學者的研究側重放在BMSC、GATA-4 以及exosome 修復受損心肌三者獨立發揮的作用,而關于BMSCGATA-4-exosome 通過miRNA-330-3p/Ap2m1 軸抑制心肌細胞凋亡從而修復心肌損傷的分子調控網絡研究尚無報道。本研究前期實驗結果作為立項依據,將首次明確BMSCGATA-4-exosome 在心肌損傷修復中的分子調控網絡。但據MIKULA 等[29]報道:通過對內質小體內化過程進行干擾,可致EGFR 數量增加,在抗凋亡過程中EGFR/ERK 途徑被激活。課題組將在后續實驗中檢測EGFR的表達。并進一步設立多個研究時間點,探討miRNA-330-3p/Ap2m1 軸的時量變化。
綜上所述,miRNA-330-3p/Ap2m1軸是BMSCGATA-4-exosome 抗心肌細胞凋亡壞死的關鍵分子軸。

