PTEN誘導激酶1抵抗胃癌細胞凋亡并誘導奧沙利鉑耐藥
吳珍珍 劉志宏 楊楠彥 吳晶晶 梁俊廣 孫麗
南方醫科大學南方醫院腫瘤內科(廣州510515)
PTEN誘導激酶1(PTEN-induced kinas 1,PINK1)是一種線粒體相關蛋白。研究報道,PINK1 可參與多種線粒體相關信號通路的調控,在帕金森病等神經系統疾病中具有重要作用[1-3]。研究顯示,在氧化應激條件下,PINK1 可通過上調抗凋亡相關基因,如Bcl-xL 等,并參與PI3K/Akt/mTOR 信號通路,起到保護神經元的作用[4-6]。近年來研究[7-11]發現,PINK1 在多種腫瘤組織中均顯著高表達,且參與腫瘤的發生發展及耐藥。氧化應激所激活的信號轉導通路亦是腫瘤進展的關鍵環節之一[12]。進一步對PINK1 是否通過氧化應激參與腫瘤進展進行了探索,發現PINK1 可對腫瘤細胞線粒體內活性氧(reactive oxygen species,ROS)平衡產生影響,通過改變ROS 產量激活下游代謝相關通路[13]。目前關于PINK1 在腫瘤中的作用研究尚處于起步階段,其在胃癌中的具體作用機制尚未見相關文獻報道。PINK1 在氧化應激過度刺激的胃癌細胞中如何起作用,PINK1 是否可通過調控氧化應激參與胃癌的發生及發展,上述問題亦未見相關研究。本研究擬在細胞水平初步探討PINK1 在胃癌細胞中的作用,以及其對于化療敏感性的影響,為開發胃癌新的治療靶點提供實驗依據。
1 材料與方法
1.1 材料
1.1.1 細胞人永生化胃上皮細胞株GES-1、人胃癌細胞株BGC803、BGC823、MKN45、MGC803、SGC7901 來自于南方醫院腫瘤科實驗室。
1.1.2 組織標本76 例接受奧沙利鉑為基礎的術后輔助治療的胃癌石蠟病理標本來自于南方醫院,應用世界衛生組織胃癌病理標準進行組織學分類及分級,術后臨床及病理分期均采用國際抗癌聯盟和美國癌癥聯合委員會(UICC/AJCC)制定的第七版胃癌分期標準。入組標準:(1)接受胃癌標準D2 根治術;(2)術后病理明確為胃腺癌;(3)術前均未接受新輔助放化療;(4)術后接受含奧沙利鉑的mFOLFOX6 方案或CapeOX 方案輔助化療,但未接受放療。所需的患者數據信息均通過查閱患者手術前以及手術后的病歷資料獲得,且所有病例隨訪資料齊全。本研究均已通過南方醫科大學倫理委員會的申請。
1.1.3 主要試劑PINK1 小干擾RNA(干擾片段序列詳見表1)、基因引物購于上海生工生物工程股份有限公司;PINK1、GAPDH 抗體購于Abcam公司。

表1 PINK1 干擾片段序列列表Tab.1 Interference fragment sequence of PINK1
1.2 方法
1.2.1 qRT-PCR檢測細胞株中PINK1及凋亡相關基因表達RNA 提取和qRT-PCR:按照Trizol 說明書使用試劑盒提取細胞的總RNA,再使用紫外分光光度儀檢測RNA 濃度及純度,并使用反轉錄試劑盒將所提RNA 逆轉錄成cDNA,利用定量即時聚合酶鏈鎖反應(quantitative real time polymerase chain reaction,qRT-PCR)的方法檢測細胞中PINK1的表達量,GAPDH 作為內參來標定并測算出相對定量值(RQ 值)(表2)。
1.2.2 小干擾RNA瞬時轉染胃癌MKN45細胞于六孔板中每孔接種5 × 105個MKN45 細胞,嚴格按照Lipofectamine 2000 說明書進行轉染,48 h 后通過qRT-PCR、Western blot 實驗來驗證轉染效果。

表2 引物序列列表Tab.2 Primer sequence list
1.2.3 Western blot 檢測轉染后MKN45 細胞中PINK1 的表達瞬時轉染RNA 干擾片段24 h 后,在冰上使用蛋白裂解液分離提取MKN45 細胞中的總蛋白,高溫變性后將蛋白樣本加入聚丙烯酰胺分離凝膠中,將蛋白電泳分離開后進行轉膜,隨后采用5%脫脂牛奶封閉1 h,4 ℃一抗孵育過夜,洗滌后用熒光二抗室溫孵育1 h,TBST 清洗3 次后使用紅外激光成像分析系統(雙色odyssey)顯示得到PINK1 和GAPDH 的蛋白顯影條帶。
1.2.4 MTT 法實驗檢測胃癌細胞增殖能力的改變將細胞接種在96 孔板中(1 × 105/孔),并設置平行孔,相應處理后予5 mg/mL 四甲基偶氮唑鹽(3-(4,5-dimethyl-2-thiazolyl)-2,5-diphenyl-2-H-tetrazolium bromide,thiazolyl blue tetrazolium bromide,MTT),即0.5%MTT 溶液孵育4 h,隨后取出加入二甲基亞砜(dimethyl sulfoxide,DMSO)150 μL 進行室溫溶解,震蕩10 min,多功能酶標儀490 nm 波長檢測吸光度值。
1.2.5 細胞劃痕實驗檢測PINK1 對于胃癌細胞遷移能力的影響將轉染小干擾RNA 的MKN45 細胞種于24 孔板中(5 × 105/孔),24 h 后待細胞貼壁長滿用100 μL 槍頭比著直尺垂直于24 孔板進行劃痕,PBS 洗滌3 次后拍照,孵箱培養24 h 后再次拍照。
1.2.6 Transwell 侵襲實驗檢測PINK1 對于胃癌細胞侵襲能力的影響將200 μL 轉染siRNA 的MKN45 細胞混懸液置于Transwell 小室上室中,同時下室加入700 μL 含10%胎牛血清1640 培基,孵育24 h 后甲醇固定10 min、結晶紫染色30 min,置于顯微鏡下觀察細胞形態并拍照、計數。
1.2.7 免疫組化將石蠟病理標本切成4 μm 厚度切片,脫蠟至水、抗原修復后,PINK1 一抗4 ℃孵育過夜,洗滌后二抗孵育1 h,二抗室溫孵育1 h,二氨基聯苯胺(diaminobenzidine,DAB)顯色1 min,蘇木素復染3 min,梯度脫水、透明,封片,鏡下觀察。染色評分分別由3 位病理專家結合臨床病理參數進行。結果根據其表達強弱分為0 ~6 分,0 分為陰性表達,1 ~5分為陽性表達,6分為強陽性表達。
1.2.8 統計學方法采用GraphPad Prism 7.0 軟件對數據進行統計分析。計量資料兩組間比較采用兩獨立樣本t檢驗;兩組以上組間比較采用方差分析。計數資料組間比較采用χ2檢驗。以P<0.05 為組間差異有統計學意義。
2 結果
2.1 構建并驗證PINK1 沉默的胃癌細胞株采用qRT-PCR 技術檢測不同胃癌細胞(BGC803、BGC823、MKN45、MGC803 和SGC7901)及永生化的上皮細胞(GES-1)中PINK1 的表達情況,發現PINK1 在胃癌細胞中顯著高表達,其中在MKN45的表達最高(圖1A)。然后構建3 條siRNA 沉默序列,分別針對PINK1 序列的555(siPINK1-1)、1030(siPINK1-2)、1728(siPINK1-3)位點,瞬轉至MKN45后PCR 驗證其沉默效率,發現siPINK1-1 沉默效果最佳(圖1B),因此隨后的實驗均采用此沉默序列。同時,進一步的蛋白實驗也證實,siPINK1-1干擾片段可以顯著抑制MKN45 細胞PINK1 的表達(圖1C、1D)。
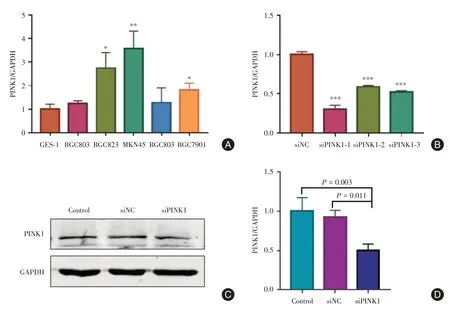
圖1 構建并驗證PINK1 沉默的胃癌細胞株Fig.1 Construction and verification of PINK1 knock-down gastric cancer cell lines
2.2 PINK1 下調可抑制胃癌細胞增殖、侵襲及轉移MTT檢測PINK1下調對胃癌細胞增殖能力的影響,結果顯示沉默PINK1表達之后,胃癌細胞的增殖能力有下調趨勢,存活細胞顯著減少(圖2A)。該結果從增殖層面證實PINK1 可能對于胃癌細胞存活有重要意義。Transwell、劃痕實驗結果顯示,相較于對照組,沉默PINK1后可顯著下調胃癌細胞的遷移能力(圖2B、圖2C,P<0.001)及侵襲能力(圖2D、圖2E),結果差異有統計學意義。以上結果顯示,PINK1 可促進胃癌細胞的增殖、侵襲及遷移能力,下調PINK1的表達可部分逆轉胃癌細胞的惡性生物學行為。
2.3 PINK1 促進胃癌細胞凋亡既往研究[14-18]證實,胃癌中存在高水平的氧化應激,而氧化應激與胃癌的發生發展聯系密切;同時PINK1 作為線粒體相關蛋白,在多個層面參與了氧化應激[4-6,13]。PINK1 可能影響了胃癌細胞的氧化應激水平,從而發揮其促癌作用。利用ROS(活性氧)試劑盒,檢測了MKN45 細胞ROS 的變化,發現沉默PINK1可促進ROS 的產生(圖3A、圖3B,P<0.001)。
檢測凋亡相關基因的表達結果顯示,相較于對照組,下調PINK1可顯著抑制MKN45細胞中Bcl-2的表達(圖3C),而Caspases-3表達無顯著差異(圖3D)。這可能與Caspases-3 作為細胞凋亡的關鍵蛋白,主要以磷酸化的形式產生作用有關,需進一步探討其蛋白水平的改變。以上結果提示在氧化應激的環境下,PINK1可抵消部分升高的ROS,從而使細胞內的ROS 在一個較為適合腫瘤細胞生存的水平,誘導腫瘤抗凋亡基因表達的上調,促進腫瘤細胞的存活。
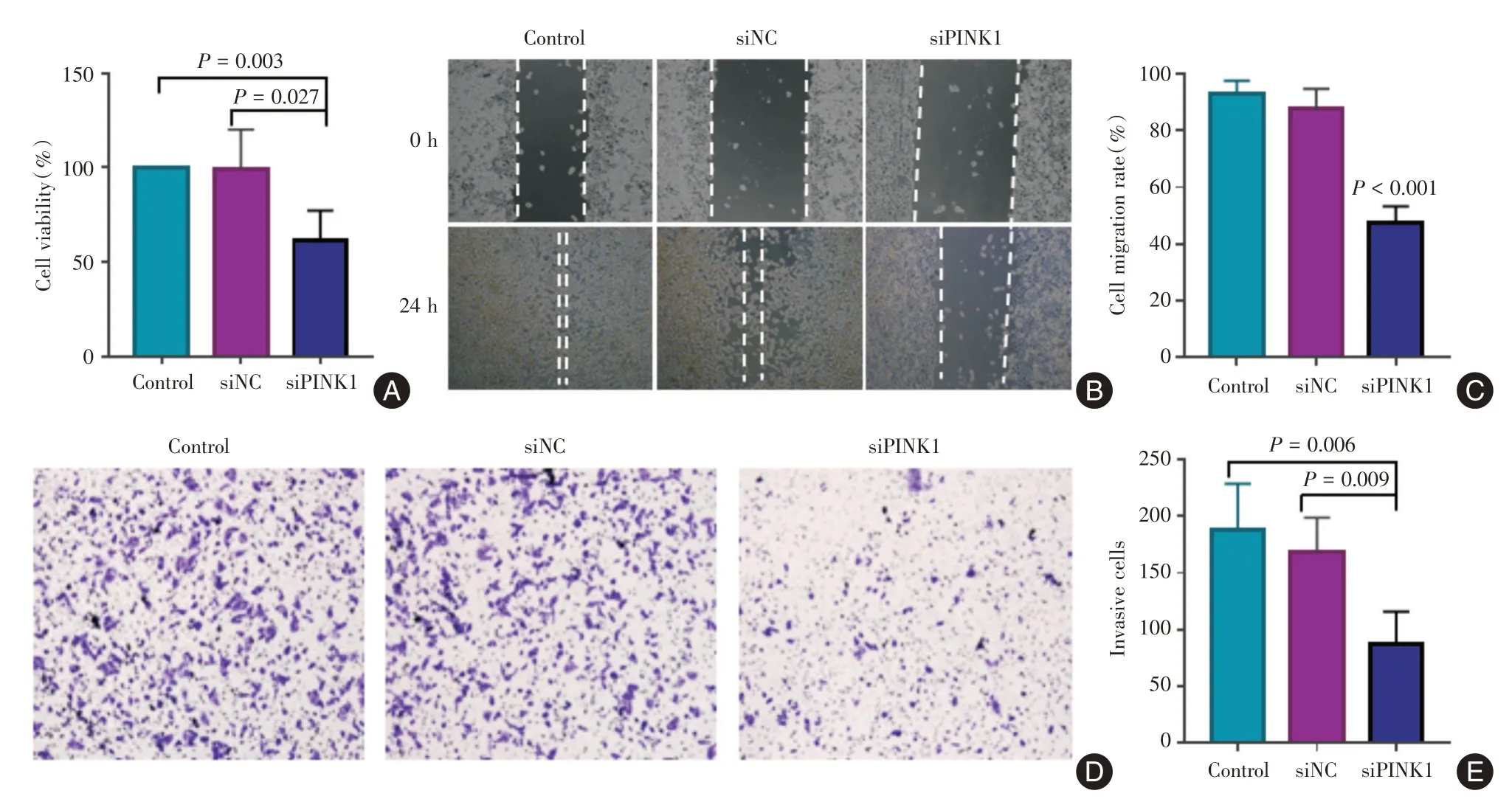
圖2 PINK1 誘導胃癌細胞增殖及遷移Fig.2 PINK1 induces proliferation and migration of gastric cancer cells
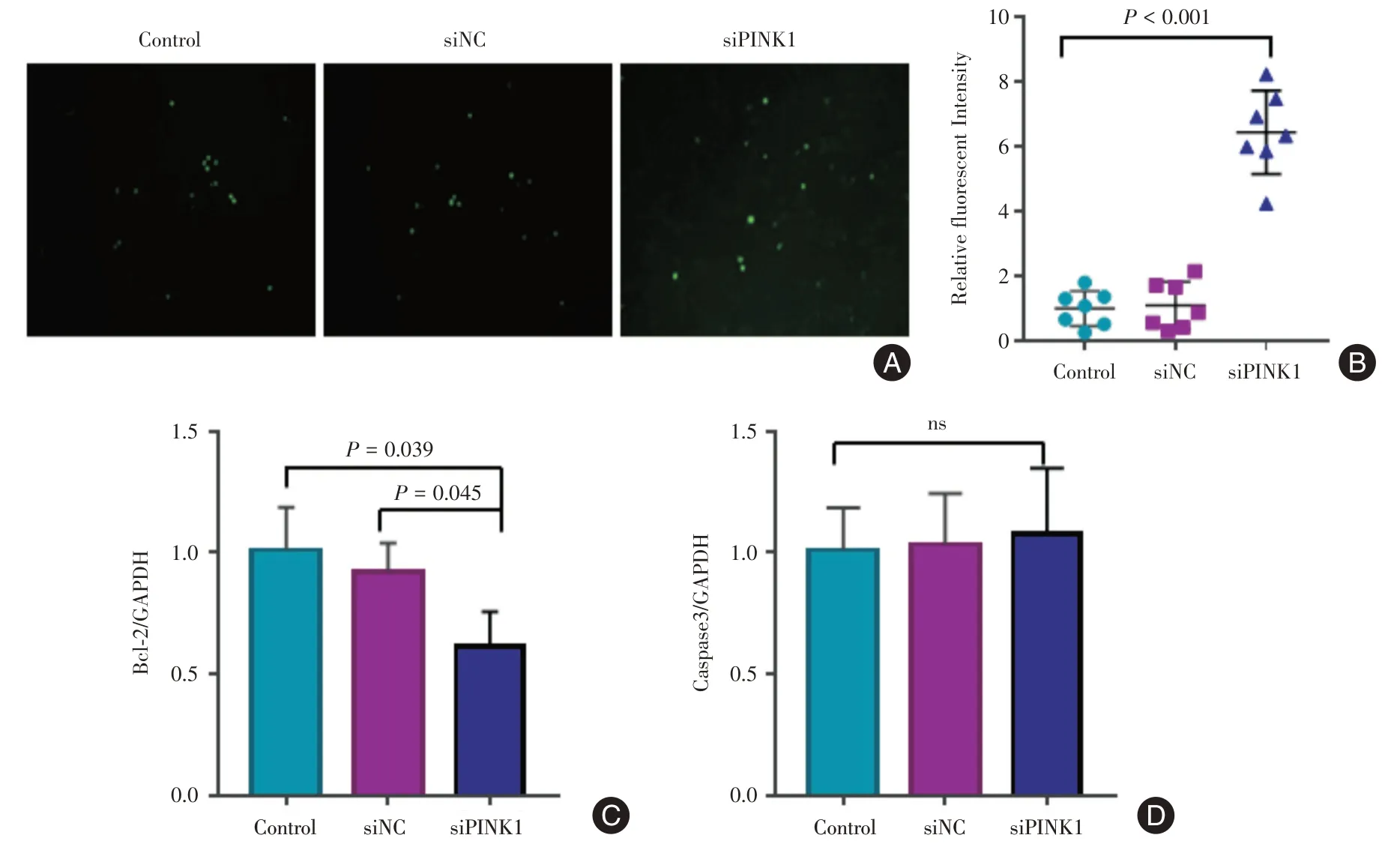
圖3 PINK1 促進胃癌細胞凋亡Fig.3 PINK1 promotes apoptosis of gastric cancer cells
2.4 下調PINK1 可誘導胃癌細胞化療增敏考慮到藥物耐藥與氧化應激適應密切相關[19-20]。隨后檢測了PINK1 是否可影響胃癌細胞的藥物敏感性。不同濃度的奧沙利鉑處理MKN45 細胞24 h,發現下調PINK1 表達可顯著改善胃癌細胞對于奧沙利鉑的敏感性,細胞增殖受到顯著抑制(圖4A)。同時檢測了野生型胃癌細胞MKN45 在不同濃度的奧沙利鉑的刺激下PINK1 的表達情況,在40 μmol/L 的刺激下PINK1的表達明顯增加(圖4B)。臨床數據顯示,76 例接受奧沙利鉑為基礎的術后輔助治療的胃癌患者石蠟病理標本進行PINK1 蛋白免疫組化檢測,其中2 例由于脫片嚴重,無法評估免疫組化結果,在后續分析中剔除。臨床數據分析發現PINK1 高表達的患者,含奧沙利鉑術后輔助治療的患者復發風險增加(圖4C)。
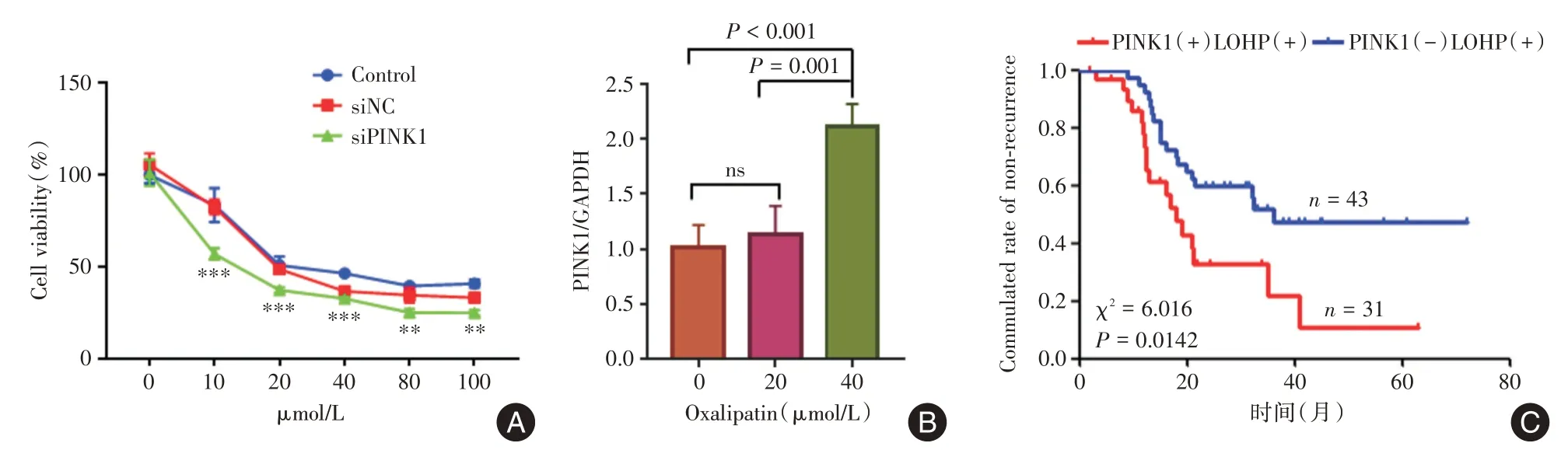
圖4 PINK1 影響胃癌奧沙利鉑藥物敏感性Fig.4 PINK1 influences oxaliplatin sensibility of gastric cancer cells
3 討論
胃癌是世界上最常見的惡性腫瘤之一,患者在現有治療手段干預下尚無法獲得滿意的總體生存率,因此尋找新的治療策略迫在眉睫[21-22]。氧化應激是機體活性氧成分與抗氧化系統之間平衡失調引起的一系列適應性的反應,而氧化應激所激活的促癌信號轉導通路則是腫瘤進展的關鍵環節之一,與胃癌的發生發展密切相關[14-18]。尋找并阻斷氧化應激刺激下腫瘤細胞中的促癌信號轉導通路,可能成為治療胃癌的新靶點[17]。
PINK1 是一種線粒體相關蛋白,可調控線粒體穩態,具有促進細胞生存、抵抗凋亡以及細胞保護等細胞生物學功能,對線粒體內ROS 的平衡具有重要作用[4-6,13]。PINK1被報道參與調控多個腫瘤生物學過程,通過影響線粒體自噬、腫瘤免疫、腫瘤干性等方面誘導腫瘤的惡性生物學行為[7-11]。然而PINK1 在胃癌中的作用目前鮮有報道。本研究首次發現PINK1 在胃癌細胞中高表達,參與調控胃癌細胞的增殖、侵襲、轉移等惡性生物學行為并促進胃癌細胞存活,初步闡明了PINK1 的致癌作用;進一步的機制探討,發現PINK1 可抑制胃癌細胞ROS 的產生,促進抗凋亡基因的表達,誘導胃癌細胞的存活。
奧沙利鉑是胃癌治療的最有效藥物之一,通過與DNA 的相互作用,阻斷DNA 復制,引起細胞周期阻滯和細胞死亡[23]。另一方面,奧沙利鉑還可以通過氧化應激反應生成過氧化氫等活性氧自由基(ROS)產生細胞毒性,導致DNA 氧化損傷[24]。氧化應激水平的改變、ROS 產生抵消均可能是導致奧沙利鉑耐受的重要原因。本研究結果顯示,奧沙利鉑可上調胃癌細胞PINK1 的表達,下調PINK1 的表達可顯著改善腫瘤細胞對于奧沙利鉑的敏感性;同時PINK1 還可以下調胃癌細胞ROS的產生。初步推測PINK1 可能是導致奧沙利鉑治療失敗的原因,而進一步的臨床數據也提示在接受奧沙利鉑輔助治療的胃癌患者中PINK1 高表達者復發風險增加。
綜上所述,本研究初步在胃癌細胞水平探索了PINK1 的促腫瘤作用,發現PINK1 通過誘導抗凋亡相關基因的轉錄,保護氧化應激下胃癌細胞存活,并誘導奧沙利鉑耐藥。然而,本研究僅在細胞水平和臨床數據上對PINK1 在胃癌中的作用進行了初步探討,在進一步闡明具體機制關鍵環節仍需要進一步補充。PINK1 在胃癌中除了氧化應激途徑是否參與其他信號通路而對胃癌的發生發展產生影響也有待更為深入的研究。目前已有研究報道將PINK1 與腫瘤免疫調節相聯系[25]。隨著腫瘤免疫治療的興起,PINK1 在腫瘤微環境與腫瘤相關免疫中的作用可能成為下一步研究關注的方向。

