基于多層螺旋CT在肺磨玻璃樣結節預后中的價值
丁必彪 張宏
(南京市江寧醫院,江蘇 南京 211100)
隨著低劑量MSCT在胸部檢查中的廣泛應用,肺小結節的檢出率越來越高,尤其是對肺內磨玻璃樣結節(ground-glass nodule ,GGN)的檢出。GGN是指在CT 圖像上表現為肺部較淺淡的密度增高影,但其內的支氣管血管束仍可顯示[1]。肺GGN可由多種病因引起,肺早期癌前病變或腺癌通常也表現為GGN[2]。因此,早期對GGN病灶的良惡性及生長趨勢做出準確判斷并制定合適處理策略至關重要。本研究隨訪并探討80個GGN臨床和影像學特征,以期根據此特征預測GGN的預后。報告如下。
1 資料與方法
1.1一般資料 收集2013年2月至2018年3月在本院行MSCT檢查,并經隨訪復查、具有手術或穿刺活檢病理的151位GGN患者共179個GGN病。納入、排除標準見相關文獻[3]經納入排除標準,排除合并肺部感染、外傷等疾病影響診斷的患者29例,排除CT檢查無1.00 mm層厚患者32例,排除臨床資料不完整及失訪者18例,剩余例共枚72例共80枚GGN納入研究。其中男性23例,平均(56.66±11.49)歲。女性49例,平均(56.14±13.14)歲。72例患者中,67例患者為肺內單發GGN,2例患者肺內檢出2個,3例患者肺內檢出3個。所有患者平均隨訪時間(14.60±12.57)個月。
1.2方法 采用Flash雙源CT掃描儀(Flash,西門子,德國),患者取仰臥位,雙手上舉,頭先進,掃描范圍為肺尖到肺底,吸氣末屏氣后進行掃描。掃描參數:管電壓120 KV,管電流自動設置,掃描層厚5 mm,標準算法和肺算法重建圖像,重建層厚為1.00 mm,層間距1.00 mm,采用縱隔窗寬:350 HU,窗位40 HU;肺窗窗寬:1500 HU,窗位:-400 HU分析圖像,并做冠矢狀位重建。圖像分析為:將所有患者胸部薄層MSCT圖像導入RadiAnt DICOM Viewer軟件(版本4.2.1,Medixant公司,荷蘭),由兩名具有十年以上工作經驗的放射科主治醫師在不知分組情況下獨立評價并測量患者圖像,分析指標包括:(1)GGN及其實性成分的大小、比例:GGN的直徑(mm)為病灶最大橫截面的最長徑,GGN中實性成分的大小(mm)為最大實性成分的長徑。計算GGN中實性成分最長徑與GGN最長徑的比值;(2)CT特征:包括形態(類圓形或多邊形)、邊緣(光滑、毛刺征、分葉征);(3)平均CT值:平均CT值的測量為在GGN最大截面分別畫取3個相同大小感興趣區域(region of interest,ROI),取3個ROI CT值的均值;(3)正常肺組織CT值:測量GGN周圍1cm以內正常肺組織,測量方法及ROI大小同前;(4)CT差:CT差值為GGN平均CT值與周圍正常肺組織CT值之差。所有測量均需避開血管,重復測量3次取平均值為最終數據。隨訪過程中,將GGN直徑增加超過2毫米,或出現新的實性成分、實性成分增大定義為惡性影像學表現(生長組),剩余為穩定組。腺癌的組織學檢查結果是根據世界衛生組織的標準進行分類[4]。
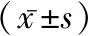
2 結 果
2.1隨訪結果 隨訪期間,4例患者肺GGN直徑增加,25例患者原實性成分增大或出現了新的實性成分。這29例患者共32個GGN歸為生長組,病理診斷為非典型腺瘤樣增生(4個),原位腺癌(11個),微浸潤腺癌(10個),高分化腺癌(6個),慢性炎癥(1個)。其余43例共48個GGN歸為穩定組,其中4個GGN經抗炎治療后病灶縮小或消失,擬炎性病灶,余44個GGN未變化,病理診斷為非典型腺瘤樣增生(23個),原位腺癌(19個),微浸潤(2個)。
2.2患者臨床及MSCT特征 患者性別、年齡、吸煙史及病灶形狀、邊緣情況在生長組與穩定組間差異均無統計學意義(P>0.05)。GGN直徑、平均CT值、CT差值、患者有無肺癌病史、GGN中實性成分大小及實性成分比例的差異組間有統計學意義(P<0.05)(表1)。兩名具有10年以上工作經驗的主治醫師測量GGN數據,測量重復性采用ICC表示,見表2,ICC>0.9,表明于MSCT圖像上測量GGN各參數具有較高的可靠性和良好的可重復性。

表1 穩定組與生長組臨床及MSCT特征

表2 GGN測量重復性檢驗
GGN直徑、平均CT值、CT差值、實性成分大小、實性成分比例對PPN的預后有意義,行ROC分析,曲線下面積(AUC)及95%置信區間分別為0.656(0.536~0.776)、0.751(0.642~0.860)、0.757(0.650~0.864)、0.628(0.496~0.759)、0.630(0.499~0.762),P值分別為0.020、0.0002、0.0001、0.056、0.052,實性成分大小及實性成分比例無明顯預測GGN預后價值(P值均大于0.05)。聯合GGN直徑、平均CT值及CT差值這三個指標的AUG為0.878(圖3),閾值分別7.5 mm(靈敏度84.4%,特異度41.7%),-539HU(靈敏度81.3%,特異度67.7%)及362HU(靈敏度71.9%,特異度75.0%)。

圖1 預測GGN預后各CT參數的ROC曲線圖
3 討 論
肺GGN可由多種病因導致,如炎癥、纖維化或腫瘤等,它是一種非特異性的表現[5-6]。GGN不能排除癌前病變與早期肺癌的可能,因此對GGN良惡性判斷至關重要。GGN直徑是良惡性鑒別的依據,通常直徑越大,浸潤性病變的可能性越大[7-9]。本研究中,GGN形態和邊緣情況在生長組與對照組中無差別,我們推測可能是由于兩組中GGN病理類型大部分為浸潤前或良性病變,并未出現浸潤性病變的形態學特征。
本研究發現GGN的CT值與其良惡性密切相關,包括GGN的平均CT值及其與正常肺組織CT差值。Kitami等指出[10],當GGN的CT值小于-600HU時,病灶可視為浸潤前病變。由于CT值是一個客觀的標準,故使用平均CT值可對GGN灶做出明確診斷,但平均CT值仍受患者年齡、部位、呼吸程度,基礎疾病的影響從而影響其準確性,GGN與周圍肺組織的CT差值作為預測指標,能克服肺組織本身的影響,具有較可靠的預測性,在本研究中,CT差值預測GGN的生長其AUC值最高(0.757[0.650~0.864]),預測效能最好。在腫瘤性病變中,若GGN中實性成分越大,其所占比例越高,惡性程度也越高。在本研究中,實性成分大小及所占比例在預測GGN預后方面價值不大,筆者考慮可能是穩定組中部分GGN為慢性炎癥,其實性成分主要為肺間質炎性增生及炎性細胞浸潤,與生長組中層疊排列的腫瘤組織表現相似,其二可能是本研究的樣本量較少,所搜集的病例未能體現組間的差異。本研究發現肺癌病史為肺GGN危險因素。在非小細胞肺癌中出現的GGN,當其直徑超過8 mm時應及時手術切除,小于8 mm時可影像學隨訪觀察。我們的研究結果表明,對于有肺癌病史的患者,其肺內GGN惡性風險明顯增高。
綜上所述,通過評估肺GGN直徑、平均CT值及CT差值,可為病灶處理策略的選擇提供重要依據。此外,患者既往有肺癌病史,也有助于肺GGN的浸潤性診斷。

